2-(2-氨基-3-吡啶基)-苯并咪唑的合成、晶体结构和荧光特性研究
2011-09-29易平贵于贤勇周继明刘容华李筱芳汪朝旭郑柏树
易平贵 王 涛 于贤勇 周继明 刘容华 李筱芳 汪朝旭 郑柏树
(理论化学与分子模拟省部共建教育部重点实验室,分子构效关系湖南省普通高等学校重点实验室,湖南科技大学化学化工学院,湘潭 411201)
2-(2-氨基-3-吡啶基)-苯并咪唑的合成、晶体结构和荧光特性研究
易平贵*王 涛 于贤勇 周继明 刘容华 李筱芳 汪朝旭 郑柏树
(理论化学与分子模拟省部共建教育部重点实验室,分子构效关系湖南省普通高等学校重点实验室,湖南科技大学化学化工学院,湘潭 411201)
在合成2-(2-氨基-3-吡啶基)-苯并咪唑的基础上,利用NMR(1H、13C、COSY、HSQC和HMBC)、MS、IR和UV进行了详细表征;通过X-ray单晶衍射仪测定了该化合物的晶体结构,实验结果表明该晶体属于三方晶系(空间群R3,a=1.8337(3)nm,b=1.8337(2)nm,c=1.7777(4)nm,V=5.1764(15)nm3,Z=18),很好地支持了波谱表征的结果。 同时,结合密度泛函计算,研究了 2-(2-氨基-3-吡啶基)-苯并咪唑的荧光光谱。结果表明,化合物的双荧光不是由同一种异构体发射的,而是来源于不同异构体:长波区500~600 nm的荧光由K构型发射,短波区350~450 nm的发射由异构体E1和E2共同产生,理论预测的光谱与实验一致。
2-(2-氨基-3-吡啶基)-苯并咪唑;核磁共振;晶体结构;荧光光谱
自1965年Weller[1-2]首次用激发态质子转移解释水杨酸甲酯的荧光光谱Stoke效应以来,分子内质子转移引起了广泛的关注[3-9]。在过去的50多年,科学家对许多具有质子转移的体系进行了研究[10-25],例如 Rozwadowski[26]和 Schilf[27]采用 hammet常数与互变异构体的平衡常数研究了取代基效应对Schiff碱及其衍生物中质子转移的影响;李浩然等[28]研究了溶剂分子在尿嘧啶分子质子转移过程中的作用;Vargas[29]研究了温度对质子转移过程中各异构体所占比例的影响。由于分子内质子转移本身物理和化学本质的复杂性以及反应的迅速性,在很多具体情况下质子转移的详细机理仍然无法完全理解,如:能否发生分子内第一单重激发态分子转移,分子内第一单重激发态质子转移有无能垒,三重激发态对激发态质子转移的影响,基态有没有两个稳定态和分子间质子反应是协同还是分步的机理,所以仍有待于对它进行深入研究[30-32]。
2-苯并咪唑系化合物是具有分子内质子转移的重要分子[33-37],也是一类性能优良的有机非线性光学材料[38-39],研究此类分子的分子内质子转移过程机制对其在光电子器件的应用具有重要意义。先前虽有关于2-(2-氨基-3-吡啶基)-苯并咪唑质子转移现象的报道,但研究主要集中在其化学特性上,鲜见介质环境对质子转移影响的研究。根据袁彦杰等[40]的研究,发现介质环境对质子转移过程有较大影响,因此研究化合物在不同溶剂中的质子转移过程具有重要意义。本文在合成2-苯并咪唑系化合物的基础上,通过多种谱学技术对标题化合物分子结构进行了详细表征,结合密度泛函计算研究了它在不同溶剂中的荧光光谱,并合理地解释了实验现象。
1 实验与方法
1.1 仪器和试剂
NMR采用Bruke AVⅡ 500 MHz核磁共振谱波谱仪测定,MS采用美国Agilent公司6120 LC/MS型质谱仪测定;UV采用SHIMADZU UV-2501PC紫外光谱仪测定;IR使用Perkin-Elmer FT红外光谱仪测定;荧光采用SHIMADZU RF-5301PC荧光光谱仪测定;熔点测定采用北京泰克X-4数字显示显微熔点仪测定,温度计未校正。
实验所用的试剂如多聚磷酸、氨水、NaCl、邻苯二胺、2-氨基烟酸等均为国产分析纯试剂,所有试剂未经进一步纯化,实验用水均为蒸馏水。
1.2 2-(2-氨基-3-吡啶基)-苯并咪唑的合成
2-(2-氨基-3-吡啶基)-苯并咪唑参照文献[41]报道的方法合成,反应路线见Scheme 1,产率约80%。m.p.217~219 ℃;UV(EtOH)λmax:346 nm;1H NMR(DMSO-d6,500 MHz,ppm):δ:6.72(dd,J=7.69,4.80 Hz,1H,Py-H),7.20(t,J=7.50 Hz,1H,Ar-H),7.25(t,J=7.50 Hz,1H,Ar-H),7.53(d,J=7.82 Hz,1H,Ar-H),7.69(d,J=7.82,1H,Ar-H),7.88(s,2H,N-H),8.09(dd,J=4.80,1.68 Hz,1H,Py-H),8.21(dd,J=7.69,1.68 Hz,1H,Py-H),12.88(s,1H,N-H);13C NMR(DMSO-d6,125 MHz,ppm):δ:157.8,151.2,150.2,143.1,135.5,134.3,123.3,122.2,118.9,112.1,111.4,106.3。IR(KBr,cm-1) ν:3 402,3 283,3 057~2 679,1 609,1 478,737;MS-ESI m/z:211[M+H]+。

Scheme 1 Systhetic route of 2-(2-amino-3-pyridyl)-benzimidazole
1.3 晶体结构测定
晶体衍射数据在Bruker Smart APEX 1000 CCD衍射仪上,采用石墨单色化的Mo Kα射线(λ=0.071073 nm),在 113 K 下运用 φ-ω 扫描技术收集。收集的数据通过SAINTPLUS程序还原,SADABS做吸收校正;晶体结构运用SHELXS-97程序由直接法解出并用SHELXL-97程序对所有非氢原子坐标和各向异性温度因子进行了全矩阵最小二乘法精修。有关晶体其他一些详细的信息列于表1。
CCDC:760505。

表1 2-(2-氨基-3-吡啶基)-苯并咪唑的晶体数据和结构精修参数Table 1 Crystal data and structure refinement for 2-(2-amino-3-pyridyl)-benzimidazole

续表1
1.4 计算方法
本文采用含时密度泛函理论(TDDFT)与单激发组态相互作用(CIS)相结合的计算方法,拟在CIS/6-31G(d,p)水平上,对气相条件下2-(2-氨基-3-吡啶基)-苯并咪唑分子异构体激发态进行了全优化,通过振动频率分析确认其稳定性,然后在TD OLYP/6-31++G(d,p)水平上进行激发态能量计算。计算溶剂作用时,在 CIS/6-31G(d,p)水平上结合 PCM[42-44]模型对异构体激发态进行了全优化,然后在TD OLYP/6-31++G(d,p)水平上结合PCM模型对已优化的激发态结构进行单点能计算,全部计算在Gaussian 03[45]软件包上完成。
2 结果与讨论
2.1 谱学表征
目标产物经NMR、IR和元素分析而确定结构。在IR谱中,3402和3283 cm-1处出现2个吸收峰,分别归属为咪唑环上-NH-和吡啶环上-NH2的νN-H伸缩振动;1609 cm-1处尖而强的吸收峰对应于νC=C伸缩振动;737 cm-1处尖锐的吸收峰则为邻取代苯环的特征吸收峰。
在1H NMR 谱中,δ=12.90 和 7.88 的单峰分别归属于咪唑环上的-NH和吡啶环上的-NH2。同时由于吡啶环上N原子的吸电诱导作用,使其位氢的化学位移趋于低场,因此δ=8.21归属于11-H(各原子编号参见图2)。根据化合物的COSY谱,可观察到谱峰 δ=8.21→6.72→8.09 存在相关,因此 10-H 和 9-H 的化学位移分别为 δ=6.72 和 8.09(而 δ=6.72、8.09和8.1谱峰的耦合常数也从另一方面支持了从COSY谱中得到的结论)。确定吡啶环上氢的化学位移后,可从化合物的HSQC谱(见图1)容易地归属出9-C、10-C 和 11-C 的化学位移分别为 δ=150.2、112.1和 135.5。 在 HMBC 谱(见图 1)中,δ=106.3 的谱峰与9-H和10-H存在远程相关,δ=157.8的谱峰与9-H和11-H存在远程相关,因此δ=106.3和157.8分别对应于8-C和12-C。

图1 2-(2-氨基-3-吡啶基)-苯并咪唑的HSQC和HMBC谱Fig.1 HSQC and HMBC spectra of 2-(2-amino-3-pyridyl)-benzimidazole
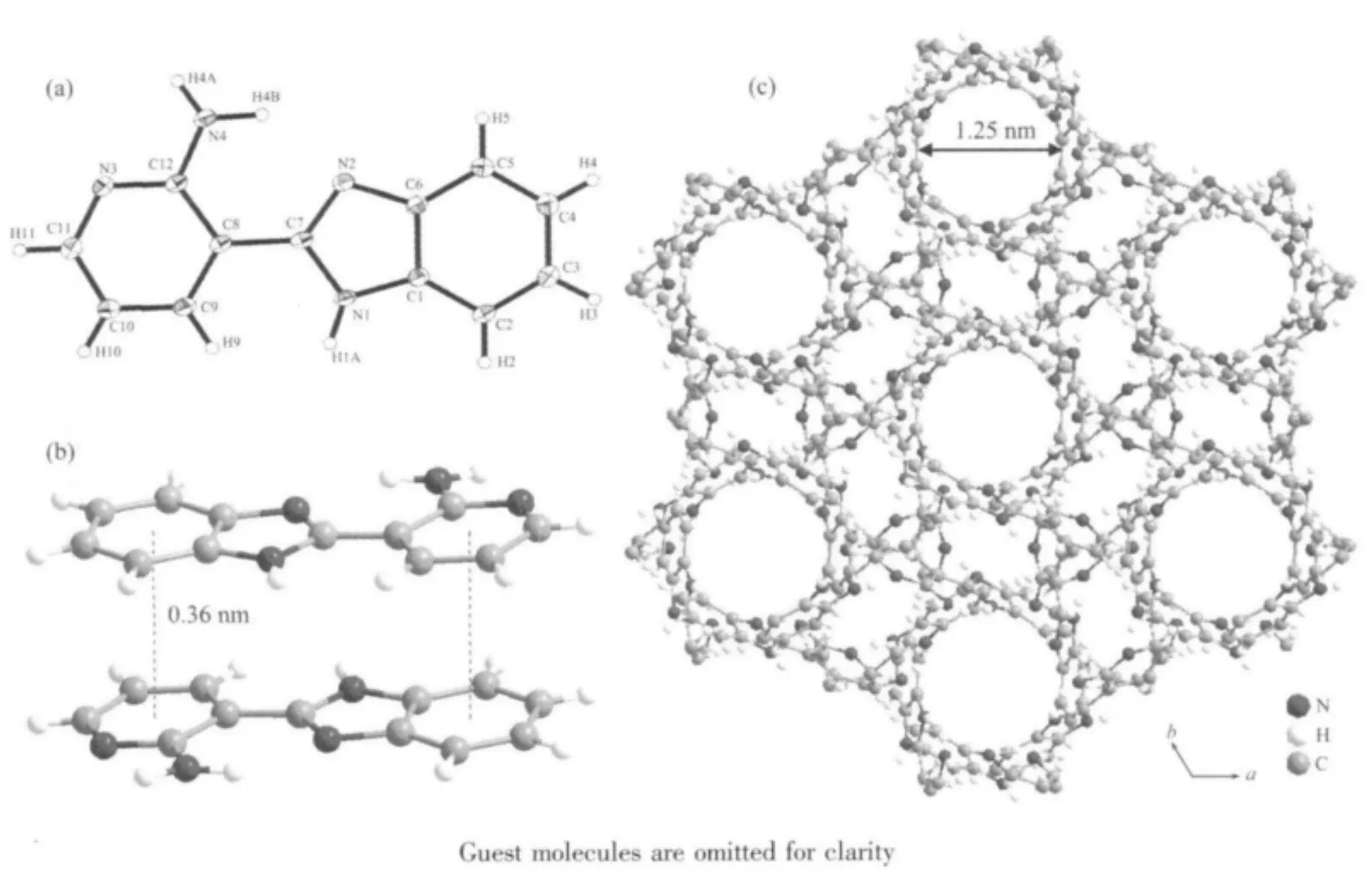
图2 (a)2-(2-氨基-3-吡啶基)-苯并咪唑的分子结构;(b)晶体中两相互平行的标题分子间的π-π堆积作用;(c)标题分子沿c轴方向的晶胞堆积图Fig.2 (a)Molecular structure of 2-(2-amino-3-pyridyl)-benzimidazole;(b)π-π interaction between two molecules in crystals;(c)Crystal packing viewed from the c axis are presented
另一方面,在HMBC谱中,可观察到δ=151.2、143.1和134.3的谱峰与1A-H存在远程相关,由于7-C位于2个N原子中间,受吸电的诱导效应大,其化学位移趋于低场,故δ=151.2归属为7-C,而9-H与之远程相关,也支持了对7-C的归属。由于1-C与1A-H的距离小于6-C的,故1-C与1A-H的交叉峰强度要大于6-C的,故而δ=143.1对应于1-C的化学位移,δ=134.3对应于6-C的化学位移。在确定1-C后,可根据与之相关的交叉峰,可知δ=111.4或122.2对应于2-C或3-C,根据它们在HSQC谱中所对应H的裂峰情况,2-C和2-H的化学位移应为δ=114.2和7.53(d),3-C和3-H的化学位移应为122.2和7.20(t)。同理,可归属4-C和4-H的化学位移分别为123.3和7.25(t),5-C和5-H的化学位移分别为118.9 和 7.69(d)。
2.2 晶体结构
2-(2-氨基-3-吡啶基)-苯并咪唑的分子结构如图2a所示(部分键长和键角见表2)。在该分子中存在2个平面:苯并咪唑环平面和吡啶环平面,两平面间的二面角为10.9°,整个分子表现为略微弯曲的平面结构,两平面的交线是C(7)-C(8)键,键长为0.146 0(2)nm,介于双键(0.132 nm)和单键(0.153 nm)之间,这可能是由于咪唑环与吡啶环形成大的共轭体而使C-C单键键长缩短,而C(12)-N(4)的键长为0.135 4(2)nm和吡啶环上C(12)-N(3)键长0.1352(2)nm十分接近,接近双键,更接近Scheme 2中的T式结构。

表2 2-(2-氨基-3-吡啶基)-苯并咪唑的部分键长和键角Table 2 Selected bond lengths(nm)and bond angles(°)of 2-(2-amino-3-pyridyl)-benzimidazole
标题化合物的晶体结构分析表明:2-(2-氨基-3-吡啶基)-苯并咪唑存在较强分子内氢键(H4B…N2,键长为0.196(3)nm,键角为∠N4-H4B…N2=132.45°)和两种类型的分子间氢键:H1A…N3,键长为0.189(2)nm,键角为∠N1-H1A…N3=164.27°;H4A…N2,键长为0.225(3)nm,键角为∠N4-H4A…N2=170.87°。另外,在两相互平行的分子中,吡啶环与苯环之间还存在较强的堆积作用,作用距离为0.36 nm(见图2b)。标题化合物的三维晶体结构正是通过以上氢键和π-π堆积等弱相互作用构筑起来的。该三维结构沿c轴方向存在一个一维孔道(见图2c),直径约为1.25 nm,而无序的溶剂水分子恰好位于孔道中央。
2.3 荧光光谱
图3是2-(2-氨基-3-吡啶基)-苯并咪唑分子在溶剂中的荧光光谱,化合物在所有溶剂中的发射光谱均存在双荧光,短波发射波长约在395 nm,长波发射波长约在535 nm,且长波区荧光强度大于短波区荧光强度。同时,结合理论计算进一步对该问题进行研究,分别计算出2-(2-氨基-3-吡啶基)-苯并咪唑的3种构型在气相以及溶剂中的荧光发射波长(λ)、谐振强度 f、基态总能量(Es0)、以 E1 基态为基准的相对能量(ΔEs0)、第一激发态总能量(Es1)和以E1激发态为基准的相对能量(ΔEs1),结果如表3所示。

图3 2-(2-氨基-3-吡啶基)-苯并咪唑在溶剂中的荧光光谱Fig.3 Fluorescence spectra of 2-(2-amino-3-pyridyl)-benzimidazole in few solvents

表 3 2-(2-氨基-3-吡啶基)-苯并咪唑激发态(S1(π,π*)1)性质的计算值Table 3 Calculated property for 2-(2-amino-3-pyridyl)-benzimidazole in the excited state(S1(π,π*)1)

Scheme 2 Machanics of intramolecular proton transfer of 2-(2-amino-3-pyridyl)-benzimidazole
根据理论计算,在溶剂中2-(2-氨基-3-吡啶基)-苯并咪唑分子内质子转移机理如Scheme 2所示,其中E1和E2为正常构型,K为质子转移构型,3种分子构型均以一定的动态平衡方式存在。从表3所得的计算结果可知:在基态下,无论是在气相或溶剂中,3种构型中E1基态能量最小,表明E1是基态时的优势构型(也与晶体结构相一致)。当在激发态时,气相中的E1与K之间的能量差约10 kJ·mol-1,而在溶剂中二者的能量差最小仅8.87 kJ·mol-1,通过分子内质子转移可以生成K,因此在激发态下除了烯氨式E1和E2外,还应该存在K构型。同时通过对E1和E2的发射波长计算可知,二者的发射波长均位于短波区,故认为E1和E2本身并不能发射双荧光,长波区强发射峰可能由其他异构体发射。根据以上分析可知,E1在激发态时可发生分子内质子转移反应而生成异构体K,计算结果也证明了K的发射能的确处于长波区域,约为509 nm,和实验值525 nm相比,仅仅相差16 nm。即实验光谱中双荧光的特征可以解释为:长波区的强发射来源于经ESIPT过程生成的异构体K,而短波区的弱峰则是E1和E2共同发射引起的。
另一方面,由图3可知,K构型的荧光强度均大于E1和E2构型的荧光强度,与计算所得二者谐振强度的大小关系相反,这是因为不同构型的荧光强度还受到浓度影响,浓度越大,荧光强度越强,所以在溶剂中K是优势构型,而K是E1通过质子转移过程生成,由此可知,E1发生质子转移生成K的速率大于激发E1发射荧光的速率。
3 结 论
本文在合成2-(2-氨基-3-吡啶基)-苯并咪唑的基础上,利用多种谱学手段结合单晶衍射对其进行详细的表征。晶体衍射结果表明该晶体属于菱形晶系,存在分子内氢键和分子间氢键,从而降低体系的能量而有利于晶体结构的稳定;另一方面,2-(2-氨基-3-吡啶基)-苯并咪唑的荧光光谱表明,化合物在所有溶剂中均存在双荧光带,短波荧光带由E1和E2结构发射,长波荧光带来源于构型E1通过质子转移过生成的构型K荧光,且长波荧光强度大于短波荧光强度,理论预测的光谱与实验一致。
[1]Weller A H.Z.Elektrochem.,1956,60:1144-1151
[2]Been H,Grellmann K H,Gurr M,et al.Discuss.Faraday Soc.,1965,39:183-193
[3]Barbara P F,Nicol P F,El-Sayed M A.J.Phys.Chem.,1991,95(25):10215-10222
[4]Nibbering E J,Elsaesser T.Chem.Rev.,2004,104(4):1887-1893
[5]Dermota T E,Zhong Q,Castleman A W.Chem.Rev.,2004,104(4):1861-1869
[6]Stolow A,Bragg A E,Neumark D M.Chem.Rev.,2004,104(4):1719-1726
[7]Kryachko E S,Nguyen M T,Zeegers-Huykens T.J.Phys.Chem.A,2001,105(10):1934-1941
[8]YI Ping-Gui(易平贵),PENG Hong-Liang(彭洪亮),YU Xian-Yong(于贤勇),et al.Acta Chim.Sinica(Huaxue Xuebao),2009,67(4):276-282
[9]Hu X B,Li H R,Liang W C,et al.J.Phys.Chem.B,2005,109(12):5935-5942
[10]Rodríguez-Santiago L,Sodupe M,Bertran J.J.Phys.Chem.A,2000,104(6):1256-1263
[11]Melhuish W H.J.Phys.Chem.,1961,65(2):229-235
[12]Catalán J,Fernández-Alonso J I.J.Mol.Stuct.,1975,27(2):59-65
[13]Catalán J,Fernández-Alonso J I.Chem.Phys.Lett.,1975,18(1):37-40
[14]Hou S Y,Hetherington W M,Korenowski G M,et al.Chem.Phys.Lett.,1979,68(3):282-284
[15]Goodman J,Brus L E.J.Am.Chem.Soc.,1978,100(24):7472-7474
[16]Smith K K,Kaufmann K J.J.Phys.Chem.,1981,85(20):2895-2904
[17]Nishiya T,Yamauchi S,Baba M,et al.J.Phys.Chem.,1986,86(22):5730-5738
[18]Gormin D A,Heldt J,Kasha M.J.Phys.Chem.,1990,94(3):1185-1192
[19]Hoshinmoto E,Yamauchi S,Hirota N,et al.J.Phys.Chem.,1991,95(25):10229-10236
[20]Olivieri A C,Sanz D S,Claramunt R.M,et al.J.Chem.Soc.,Perkin Trans.,1993:1597-1604
[21]Swinney T C,Kelley D F.J.Chem.Phys.,1993,99(1):211-217
[22]Drokidis X,Goncalves V,Savin A,et al.J.Phys.Chem.A,1998,102(26):5065-5072
[23]Sobolewski A L,Domcke W.Chem.Phys.Lett.,1999,310(5):548-554
[24]Mordzinski A,Grabowska A.Chem.Phys.Lett.,1982,90(2):122-127
[25]Chou P T,Studer S L,Martinez M L.Chem.Phys.Lett.,1991,178(4):393-398
[26]Rozwadowski Z,Majewski E,Dziembowska T,et al.J.Chem.Soc.,Perkin Trans.2,1999:2809-2817
[27]Schilf W,Kamieński B,Szady-Chelmieniecka A,et al.J.Mol.Struct.,2004,700:105-114
[28]Hu X B,Li H R,Liang W C,et al.J.Phys.Chem.B,2004,108(34):12999-13007
[29]Vargas V,Amigo L.J.Chem.Soc.,Perkin Trans.2,2001:1124-1131
[30]Faxen K,Gilderson G,Adelroth P,et al.Nature,2005,437:286-293
[31]Catalán J,Valle J C D.J.Am.Chem.Soc.,1993,115(10):4321-4332
[32]Lu C,Hsieh R M R,Lee I R,et al.Chem.Phys.Lett.,1999,310(2):102-110
[33]Williams D L,Heller A.J.Phys.Chem.,1970,74(26):4473-4481
[34]Sinha H K,Dogra S K.Chem.Phys.,1986,102(33):337-347
[35]Mukherjee T K,Datta A.J.Phys.Chem.B,2006,110(6):2611-2618
[36]Penedo J C,Lustres J L P,Lema I G,et al.J.Phys.Chem.A,2004,108(29):6117-6125
[37]XU Weng-Guo(徐文国),FENG Ji-Kang(封继康),SUN Jia-Zhong(孙家钟).Chem.J.Chin.Univ.(Gaodeng Xuexiao Huaxue Xuebao),1993,12:1700-1708
[38]Zhang G,Wang H,Yu Y.Applied Physics B,2003,76:677-685
[39]Balamurali M M,Dogra S K.Chem.Phys.,2004,305(2):95-103
[40]YUAN Yan-Jie(袁彦杰),HE Rong-Xing(何荣幸),WANG Hui(王辉),et al.Chem.J.Chin.Univ.(Gaodeng Xuexiao Huaxue Xuebao),2009,30:992-1001
[41]Middleton R W,Wiberly J.Heterocyclic.Chem.,1980,17(6):1757-1765
[42]Cancès M T,Mennucci B,Tomasi J.J.Chem.Phys.,1997,107(8):3032-3041
[43]Cossi M,Barone V,Mennucci B.J.Chem.Phys.Lett.,1998,286(2):253-260
[44]Mennucci B,Tomasi J.J.Chem.Phys.,1997,106(12):5151-5158
[45]Frisch M J,Trucks G W,Schlegel H B,et al.Gaussian03,Revision B03,Gaussian,Inc.,Pittsburgh PA,2003.
Synthesis,Crystal Structure and Fluorescence Characteristics on 2-(2-Amino-3-pyridyl)-benzimidazole
YI Ping-Gui*WANG Tao YU Xian-Yong ZHOU Ji-Ming LIU Rong-Hua LI Xiao-Fang WANG Zhao-Xu ZHENG Bai-Shu
(Key Laboratory of Theoretical Chemistry and Molecular Simulation of Ministry of Education,Hunan Province College Key Laboratory of QSAR/QSPR,School of Chemistry and Chemical Engineering,Hunan University of Science and Technology,Xiangtan,Hunan 411201,China)
2-(2-amino-3-pyridyl)-benzimidazole was synthesized and characterized by NMR (1H,13C,COSY,HSQC,and HMBC),MS,IR,and UV techniques.The crystal structure was determined by X-ray singlecrystal diffraction.The diffraction experiment confirmed the results of spectroscopic analysis and showed that the crystal belongs to rhombohedral,space group R3 with unit cell parameter a=1.833 7(3)nm,b=1.833 7(2)nm,c=1.777 7(4)nm,V=5.1764(15)nm3,Z=18.The emission spectra of the isomers of 2-(2-amino-3-pyridyl)-benzimidazole were calculated by means of the density functional theory.These results show that the dual fluorescence of 2-(2-amino-3-pyridyl)-benzimidazole is produced by its different tautomers,but not by the same isomer:the longwavelength (500~600 nm)emission is from K tautomer,and the short wavelength band (350~450 nm)is produced by E1 and E2.The results of density functional calculations provide a reasonable explanation on the experimental phenomena.CCDC:760505.
2-(2-amino-3-pyridyl)-benzimidazole;NMR;crystal structure;fluorescence spectra
O626.23
:A
:1001-4861(2011)03-0480-07
2010-06-20。收修改稿日期:2010-11-09。
国家自然科学基金(No.20772027,20803020,20971041)和湖南省教育厅(No.09K081,09B032)资助项目。
*通讯联系人。 E-mail:pgyi@hnust.cn,Tel:+86-731-58290187,Fax:+86-731-58290509;会员登记号:S060006760M。
