硫酸长春碱与DNA相互作用的机理研究
2010-12-09张琼梅毕和平
刘 炜,张琼梅,毕和平
(海南师范大学 化学与化工学院,海南 海口 571158)
硫酸长春碱与DNA相互作用的机理研究
刘 炜,张琼梅,毕和平
(海南师范大学 化学与化工学院,海南 海口 571158)
应用荧光光谱法、紫外光谱法和粘度法研究了硫酸长春碱和鲱鱼精DNA分子间的相互作用.在pH为7.4的Tris-HCl缓冲溶液体系中,测量不同DNA浓度下硫酸长春碱的荧光发射光谱,DNA对硫酸长春碱产生了较强的荧光猝灭作用.运用位点模型计算了两个不同温度下硫酸长春碱与DNA的结合常数和结合位点数,根据热力学参数确定了硫酸长春碱与DNA之间的作用力以氢键和范德华力为主;结合荧光探针实验以及粘度实验结果进一步证明硫酸长春碱是以沟槽结合的方式与DNA结合.
硫酸长春碱;DNA;相互作用;机理
核酸是重要的生命物质基础,对生物的生长、发育和繁殖等有重要作用.一些药物分子与DNA的相互作用会影响到DNA的生理和物理化学性质,改变DNA的转录和复制.在医药研究中,DNA与靶向分子相互作用的研究不仅可以阐述一些抗肿瘤、抗病毒药物以及致癌物的作用机理,而且对进一步指导新型药物的设计合成的研究都具有重要意义[1-2].
长春碱为夹竹桃科植物长春花中提取的一种有抗癌活性的生物碱,目前尚未见有关其与DNA相互作用的研究报道.本文主要研究硫酸长春碱与DNA相互作用的机理,获得硫酸长春碱与DNA相互作用的信息,包括反应的结合常数、结合位点数、热力学参数以及结合方式等,为研究硫酸长春碱的抗癌机理提供了重要信息.图1为硫酸长春碱的结构式.
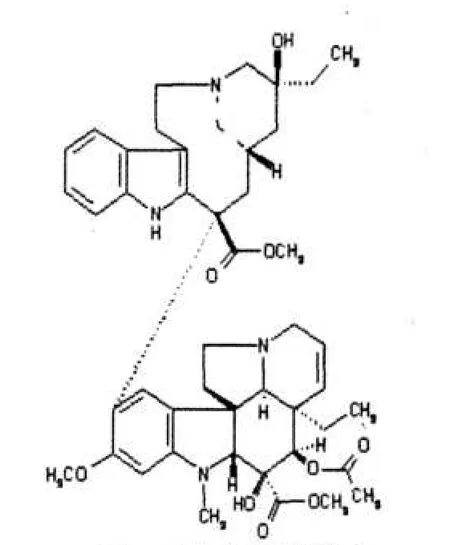
图1 硫酸长春碱结构式Fig.1 Stucture of Vinblastine sulfate
1 实验部分
1.1 仪器与试剂
RF-5301荧光分光光度仪(Hitachi,日本);TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);PHSJ-4A型pH计(上海精密科学仪器公司);鲱鱼精DNA(sigma,美国);硫酸长春碱(海南希源化工有限公司,纯度>98%);其它所用试剂均为分析纯试剂,实验用水均为二次蒸馏水.
1.2 实验方法
在10 mL容量瓶中,依次加入等量pH7.4的Tris-HCl缓冲溶液,固定量的硫酸长春碱溶液和不同量的DNA溶液,并用二次蒸馏水稀释到刻度,摇匀,在荧光仪上进行荧光光谱和吸收光谱的测定.荧光激发波长选择271 nm,发射波长为363 nm,狭缝宽度均为5 nm.
在10 mL容量瓶中,依次加入等量pH7.4的Tris-HCl缓冲溶液,固定量的DNA溶液和不同量的硫酸长春碱溶液,并用二次蒸馏水稀释到刻度,摇匀,进行粘度的测定.
2 结果与讨论
2.1 DNA对硫酸长春碱荧光光谱的影响
图2为pH7.4tris-HCl缓冲液中DNA存在下硫酸长春碱的荧光发射光谱.从图2中可以看出,硫酸长春碱(a:2×10-5mol/L)在363 nm处有一最大发射峰,DNA存在可使硫酸长春碱363 nm处的荧光发射强度发生猝灭,随着DNA浓度增大(b→d:6.8×10-5mol/L,1.36×10-4mol/L,2.04×10-4mol/L),猝灭程度逐渐增强,表明DNA和硫酸长春碱可能形成了复合物.
2.2 DNA对硫酸长春碱紫外吸收光谱的影响
图3为pH7.4 tris-HCl缓冲液中DNA存在下硫酸长春碱的紫外吸收光谱.从图3中可以看出,硫酸长春碱(a:2×10-5mol/L)在271 nm处有一紫外吸收峰,随着DNA浓度的增大(b→c:6.8×10-5mol/L,1.36×10-4mol/L),硫酸长春碱的紫外吸收峰先发生降低和蓝移,后发生显著升高和蓝移.由于有机分子与DNA以嵌入或沟槽方式结合时会导致有机分子的紫外吸收峰强度发生升高或降低,同时最大吸收峰波长会发生蓝移或红移[3],因此硫酸长春碱与DNA可能是以嵌入或沟槽的方式结合.

图2DNA存在下硫酸长春碱的荧光发射光谱Fig.2 The fluorescence emission spectra of vinblastine sulfate in the presence of DNA
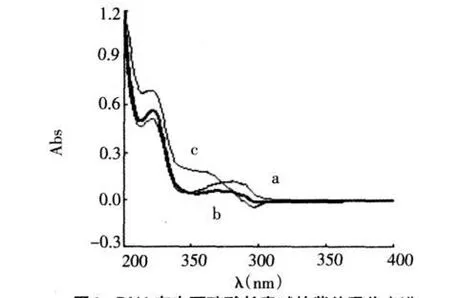
图3DNA存在下硫酸长春碱的紫外吸收光谱Fig.3 The UV absorption spectra of vinblastine sulfate in the presence of DNA
2.3 DNA与硫酸长春碱二元络合物的组成及其结合常数
根据静态猝灭公式
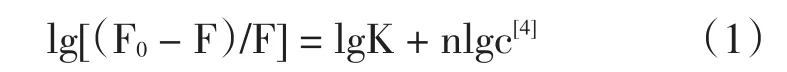
(F0与F分别代表总的和游离态的药物的荧光强度,K为硫酸长春碱与猝灭剂之间的结合常数,c为猝灭剂的平衡浓度,n为结合位点数),由式(1)分别作出不同温度下硫酸长春碱-DNA体系的关系图,结果分别见图4和图5,通过斜率和外推截距可以求出硫酸长春碱与猝灭剂之间的结合常数和结合位点数.由图4可知,25℃时硫酸长春碱与DNA之间的结合常数为2.66×104,结合位点数为1.195,线性相关系数为0.991 1;由图5可知,40℃时硫酸长春碱与DNA之间的结合常数为1.05×104,结合位点数为1.071 9,线性相关系数为0.983 9.
2.4 硫酸长春碱与DNA结合反应的热力学性质及作用力
药物小分子与生物大分子的作用力包括氢键、范德华力、静电引力、疏水作用力等,药物不同,与DNA作用力类型也不同.当温度变化不大时,反应的焓变可视作常数,根据热力学公式可以计算药物小分子与生物大分子作用间的有关热力学参数:
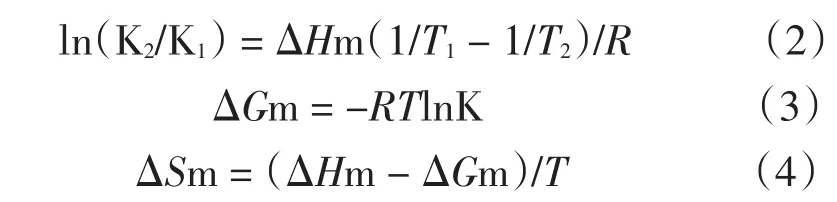
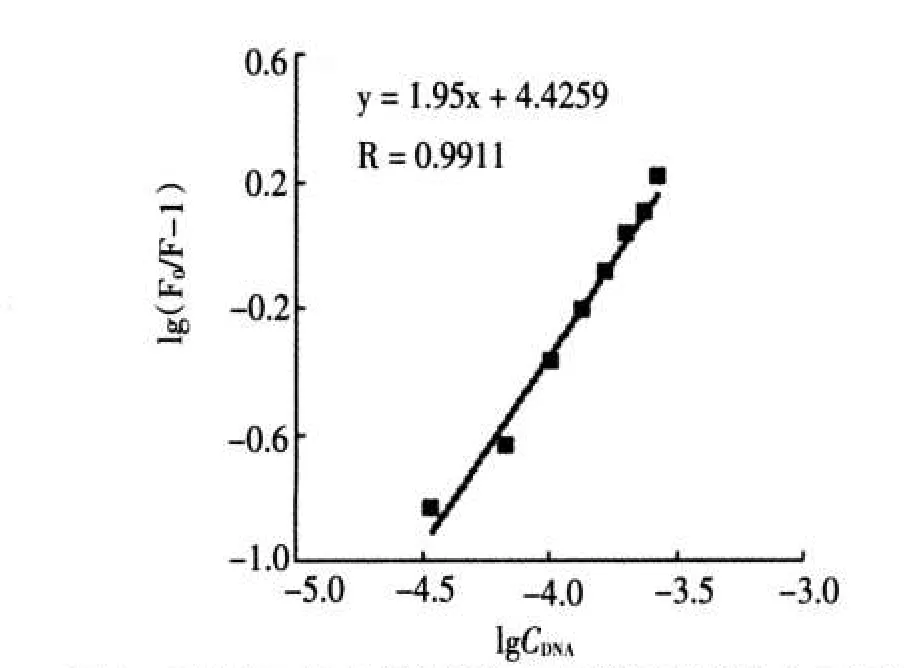
图425℃时DNA和硫酸长春碱的结合常数及结合位点数Fig.4 The binding constant and sites of vinblastine sulfate-DNA at 25℃

图540℃时DNA和硫酸长春碱的结合常数及结合位点数Fig.5 The binding constant and sites of vinblastine sulfate-DNA at 40℃
根据药物小分子与生物大分子作用的有关热力学参数可以简单判断其相互作用类型[5]:若ΔH>0及ΔS>0则主要表现为疏水作用,ΔH<0及ΔS>0主要表现为静电作用,ΔH<0及ΔS<0主要表现氢键或者范德华作用.
根据硫酸长春碱与DNA的结合常数K1(298 K)=2.66×104,K2(313K)=1.05×104,按式(2)~(4)可以求得二者结合过程的热力学函数:ΔHm=-48.2kJ·mol-1,ΔGm(298K)=-25.2kJ·mol-1,ΔSm(298K)=-77J·K-1·mol-1,由此可初步判断硫酸长春碱与DNA间是以氢键或者范德华作用力结合为主.
2.5 硫酸长春碱对小檗碱-DNA体系荧光强度影响的研究
盐酸小檗碱(BR)是以治疗肠道痢疾而著称的黄连素,可以专一性地插入DNA双螺旋的碱基对之间,使本身很弱的荧光得到显著性增强,当盐酸小檗碱从双螺旋中出来时,荧光又显著性降低,因此可作为荧光探针研究DNA与小分子化合物的相互作用[6].若硫酸长春碱和DNA是以嵌入的方式结合,则硫酸长春碱可与BR竞争DNA的结合位点,将BR从DNA分子中挤出,从而使BR-DNA体系的荧光强度降低.实验结果表明,随着硫酸长春碱浓度的增大,BR-DNA体系荧光强度基本不变,说明了硫酸长春碱与DNA之间不是嵌入结合.
2.6 粘度研究
具有光学活性的探针对于探讨键合模式一般可以提供必要的但不是充分的证据[7],粘度测定是检测配合物与DNA是否以嵌入方式结合的最有效的方法.小分子配合物通过经典嵌入式与DNA作用时,DNA相邻碱基对的距离会增大以容纳配体,导致DNA双螺旋伸长,DNA溶液的粘度增加;当以静电、沟槽结合等非嵌入方式与DNA作用时,DNA溶液的粘度度变化不明显[8].
在相同浓度的DNA及缓冲体系溶液中加入不同浓度的长春碱测量其粘度.由实验结果,按式(5)计算相对粘度:

式中t0为空白溶液流经毛细管所需时间,t为含不同量长春碱的DNA溶液流经毛细管所需时间,以(η/η0)1/3对结合比率r作图,η0为未加入硫酸长春碱时DNA的粘度,随着长春碱浓度增大,DNA溶液的粘度基本不变,因此可知长春碱与DNA之间不是以嵌入方式结合.
2.7 作用机理探讨
小分子探针与双螺旋DNA结合方式主要包括静电式、嵌入式和沟槽式3种模式.根据硫酸长春碱与DNA的作用力主要为氢键或者范德华作用力,可以排除静电结合的方式;如果小分子与DNA键合作用是通过经典嵌入式,则药物分子-DNA体系溶液的粘度应该增加,然而粘度实验的结果显示硫酸长春碱-DNA体系溶液的粘度不变,而且硫酸长春碱对BR-DNA体系荧光强度不产生猝灭作用,结合硫酸长春碱和DNA反应的紫外吸收谱图,说明长春碱与DNA应该是以沟槽结合的方式相互作用.
[1]Vrana O,Brabec V.Electrochemical analysis of antitumor platinum drugs and their complexes with DNA[J].Bio⁃electrochem.Bioenerg,1988,19(1):145-160.
[2]Zhao Y D,Pang D W,Wang Z L.Electrochemical studies of antitumor drugs fundamental electrochemical characteris⁃tics of and iron(II)schiff base complex and its interaction with DNA[J].Acta chimica sinica,1998,56(2):178-183.
[3]Kumar C V,Asuncion H E.DNA binding studies and site selective fluoscence sensitization of an anthryl probe[J].J Am Chem Soc,1993,115:8547-8553.
[4]冯喜增,金瑞祥,曲芸,等.各种离子对血卟啉与牛血清白蛋白相互结合反应的影响研究[J].高等学校化学学报,1996,17(6):866-869.
[5]Ross D P,Sabramania N S.Thermodynamics of protein as⁃sociation reactions:forces contributing to stability[J].Bio⁃chemistry,1981,20:3096-3102.
[6]贺吉香,江崇球,高明霞,等.盐酸小檗碱与脱氧核糖核酸相互作用的研究[J].光谱学与光谱分析,2003,23(4):755-758.
[7]Sigma D S,Mazuder A,Perrin D M.Chemical nucleases[J].Chem Rev,1993,93:2295-2316.
[8]卓琳.DNA与小分子相互作用的研究进展[J].重庆工商大学学报:自然科学版,2005,22(5):440-445.
[9]Satyanarayana S,Daborusak J C,Chaires J B.Tris(phenoan⁃throline)ruthenium(Ⅱ)enantiomer interactions with DNA:mode and specificity of binding[J].Biochemistry,1992,31:9319-9324.
Study on the Interaction Between Vinblastine Sulfate and DNA
LIU Wei,ZHANG Qiongmei,BI Heping
(College of Chemistry and Chemical Engineering,Hainan Normal University,Haikou571158,China)
The interaction of vinblastine sulfate with DNA was studied using UV spectrometry,fluorescence spectrome⁃try and viscosity method.Fluorescence emission spectra of vinblastine sulfate with various concentration of DNA at pH 7.4 tris-HCl buffer solution was measured.The results showed that the fluorescence intensity of vinblastine sulfate was quenched when DNA was added.The binding constant K and the binding sites n were calculated at two different centi⁃grade.The main binding force between vinblastine sulfate and DNA is hydrogen bonding or van der Waals force accord⁃ing to thermodynamic parameters.It was proved that vinblastine binds with DNA in a mode of groove binding combined with the results of fluorescence probe test and viscosity test.
vinblastine sulfate;DNA;interaction;mechanism
O 657.32
A
1674-4942(2010)04-0403-04
2010-09-19
海南省教育厅项目(Hjkj2009-39),海南省自然科学基金项目(209004)
黄 澜
