取代度相同的N-酰化低聚壳聚糖清除自由基作用的研究
2010-08-27孙涛银旭红谢晶李立赖克强周冬香
孙涛, 银旭红, 谢晶, 李立, 赖克强, 周冬香
(上海海洋大学食品学院,上海 201306)
取代度相同的N-酰化低聚壳聚糖清除自由基作用的研究
孙涛, 银旭红, 谢晶, 李立, 赖克强, 周冬香
(上海海洋大学食品学院,上海 201306)
低聚壳聚糖经N-酰化得到取代度相同的N-马来酰低聚壳聚糖和N-邻苯二甲酰低聚壳聚糖,其取代度均为0.25。用红外光谱对其结构进行表征,凝胶色谱测定其相对分子质量大小。并考察了其对羟基自由基(.OH)和1,1-二苯基苦基苯肼自由基(DPPH)的清除能力。结果表明:取代度相同,N-邻苯二甲酰低聚壳聚糖对.OH、DPPH的清除能力优于N-马来酰低聚壳聚糖。这说明取代度相同时,取代基的结构会影响N-酰化低聚壳聚糖对自由基的清除活性。
低聚壳聚糖;N-酰化;抗氧化;取代度
自由基引起的氧化对机体具有巨大的损伤作用,如引起蛋白质损伤、酶失活、导致衰老、肿瘤、动脉硬化等多种疾病[1-2]。因此筛选高效的活性氧清除剂具有重要的意义。低聚壳聚糖是壳聚糖的降解产物,其分子单元结构中有大量的氨基和羟基,具有良好的抗氧化性[3-5],同时也决定了它可以进行多种化学改性。N-酰化改性是低聚壳聚糖的一种重要改性方式,研究报道N-酰化壳聚糖具有良好的吸湿保湿和抑菌作用[6-7],但是其抗氧化性,尤其是其N-取代基结构和取代度与其抗氧化性能之间的关系还尚未见报道。作者通过制备取代度相同的N-马来酰和N-邻苯二甲酰化低聚壳聚糖,通过考察其对羟基自由基·OH和DPPH的清除活性,研究了取代基团的结构对N-酰化低聚壳聚糖的抗氧化活性的影响,为低聚壳聚糖衍生物抗氧化性能的进一步研究提供理论基础。
1 材料与方法
1.1 材料
低聚壳聚糖,购自浙江金壳生物化学有限公司(凝胶色谱测定其相对分子质量为5 000 000);鲁米诺,DPPH,购自Sigma公司;其余试剂均为分析纯,购自上海化学试剂公司;磁力搅拌器,p H计,分光光度计,电导率仪,EQUNOX55傅立叶红外-拉曼光谱仪,Waters 515型凝胶色谱仪。
1.2 壳聚糖衍生物的制备
称取5.0 g低聚壳聚糖加入100.0 mL蒸馏水溶解,搅拌溶解,称取1.0 g马来酸酐(0.5 g邻苯二甲酸酐),用20.0 mL丙酮溶解,然后缓慢加入反应器,在室温下搅拌反应15 h,然后用丙酮沉淀,过滤,产物用丙酮反复洗涤,最后在60℃烘干,得到N-马来(邻苯二甲)酰低聚壳聚糖衍生物[8]。
1.3 结构表征
1.3.1 红外光谱 红外光谱在EQUNOX55傅立叶红外-拉曼光谱仪上进行,采用KBr压片法制样,测定波数范围为500~4 000 cm-1,分辨率为0.8 cm-1。
1.3.2 相对分子质量的测定 凝胶色谱法测定N-酰化低聚壳聚糖相对分子质量大小。测试条件如下:柱子:TOSOH BIOSEP TSK-Gel G4000SWXL (D7.8 mm×300 mm);流动相:0.2 mol/L醋酸钠和醋酸缓冲溶液,p H=4.8;色谱仪:Waters 515型凝胶色谱仪,检测器:Waters 2410示差折光检测器(美国Waters公司);进样量:50μL;柱温:40℃;标准品:葡聚糖。
1.3.3 取代度的测定 准确称量N-酰化低聚壳聚糖0.100 0 g置500 mL烧杯内,准确加入0.103 8 mol/L HCl标准溶液20.00 mL溶解样品,再加入去离子水200 mL稀释、混匀,用0.468 5 mol/L NaOH标准溶液返滴,测定电导率值,得电导率-氢氧化钠体积关系图,添加趋势线,求其回归方程,从而计算N-酰化低聚壳聚糖的取代度[9]。
1.4 对羟基自由基·OH的清除
用p H=7.40的0.05 mol/L KH2PO4-NaOH缓冲溶液分别配制浓度为6.4×10-4mol/L的鲁米诺溶液、0.012 mol/L H2O2和0.8 mg/mL亚铁氰化钾溶液。以缓冲液作为溶剂,配制成系列不同浓度的样品溶液。用流动注射化学发光分析仪依次测定从稀到浓的样品溶液,读出峰面积。清除率= (A0-Ai)/A0×100%。式中A0为空白溶液峰面积,Ai为样品溶液峰面积。经SOD,过氧化氢酶及甘露醇检测,该体系产生的自由基羟基自由基· OH[10]。
1.5 对DPPH自由基的清除
在装有2.0 mL的浓度为1×10-4mol/L DPPH无水乙醇溶液的比色管中,加入不同浓度的样品溶液2.0 mL,摇匀,33℃避光静置30 min,在517 nm处测量吸光度Ai。用去离子水代替样品溶液,得吸光度A0,无水乙醇代替DPPH,得吸光度Aj。清除率=[1-(Ai-Aj)/A0]×100%[11]。
2 结果与讨论
2.1 红外光谱
图1是低聚壳聚糖及其N-酰化低聚壳聚糖的红外光谱图。NMCOS中1 640 cm-1为烯烃的VC=C振动峰;1 707 cm-1附近出现为不饱和羧基因共轭作用的C=O振动吸收峰;860 cm-1附近为C-H面外振动吸收峰,在壳聚糖未见此峰,这些峰证实了NMCOS中马来酸基的存在[12]。在NPCOS中,1 640 cm-1为烯烃的VC=C振动峰;在750 cm-1附近的吸收峰为邻二取代苯的δAr-H面外弯曲振动峰,这些峰证明了邻苯二甲酸基的存在[13]。NMCOS和NPCOS在1 560 cm-1附近的仲酰胺的δNH振动峰在衍生物中明显增大,同时在1 320 cm-1附近出现VC-N伸缩振动峰,并且在1 073 cm-1和1 023 cm-1处的C3仲羟基和C6伯羟基的C-O的伸缩振动吸收峰与壳聚糖相比没有明显变化,这均证明反应发生在氨基上[7]。凝胶色谱法测得NMCOS和NPCOS的相对分子质量大小分别为5 733和5 029。电导法测定其取代度均为0.25。
2.2 对羟基自由基·OH的清除能力的影响
羟基自由基·OH是一种化学性质很活泼的自由基,它易与生物大分子发生反应,如氨基酸、蛋白质和DNA,对机体危害极大,与衰老、肿瘤等密切相关[15]。
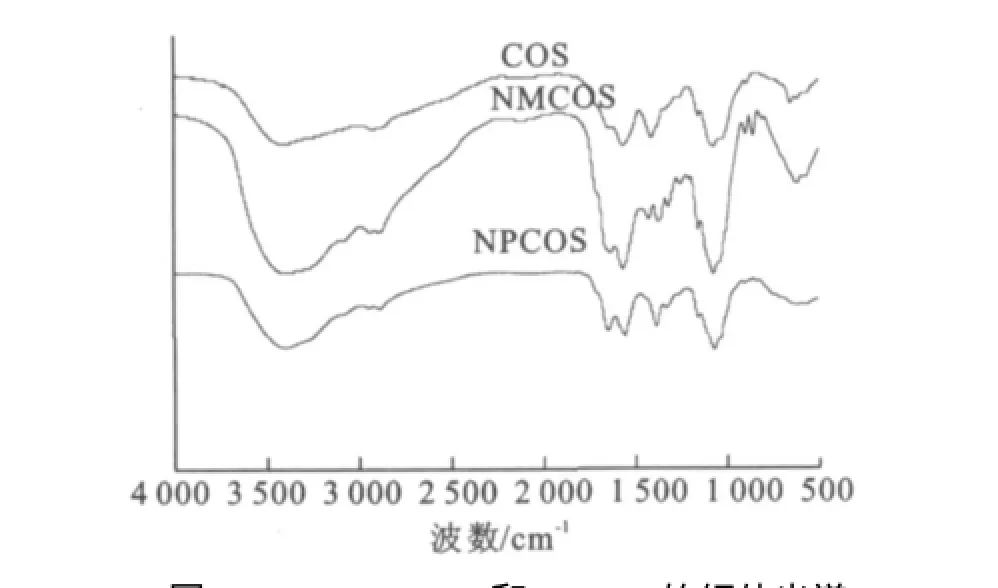
图1 COS、NMCOS和NPCOS的红外光谱Fig.1 FTIR spectra of COS、NMCOS and NPCOS
NMCOS和NPCOS对羟基自由基.OH的清除活性如图2。随着浓度的增加,NMCOS和NPCOS对羟基自由基·OH的清除能力逐渐增强。NPCOS清除羟基自由基·OH的IC50(清除率达到50%时所需自由基清除剂的浓度)为0.06 mmol/ L,而NMCOS没有达到IC50。即取代度相同时, NPCOS对羟基自由基·OH的清除能力更强。
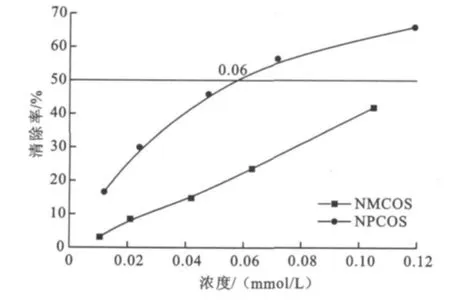
图2 NMCOS和NPCOS对羟基自由基的清除Fig.2 Scavenging effects of NMCOSand NPCOS on hydroxyl radical
低聚壳聚糖及其衍生物中有大量的羟基和氨基,对羟基自由基·OH有如下作用[16]:(1)羟基的氢原子与羟基自由基·OH作用而达到清除目的; (2)氨基和羟基自由基·OH反应生成稳定的大分子自由基;(3)NH2先与溶液中的氢作用形成氨正离子NH3+,再与羟基自由基·OH作用形成稳定物质。对取代度相同的NMCOS和NPCOS,氨基与羟基数目相同。而清除羟基自由基·OH的活性不同,这与取代基团有关。NMCOS和NPCOS均是在低聚壳聚糖氨基上引入取代基,NMCOS的取代基是-COCH=CHCOO-,NPCOS的取代基是-COC6H4COO-,两种基团都是吸电子基团,能降低低聚壳聚糖主链上的电子云密度,使分子内、分子间生成氢键的几率降低,使氨基与羟基的活性增强,易与自由基反应。但是-COC6H4COO-的吸电子效应比-COCH=CHCOO-的吸电子效应强,故取代度相同时,NPCOS对羟基自由基·OH的清除能力比NMCOS强。
2.3 对DPPH的清除能力的影响
图3是NMCOS和NPCOS对DPPH的清除曲线图。NMCOS和NPCOS对DPPH的清除能力均随着浓度的增加而增强。NMCOS和NPCOS的IC50分别是1.2 mmol/L和0.88 mmol/L。NPCOS清除DPPH的能力比NMCOS强。
稳定的DPPH体系是一种广泛用于评价抗氧化剂自由基清除能力的方法。其主要原理是DPPH可以接受自由基清除剂提供的电子或氢从而形成稳定分子。在低聚壳聚糖及其衍生物中,主要是氨基和羟基提供氢与DPPH结合,从而达到清除DPPH的目的。在本体系中,NMCOS和NPCOS取代度相同,氨基和羟基数目相同,但-COC6H4COO-基团的吸电子作用比-COCH=CHCOO-基团的吸电子作用强,从而NPCOS的供氢能力比NMCOS强,故清除DPPH的能力强。
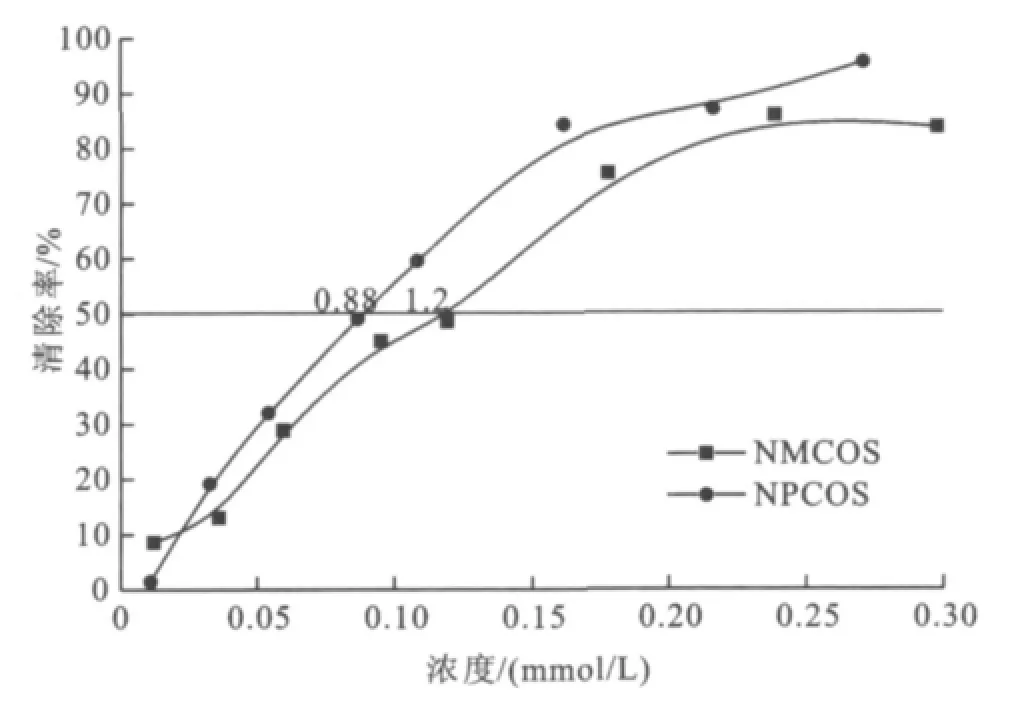
图3 NMCOS和NPCOS对DPPH自由基的清除Fig.3 Scavenging effects of NMCOS and NPCOS on DPPHradical
3 结 语
作者对低聚壳聚糖进行酰化,制得取代度相同的NMCOS和NPCOS。并且考察了其对羟基自由基·OH和DPPH的清除能力。结果表明:取代度相同时,尽管氨基和羟基的数目相同,但是NMCOS和NPCOS对羟基自由基·OH和DPPH的清除效果不同。这说明不同的N-取代基对低聚壳聚糖清除自由基的影响不同。与NMCOS相比,NPCOS引进的-COC6H4COO-的吸电子能力比-COCH=CHCOO-较强,故其清除羟基自由基· OH和DPPH的能力较强。这一结果为低聚壳聚糖及其衍生物的的深入研究有指明了方向。
[1]Joshua A,Sonnen,John C,et al.Montine.Free radical-mediated damage to brain in alzheimer’s disease and its transgenic mouse models[J].Free Radic Biol Med,2008,3:219-230.
[2]Nordberg J,Arner E SJ.Reactive oxygen species,antioxidants,and the mammalian thioredoxin system[J].Free Radic Biol Med,2001,31:1287-1312.
[3]LIU Hong-Tao,LI Wen-Ming,XU Gang,et al.Chitosan oligosaccharides attenuate hydrogen peroxide-induced stress injury in human umbilical vein endothelial cells[J].Pharm Res,2009,59:167-175.
[4]姚倩,孙涛,徐轶霞,等.壳聚糖/壳寡糖衍生物的制备及其抗氧化性能研究[J].食品与生物技术学报,2009,28(2): 188-191.
YAO Qian,SUN Tao,XU Yi-xia,LIU Yan-yang.Preparation of chitosan/chitosan oligosaccharide derivatives and their antioxidant activities[J].Journal of Food Science and Biotechnology,2009,28(2):188-19.(in Chinese)
[5]银旭红,孙涛,姚倩,等.低聚壳聚糖Zn(Ⅱ)配合物清除DPPH活性的研究[J].食品与生物技术学报,2009,28(3): 329-331.
YIN Xu-hong,SUN Tao,YAO Qian,et al.DPPH scavenging activity of chitosan oligosaccharide zinc complexes[J]. Journal of Food Science and Biotechnology,2009,28(3):329-331.(in Chinese)
[6]孟晓荣,张敏,赵亚娟等.壳聚糖及其水溶性衍生物的制备与结构表征[J].陕西师范大学学报,2007,35:62-65.
MENG Xiao-rong,ZHANG Min,ZHAO Ya-juan,et al.Preparation and performance of chitosan and its water-souble derivatives[J].Journal of Shaanxi Normal University,2007,35:62-65.(in Chinese)
[7]易喻,杨好,应国清,等.N–邻苯二甲酰化壳聚糖的合成与性能[J].化工进展,2006,25:542-545.
YI Yu,YANG Hao,YING Guo-qing,et al.Synthesis and properties of N-phthaloyl-chitosan[J].Chemical Industry and Engineering Progress,2006,25:542-545.(in Chinese)
[8]Vale′ry A,Romuald C,Dragoslav M,et al.Reactive oxygen species and superoxide dismutases:Role in joint diseases [J].Joint Bone Spin,2007,74:324-329.
[9]王周玉,蒋珍菊,李富生,等.水溶性N-酰化壳聚糖的合成与表征[J].四川工业学院学报,2004,23:73-75.
WANG Zhou-yu,J IANG Zhen-ju,LI Fu-sheng,et al.Synthesis and Characterization of Water-soluble N-acyl Chitosan [J].Journal of Sichuan University of Science and Technology,2004,23:73-75.(in Chinese)
[10]霍秀颖,张小华,吴清.电导滴定测定N-琥珀酰壳聚糖取代度[J].北京医药大学学报.2007,30:700-702.
HUO Xiu-ying,ZHANG Xiao-hua,WU Qing.Determination of substitution degree of N-succinyl-chitosan by conductometric titration[J].Journal of Beijing University of Traditional Chinese Medicine,2007,30:700-702.(in Chinese)
[11]Sun Tao,Xie Weng-ming,Xu PX.Superoxide anion scavenging activity of graft chitosan derivatives[J].Carbohydr Polym,2004,58(4):379-382.
[12]陆占国,郭红转,封丹.芫荽茎叶精油成分及清除DPPH自由基能力研究[J].食品与发酵工业,2006,32:24-27.
LU Zhang-guo,GUO Hong-zhuan,FENG Dan.Study on chemical constituent of coriander leaf essential oil and scavenging capacity against the DPPH radical[J].Food and Fermentation Industries,2006,32:24-27.(in Chinese)
[13]王周玉,蒋珍菊,胡星琪.水溶性N-马来酰化壳聚糖的合成[J].应用化学,2002,19:1002-1004.
WANG Zhou-yu,J IANG Zhen-ju,HU Xing-qi.Synthesis of Water-soluble N-Maleoyl chitosan[J].Chinese Journal of Applied Chemistry,2002,19:1002-1004.(in Chinese)
[14]Hirano S,Ohe Y,Ono H.Selective N-acylation of chitosan[J].Carbohydr Res,1976,47:315-320.
[15]I.-Chuan Sheih,Tung-Kung Wu,Tony J.Fang Antioxidant properties of a new antioxidative peptide from algae protein waste hydrolysate in different oxidation systems[J].Biores Technol,2009,100(13):3419-3425.
[16]Xie W M,Xu P X,Liu Q.Antioxidant activity of water-soluble chitosan derivatives[J].Bioorg Med Chem Lett,2001, 11:1699-1701.
(责任编辑:朱明)
The Radical Scavenging Effect of N-Acyl Chitosan Oligosaccharide
SUN Tao, YIN Xu-hong, XIE Jing, LI Li, LAI Ke-qiang, ZHOU Dong-xiang
(College of Food Science,Shanghai Ocean University,Shanhai 201306,China)
N-maleyl chitosan oligosaccharide(NMCOS)and N-phthaloyl chitosan oligosaccharide (NPCOS)with the same substituting degrees(0.25)were synthesized.The structure were characterized byFTIRspectra,themolecularweightwasmeasuredbyGelPermeation Chromatog-raphy(GPC).Their antioxidant activity were evaluated by the scavenging of hydroxyl radical(.OH)and 1,1-Diphenyl-2-picrylhydrazyl radical(DPPH).The results showed NPCOS have stronger hydroxyl and DPPH radical scavenging activity than that of NMCOS.The resultspresentedheredemonstratedthattheantioxidantactivityofN-acylChitosan Oligosaccharide with the same substituting degrees was determined by the substituting groups.
chitosan oligosaccharide,N-acyl,antioxidant activity,substituting degree
TS 202.3
:A
1673-1689(2010)03-0406-04
2009-06-15
上海市教育委员会科研项目(07zz134),上海市重点学科建设项目专项基金(T1102),上海市生物医药和农业科技领域重点科技项目(08391911500),2009年上海市优秀学科带头人计划(09XD1402000)。
孙涛(1970-),女,黑龙江依兰人,理学博士,副教授,主要从事多糖的改性及生物功能的开发。Email:taosun@shou.edu.cn
