高效液相色谱-二极管阵列-离子阱质谱法对红花水提物中有效成分群的定性分析*
2010-07-29王晓雯张亚军赵新锋
王晓雯 ,彭 宁 ,张 鹏 ,左 燕 ,张亚军 ,赵新锋
(1.陕西省人民医院药剂科,陕西 西安 710068; 2.西北大学生命科学学院,陕西 西安 710069)
红花为菊科一年生草本植物红花 Carthamus tinctorius L.的干燥花,具有活血通经、散瘀止痛的功效[1]。药理研究表明,黄酮类和色素类成分为红花扩张血管、增加冠脉流量和改善心脑血液循环的主要有效成分[2]。赵明波等[3]以羟基红花黄色素A为基准物,对不同产地的红花药材进行了指纹图谱分析。但除了基准物,上述研究未能对色谱峰进行归属,其原因在于缺少红花药材有效成分群的定性分析方法。笔者采用高效液相色谱-二极管阵列-离子阱质谱(HPLC-DAD-MSn)法对红花水提物中的黄酮类成分进行了定性分析,旨在为红花指纹图谱研究中色谱峰的归属提供参考,现报道如下。
1 仪器与试药
Agilent 1100系列高效液相色谱仪(美国安捷伦公司),包括在线真空脱气机、二元梯度泵、柱温箱、二极管阵列检测器;SL型离子阱质谱(美国安捷伦公司);Maxima超纯水机(美国基因公司);Sartorius BP221S型万分之一电子天平(美国Sartorius公司)。红花药材(新疆产,经陕西省食品药品检验所鉴定);槲皮素化学对照品(中国药品生物制品检定所,批号为100081-200406);羟基红花黄色素A化学对照品(中国药品生物制品检定所,批号为11637-200503);色谱纯乙腈(Fisher公司,美国),超纯蒸馏水(自制),其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件
色谱柱:Agilent SB-C18柱(150 mm ×2.1 mm,5 μm);流速:0.2 mL/min;柱温:30℃;检测波长:0~10.0 min为280 nm,10.0~25.0 min为 370 nm,25.0~45.0 min为 430 nm;流动相:A为0.2%的甲酸水溶液,B为甲醇,梯度洗脱,0~20.0 min为30%B,20.0~30.0 min为 30%B→65%B,30.0~45.0 min为 65%B。在此条件下,红花水提物的高效液相色谱图见图1。
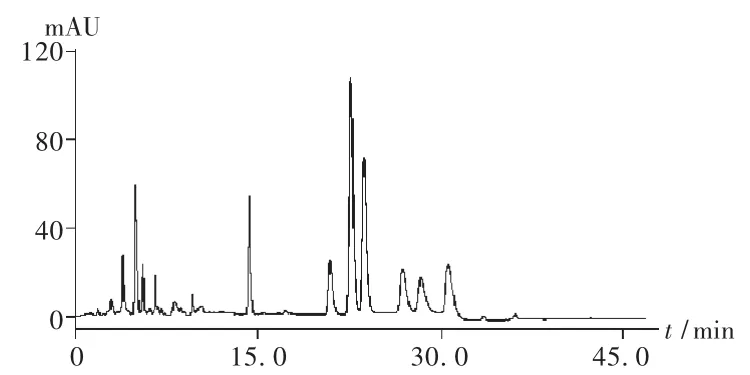
图1 红花水提物高效液相色谱图
2.2 质谱条件
电喷雾负离子模式(ESI-)电离,雾化气压强为275 kPa,干燥气流速为7.0 mL/min,干燥气温度为325℃,毛细管电压为-4200 V,扫描范围为50~1500 amu。在此条件下,红花水提物的ESI-MS总离子流图见图2。
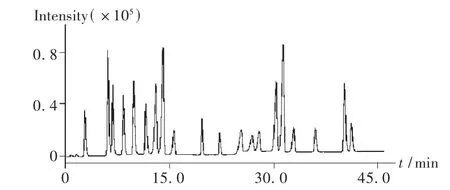
图2 红花水提物总离子流图
2.3 溶液制备
分别精密称取槲皮素和羟基红花黄色素A对照品0.012 g和0.016 g,以30.0%的甲醇水溶液溶解,分别置2个25.0 mL具塞量瓶中,加甲醇至刻度,制备成质量浓度分别为0.48 g/L和0.64 g/L的对照品溶液,4℃冷藏备用。取干燥至恒重的红花药材10.0 g,置250 mL圆底烧瓶中,加10倍量水,加热回流1.5 h,重复3次,抽滤,合并滤液,减压浓缩至膏状物,真空干燥,研磨成粉,以30.0%的甲醇水溶液定容于500.0 mL具塞量瓶中,即红花药材供试品溶液。4℃冷藏备用。
2.4 方法学考察
线性关系考察:分别精密吸取2.3项下槲皮素和羟基红花黄色素A对照品溶液适量,用30.0%的甲醇水溶液稀释为系列对照品溶液。在拟订的分析条件下,分别进样10.0 μL,对离子阱质谱的多级反应模式(MRM)进行分析。槲皮素选择 m/z 301.1→m/z 283.0为离子对,羟基红花黄色素A选择 m/z 611.2→m/z 449.1为离子对,测定提取离子流图的峰面积。分别以槲皮素和羟基红花黄色素A提取离子流图的峰面积对其质量浓度进行线性回归,得回归方程分别为 Y=12.4 X+1.2(r=0.9998)和 Y=5.1 X+0.4(r=0.9997),质量浓度线性范围分别为0.48~48.0 μg/mL和0.64~320 μg/mL。
精密度试验:按2.3项下供试品溶液制备方法制备供试品溶液,用30%甲醇水溶液稀释10倍后,连续进样5次,每次10.0 μL,在拟订的分析条件下,分别测定槲皮素和羟基红花黄色素A的提取离子流图的峰面积,计算得其标准偏差 RSD分别为1.2%和0.87%。
稳定性试验:按2.3项下供试品溶液制备方法制备供试品溶液,以30%甲醇水溶液稀释10倍后,每2 h进样1次,每次10.0 μL,在拟订的分析条件下测定峰面积。结果48 h内槲皮素和羟基红花黄色素A峰面积的 RSD分别为1.3%和1.0%,表明供试品溶液在48 h内具有良好的稳定性。
重复性试验:按2.3项下供试品溶液制备方法制备5份供试品溶液,以30%甲醇水溶液稀释10倍后,分别进样,每份每次10.0 μL,在拟订的分析条件下测定峰面积。结果槲皮素和羟基红花黄色素A峰面积的 RSD分别为1.1%和1.2%。
回收率试验:取适量已知槲皮素和羟基红花黄色素A含量的红花药材5份,精密加入2.3项下槲皮素和羟基红花黄色素A对照品溶液适量后,按2.3项下方法制备成供试品溶液。以30%甲醇水溶液稀释10倍后,在拟订的分析条件下分别进样10.0 μL,测定峰面积,计算回收率。结果槲皮素和羟基红花黄色素A的平均回收率分别为98.7%和99.2%。
2.5 样品含量测定
按2.3项下供试品溶液制备方法制备红花供试品溶液5份,以30%甲醇水溶液稀释10倍后,在拟订的分析条件下进样,外标法计算含量。结果红花药材中槲皮素和羟基红花黄色素A的平均含量分别为0.13%和1.14%。
2.6 有效成分群定性分析
取2.3项下制备的供试品溶液,以30%甲醇水溶液稀释10倍后,在拟订的分析条件下进样10.0 μL。通过二极管阵列全扫描技术,按拟订的色谱条件设定单通道多波长,获得药材供试品溶液的紫外色谱图。比较紫外色谱图和全扫描总离子流图,二者基本对应。然而,紫外色谱图中有个别吸收很大的峰,在相应的总离子流图中强度却较弱,提示这些化合物在拟订的质谱条件下很难被离子化;此外,总离子流图上有许多强度较大的峰,在相应的紫外色谱图上却没有明显的吸收,推测红花药材中含有大量的紫外吸收弱、易离子化的化合物。在获得药材供试品溶液全扫描总离子流图的基础上,利用离子阱质谱的步进式碰撞技术,通过改变电场梯度和能量梯度,获得总离子流图中各峰的多级碎片信息,通过对照并结合相关文献[4-5]对各峰进行归属(见表1),定性分析了19种化学成分,其中1种为未知化学成分。
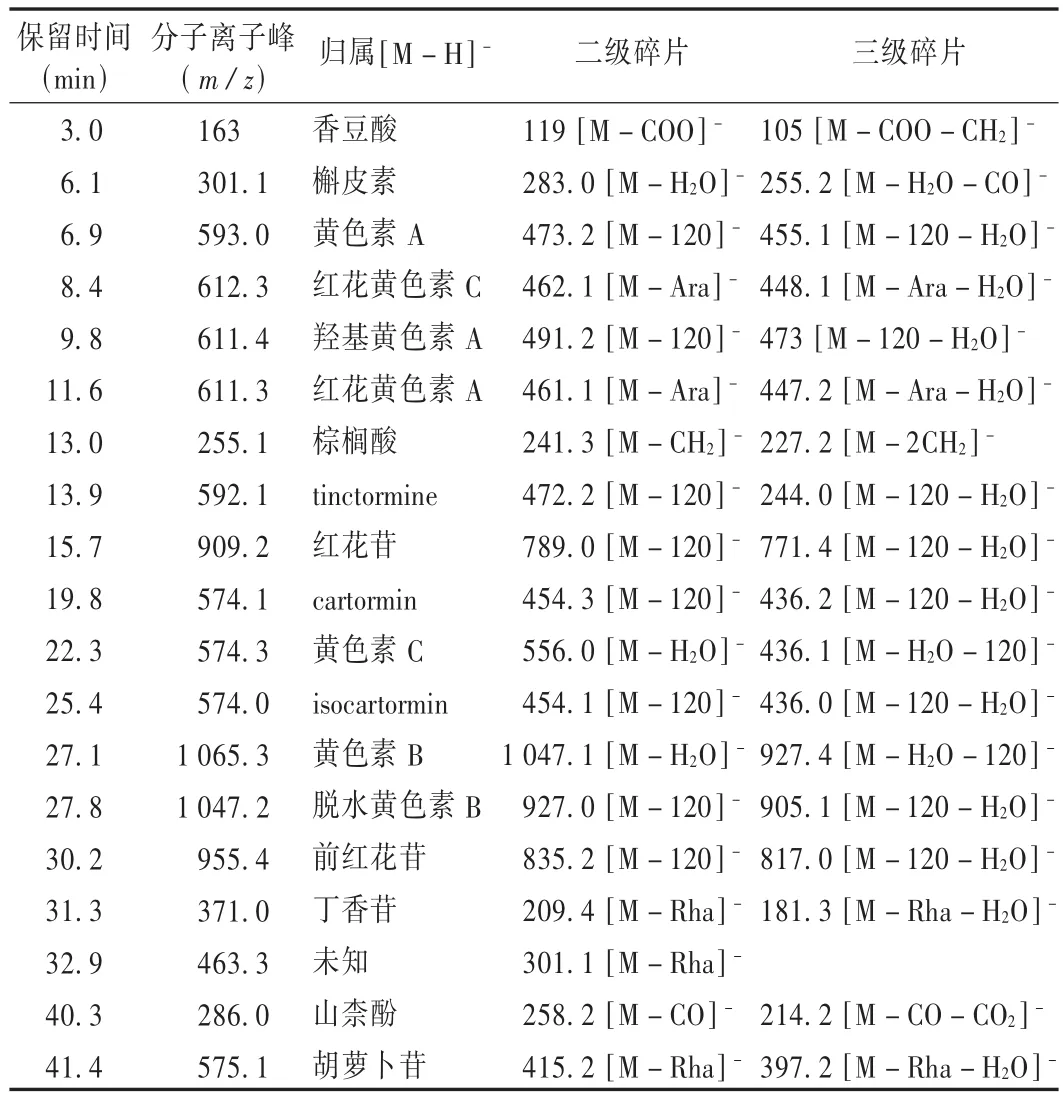
表1 红花水提物电喷雾质谱解析表
3 讨论
总结红花中查耳酮类化合物在负离子模式下的裂解特征,发现该类化合物的结构中糖与苷元以C—苷键形式连接,通常情况下C—苷键较难发生断裂。因此,在负离子模式下,[M-H]-离子主要发生3'位或4'位取代基上的消除反应,以延长苷元结构中的共轭体系,如常可见丢失中性片断(相对分子质量为120)后所得基峰碎片离子。而对于多数糖苷类(包括黄酮苷类)化合物,在负离子模式下,主要发生糖苷键断裂,产生丢失糖片断后所得的碎片离子。该特性可用于区分醌型查耳酮类化合物与黄酮类化合物。
通过HPLC-ESI-MSn分析,对红花水提物中19种化学成分进行质谱解析,在确定18种化学成分的基础上,初步发现了1种未知的化学成分,对这种化学成分结构的定性还需进一步的研究。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:化学工业出版社,2005:103-104.
[2]康 丽,颜晓燕,辛志伟.红花的药理作用研究进展[J].西南军医,2008,10(6):136-138.
[3]赵明波,邓秀兰,王亚玲,等.红花RP-HPLC指纹图谱的建立及其质量研究[J]. 药学学报,2004,39(3):212-216.
[4]姜建双,夏鹏飞,冯子明,等.红花化学成分研究[J].中国中药杂志,2008,33(24):2911-2913.
[5]周玉枝,陈 欢,乔 莉,等.红花化学成分研究[J].中国药物化学杂志,2007,17(6):380-382.
