表面活性剂存在下HEPES缓冲溶液中制备纳米金颗粒
2010-05-29曾琦斐
曾琦斐
(湖南环境生物职业技术学院,湖南 衡阳 421005)
0 引 言
纳米金颗粒以其良好的稳定性、小尺寸效应、表面效应、光学效应以及独特的生物亲和性,在许多领域显示出了潜在的应用价值,引起了广大科技工作者的浓厚兴趣[1-2].已有很多种制备纳米金的工艺方法[1],如溶胶凝胶法、气相蒸发法、水热法、溶剂还原法、相转移法、真空蒸镀法、微波合成法等.在这些合成方法中常使用柠檬酸钠、硼氢化钠或水合肼等还原性较强的还原剂制得纳米金颗粒[3-5],但较难控制其还原速率.另外,在纳米金颗粒的液相合成中,常使用不同类型的模板剂、表面活性剂或巯基烷烃化合物保护剂[5-7],控制纳米金颗粒的形貌和大小;但还原性较强的还原剂和有机试剂的使用,尤其是高分子有机物模板剂,往往会对环境造成不同程度的污染,也对生物方面的应用有所限制.
HEPES是一种氢离子缓冲剂,能较长时间控制恒定的pH范围,并且对细胞无毒性作用.最近,Xie和Sun等报道了在HEPES(N-(2-羟乙基)哌嗪-N'-2-乙烷磺酸)缓冲溶液里分别合成了Au,Ag纳米颗粒[8-9].在生物缓冲体系里制备纳米金颗粒对纳米材料在生物方面的应用将起到较大的推动作用.本实验发现,使用该方法不仅能够在常温下可以得到纳米金颗粒.在不同表面活性剂存在下,纳米金颗粒形貌大小有一定的差别,使用PVP能得到粒径分布较窄的单分散球形金纳米颗粒,工艺简便,成本低廉.
1 实验方案
1.1 仪器与试剂
四水合氯金酸(HAuCl4·4H2O),聚乙烯吡咯烷酮(PVP,分子量为10 000),聚乙二醇(PEG,分子量为4 600),N-(2-羟乙基)哌嗪-N'-2-乙烷磺酸(HEPES) 均由美国Aldrich公司提供.使用前没有采取进一步处理.
分别采用X-射线衍射仪(XRD)、透射电子显微镜(TEM)、X射线能谱仪(EDS)和电子衍射(ED)等对产物的组成、形貌尺寸和晶系等进行了表征分析.XRD使用荷兰Philips PW1830型X-射线衍射仪,测试条件:Cu靶Kα线(λ=0.154 06 nm),扫描范围30~80 °,扫描速度1 °/min.TEM使用Philips Tecnai 20型透射电子显微镜(TEM),荷兰Philips生产,工作电压200 kV.EDS使用Philips Tecnai 20 上的 Oxford incax-sight EDX 附件设备,工作电压200 kV.紫外-可见光吸收使用双光束Varian cary-50型紫外-可见分光光度计测量.溶液pH值使用Aldrich 生产的Corning 440 pH meter型pH计测量.
1.2 50 mmol/L HEPES(pH 7.4)缓冲溶液的配制
HEPES (2.38 g,10 mmol) 首先溶于180 mL 去离子水中,超声、振荡直到完全溶解,使用pH计测得溶液的pH值约为5.4,慢慢滴加0.1 mol/L NaOH溶液,搅拌,直到pH调整为7.4,然后用去离子水定容至200 mL.
1.3 纳米金颗粒的制备
样品a:1 mL 10 mmol/L HAuCl4溶液滴入9 mL上述配制的HEPES缓冲溶液中,搅拌几分钟后,溶液颜色变为红色,即可得到纳米金溶胶.
样品b:1 mL HAuCl4(10 mmol/L)溶液滴入含有0.1 g PVP的9 mL HEPES(50 mmol/L) 缓冲溶液中,搅拌几分钟后,溶液颜色变为红色,即可得到纳米金溶胶.
样品c:1 mL HAuCl4(10 mmol/L)溶液滴入含有0.1 g PEG的9 mL HEPES(50 mmol/L) 缓冲溶液中,搅拌几分钟后,即可得到纳米金溶胶.
2 结果与讨论
2.1 XRD分析
图1是在HEPES缓冲溶液中制得的纳米金颗粒的XRD图.图中所有的衍射峰均可与标准图谱JCPDF No.04-0784相吻合,可以看出,2θ在38.2 °,44.4 °,64.5 °,77.5 °处,出现的4个衍射峰均为金的特征衍射峰,分别与面心立方(face-center-cubic,FCC)结构Au(111)、(200)、(220)和(311)晶面相对应,没有其他杂峰出现,说明在常温下就可得到纯度高,结晶性好的纳米金颗粒.
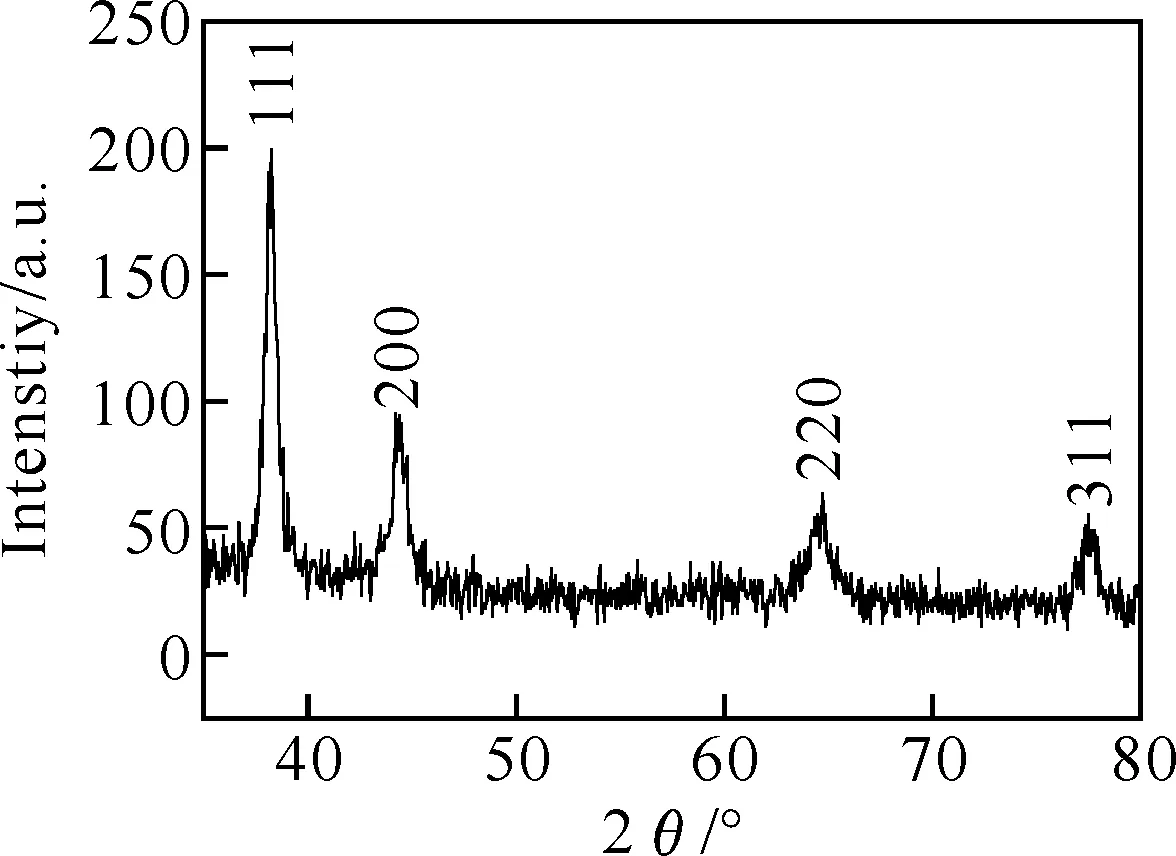
图1 常温下在HEPES缓冲溶液里制得的纳米金颗粒的XRD谱(样品a)
2.2 紫外-可见光光谱分析
紫外-可见光谱对高分散和缔合态存在的金属颗粒有完全不同的响应,通过分析其谱图,可以得到有关颗粒粒度和结构等重要信息[10].通过记录不同时间的紫外吸收光谱可观测纳米金颗粒在HEPES缓冲溶液中的反应动力学.不同反应时间段生成的金颗粒紫外-可见光吸收如图2所示,在5 min可观察到纳米金溶胶的紫外-可见吸收峰,随着反应时间延长最大吸收强度逐渐增大,一直到1 h后,最强吸收波长基本不变.但金溶胶的最大紫外吸收峰位置基本不发生变化,说明颗粒大小随时间变化很小.
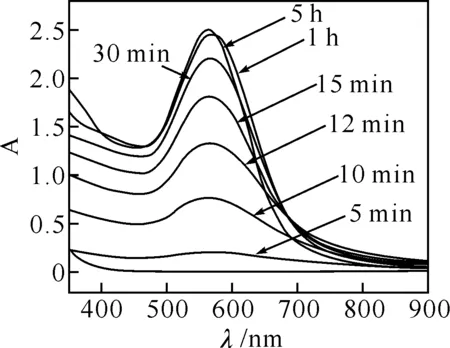
图2 不同反应时间下所得纳米金溶胶的紫外-可见吸收光谱(样品a)
2.3 TEM、HRTEM和ED分析
图3a是在HEPES缓冲溶液中制得的纳米金颗粒的TEM照片,从图中可知,在反应溶液中,不加入PVP时,可以得到分散性较好的球形与准球形金颗粒,平均粒径为25 nm左右.图4a插图是该区域的电子衍射图,它是由几个衍射环组成的,表面这片区域是多晶结构图,它是由很多不同的单晶纳米金颗粒的电子衍射组成的.图3b是单个纳米金颗粒的HRTEM照片,由相邻条纹间距算出平均相邻晶面间距为0.236 nm,与面心立方结构Au的(111)晶面相对应. 由图3c的EDS测试结果可知,样品中只含有元素Au,C和Cu的信号来自做TEM测试使用的铜网.实验结果表明,金溶胶的制备过程中,HEPES缓冲溶液不仅可以还原HAuCl4得到纯度很高的纳米金颗粒,而且能有效防止颗粒间团聚现象的发生.
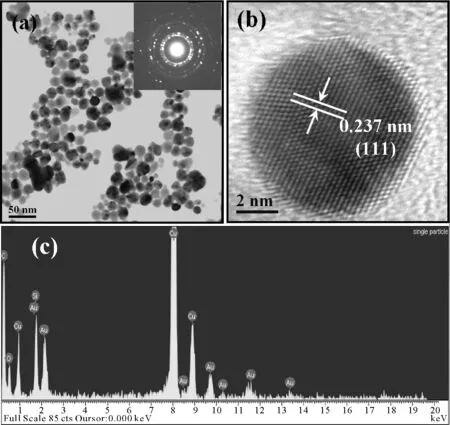
图3 在HEPES缓冲溶液中制得的金纳米颗粒的表征数据
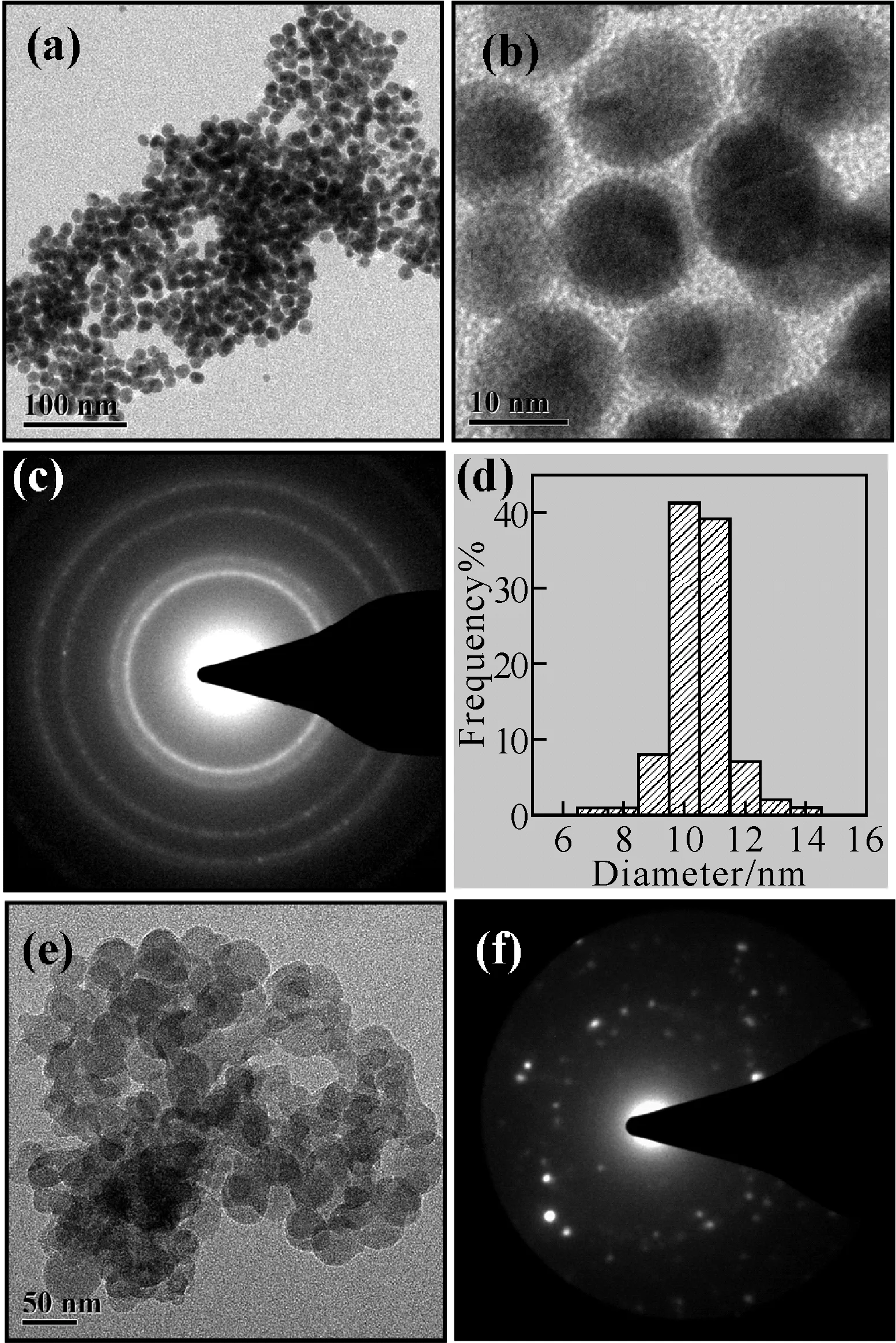
图4 在不同表面活性剂存在条件下得到的金纳米颗粒
当HEPES缓冲溶液里含有PVP时,可以得到大小均一、分散性好的球形纳米金颗粒(见图4a),颗粒直径主要分布在10 nm左右(见图4a图),从图4b可以更清晰的看到球形纳米金颗粒,在插图中可以清楚地看到衍射环.实验数据说明,PVP对颗粒的大小有很重要的影响.PVP是一种表面结晶抑制剂[14],由于金是疏水性的,当被PVP的疏水链包裹,极性的含氧和氮原子的五元环朝向溶液,PVP使金颗粒很好的悬浮在溶液中,避免了金颗粒间的接触,所以在PVP存在的条件下,得到的纳米金颗粒粒径较小[15].当使用PEG替代PVP,得到了分散性差的纳米金颗粒(图4e).这可能是由于PEG的加入量超过饱和吸附浓度,悬浮体系中多余的高分子链相互缠绕在一起从而使颗粒团聚[16].
3 结 语
在常温条件下,在HEPES缓冲溶液反应体系中,在没有加入任何表面活性剂,成功制备了单分散球形纳米金溶胶颗粒,平均粒径为25 nm左右.这是由于HEPES内含有哌嗪环可以产生N自由基,能通过吸附作用能够有效阻止金晶核长大以及颗粒间团聚现象的发生.因此,HEPES不仅可以作为还原剂,还可以作为表面活性剂以稳定纳米金颗粒.在PVP存在的条件下,可以得到大小均一,粒径分布范围窄(约10 nm),且稳定性好的纳米金颗粒.而在PEG存在的条件下得到了团聚的纳米金颗粒.
参考文献:
[1]Daniel M C,Astruc D.Gold Nanoparticles:Assembly,Supramolecular chemistry,quantum-size-related properties,and applications toward biology,catalysis,and nanotechnology[J].Chem Rev,2004,104:293-346.
[2]Ghosh S K,Pal T.Interparticle coupling effect on the surface plasmon resonance of gold nanoparticles:from theory to applications[J].Chem Rev,2007,107:4797-4862.
[3]Chen H M,Liu R S,Tsai D P.A versatile route to the controlled synthesis of gold nanostructures[J].Cryst Growth Des,2009,9(5):2079-2087.
[4]Mandal D,Maran A,Yaszemski M J,et al.Cellular uptake of gold nanoparticles directly cross-linked with carrier peptides by osteosarcoma cells[J].J Mater Sci:Mater Med,2009,20:347-350.
[5]Mandal S,Arumugam S K,Adyanthaya S D,et al.Use of aqueous foams for the synthesis of gold nanoparticles of variable morphology[J].J Mater Chem,2004,14:43-47.
[6]Sun Y,Xia Y.Shape-controlled synthesis of gold and silver nanoparticles[J].Science,2002,298:2176-2179.
[7]Agasti S S,You C C,Arumugam P,et al.Structural control of the monolayer stability of water-soluble gold nanoparticles[J].J Mater Chem,2008,18:70-73.
[8]Xie J,Lee J Y,Wang D I C.Seedless,surfactantless,high-yield synthesis of branched gold nanocrystals in HEPES buffer solution[J].Chem Mater,2007,19:2823-2830.
[9]Sun R W Y,Chen R,Chung N P Y,et al.Silver nanoparticles fabricated in Hepes buffer exhibit cytoprotective activities toward HIV-1 infected cells[J].Chem Commun,2005:5059-5061.
[10]Sau T K,Pal A,Pal T.Size regime dependent catalysis by gold nanoparticles for the reduction of eosin[J].J Phys Chem B,2001,105(38):9266-9272.
[11]Grady J K, Chasteen N D,Harris D C.Radicals from “Good’s” buffers[J].Anal Biochem,1988,173:111-115.
[12]Danen W C, Rickard R C.Nitrogen-centered free radicals, IV. Electron spin resonance study of transient dialkylaminium radical cations[J].J Am Chem Soc, 2002,94:3254-3256.
[13]谢娟,王延吉,李艳廷,等.粒径可控纳米金的制备及表征[J].黄金,2008,29:3-6.
[14]Zhang Z T,Zhao B,Hu L M.PVP protective mechanism of ultrafine silver powder synthesized by chemical reduction processes[J].J Solid State Chem,1996,121:105-110.
[15]兰新哲,金志浩,赵西成,等.PVP保护还原法制备纳米金溶胶[J].稀有金属材料与工程,2003,32:50-53.
[16]刘付胜聪,肖汉宁,李玉平,等.纳米TiO2表面吸附聚乙二醇及其分散稳定性的研究[J].无机材料学报,2005,20:310-316.
