岩陀黄酮与黄芩多糖复合物安全性评价
2022-12-20王余磊宋春莲卜仕金舒相华
■潘 琼 王余磊 宋春莲 卜仕金 舒相华*
(1.云南农业大学动物医学院,云南 昆明 650201;2.扬州大学兽医学院,江苏 扬州 225009)
中兽药是中国传统兽医学的重要组成部分,历史悠久[1]。在“限抗”与病毒性疫病肆虐的双重压力下,中兽药作为新兴产业受到越来越多的重视,主要是因为中药具有多方位调节和治疗作用,可提高动物机体的免疫力和抗应激能力,中长期使用仅有低毒副作用,药物残留少,能促进生产性能发挥的同时满足日益严格的食品安全需求[2]。
岩陀为虎耳草科鬼灯檠属植物羽叶鬼灯檠(Rodgersia pinnata franch.)或西南鬼灯檠(Rodgersia sumbucifolia hemsl.)的干燥根茎[3],用于治疗骨折、风湿痛、消化不良等疾病[4]。黄酮类化合物具有抗炎、抗菌、抗病毒、降血糖、降血脂、抗肿瘤、抗氧化等多种生物活性[5]。已有研究表明岩陀黄酮对大鼠的免疫功能有促进作用[6]。黄芩(Scutellaria baicalensisGeorgi)为唇形科植物黄芩的干燥根,黄芩多糖是黄芩黄酮提取过程中的副产物,比较容易获得,具有抗肿瘤、调节血糖和血脂、抗氧化性、抑菌抗炎和调节免疫等作用[7]。本试验通过急性经口毒性试验、遗传毒性试验对岩陀黄酮和黄芩多糖复合物的毒性进行了初步研究,为岩陀黄酮和黄芩多糖联用在中兽医药领域的应用提供科学依据。
1 材料和方法
1.1 材料
1.1.1 试验动物
清洁级健康Wistar 大鼠,体重180~200 g;ICR 小鼠雄性,体重18~20 g,均由扬州大学比较医学中心提供,试验动物生产许可证号:SCXK(苏)2017-0007,试验动物使用许可证号:SYXK(苏)2017-0044。试验期间大、小鼠自由采食和饮水。试验前适应性饲养7 d,灌胃前12 h禁食不禁水。
1.1.2 受试药物
岩陀黄酮与黄芩多糖复合物:岩陀粗黄酮含量为41.1%;黄芩粗多糖含量为40.3%,两者按1∶1混合制成淡黄色粉末复合物,由云南农业大学中兽医实验室提供,4 ℃保存。
1.1.3 试验菌株
细菌回复突变试验(Ames text)选用组氨酸营养缺陷型鼠伤寒沙门菌TA97、TA98、TA100 和TA102,由MOLTOX 公司提供。菌株储存于-80 ℃。试验菌于37 ℃水浴振荡培养24 h,4 ℃保存。菌株均经过生物学鉴定合格后进行试验。
1.1.4 试验试剂
标准诱变剂:叠氮化钠、2-乙酰氨基芴、敌克松、甲基磺酸甲酯均为分析纯;环磷酰胺(20110703),山西普德药业有限公司生产,国药准字H14023686;多氯联苯(20150404),山西普德药业有限公司生产,国药准字H14023686。
其他试剂:营养肉汤培养基、营养肉汤琼脂培养基、1%羧甲基纤维素钠、二甲基亚砜、1%伊红染色液、氯化钾、甲醇(分析纯)、PBS缓冲溶液等。
1.1.5 试验仪器
D98-9052B-2 隔水式电热恒温培养箱、Centrifuge 5415R 高速冷冻离心机、电热恒温水浴箱、菌落计数器、万分之一电子天平、CX2型OLYMPUS显微镜及灌胃针头等。
1.2 方法
1.2.1 大鼠经口急性毒性试验
试验分组:2 个试验组,分别选择Wistar 大鼠雌、雄各10 只,雌雄分笼饲养。大鼠禁食12 h 后分别称体重、编号。
染毒和观察:在4 h内经口灌服岩陀黄酮与黄芩多糖复合物溶液数次进行染毒,染毒剂量达到9 g∕kg·BW。攻毒后分别在30 min、2 h、4 h进行观察,之后每天观察1 次,连续14 d。主要观察大鼠采食饮水情况、有无中毒症状及毒性反应出现和消失的时间、中毒表现和死亡时间。14 d结束后处死存活大鼠,进行病理变化检查。
1.2.2 鼠伤寒沙门氏菌回复突变试验
增菌培养及生物学特性鉴定:将冷冻保存的TA97、TA98、TA100 和TA102 菌株培养物接种于营养肉汤培养基,37 ℃,100 r∕min 培养10 h。细菌浓度大于2×109CFU∕mL。试验前采用鼠伤寒沙门氏菌回复突变试验标准判断法[8]进行菌株的生物学特性和自发回变菌落数的检测,符合标准进行后续试验。
大鼠肝微粒体酶的诱导和S9 的制备:150~200 g Wistar 大鼠3 只,采用多氯联苯作为诱导剂,按500 mg∕kg·BW剂量腹腔注射后第5天脱颈处死,处死前12 h 禁食。无菌操作取出肝脏,除去结缔组织,预冷无菌0.15 mol∕L 氯化钾溶液润洗肝脏后,每克肝脏加入0.15 mol∕L 氯化钾溶液3 mL。冰浴匀浆后4 ℃,9 000 g 离心10 min,取上清液分装,-80 ℃保存备用,即为S9。
阳性对照设定:(+S9 组别)TA97、TA98、TA100、TA102菌株阳性对照均为2-乙酰氨基芴(2-AF);(-S9组)TA97、TA98 菌株为5 mg∕mL 敌克松,TA100 菌株为叠氮钠,TA102菌株为甲基磺酸甲酯。
受试药物的配制:采用平板掺入法。准确称取受试药物1.000 g,高压灭菌后加无菌二甲基亚砜(DMSO)配制为浓度100 mg∕mL 的母液,取适量分别稀释为10.000、2.000、0.400、0.080、0.016 mg∕皿。
试验步骤:取2 mL 45 ℃水浴保温的顶层培养基,依次加入受试药物溶液0.1 mL,测试菌液0.1 mL(+S9 组同时加入10% S9 混合液0.5 mL),迅速混匀,倒在底层培养基上,轻柔晃动使顶层培养基均匀分布,37 ℃培养48 h,观察结果,每组8个重复。若第一次平板掺入法结果为阴性,重复一次试验;若第一次平板掺入法结果为阳性,重复两次试验。
1.2.3 小鼠精子畸形试验
动物分组及染毒:将50 只雄性小鼠随机均分为高(2 500 mg∕kg·BW)、中(1 250 mg∕kg·BW)、低(625 mg∕kg·BW)复合物剂量组、阳性对照组(环磷酰胺40 mg∕kg·BW)和阴性对照组(纯化水),5 个处理组。使用1%羧甲基纤维素钠对复合物和环磷酰胺进行梯度稀释,按相同体积不同剂量进行灌胃,阴性对照给予相同体积纯化水。连续染毒5 d,第35天取材[9]。
染毒后取材:脱颈法处死小鼠,取出两侧副睾,在无菌PBS中用眼科剪将副睾纵向剪2刀,静止3 min,轻轻摇动,用4层擦镜纸过滤去除组织碎片,吸滤液至载玻片涂片,自然风干后用甲醇固定10 min,待干燥后用1%伊红染色1 h,以常水冲洗干净,自然风干后镜检[10]。
1.2.4 小鼠骨髓细胞微核试验
分组:50只小鼠随机分为5组,每组10只,雌雄各半,分笼饲养。复合药物组设高、中、低三个剂量组,即2 500 mg∕kg·BW、1 250 mg∕kg·BW、625mg∕kg·BW,阳性对照组(环磷酰胺)和阴性对照组(1%羧甲基纤维素钠)。
染毒[11]:1%羧甲基纤维素钠梯度稀释受试复合物,按不同浓度、相同体积灌胃,现用现配。阳性对照按0.01 mL∕g·BW 腹腔注射环磷酰胺,阴性对照按0.01 mL∕g·BW口服1%羧甲基纤维素钠。30 h内给药两次,每次给药间隔24 h,第36 h取胸骨骨髓进行制片。
观察:每只小鼠制2 张片,双盲法在油镜下选择细胞分散好、形态完整及染色良好的部位,进行计数。计数1 000个嗜多染红细胞(PCE)含微核嗜多染红细胞数(MN)及成熟红细胞(RBC)数,求出PCE∕RBC、MN∕PCE[12]。
1.3 数据统计
采用GraphPad Prism 8.0.1软件进行分析统计。
鼠伤寒沙门氏菌回复突变试验:菌株回变菌落数表述为“()∕皿”,受试物的回变菌落数是溶剂对照组的2 倍以上,且具有剂量反应关系的判为阳性,达不到2倍以上则判定为合格。
小鼠精子畸形试验精子畸形率按X2检验(α=0.05)作统计学处理,评价精子畸形阳性的标准为畸形率至少为阴性对照组的倍量或经统计有显著意义,并有剂量反应关系。
精子畸形率(%)=[畸形精子数∕(正常精子检测数+畸形精子数)×100
小鼠骨髓细胞微核试验:每一试验动物作为一个观察组,每一组动物雌雄合并计算该组微核数的均值,如一组动物内雌雄之间微核有明显的性别差异时,则分别计算。分析测试结果用“”表示,微核发生率按X2检验(α=0.05)作统计学处理。
2 结果与分析
2.1 大鼠经口急性毒性试验(见表1)
由表1可知,观察期内所有大鼠临床表现正常,无明显神经症状,皮肤和被毛无异常,且采食、饮水和排便等正常,未表现中毒反应,第15天所有大鼠均存活。试验结束后剖检20只大鼠,眼观病理学检查均未发现明显病理变化。结果表明,岩陀黄酮与黄芩多糖复合物对大鼠的经口染毒半致死量(LD50)大于5 g∕kg·BW,依据国标GB 15193.3—2014剂量分类表,属于实际无毒。

表1 大鼠急性毒性试验结果
2.2 鼠伤寒沙门氏菌回复突变试验[13](见表2)
由表2可知,两次鼠伤寒沙门氏菌回复突变试验结果基本一致。岩陀黄酮与黄芩多糖复合物每皿剂量在10~0.016 mg范围内,4种试验用鼠伤寒沙门氏菌株菌苔生长正常,各菌株反应均为合格;有或无代谢活化系统(S9)时,每皿平均回变菌落数与阳性诱变剂组比较差异显著,与对照(DMSO)比较无统计学意义,未见剂量反应关系,结果为合格。
表2 岩陀黄酮与黄芩多糖复合物的鼠伤寒沙门氏菌回复突变试验结果()
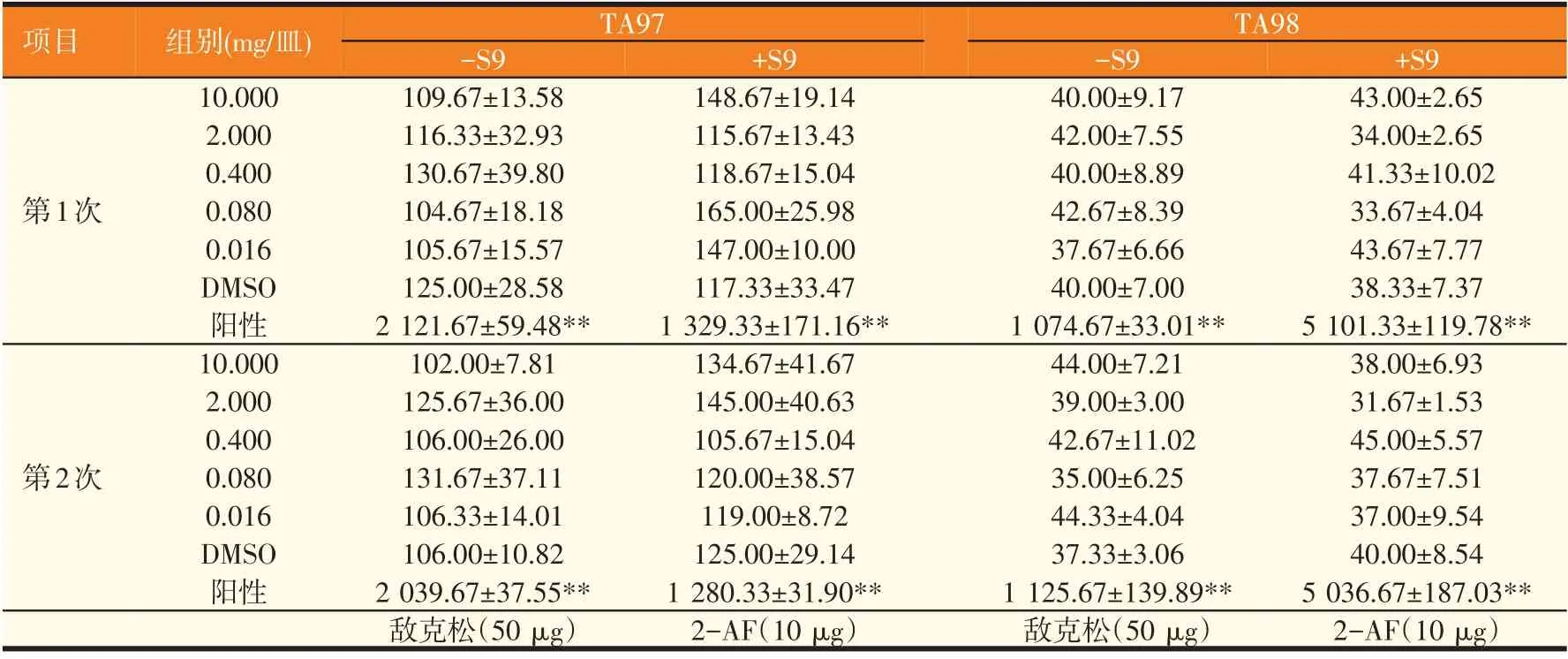
表2 岩陀黄酮与黄芩多糖复合物的鼠伤寒沙门氏菌回复突变试验结果()
项目第1次第2次组别(mg∕皿)10.000 2.000 0.400 0.080 0.016 DMSO阳性10.000 2.000 0.400 0.080 0.016 DMSO阳性TA97-S9 109.67±13.58 116.33±32.93 130.67±39.80 104.67±18.18 105.67±15.57 125.00±28.58 2 121.67±59.48**102.00±7.81 125.67±36.00 106.00±26.00 131.67±37.11 106.33±14.01 106.00±10.82 2 039.67±37.55**敌克松(50 μg)+S9 148.67±19.14 115.67±13.43 118.67±15.04 165.00±25.98 147.00±10.00 117.33±33.47 1 329.33±171.16**134.67±41.67 145.00±40.63 105.67±15.04 120.00±38.57 119.00±8.72 125.00±29.14 1 280.33±31.90**2-AF(10 μg)TA98-S9 40.00±9.17 42.00±7.55 40.00±8.89 42.67±8.39 37.67±6.66 40.00±7.00 1 074.67±33.01**44.00±7.21 39.00±3.00 42.67±11.02 35.00±6.25 44.33±4.04 37.33±3.06 1 125.67±139.89**敌克松(50 μg)+S9 43.00±2.65 34.00±2.65 41.33±10.02 33.67±4.04 43.67±7.77 38.33±7.37 5 101.33±119.78**38.00±6.93 31.67±1.53 45.00±5.57 37.67±7.51 37.00±9.54 40.00±8.54 5 036.67±187.03**2-AF(10 μg)
结果表明:受试药物对TA97、TA98、TA100 和TA102 四种试验用鼠伤寒沙门氏菌株在加S9 和不加S9试验中结果均为阴性,可见本试验条件下岩陀黄酮与黄芩多糖复合物对鼠伤寒沙门氏菌无致突变性。
2.3 小鼠精子畸形试验(见表3)
由表3 可知,岩陀黄酮与黄芩多糖复合物3 个剂量组的精子畸形率经统计学处理与阴性对照组比较差异不显著性(P>0.05),阳性对照组与3 个给药剂量组、阴性对照组比较差异均极显著(P<0.01)。岩陀黄酮与黄芩多糖复合物致小鼠精子畸形试验结果为阴性,可判断该复合物不具有生殖遗传毒性。
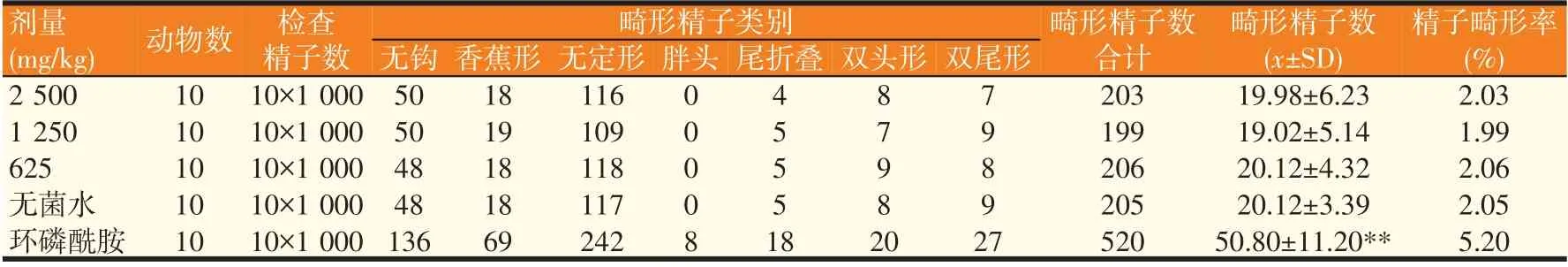
表3 岩陀黄酮与黄芩多糖复合物对小鼠精子畸形发生率影响(n=10)
2.4 小鼠骨髓细胞微核试验分析(见表4)
表2(续) 岩陀黄酮与黄芩多糖复合物的鼠伤寒沙门氏菌回复突变试验结果()
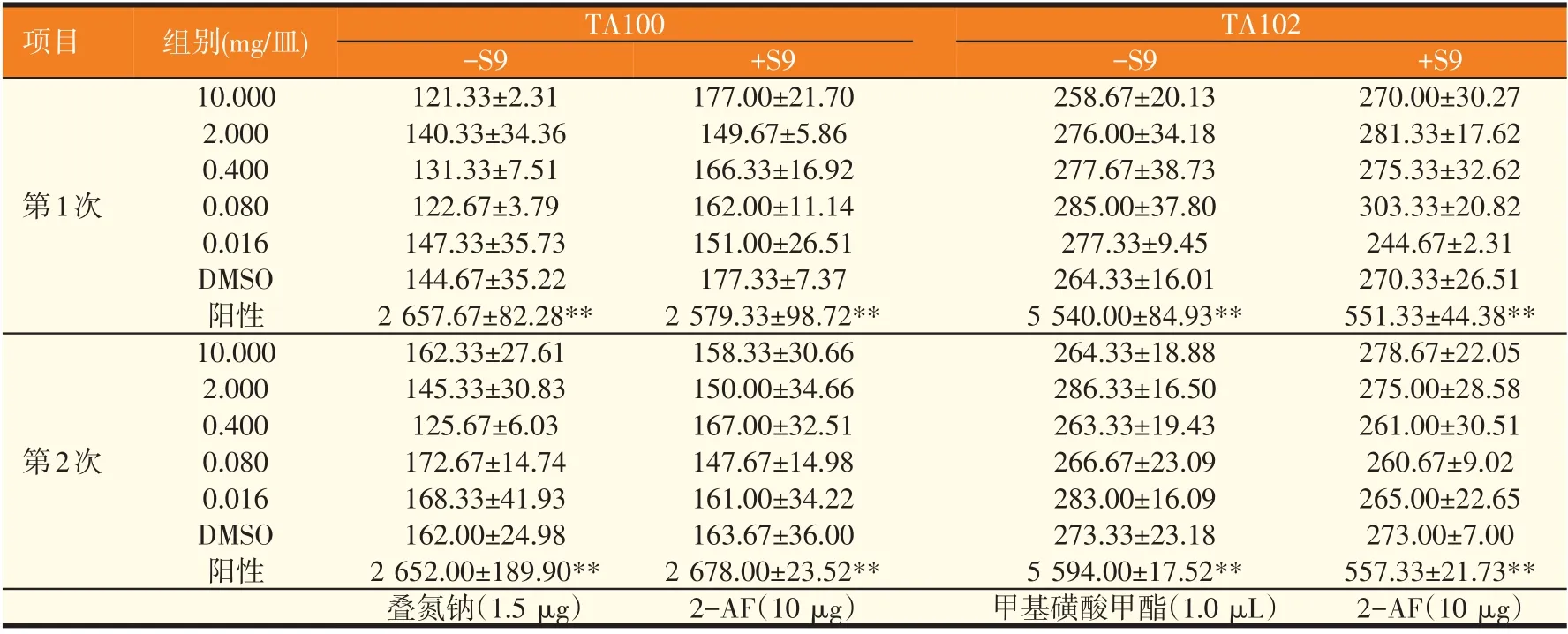
表2(续) 岩陀黄酮与黄芩多糖复合物的鼠伤寒沙门氏菌回复突变试验结果()
注:“**”表示各试验组与阳性对照组比较P<0.01,差异极显著。
项目第1次第2次组别(mg∕皿)10.000 2.000 0.400 0.080 0.016 DMSO阳性10.000 2.000 0.400 0.080 0.016 DMSO阳性TA100-S9 121.33±2.31 140.33±34.36 131.33±7.51 122.67±3.79 147.33±35.73 144.67±35.22 2 657.67±82.28**162.33±27.61 145.33±30.83 125.67±6.03 172.67±14.74 168.33±41.93 162.00±24.98 2 652.00±189.90**叠氮钠(1.5 μg)+S9 177.00±21.70 149.67±5.86 166.33±16.92 162.00±11.14 151.00±26.51 177.33±7.37 2 579.33±98.72**158.33±30.66 150.00±34.66 167.00±32.51 147.67±14.98 161.00±34.22 163.67±36.00 2 678.00±23.52**2-AF(10 μg)TA102-S9 258.67±20.13 276.00±34.18 277.67±38.73 285.00±37.80 277.33±9.45 264.33±16.01 5 540.00±84.93**264.33±18.88 286.33±16.50 263.33±19.43 266.67±23.09 283.00±16.09 273.33±23.18 5 594.00±17.52**甲基磺酸甲酯(1.0 μL)+S9 270.00±30.27 281.33±17.62 275.33±32.62 303.33±20.82 244.67±2.31 270.33±26.51 551.33±44.38**278.67±22.05 275.00±28.58 261.00±30.51 260.67±9.02 265.00±22.65 273.00±7.00 557.33±21.73**2-AF(10 μg)
由表4可知,岩陀黄酮与黄芩多糖复合物高、中、低三个剂量组致小鼠骨髓嗜多染红细胞微核率与阴性对照组相比,差异无显著性(P>0.05),与阳性对照组相比差异有显著性(P<0.01),可判断岩陀黄酮与黄芩多糖复合物不具有遗传毒性。
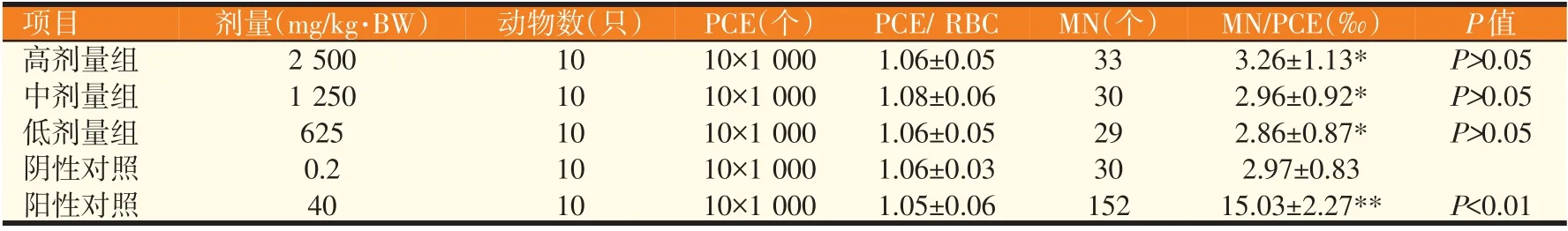
表4 岩陀黄酮与黄芩多糖复合物对动物骨髓嗜多染红细胞微核发生率(n=10)
3 讨论
中兽药是我国传统兽医学重要组成部分,被广泛应用于预防和治疗畜禽疾病、促进动物生长、提高饲料报酬。岩陀富含黄酮类成分,可通过乙醇提取。研究表明岩陀乙醇提取物对金黄色葡萄球菌、大肠埃希菌、白色念珠菌等多种细菌有良好抑制效果[13-14];岩陀乙醇浸膏在抑制病毒试验中不仅能抑灭DNA 病毒,而且能抑制RNA病毒[15];岩陀黄酮在大鼠试验中能够显著缓解由环磷酰胺导致的免疫抑制情况[6]。黄芩多糖是提取黄芩苷的副产物,比较容易获得[16]。黄芩多糖具有抗氧化、抗炎活性,饲料中添加一定比例的黄芩多糖能够显著提升肉仔鸡的体重、降低料重比、提高仔鸡生长性能,还能提高仔鸡免疫功能[17]。中药的联用可以提高药效并提升动物综合免疫力。刘伟等[18]研究表明益母草、野菊花复方水煎液的降压作用比单方水煎液降压作用明显。张雪等[19]研究表明灯盏花黄酮和马蹄香多糖复合物可刺激仔猪淋巴细胞增殖,调节免疫抑制大鼠的免疫功能。所以本试验认为岩陀黄酮和黄芩多糖提取复合物具有兽药开发利用价值。
前人对岩陀黄酮和黄芩多糖的功效研究已经非常深入,但缺乏岩陀黄酮和黄芩多糖提取复合物的安全性研究。为了确定在饲料中添加药用植物产品的安全性,必须利用各种试验模型进行系统的毒理学研究,以预测其毒性,并为选择动物安全剂量设定标准。
急性毒性试验主要测定LD50,观察急性中毒表现并初步估计试验药物对人类或动物的危害性。鄢鹏飞等[20]通过急性毒性试验确定富硒油菜粉LD50为11.75 g∕kg·BW,确定其为实际无毒物质。本试验通过岩陀黄酮与黄芩多糖复合物LD50大于10 g∕kg·BW,判定其为实际无毒物质,但未确定实际LD50,应在急性毒性试验中设置不同浓度,为岩陀黄酮与黄芩多糖复合物的安全剂量范围提供有效参考数据。
细菌回复突变试验用于鉴定可产生基因损伤导致基因突变的物质,其敏感性、特异性、准确性较高[21];精子畸形试验可识别诱发精子致病功能障碍的化学物质,灵敏可靠;微核试验可检测到诱变物质改变细胞分裂过程中染色体的分布[22]。回复突变试验、小鼠骨髓细胞微核试验和精子畸形试验结果阴性,表明岩陀黄酮与黄芩多糖复合物在本试验条件下无遗传毒性。
4 结论
在本试验条件下,岩陀黄酮与黄芩多糖复合物属实际无毒物质,在2 500 mg∕kg·BW 内试验动物未出现急性毒性和遗传毒性反应,可初步推断中药岩陀黄酮与黄芩多糖复合物在2 500 mg∕kg·BW范围内作为中兽药安全性较好。
