Aurivillius结构Bi2MoxW1-xO6铁电功能晶体的生长与性质表征
2022-12-10丁小南田相鑫高泽亮刘敬权
丁小南,田相鑫,赵 鹏,高泽亮,刘敬权
(1.临沂大学材料科学与工程学院,临沂 276000;2.中材人工晶体研究院有限公司,北京 100018;3.山东大学晶体材料国家重点实验室,济南 250100)
0 引 言
由于能够实现机械信号与电信号的相互转换,压电及铁电功能材料在高灵敏传感技术、自动控制、计量检测、通信、导航等领域具有广泛的应用。目前,基于BaTiO3钙钛矿陶瓷的铁电电容器已经成为现代电子技术领域不可或缺的基本元器件,被广泛应用于手机、个人及工业电脑等电子设备的电路主板中[1]。近年来,随着航空航天、矿山勘探、汽车制造等产业的持续发展,对基于压电及铁电功能材料的传感系统在高温、高压等极端条件下的服役性能也提出了更高的要求。但是,为了保证压电/铁电材料工作的稳定性和可靠性,在高温条件下工作时,一般将其服役温度限制在材料居里温度的一半以下。例如汽车压电喷油器中使用的PZT(Pb(Zr, Ti)O3)压电陶瓷的居里温度约为360 ℃,因此其使用温度一般不能超高180 ℃,实际上严重限制了内燃机在特殊环境中的性能。因此,探索具有高居里温度的新型压电/铁电材料,研究居里温度及电学性能与晶体组成、晶体结构之间的关系,实现对其电学性质的连续调控以满足不同服役工况的要求,具有重要的研究意义。Aurivillius结构氧化物常表现出大的自发极化(Ps=30~50 μC/cm2),并具有高的居里温度(Tc>600 K)、低的漏电流和良好的抗疲劳特性、谐振频率的时间和温度稳定性好、机械品质因数高和易烧结等优点,是一类潜在的高温压电/铁电传感材料,并在多铁功能材料、非易失性存储器等相关应用领域表现出良好的应用与研究前景[1-5]。此外,近些年来,Aurivillius化合物在高效储能、催化等绿色能源领域也受到了广泛的研究关注[6-10]。
Aurivillius型化合物在晶体结构上具有特殊的层状特性,其结构通式可以写成(Bi2O2)(An-1BnO3n+1),其中A为Pb2+、Sr2+、La3+、Bi3+等金属阳离子,而B为Ti4+、W6+、Mo6+、Ta5+、Nb5+等过渡金属阳离子[11-14]。如图1所示,这类化合物在晶体结构上表现出明显的层状特征,Bi3+与O2-构成[Bi2O2]2+类萤石结构层,B位阳离子则与O构成[BO6]八面体并以共顶点相连的形式构成类钙钛矿结构层,结构通式中的n即代表由B位阳离子与O2-形成的类钙钛矿层的数目,A位阳离子则位于类钙钛矿层的八面体之间,以保持材料的电荷平衡。代表性的材料有Bi2WO6(n=1)、Bi2MoO6(n=1)、Bi2W2O9(n=2)、Bi2SrNb2O9(n=2)、Bi4Ti3O12(n=3)等。从图1中也可以看出,随着类钙钛矿层n的增加,Aurivillius型氧化物在晶体结构上也逐渐趋近于真正的钙钛矿(n=∞)。除了类钙钛矿层的层数可以发生改变之外,Aurivillius结构中还存在“共生”的现象,即[Bi2O2]2+类萤石结构层之间存在不同种类或者不同层数的类钙钛矿层,如Bi7Ti4NbO27可以认为是由Bi3TiNbO9(n=2)和Bi4Ti3O12(n=3)在晶体结构层面上交替排列形成的,SrBi8Ti7O27可以看作是由Bi4Ti3O12和SrBi4Ti3O15(n=4)交替排列形成的,而Bi5Ti1.5W1.5O15则可以认为是由Bi3Ti1.5W0.5O9(n=2)和Bi2WO6(n=1)在交替生长过程中形成的,这种共生现象能够有效打破相邻类钙钛矿层之间的极性抵消效应,增强材料的铁电性[15-18]。Aurivillius型化合物这种开放的晶体结构以及“共生”的特点使得此类化合物中可以产生更加丰富的晶体结构类型和功能性质,而且氧化物超晶格中类钙钛矿结构层的[BO6]八面体阴离子基团属于低刚度基团,能够发生多种形式的畸变、倾斜和扭转,对力、电、光、磁、声、热等多种外场产生响应和耦合,这也是晶体中自发极化与极化反转的重要来源,而且A位阳离子也可以对类钙钛矿型的无机框架产生重要影响,进而可以实现对晶体能带结构的影响和调控[19-24]。因此,Aurivillius型化合物是一类重要的多功能晶体,基于良好单晶体的结构解析和功能性质研究在理论和实际应用上都具有重要的意义。
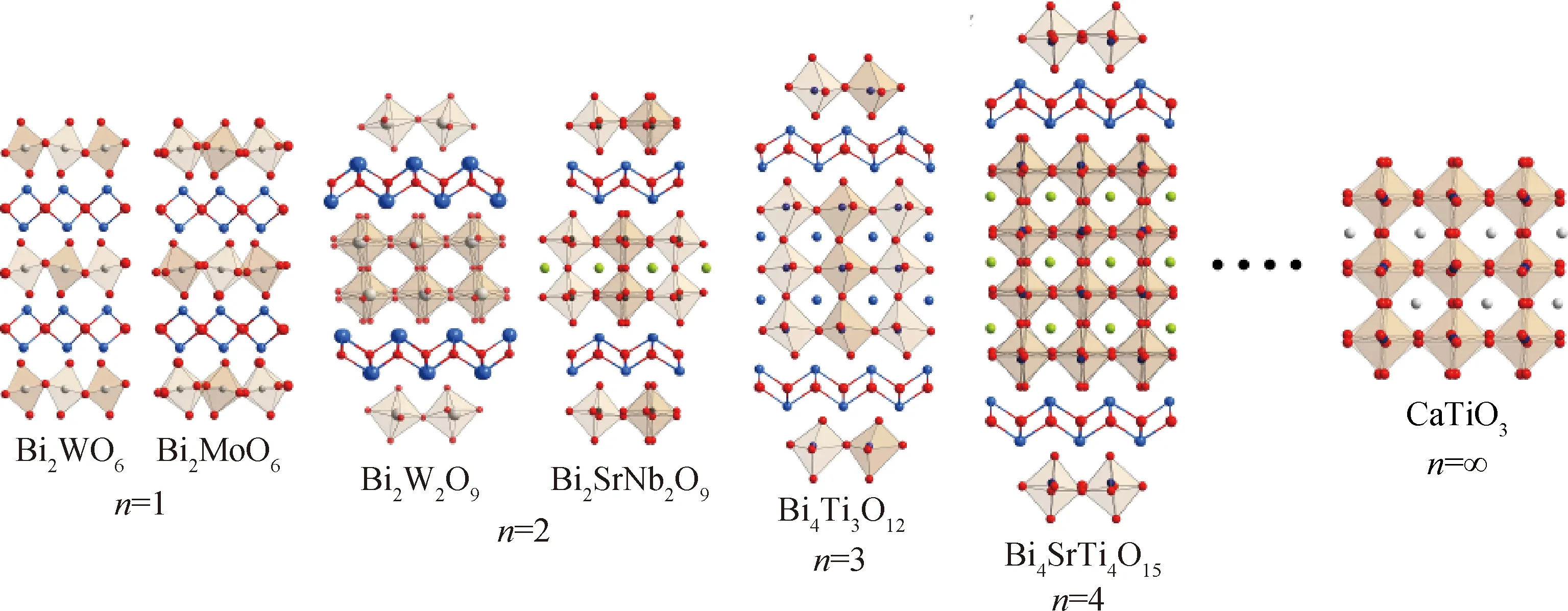
图1 Aurivillius结构氧化物晶体的结构示意图Fig.1 Schematic illustration of the Aurivillius oxides crystal structure
Bi2WO6、Bi2MoO6、Bi2W2O9是Aurivillius体系中组成最简单的三种化合物,而且也是这一体系中仅有的三种A位阳离子空缺的化合物(见图1)。其中,Bi2WO6由于具有极高的居里温度(~936 ℃),制备简单且具有优异的催化性能等优点,是目前Aurivillius体系中研究最多的化合物之一[25-28]。随着温度的变化,Bi2WO6表现出复杂的晶体结构转变,在熔点以下,Bi2WO6具有单斜A2/m空间群的晶体结构(此时一般记为γ′-Bi2WO6),随后在960 ℃左右发生结构重建型相变,转变成顺电性的Fmmm空间群,这也就决定了Bi2WO6单晶体的生长不能采用熔体法,只能使用助熔剂法在相变点以下进行晶体生长。温度继续降低时,Bi2WO6会发生铁电-顺电相变变成铁电性的B2cb空间群(~936 ℃),然后在640~660 ℃附近以铁电-铁电相变的形式进入Aba2空间群结构的室温铁电相(又记为γ-Bi2WO6)。值得注意的是,这样的复杂相变过程在Aurivillius体系中是比较常见的。例如在室温下与Bi2WO6同构的Bi2MoO6,随温度变化时也表现出与Bi2WO6非常相似的结构演化现象:室温Bi2MoO6为铁电相(记为γ-Bi2MoO6),P21ab空间群;随温度升高,其在310 ℃左右发生铁电-铁电相变,转变为γ′-Bi2MoO6,mm2点群;继续升温,其在604 ℃附近发生铁电-顺电相变,转变为γ′-Bi2MoO6,mmm点群;在继续升温过程中,于680 ℃左右发生结构重建型相变,转变为γ′-Bi2MoO6,单斜晶系P21/c空间群[29]。但是,与Bi2WO6不同的是,Bi2MoO6在680 ℃附近的结构重建型相变为不可逆相变,一旦P21/c结构的Bi2MoO6形成,随后的降温过程中结构不再发生相变,P21/c的晶体结构会保存至室温。
理论研究表明,Bi2WO6晶体的结构转变主要与类钙钛矿层中[WO6]八面体基团不稳定畸变模有关,即Bi2WO6晶体的自发极化、极化反转以及相转变过程与类钙钛矿型的阴离子层密切相关[30]。因此,在Bi2WO6晶体的基础上对类钙钛矿结构层进行修饰,对深入理解以Bi2WO6为代表的Aurivillius型化合物的结构转变规律,调控晶体的功能性质具有重要意义。例如,在铁电性方面,Noguchi等利用Mn掺杂降低了Bi2WO6晶体的漏电流,并获得了3.8 μC/cm2的剩余极化强度,而南策文院士团队则利用激光分子束外延的方式在SrTiO3多铁衬底上生长了Bi2WO6薄膜,实现了面内的铁弹性取向切换,成功将机械变形与纳米电子/磁电应用进行了耦合。Castro等则合成了Bi2Mo0.25W0.75O6多晶陶瓷,其铁电-顺电相变温度在908 ℃附近,介于Bi2WO6与Bi2MoO6之间[31-33]。但是,也正是由于这种层状结构,Aurivillius体系化合物的体块单晶生长比较困难,特别是类钙钛矿层数n比较小时。对于Bi2WO6晶体,由于存在破坏性的结构重建相变,只能采用助熔剂法进行晶体的生长,NaF-Na2WO4-WO3体系、Li2B4O7、NaVO3-B2O3体系等先后被用作助熔剂生长得到了Bi2WO6单晶,但是晶体尺寸都很小,厚度小于1 mm,而且往往存在着较多裂纹等晶体缺陷,限制了对Bi2WO6晶体结构演变和功能性质的深入、全面分析[34-38]。
本文从Bi2WO6-Bi2MoO6体系结构演化、性能调控以及二者之间的关系的角度出发,探索Bi2MoxW1-xO6固溶体系的形成范围与制备条件,探索晶体生长条件,并通过晶体结构解析与电学性质测定初步分析不同Mo、W比例对材料性能的调控作用。具体地,采用固相反应法对Bi2WO6-Bi2MoO6体系进行了系统研究。
1 实 验
1.1 Bi2WO6的固相合成与Bi2MoxW1-xO6固溶体系的探索
本文中Bi2MoxW1-xO6系列晶体的合成与生长使用的原料为Bi2O3(typically,纯度99.99%, Alfa-Aesar)、MoO3(纯度99.95%, Alfa-Aesar)、WO3(纯度98%, Alfa-Aesar)、Li2CO3(纯度99.99%, 上海阿拉丁生化科技股份有限公司)和H3BO3(纯度99.99%,Alfa-Aesar),所有原料在实验中均为直接使用,没有经过额外的提纯处理。
Bi2WO6的固相合成。按照化学计量比称取Bi2O3与WO3,充分研磨并混合均匀后,在压片机上以6 MPa的压力压制成片,置于刚玉坩埚中在700 ℃烧结不少于48 h,中间配合不少于两次的重新研磨、压片。700 ℃烧结结束后在空气中冷却。
Bi2MoxW1-xO6系列固溶体材料的固相合成。采用高温固相反应的方式进行合成,为了详细研究Bi2MoxW1-xO6体系能够形成固溶体的范围、形成的结构以及合成的温度,本文取x=0、0.2、0.4、0.5、0.6、0.8、1.0,即对应原料配比n(Bi2O3)∶n(WO3)=1∶1(Mo 0#),n(Bi2O3)∶n(MoO3)∶n(WO3)=1∶0.2∶0.8(Mo 20#),n(Bi2O3)∶n(MoO3)∶n(WO3)=1∶0.4∶0.6(Mo 40#),n(Bi2O3)∶n(MoO3)∶n(WO3)=1∶0.5∶0.5(Mo 50#),n(Bi2O3)∶n(MoO3)∶n(WO3)=1∶0.6∶0.4(Mo 60#),n(Bi2O3)∶n(MoO3)∶n(WO3)=1∶0.8∶0.2(Mo 80#),n(Bi2O3)∶n(MoO3)=1∶1(Mo 100#),共计7个不同的配比,分别在500 ℃、570 ℃、700 ℃、870 ℃四个不同的温度下进行烧结,其中500 ℃烧结时间不少于72 h,其他三个温度烧结时间不少于48 h,中间配合三次重新研磨、压片,烧结结束后在空气中冷却。合成样品的相组成与相纯度采用粉末X射线衍射(powder X-ray diffraction, PXRD)分析进行确定。
1.2 Bi2WO6及Bi2Mo0.15W0.85O6单晶的助熔剂法生长
Bi2WO6虽然是一致熔融化合物,熔点为1 083 ℃,但是该晶体在960 ℃附近存在结构重建型相变,晶体结构由单斜晶系A2/m空间群转变为正交晶系Fmmm空间群[29]。因此,Bi2WO6晶体以及富钨的Bi2Mo0.15W0.85O6晶体的生长需要采用助熔剂法,在远低于材料熔点的温度下进行生长,以避免晶体在结构重建型相变过程中发生严重碎裂而无法获得完整晶体。此外,Bi2WO6晶体铁电-顺电转变的居里温度在930 ℃附近,要想获得完整的单畴铁电单晶,也必须采用助熔剂法在居里温度以下生长Bi2WO6单晶。助熔剂法晶体生长一般情况下优先选择自助熔剂体系,可以有效避免溶剂原子进入晶体造成光学质量下降。但是,由于WO3的熔点较高,而Bi2O3与MoO3在高温(大于700 ℃)下非常容易升华,不适合作为Bi2WO6与Bi2Mo0.15W0.85O6晶体生长所需的助熔剂。
碱金属硼酸盐一直以来都是氧化物晶体生长的优异助熔剂,Takeda等[36-37]曾采用LiBO2、Li2B4O7及Na2B4O7作为助熔剂进行了Bi2WO6晶体的生长探索,在摩尔比n(Bi2WO6)∶n(Li2B4O7)=7∶3的体系中生长得到了0.7 mm厚的Bi2WO6单畴晶体。另外,采用Li2B4O7-WO3作为复合助熔剂,本课题组成功生长得到了同样具有Aurivillius型结构的Bi2W2O9晶体的厘米级单晶,厚度达到了11 mm[27]。为了进一步降低晶体生长温度,本文对Li2B4O7-Bi2O3及Li2B4O7-MoO3的混合物作为助熔剂生长Bi2WO6及Bi2MoxW1-xO6晶体进行了详细探索,最终证明n(Bi2WO4)∶n(Li2B4O7)∶n(Bi2O3)=2∶2∶1(摩尔比)是能够适应Bi2WO6晶体生长的助熔剂体系,而n(Bi2O3)∶n(MoO3)∶n(WO3)∶n(Li2B4O7)=1∶1∶1∶1时能够生长得到厚度不小于1 mm的Bi2Mo0.15W0.85O6晶体。具体地,首先采用Li2CO3与H3BO3合成生长所需的Li2B4O7,按照化学计量比称量Li2CO3与H3BO3进行研磨和充分的机械混合,压制之后置于铂坩埚中,由室温缓慢升至400 ℃并恒温不少于10 h,随后缓慢升温至750 ℃再次恒温不少于10 h,使得Li2CO3与H3BO3充分反应并释放CO2与H2O,防止反应过于剧烈导致的溢料。随后将合成的Li2B4O7升温至900 ℃,形成均匀澄清的溶液待用。
对于Bi2WO6晶体的生长,将Bi2O3与WO3按照2∶1的比例称量后充分混合,少量多次加入到澄清的Li2B4O7溶液中。加入完毕后,将整个溶液体系在900 ℃恒温不少于24 h。此外,合成Li2B4O7助熔剂之后,也可以将Bi2O3与固相合成的Bi2WO6多晶充分混合之后加入Li2B4O7溶液,然后在900 ℃恒温不少于24 h。将铂籽晶夹头轻触液面并降温,记录降温过程中籽晶夹头上首次出现Bi2WO6晶片的温度作为晶体生长的饱和温度。随后重新升温至900 ℃恒温10 h,将已经产生的微晶完全重溶,将Bi2WO6小晶片绑在籽晶夹头上作为籽晶,在饱和温度以上1~3 ℃轻触液面,然后在5 h内将温度降至饱和温度,随后以0.1~0.3 ℃/d的速率降温,直至生长得到目标尺寸的晶体。生长过程中,控制晶转速率在5~15 r/min。Bi2Mo0.15W0.85O6晶体的生长与Bi2WO6晶体的生长类似,按照n(Bi2O3)∶n(MoO3)∶n(WO3)∶n(Li2B4O7)=1∶1∶1∶1的比例将Bi2O3、MoO3、WO3与Li2B4O7溶液混合并加热获得均一溶液。采用铂籽晶夹头测定饱和温度,以Bi2WO6晶片作为籽晶,可以生长得到不小于1 mm厚度的单畴Bi2Mo0.15W0.85O6晶体。值得注意的是,通过多次重复生长实验,Bi2Mo0.15W0.85O6晶体的生长温度比Bi2WO6晶体低约50 ℃。
此外,由于Bi2WO6及Bi2MoxW1-xO6(0≤x≤1)系列晶体具有典型的Aurivillius层状结构,晶体生长时层片状生长习性非常强烈,本文针对晶体生长习性对晶体生长炉的温场进行设计。经过多次反复试验发现,对于φ120 mm内径晶体生长熔盐炉,合适的温度场配置应该是生长坩埚中上方具有相对较大的温度梯度。因此,需要将铂坩埚下方耐火砖的高度调整至距离炉膛顶部1/3~1/4左右的位置,而且晶体生长过程中坩埚上方保温纤维卷的厚度不宜过高,能够保持炉膛内部温度场稳定即可。
1.3 性能测试与表征
PXRD图谱使用Bruker D8 Advance多功能X射线衍射仪进行收集。衍射光源采用Cu Kα射线,波长为0.154 18 nm。PXRD测试时,管电压和管电流分别设置为40 kV和40 mA,扫描的角度范围设置为5o≤2θ≤90°。扫描方式采用步进扫描,步长为0.02°,每步的积分时间设置为2 s。
掺Mo晶体中W与Mo的比例采用能量色散谱(EDS)进行分析。本文采用Hitachi S-4800超高分辨率扫描电镜配备的能谱仪测定了晶体的元素组成情况。为了避免粘在晶体表面的助熔剂对测试结果产生影响,测试前先将晶粒浸于稀盐酸中20 min,确保测试结果的准确度。
Bi2Mo0.15W0.85O6单晶的结构用Bruker AXS SMART APEX-Ⅱ CCD面探测器单晶衍射仪进行数据收集,采用波长为0.071 073 nm的Mo Kα射线作为光源,配合石墨单色器进行射线的单色化,扫描方式为ω扫描。收集的单晶衍射数据采用APEX-Ⅱ软件包中的INTEGRATE程序进行数据的还原,以SCALE程序进行数据校正。单晶结构的解析采用SHELXTL软件进行,以XPREP程序进行单晶结构空间群的分析指认,采用XS和XL程序进行结构的解析和精修,获得的晶体结构采用PLATON软件进行结构对称性的检查。
2 结果与讨论
2.1 室温铁电相Bi2WO6多晶的固相合成
如图2所示,采用固相反应法在700 ℃烧结多次之后,样品的PXRD图谱与根据Bi2WO6室温铁电相(Aba2空间群)晶体结构计算的理论衍射图谱吻合良好,说明在700 ℃进行烧结能够获得纯的Bi2WO6室温铁电相[25]。
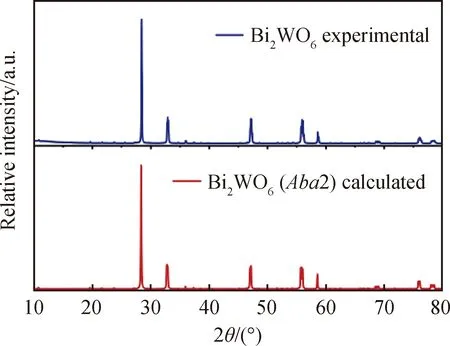
图2 固相法合成的Bi2WO6多晶的PXRD图谱与理论图谱的对比Fig.2 Comparison of PXRD pattern of Bi2WO6 polycrystalline synthesized by solid phase method and theoretical pattern of Bi2WO6 polycrystalline
2.2 Bi2MoxW1-xO6 (0≤x≤1)体系的合成探索
在图1中可以明显看出,Bi2WO6与Bi2MoO6是两种典型的A位阳离子缺失的Aurivillius结构氧化物,其室温结构同构,都具有正交晶系mm2点群的对称性。在功能性质上,Bi2WO6的居里温度达到了936 ℃,而Bi2MoO6的居里温度只有604 ℃,存在约300 ℃的差别。探索Bi2WO6与Bi2MoO6形成固溶体的情况对于研究晶体结构稳定性、调控晶体的光电功能性质具有重要的研究意义。为此,本文在500 ℃、570 ℃、700 ℃以及870 ℃,对Bi2MoxW1-xO6体系中x=0、0.2、0.4、0.5、0.6、0.8、1.0共计7个不同比例的样品进行了固相烧结。在500 ℃时,样品在马弗炉中烧结72 h,样品的PXRD图谱如图3(a)所示,可以看出在500 ℃烧结72 h无法合成纯相的Bi2WO6多晶,样品中仍然存在一定量的WO3(PDF No.20-1323),并产生了富铋的Bi14W2O27(PDF No.39-0061)结晶相。随着样品中Mo含量的增加,富铋钨酸盐相Bi14W2O27逐渐减少,但是在Mo 20#、Mo 40#、Mo 50#样品中产生了少量的富铋钼酸盐相(可能是Bi4MoO9,PDF No. 36-0115)。当n(Mo)∶n(W)比例达到4∶1及更高时可以获得纯相的Bi2MoxW1-xO6(0.8≤x≤1.0)固溶体多晶。图3(b)~(c)为Bi2MoxW1-xO6系列样品在570 ℃烧结48 h的情况,由图中可以看出,当Mo的含量较少(0≤x≤0.5)时,没有获得纯相的Bi2MoxW1-xO6固溶体,样品中含有少量的WO3和Bi14W2O27结晶相,当Mo的含量达到60%(x=0.6)以上时,可以获得纯相的Bi2MoxW1-xO6固溶体,而且在Mo 60#样品中32.66°、47.10°及55.65°附近的衍射峰与Bi2WO6相比出现了一定的展宽,但是并未出现明显的Bi2MoO6室温相的劈裂特征,与此同时Mo 80#样品中则出现了明显的劈裂,表明Mo 60#样品在衍射特征上仍然与Bi2WO6室温相更为接近,而Mo 80#则已经更接近Bi2MoO6了。此外,值得注意的是,570 ℃烧结48 h的Mo 100#样品中,出现了富铋钼酸盐的特征衍射峰,表明Bi2MoO6室温铁电相的合成温度应该在500 ℃左右。
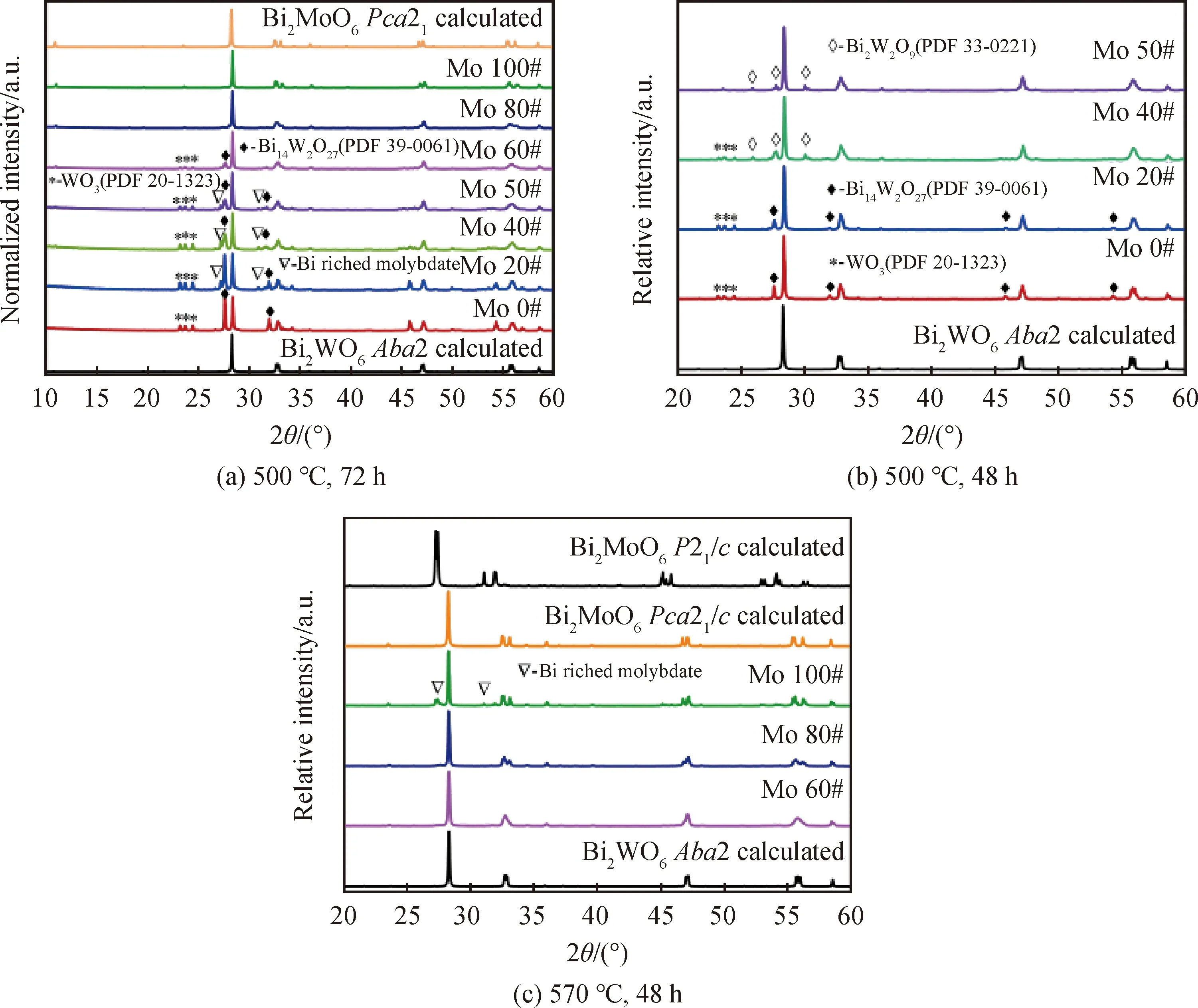
图3 不同Mo与W比例Bi2MoxW1-xO6样品在不同温度及不同时间下烧结的PXRD图谱Fig.3 PXRD patterns of Bi2MoxW1-xO6 samples with different Mo and W ratios sintered at different temperatures for different time
从图3中可以看出,固相烧结温度在570 ℃以下时难以获得富钨的Bi2MoxW1-xO6固溶体。图4(a)为在700 ℃烧结48 h的PXRD图谱,可以看出,0≤x≤0.6时,可以获得单相的Bi2MoxW1-xO6固溶体,并且随着Mo含量的增加,样品衍射特征逐渐由Bi2WO6室温铁电相向Bi2MoO6室温铁电相的衍射特征转变。但是,当Mo的含量达到80%时(Mo 80#),样品中开始出现高温相Bi2MoO6(P21/c空间群)的特征衍射峰,在Mo 100#样品中获得了单一的Bi2MoO6高温相。此外,700 ℃烧结时,含Mo为60%(Mo 60#)的Bi2Mo0.6W0.4O6固溶体仍能保持铁电相结构不变。
此外,不同配比的样品在870 ℃的高温同样进行了48 h的烧结实验,如图4(b)所示,可以看出,x≤0.5的Bi2MoxW1-xO6固溶体仍然能够在870 ℃保持铁电相结构不变,但是x>0.5的固溶体中已经开始出现单斜晶系的顺电相,Mo含量达到80%以上时,样品基本上已经完全转变为高温顺电相。
基于Bi2MoxW1-xO6体系在不同温度的固相合成实验可以看出,x在0到1的范围内连续变化时,Bi2WO6与Bi2MoO6能够形成连续固溶体。相对于Bi2MoO6,Bi2MoxW1-xO6固溶体系中W的加入能够有效稳定固溶体的室温铁电相,提高铁电相稳定存在的温度范围。因此,可以通过控制体系中W、Mo的比例实现对晶体结构转变温度、居里温度等性质的调控,也有理由相信,通过形成Bi2MoxW1-xO6固溶体,可以实现对Bi2WO6-Bi2MoO6体系铁电性质在一定范围内的连续调控。
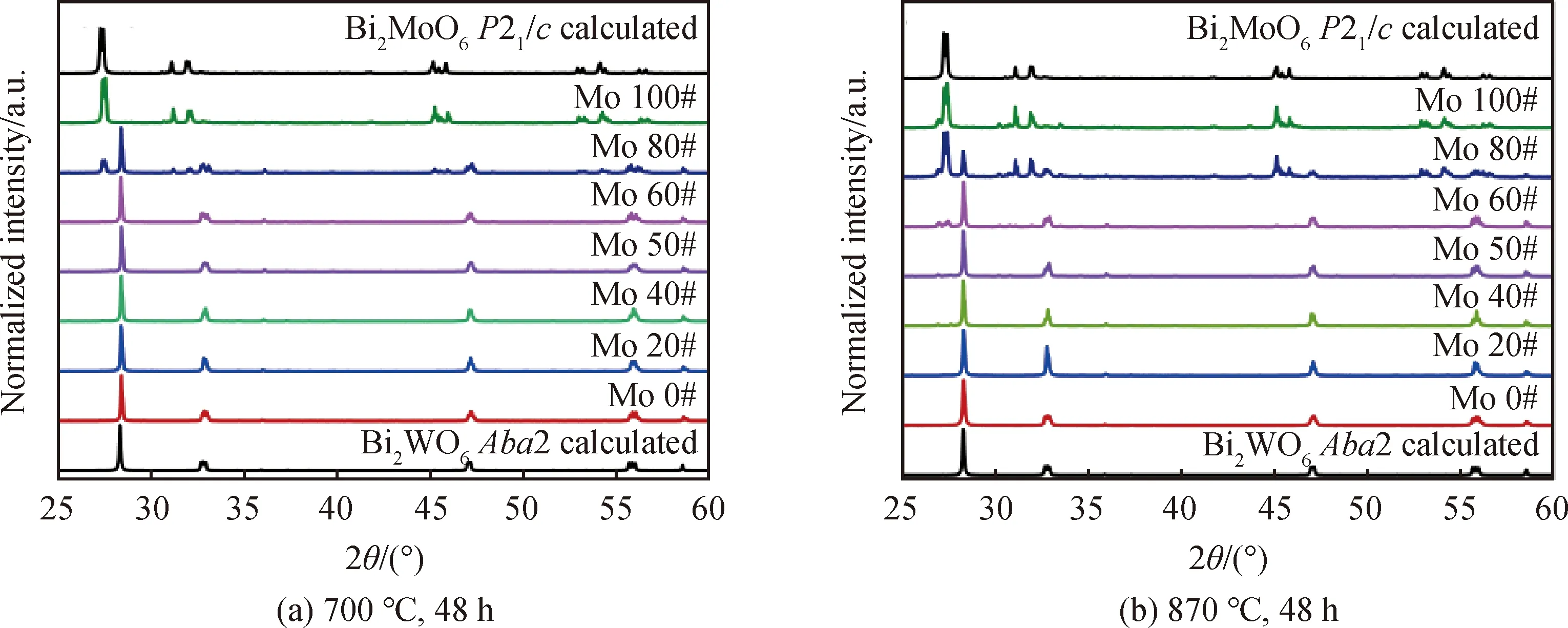
图4 不同Mo与W比例Bi2MoxW1-xO6样品在700 ℃及870 ℃烧结的PXRD图谱Fig.4 PXRD patterns of Bi2MoxW1-xO6 samples with different Mo and W ratios sintered at 700 ℃ and 870 ℃, respectively
2.3 Bi2WO6与Bi2Mo0.15W0.85O6单晶的助熔剂法生长
单晶生长对于晶体结构解析、各向异性功能性质的全面表征以及晶体的应用均具有重要意义。由于Bi2WO6在熔点以下存在晶体结构的重建型相变,因此只能采用助熔剂法进行晶体的生长。助熔剂法也是获得单畴晶体的可行方法。相对于n=2的Bi2W2O9,n=1的Bi2WO6及Bi2MoxW1-xO6系列固溶体单晶在生长时表现出更为强烈的层片状生长习性,垂直萤石结构层/类钙钛矿结构层方向的晶体厚度提升困难。为此,本文针对材料的结构特性对熔盐炉的温场进行调整,采用了较大温度梯度的温场。此外,对晶体生长的助熔剂体系进行了详细的探索,最终证明n(Bi2WO4)∶n(Li2B4O7)∶n(Bi2O3)=2∶2∶1(摩尔比)是适合Bi2WO6单畴晶体生长的助熔剂体系。如图5(a)~(c)所示为采用这一体系生长的Bi2WO6晶体,经X射线衍射定向发现,晶体的最大显露面为晶体学(010)晶面,与晶体结构的层片方向平行。此外,在实验中可以发现,Bi2WO6晶体的生长温度低于其居里点,基于Bi2WO6晶片,采用d33准静态压电测试仪测量晶体不同位置的压电系数,发现测量值一致(~4 pC/N)。采用偏光显微镜观察Bi2WO6及Bi2Mo0.15W0.85O6晶片,测试晶片完全消光。综合晶体生长温度、压电系数测量和偏光显微镜测试,证明所生长的晶体为单畴晶体。图5(a)、(b)中所展示的Bi2WO6晶体厚度达到了~2 mm,而且晶体宏观形貌较好,光学透过性良好,只有一个较大的裂纹,可能与晶体提离液面过程中产生了较大的热应力有关。图5(c)中的晶体同样是在这一体系中生长得到,最大尺寸达到了40 mm左右,晶体厚度约1 mm,充分说明该体系对于Bi2WO6单畴晶体的生长是适合的。
对于Bi2MoxW1-xO6固溶体的生长,如直接在Bi2WO6晶体生长体系中加入少量的MoO3,得到的晶体中检测不到Mo的掺入,若增大MoO3的加入量,结晶的物相中会出现杂相。经过反复尝试与生长实验,对于Bi2MoxW1-xO6固溶体单晶的生长,Li2B4O7-WO3-MoO3是一个较为合适的助熔剂体系。图5(d)所示是体系配比为n(Bi2O3)∶n(MoO3)∶n(WO3)∶n(Li2B4O7)=1∶1∶1∶1(摩尔比)时生长得到的Bi2MoxW1-xO6固溶体单晶,厚度约1 mm,最大尺寸19 mm,X射线衍射定向实验表明,该晶片的最大显露面同样为晶体学(010)晶面。从图中可以看出该晶体宏观质量良好,经d33准静态压电测试和偏光显微测试确认为单畴晶体。为了确认晶体中Mo的具体含量,取质量良好的晶体进行EDS测试,结果如图6所示,可以确认Mo在晶体中的成功掺入,n(Mo)∶n(W)≈0.147∶0.853(摩尔比),结合晶体结构的精修(见本文2.4节)结果,确认图5(d)中所示晶体的分子式为Bi2Mo0.15W0.85O6。

图5 采用助熔剂法生长的Bi2WO6与Bi2Mo0.15W0.85O6单晶照片。(a)~(b)Bi2WO6单畴晶体,厚度~2 mm;(c)Bi2WO6单畴晶体,最大尺寸~40 mm;(d)Bi2Mo0.15W0.85O6单畴晶体Fig.5 Photos of Bi2WO6 and Bi2Mo0.15W0.85O6 single crystals grown by the flux method. (a)~(b) Bi2WO6 single domain crystal with thickness of about 2 mm; (c) Bi2WO6 single domain crystal with the largest dimension of about 40 mm; (d) Bi2Mo0.15W0.85O6 single domain crystal
2.4 Bi2Mo0.15W0.85O6晶体的结构
晶体结构决定了晶体的功能性质,准确测定晶体结构是晶体功能性质的全面表征和实际应用的前提。基于生长的Bi2Mo0.15W0.85O6晶体,采用单晶X射线衍射仪测定了其晶体结构,精修结果和相关参数列于表1。通过晶体结构的精修,结合EDS测试结果确定了晶体的分子式为Bi2Mo0.15W0.85O6,图7为Bi2Mo0.15W0.85O6的晶体结构示意图。
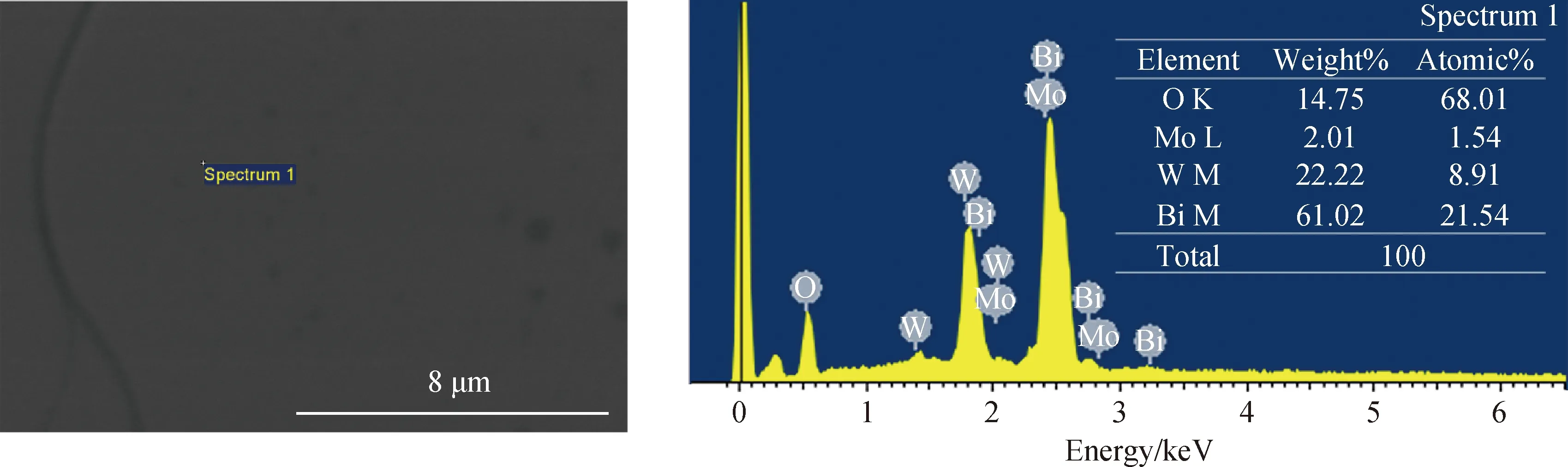
图6 Bi2Mo0.15W0.85O6单晶的EDS结果Fig.6 EDS results of Bi2Mo0.15W0.85O6 single crystal
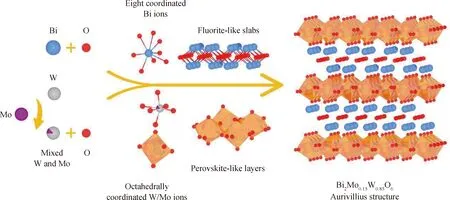
图7 Bi2Mo0.15W0.85O6晶体结构示意图Fig.7 Schematic diagram of the crystal structure of Bi2Mo0.15W0.85O6

表1 Bi2Mo0.15W0.85O6晶体结构解析结果Table 1 Crystallographic structural refinements of Bi2Mo0.15W0.85O6
与Bi2WO6室温铁电相一样,Bi2Mo0.15W0.85O6具有典型的Aurivillius结构,属于正交晶系,Aba2 (No.41)空间群,晶胞参数a=0.544 95(9) nm,b=1.638 3(3) nm,c=0.546 94(9) nm,Z=4。与此同时,Bi2WO6室温铁电相的晶胞参数分别为a=0.543 6 nm,b=1.642 699 nm,c=0.545 7 nm,Bi2MoO6室温铁电相的晶胞参数分别为a=0.548 7(2) nm,b=1.622 6(6) nm,c=0.550 6(2) nm,固溶体Bi2Mo0.15W0.85O6的晶胞参数介于两个端际化合物之间[25,39]。在Bi2Mo0.15W0.85O6晶体中,Mo6+与W6+以统计规律占据[W/MoO6]阴离子八面体的中心离子位置,由于二阶Jahn-Teller效应,d0过渡金属W6+/Mo6+并未占据八面体的中心位置,如图8(a)所示,与六个配位O2-之间形成了两个较“短”的键(0.176(2) nm及0.177(3) nm),两个相等的“中等”长度的键(0.184 6(14) nm),以及两个较“长”的键(0.218(3) nm及0.224(3) nm)。根据Goodenough和Halasyamani等的计算和统计结果,这种“两短-两中-两长”型的键长配置说明Bi2Mo0.15W0.85O6晶体阴离子配位八面体中W6+/Mo6+沿着局域C2[110]方向产生畸变[22,40-41]。Bi3+与八个O2-形成[BiO8]基团,如图8(b)所示,八个Bi—O键键长在0.219 9(17)~0.311 0(33) nm之间。同样地,Bi2WO6及Bi2MoO6室温铁电相的晶体结构中,[WO6]、[MoO6]八面体基团也都采用这种“两短-两中-两长”型的键长配置,因此,二者形成固溶体并未改变晶体中阴离子基团的键长配置情况。
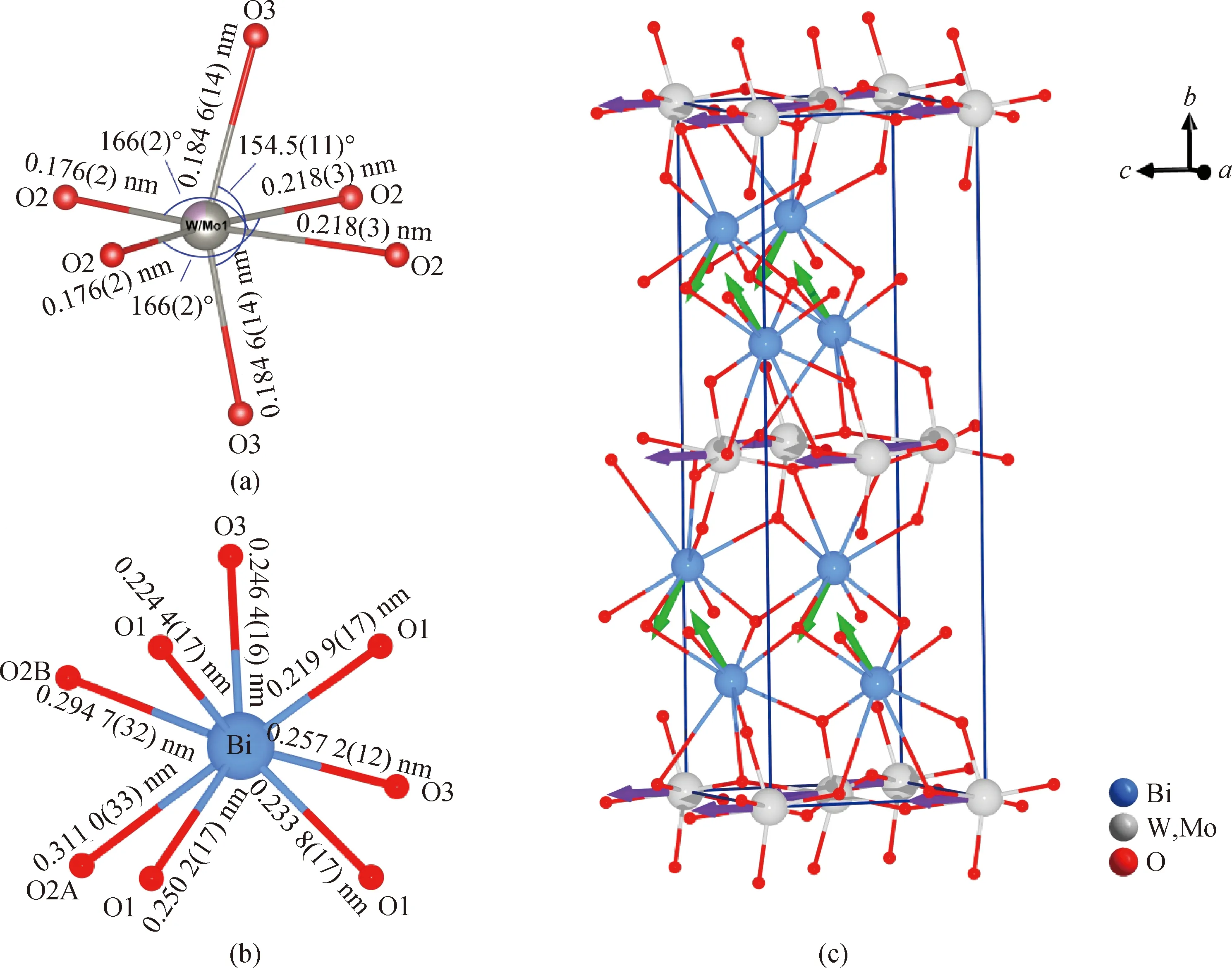
图8 Bi2Mo0.15W0.85O6晶体中不同配位基团与晶体结构示意图。(a)Bi2Mo0.15W0.85O6晶体中的阴离子配位八面体及键长、键角;(b)Bi2Mo0.15W0.85O6晶体中Bi3+阳离子的配位情况;(c)Bi2Mo0.15W0.85O6晶体晶胞中[W/MoO6]八面体及[BiO8]多面体中的局域偶极矩方向Fig.8 Schematic diagrams of different coordination groups and crystal structure of Bi2Mo0.15W0.85O6 crystals. (a) Anionic octahedron and the bond length, angles in Bi2Mo0.15W0.85O6; (b) coordination of Bi3+ cations in Bi2Mo0.15W0.85O6; (c) directions of the local dipole moments of the [W/MoO6] octahedra and [BiO8] polyhedra
晶体的功能性质与晶体结构之间有着密切联系,为此,本文对Bi2Mo0.15W0.85O6的晶体结构进行了进一步深入分析,根据Halasyamani等[22]提出的方法估算了晶体中[W/MoO6]八面体的畸变情况及产生的偶极矩大小,同时对[BiO8]基团的畸变情况也进行了估算。如表2所示,Bi2Mo0.15W0.85O6晶体中[W/MoO6]八面体的畸变程度参数Δd=0.865,大于0.80,属于强畸变的范畴,局域偶极矩为5.890 Debye,与钼碲酸盐非线性光学晶体β-BaTeMo2O9中[MoO6]八面体的局域偶极矩相当,大于Aurivillius化合物中Bi2W2O9晶体中WO6的局域偶极矩,说明Bi2WO6可能具有大的自发极化[27,42]。此外,本文对[BiO8]的局域偶极矩也进行了估算,由于Bi3+属于具有立体化学活性孤对电子的主族阳离子,在偶极矩的计算过程中将未成键孤对电子的影响纳入,其价态设置为-2,与Bi3+的距离设置为0.098 nm[43]。如表2所示,[BiO8]基团的局域偶极矩为7.724 Debye,高于[W/MoO6]基团,意味着[BiO8]基团在Bi2Mo0.15W0.85O6晶体的极性方面也具有重要的影响。极性基团之间的相对排布方式对于晶体是否呈现极性以及极性大小同样至关重要。图8(c)展示了Bi2Mo0.15W0.85O6晶体中不同基团自发极化的排布方向,由图中可以看出,[W/MoO6]基团的局域偶极矩方向均指向晶体学c轴方向,没有相互抵消的情况,有利于单畴晶体产生更大的自发极性。[BiO8]基团的偶极矩方向与晶体学c轴存在一定的夹角,但是由于晶体对称性的限制,在晶体学的a轴和b轴方向的偶极矩分量相互抵消,仅剩余沿极性轴c轴方向的偶极矩分量,如图8(c)和表2所示。此外,值得注意的是,Bi2Mo0.15W0.85O6晶体中每层[W/MoO6]类钙钛矿层的畸变方向均一致,从而导致了沿极性方向较大的晶胞净偶极矩,因而表现出明显的自发极化。这种现象在Aurivillius系列化合物中也呈现出明显的规律性,类钙钛矿层数目n为奇数的Aurivillius化合物往往具有铁电性,而n为偶数的Aurivillius化合物由于相邻类钙钛矿层的极化方向相反而抵消,常常没有铁电性或者极性很弱。
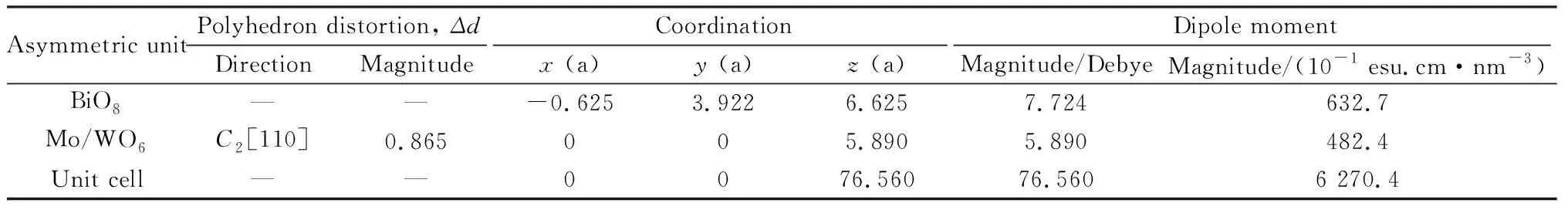
表2 Bi2Mo0.15W0.85O6单晶体中BiO8体系和MoO6、WO6的畸变方向与大小Table 2 Distortion directions and magnitudes of the BiO8, MoO6, and WO6 in Bi2Mo0.15W0.85O6 single crystals
2.5 Bi2WO6与Bi2Mo0.15W0.85O6晶体的变温介电性质分析
基于良好单晶,在室温至500 ℃范围内测定并对比了Bi2WO6与Bi2Mo0.15W0.85O6晶体极性轴方向的介电常数,如图9所示。Bi2WO6晶体室温介电常数ε33测定为70,对应介电损耗约为4.5%。Bi2Mo0.15W0.85O6晶体的室温介电常数ε33为102,介电损耗约为9.9%。可以看出,晶体中W与Mo的混合占位提高了晶体的介电常数,介电损耗也略有升高。此外,从图9中可以看出,随着温度升高,Bi2WO6、Bi2Mo0.15W0.85O6晶体的介电常数和损耗分别在430 ℃和330 ℃附近存在异常变化峰,这一异常变化峰表明晶体出现介电弛豫的现象,而晶体中Mo6+对W6+的部分取代降低了介电弛豫现象出现的温度范围。因此,综合Bi2WO6、Bi2Mo0.15W0.85O6晶体的变温介电常数和介电损耗测试结果可以看出,相对于Bi2WO6晶体,形成Bi2MoxW1-xO6固溶体能够提高晶体的介电常数,并且降低介电弛豫出现的温度范围,可以实现对晶体功能性质的有效调控。
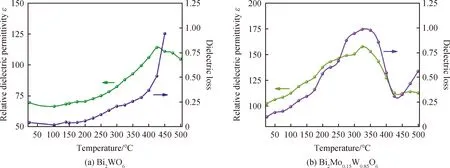
图9 Bi2WO6与Bi2Mo0.15W0.85O6晶体的介电常数与介电损耗随温度变化曲线Fig.9 Variations of the dielectric permittivity and loss of Bi2WO6 and Bi2Mo0.15W0.85O6 crystals with temperatures
2.6 Bi2WO6与Bi2Mo0.15W0.85O6晶体的变温电阻率分析
为进一步探究形成的固溶体对晶体功能性质的影响和调控作用,测定了Bi2WO6、Bi2Mo0.15W0.85O6在100 ℃以下的电阻率并进行了对比,如图10所示。对于Bi2WO6晶体,在-20 ℃时电阻率就达到了9.6×109Ω·cm,随温度升高,电阻率逐渐下降,100 ℃时电阻率降至约9.4×107Ω·cm,在整个测试温度范围内,电阻率没有出现明显的异常变化,表明在-20 ℃至100 ℃范围内Bi2WO6晶体结构稳定,没有出现明显的结构相变。对于Bi2Mo0.15W0.85O6晶体,温度降至-50 ℃时电阻率才达到109量级(9.4×109Ω·cm),温度升至100 ℃时,Bi2Mo0.15W0.85O6晶体的电阻率降至2.4×107Ω·cm。在整个测试的温度范围内,Bi2WO6、Bi2Mo0.15W0.85O6晶体表现出高的电阻率且电阻率随温度升高而降低,而且固溶体Bi2Mo0.15W0.85O6晶体的电阻率均低于Bi2WO6晶体,二者的电阻率差距随温度升高而降低,呈现出典型的绝缘体特征。此外,在整个测试温度范围内,Bi2WO6与Bi2Mo0.15W0.85O6晶体的电阻率均未出现异常变化,表明材料在测试温度范围内同样具有良好的结构稳定性。
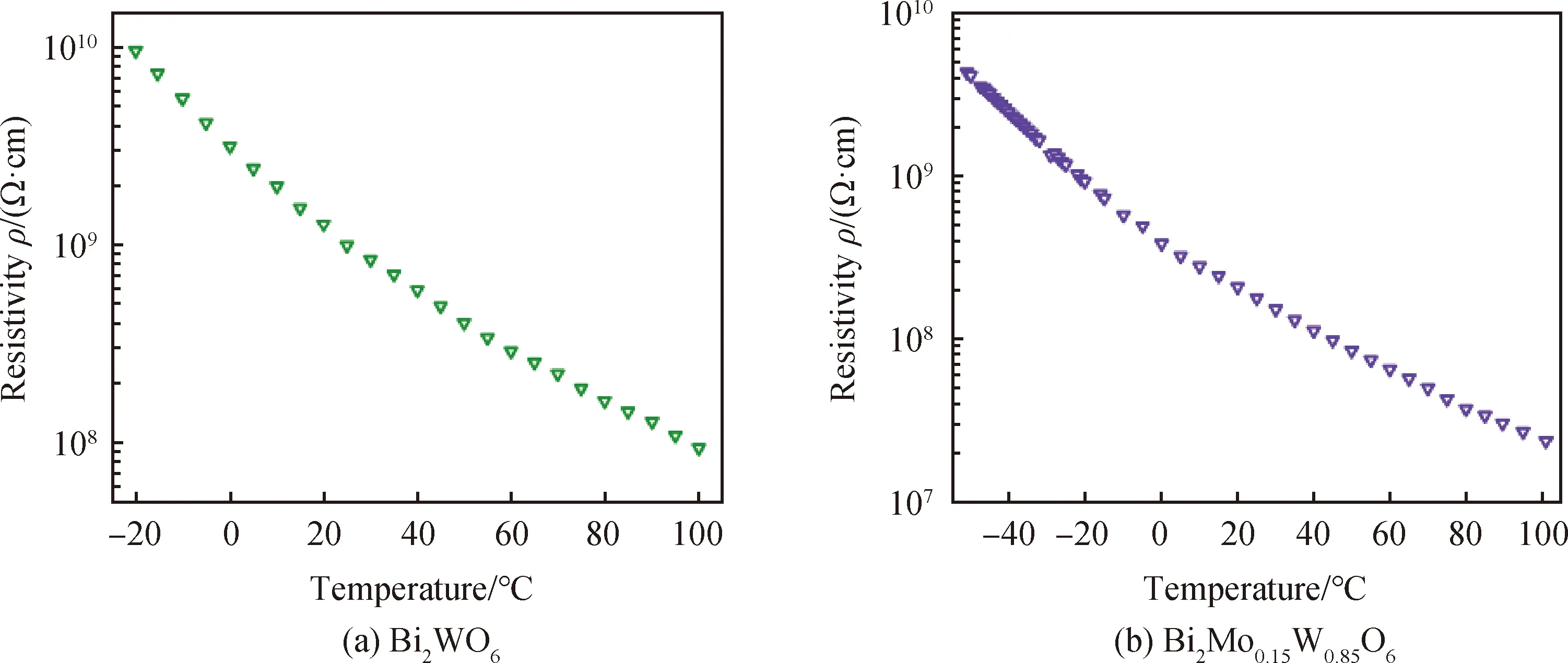
图10 Bi2WO6与Bi2Mo0.15W0.85O6晶体的电阻率随温度变化曲线Fig.10 Variations of the resistivity of Bi2WO6 and Bi2Mo0.15W0.85O6 crystals with temperatures
3 结 论
调整固溶体晶体的成分和组成是调控晶体性质的有效手段,本文通过固相反应法对Aurivillius结构铁电晶体Bi2MoxW1-xO6固溶体系进行详细探索,确认了x可以在0~1连续变化。鉴于Bi2WO6与Bi2MoO6在铁电性质上差别较大,可以通过在大范围内调整Mo与W的比例实现对Bi2MoxW1-xO6体系晶体性质进行连续调控。在此基础上,本文详细探究了Bi2MoxW1-xO6晶体的助熔剂生长体系,发现n(Bi2WO6)∶n(Li2B4O7)∶n(Bi2O3)=2∶2∶1(摩尔比)是适合Bi2WO6单畴晶体生长的助熔剂体系,而在n(Bi2O3)∶n(MoO3)∶n(WO3)∶n(Li2B4O7)=1∶1∶1∶1(摩尔比)时可以获得Bi2Mo0.15W0.85O6固溶体单晶。通过晶体生长温场的针对性设计和晶体生长参数的优化,成功生长得到了厚度不小于2 mm的Bi2WO6单畴晶体以及厘米级的、厚度约1 mm的Bi2Mo0.15W0.85O6单畴晶体。对Bi2Mo0.15W0.85O6晶体的结构解析表明,该晶体具有典型的Aurivillius型晶体结构,属于正交晶系Aba2(No.41)的空间对称性,晶体的极性可能来源于[W/MoO6]基团与[BiO8]基团大的畸变以及二者在空间的近同向排列。通过测定对比Bi2WO6、Bi2Mo0.15W0.85O6晶体在不同温度的介电常数与电阻率发现,形成Bi2Mo0.15W0.85O6固溶体可以提高Bi2WO6的介电常数,降低其电阻率。此外,在测试温度范围内,Bi2WO6与Bi2Mo0.15W0.85O6晶体均表现出良好的结构稳定性,没有发生结构重建性相变。本文的研究对新型铁电功能晶体的探索、晶体生长与性能调控均具有参考意义。
