上海交通大学医学院临床试验研究现状分析
2022-10-21彭树涛仇晓春
彭树涛,仇晓春
1.上海交通大学医学院医学教育研究所,上海 200025;2.上海交通大学医学院图书馆,上海 200025
临床试验(clinical trial)是旨在揭示或证实某项产品的临床或药物学效应,识别、研究产品的不良反应、安全性或效果,试验药物的吸收、分布、代谢以及排出而在人身上进行的研究[1]。临床试验是新药研发中一个不可缺少的环节,是临床药物治疗安全性和有效性的直接证据来源。为推动药物临床试验规范开展和提升研究质量,2003 年我国颁布了《药物临床试验质量管理规范》。近年来我国的临床试验研究数量也日益增多,研究方向与研究内容涉及医学领域的各个主题。上海交通大学医学院(简称上海交大医学院)是临床医学专业位居国内领先地位的医学院校。本研究全面回顾该校临床试验研究的状况,分析10 年来交大医学院临床试验和临床研究论文的特点,希冀为今后临床学科的发展布局与临床创新团队的建设提供可靠依据。
1 资料与方法
1.1 临床试验注册信息检索
Dimensions数据库是由施普林格·自然出版集团开发的全球科研文献、临床试验、专利等科研信息大数据平台。在Dimensions 系统中分别按地区(全球、中国;北京、上海、广州等我国内地城市)检索2012—2021年科研人员注册的临床试验信息,并采用上海交大医学院和各附属医院名称及相关变体名称,重点检索该校所有医学与卫生领域临床试验注册信息;同时在中国临床试验注册中心(www.chictr.org.cn)和美国临床试验注册网站(clinicaltrials.gov)检索后,与上述结果逐条进行数据核对,并去除重复部分。
1.2 临床试验论文信息检索
在PubMed数据库中检索2012—2021年上海交大医学院作为第一或通信作者所在机构发表的临床研究论文。
1.3 统计学方法
采用健康研究分类系统(Health Research Classification System,HRCS)[2-3]和国际放射防护委员 会 (International Commission on Radiological Protection,ICRP)肿瘤分类标准[4]对注册临床试验进行分类。采用EXCEL 2016 软件对检索到的每条临床试验信息进行第一负责机构名称规范化处理,并按学科领域、疾病类型、肿瘤分类等对每项临床试验进行标注。采用VOSviewer 1.6.18 软件对检索到临床研究论文的主题分布、机构合作等情况进行可视化分析。
2 结果
2.1 2012—2021 年中国注册临床试验数在全球的占比
2012—2021 年全球新注册的临床试验项目总数为400 968 项。其中有中国研究人员参与的为54 652项,占全球总数的13.63%,位列全球第2位,仅次于美国的107 880 项。这10 年中,全球每年新注册的临床试验数逐年增长,但中国的临床试验数在2021 年后有所下降(图1)。
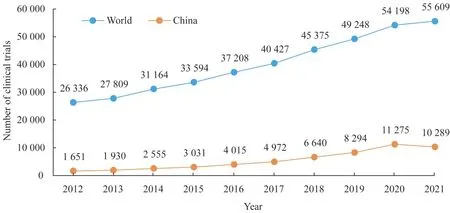
图1 2012—2021年全球与中国临床试验注册数Fig 1 Number of clinical trial registrations in the world and in China from 2012 to 2021
2.2 2012—2021年中国三大城市临床试验注册情况
2012—2021 年北京、上海、广州是中国开展临床试验研究最多的3 个城市。3 个城市的临床试验数量自2012 年起持续增长直至2020 年,然而在2021 年均出现不同程度的下降,其中上海的降幅较为明显(图2)。

图2 2012—2021年北京、上海与广州的临床试验注册数Fig 2 Number of clinical trial registrations in Beijing,Shanghai and Guangzhou from 2012 to 2021
2.3 2012—2021年上海交大医学院的临床试验项目
2012—2021 年上海交大医学院每年新注册的与在研的临床试验项目数基本呈现逐年递增趋势。在研临床试验由2012 年的104 项增加到2021 年的2 348项,但每年新注册的临床试验在2020 年上升至1 023项后,下降至2021年的620项(图3)。
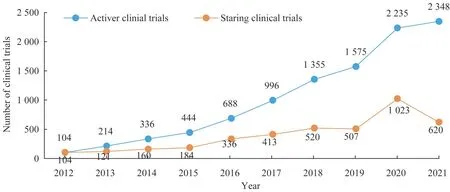
图3 2012—2021年上海交大医学院临床试验数Fig 3 Clinical trials of Shanghai Jiao Tong University School of Medicine(SJTUSM)from 2012 to 2021
2.4 2012—2021 年上海交大医学院注册临床试验学科分布情况
2012—2021 年上海交大医学院科研人员在国内外临床试验平台共注册3 970 项临床试验,其中44.4%在中国临床试验平台注册,55.0%在美国临床试验平台注册,在其他平台上注册的仅占0.6%;并且其中85.5%的临床试验由研究者发起。HRCS 是英国临床研究合作组织开发的用于对所有类型的健康研究进行分类和分析的标准[2-3]。本研究采用HRCS 分类标准对3 970 项临床试验进行分类,发现该校这10 年临床试验主要分布于20 个专业领域,数量最多的前5 位分别是肿瘤、心血管疾病、口腔与胃肠道疾病、精神疾病和代谢与内分泌系统疾病(图4)。
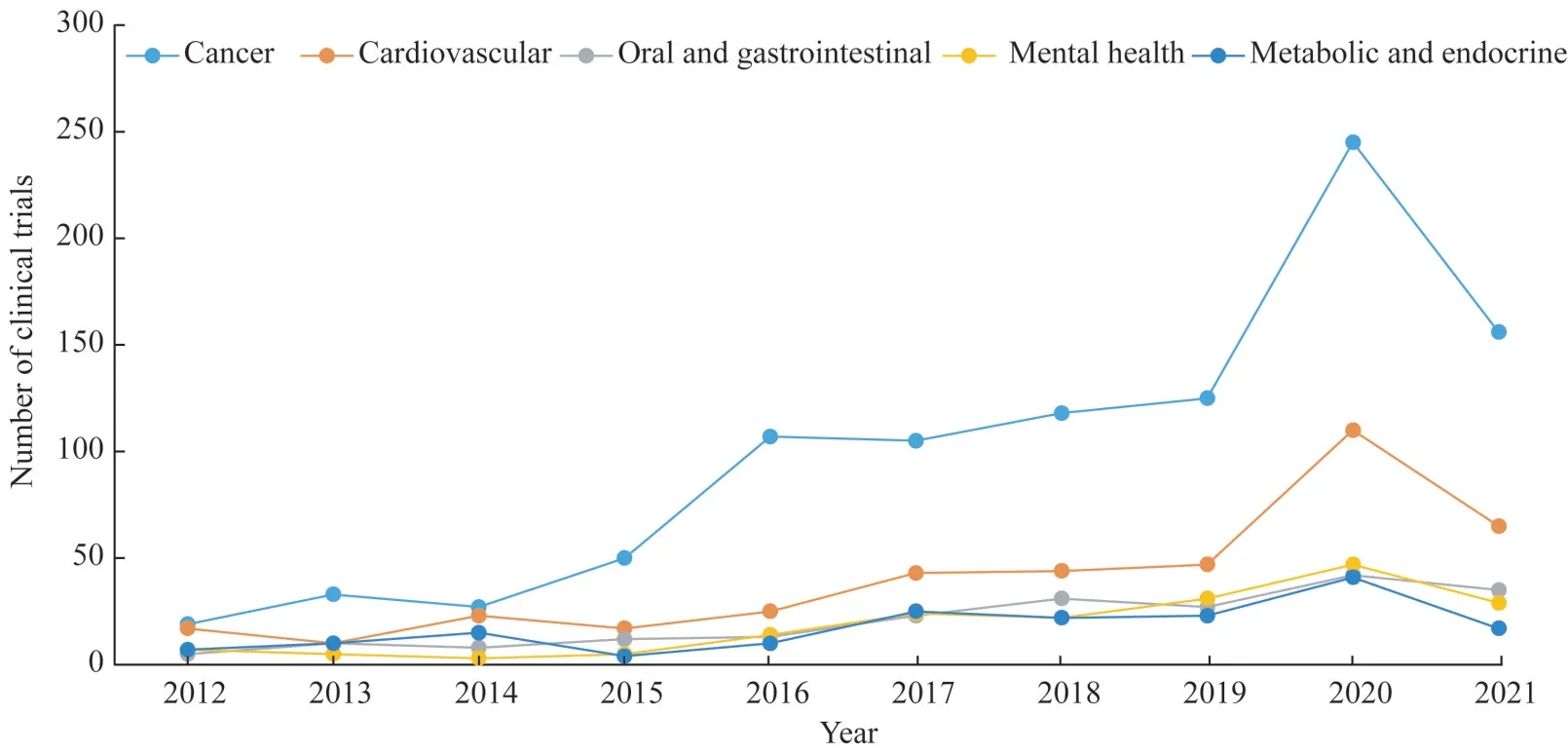
图4 2012—2021年上海交大医学院临床试验数量最多的前5个专业领域Fig 4 Top 5 professional fields with the largest number of clinical trial researches of SJTUSM from 2012 to 2021
2.5 2012—2021 年上海交大医学院肿瘤领域临床试验注册情况
肿瘤领域是临床试验的重要学科。采用ICRP 肿瘤分类标准[4]对2012—2021 年上海交大医学院注册开展的985 项肿瘤领域的临床试验进行分类发现,这些研究共涉及该标准中的47 种类型,其中肺癌的临床试验位列首位(图5)。按ICRP 分类的各类肿瘤的系统治疗研究共593 项,排名位居首位,其次是患者护理和生存分析、肿瘤发生与生物标志物研究等。
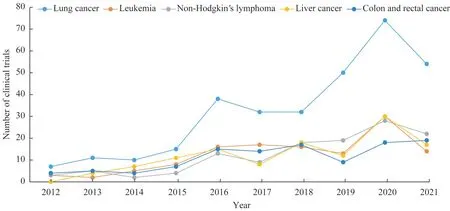
图5 2012—2021年上海交大医学院肿瘤临床试验数量排名的前5个类型Fig 5 Top 5 types of cancer clinical trials of SJTUSM from 2012 to 2021
2.6 2012—2021年各附属医院主持临床试验情况
2012—2021 年上海交大医学院开展的3 970 项临床试验中有2 817 项是各附属医院牵头注册的,占总数的71%;其中第六人民医院(六院)主持的临床试验最多,达523 项(图6),其次为瑞金医院和仁济医院。

图6 2012—2021年上海交大医学院各附属医院注册的临床试验数Fig 6 Number of registered clinical trials in affiliated hospitals of SJTUSM from 2012 to 2021
2.7 2012—2021年临床研究类论文主题分布
在PubMed数据库中检索2012—2021年上海交大医学院作者发表的论文共计60 075篇,其中以上海交大医学院为第一或通信作者的机构发文数为35 327篇,这些论文被标注为临床研究的为1 898 篇,占总数的5.4%。如图7所示,上述临床研究的主题分布在胃肠病、心脏病、肿瘤、放射、口腔正畸、糖尿病等领域,并且人工智能、新型冠状病毒肺炎疫情等正逐步成为近年来新兴的研究主题。
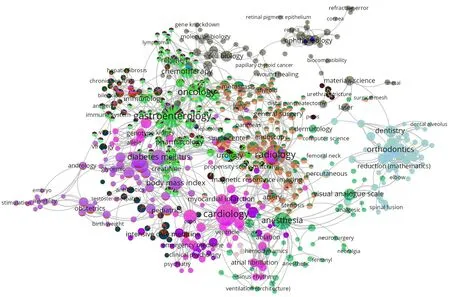
图7 2012—2021年上海交大医学院临床研究论文主题分布Fig 7 Themes of clinical research of SJTUSM from 2012 to 2021
2.8 2012—2021年临床试验论文合作机构分布
对2012—2021 年以上海交大医学院为第一或通信作者发表的1 898 篇临床试验研究论文的合作机构进行聚类分析发现,同城的复旦大学各附属医院是该校临床试验合作的主要机构,其次为北京大学、同济大学、海军军医大学、南京医科大学、中山大学、四川大学、中国科学院等,波士顿儿童医院、加州大学洛杉矶分校、梅奥诊所、香港大学则是上海交大医学院临床试验在中国大陆以外的主要合作机构(图8)。
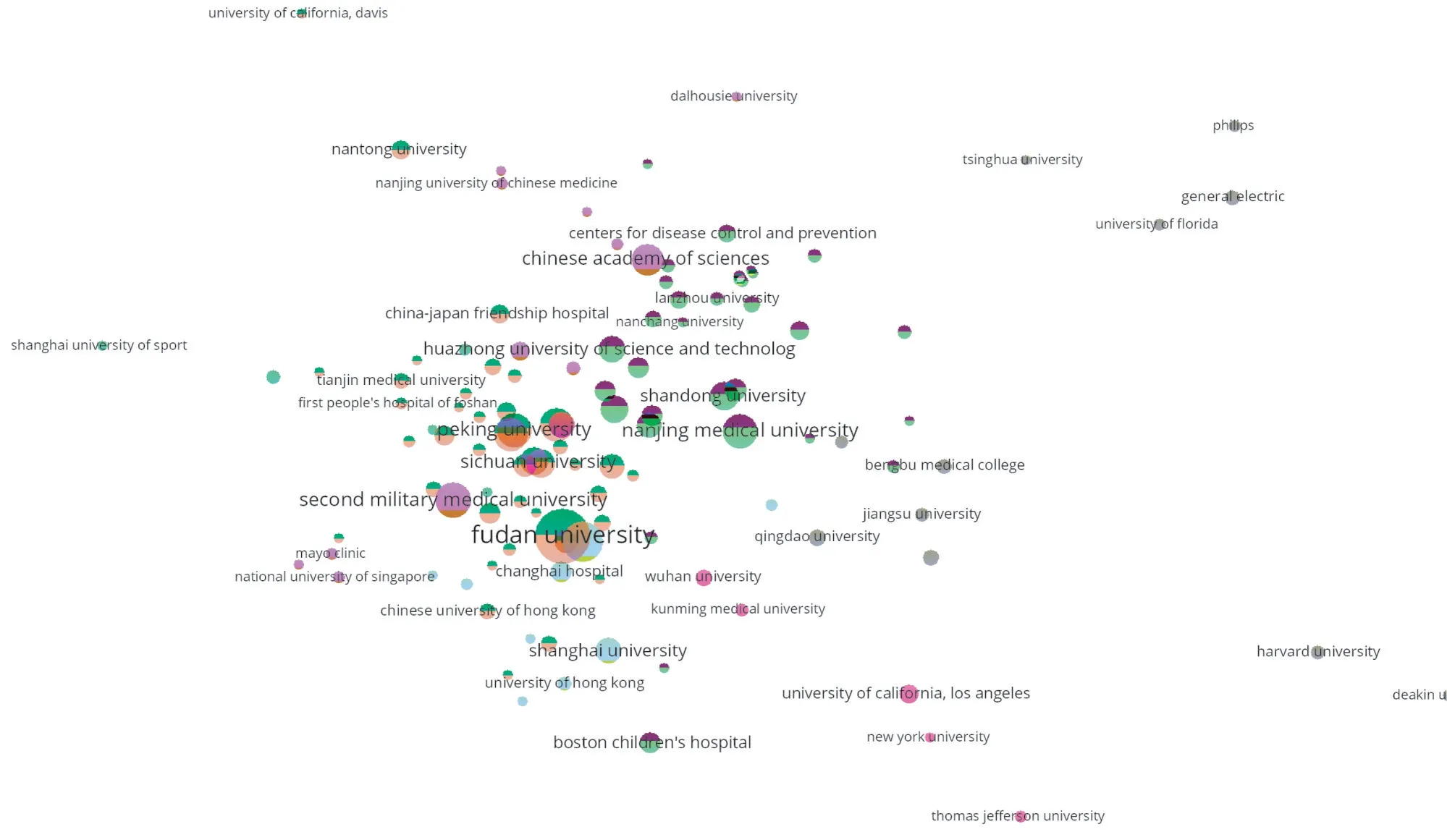
图8 2012—2021年上海交大医学院临床研究机构合作图谱Fig 8 Cooperative atlas of clinical research institutions with SJTUSM from 2012 to 2021
2.9 2012—2021年临床试验论文主要作者分布
如图9所示,对2012—2021年以上海交大医学院为第一或通信作者发表的1 898 篇临床试验研究论文的主要作者进行聚类分析发现,贾伟平、包玉倩、李燕、王继光、宁光、王卫庆、陈楠、张长青、许建荣、杨驰等在糖尿病、高血压以及骨科、放射科、肾脏科等领域已经形成核心研究团队。

图9 2012—2021年上海交大医学院临床论文主要作者研究领域分布Fig 9 Research fields distribution of main authors of clinical research in SJTUSM from 2012 to 2021
3 讨论
3.1 规范的临床试验是医学科研的重要环节
医学是一门源于实践、反馈实践的科学,临床试验是连接临床医学与生命科学以及生物技术的重要环节。美国国立卫生研究院(National Institutes of Health,NIH)在美国全国范围内设立临床研究中心,鼓励临床创新研究,加强对临床试验的管理[5]。包括2 名诺贝尔奖获得者在内的6 名科学家在2019 年提出了重振临床科学家计划[6]。临床研究也是我国医学界实现“原始创新”与提供“中国临床证据”的关键抓手。2012 年我国启动了国家临床医学研究中心的建设工作,至今已建设了50 个国家临床医学研究中心。国际临床试验注册制度旨在保障临床研究的质量和规范,促进研究结果透明化,降低医学论文发表的偏倚,增加研究过程的科学性和效能,并对受试者和研究者尽到伦理学义务。2004 年国际医学期刊编辑委员会发布声明,在《美国医学会杂志》《新英格兰医学杂志》等国际知名医学期刊上发表的临床试验文章必须经过临床试验注册[7]。受药品市场和研发全球化的影响,全球临床试验数量快速增长,越来越多的国际多中心临床试验在中国开展。我国学者注册的临床试验和发表的临床研究论文增长迅速,但相较于欧美等西方发达国家,我国的临床试验起步较晚,专业化、专职化临床试验研究者团队建设滞后,研究型临床医师相对短缺[8]。近年来上海申康医院发展中心成立了临床研究促进中心,积极推动本市三级甲等医院开展高质量临床研究。
3.2 上海交大医学院临床试验研究学科特点明显
本研究检索的临床试验注册平台汇集了中国、美国、欧盟、英国、日本、澳大利亚/新西兰、伊朗和印度8 个知名的临床试验注册系统的基本元数据。研究发现,2012—2021 年中国参与的临床试验占同期全球临床试验注册总数的13.63%,仅次于美国,列全球第2位。
上海交大医学院新注册开展的临床试验主要在中国和美国的临床试验注册平台进行注册,分别占总数的44.4%和55.0%,在其他临床注册平台上注册的临床试验仅占0.6%。对同期新注册的临床试验和已发表的临床试验研究论文进行学科主题分析,均显示除胃肠病学、心脏病学、肿瘤学、内分泌学与国内外研究的重点一致外,该校在放射学、口腔正畸学等领域也具有明显的学科优势,眼科学发展迅猛,在这些核心临床学科的带动下,相关关联学科群正逐步形成。同时图7 也显示人工智能、新型冠状病毒肺炎疫情等领域正逐步成为该校近年来新兴的研究主题,这也预示着该校在医工、医理交叉及疫情防控方面的学科布局正在取得一定的成绩。
3.3 多中心临床试验日益成为临床研究的主流
多中心临床试验(multi-regional clinical trial,MRCT)是指在多家临床研究中心同时招募受试者,此举可大幅提高研究效率,加速临床试验进度,相比单中心临床试验,其研究结论外推性更好[9]。近年来MRCT 已成为上海交大医学院临床试验研究的常态。图8显示近10年来以上海交大医学院为第一或通信作者所在机构发表的临床研究论文,除与复旦大学、北京大学、中科院等的众多国内医疗机构开展多中心研究外,也与梅奥诊所、波士顿儿童医院等国外著名医疗机构开展国际多中心合作。按照吴一龙教授对我国临床医师参与临床试验的3 个阶段划分,该校的临床试验研究目前已进入全面成长期[10],并且已在多个领域主导全球MRCT。
3.4 研究者发起的临床试验占主导地位,临床科研创新团队初步形成
临床试验按申办方不同分为两大类。一类是由制药企业发起的研究(industry sponsored trial,IST),以产品上市为目的,旨在对药物的安全性、有效性和不良反应进行客观、科学的评价,从而为药品审批提供重要依据。另一类研究的发起者并非商业实体,研究目的是基于临床工作中发现需要研究的科学问题,旨在扩展和优化现有的治疗;这类研究的发起者多是医疗机构的临床研究者,称为研究者发起的研究(investigator initiated trial,IIT)。近10 年来上海交大医学院开展的临床试验中85.5%由临床研究者发起,并且这一比例也在逐年上升,说明临床科研人员开展临床试验的主动性也在日益提升,这将推动临床科学家队伍的形成。图9 显示了已经形成的各学科领域临床科学家团队。此外,各附属医院间的临床创新科研合作日益紧密,有力地推动了上海交大医学院各临床学科的进一步发展;同时也发现部分学科跨院合作机制仍有发展前景,如瑞金医院与六院内分泌学科的团体合作仍有进一步提升的空间。
3.5 近年临床试验研究大幅下降原因有待进一步分析
2012—2021 年全球每年新注册的临床试验呈现稳步上升的趋势,但我国的临床试验数在2021 年则出现了小幅下降。分析其原因,可能是2020 年初的新型冠状病毒肺炎疫情带来了一波临床试验的增长。上海地区2020 年的临床试验注册数增幅尤其明显,这可能与上海申康医院发展中心的新一轮临床三年行动计划于2020 年启动有关,而在2021 年又回复到以往的水平。北京、上海、广州这3 个国内临床试验研究的主要城市也出现了不同程度的下降,但上海地区的降幅尤为明显。与此对应,2021 年上海交大医学院在研临床试验再创新高达到2 348 项的同时,2021年新注册临床试验数有较为明显的下降,具体原因有待进一步分析。
本研究虽然收集了上海交大医学院同期的临床试验注册信息及发表的临床研究论文,但两者之间并不存在完全的对应关系。因为据日本学者[11]调查发现大约有46.4%的注册临床试验并没有发表论文。大规模的临床试验是循证决策的基础,临床试验是一个广阔且不断发展的医学科研领域。本研究的结果可为今后交大医学院的临床学科发展布局与临床创新团队建设提供依据,也可为其他医药院校的临床研究提供参考。
利益冲突声明/Conflict of Interests
所有作者声明不存在利益冲突。
All authors disclose no relevant conflict of interests.
作者贡献/Authors'Contributions
仇晓春负责研究设计;彭树涛负责论文写作和修改。所有作者均阅读并同意最终稿件的提交。
The study was designed by QIU Xiaochun.The manuscript was drafted and revised by PENG Shutao.All the authors have read the last version of paper and consented for submission.
·Received:2022-06-16
·Accepted:2022-08-10
·Published online:2022-08-28
参·考·文·献
[1] 金丕焕,邓伟. 临床试验[M]. 上海:复旦大学出版社,2004.JIN P H, DENG W. Clinical trials[M]. Shanghai: Fudan University Press,2004.
[2] VUKUGAH T A,NTOH V N,AKOKU D A,et al. Research questions and priorities for pediatric tuberculosis:a survey of published systematic reviews and meta-analyses[J]. Tuberc Res Treat,2022,2022:1686047.
[3] UK Clinical Research Collaboration. Health Research Classification System[EB/OL]. [2022-04-20]. http://hrcsonline. net/wp-content/uploads/2018/01/HRCS_Main_Handbook_v2_Feb2018.pdf.
[4] 姚杏红,李勇,张怀文,等. 依据不同ICRP报告计算儿童全中枢神经系统放疗患者体内有效剂量的变化[J]. 实用癌症杂志, 2022,37(2):345-348.YAO X H, LI Y, ZHANG H W, et al. Comparsion of effective dose in pediatric patients with craniospinal irradiation according to different ICRP report[J]. Pract J Cancer,2022,37(2):345-348.
[5] PINCUS H A, ABEDIN Z, BLANK A E, et al. Evaluation and the NIH clinical and translational science awards: a "top ten" list[J].Eval Health Prof,2013,36(4):411-431.
[6] JAIN M K, CHEUNG V G, UTZ P J, et al. Saving the endangered physician-scientist: a plan for accelerating medical breakthroughs[J].N Engl J Med,2019,381(5):399-402.
[7] DE ANGELIS C,DRAZEN J M,FRIZELLE F A,et al. Clinical trial registration: a statement from the International Committee of Medical Journal Editors[J]. Lancet,2004,364(9438):911-912.
[8] 梁宇光,王谦,丁倩等. 关于加强临床试验研究者团队建设的对策探讨[J]. 中国食品药品监管,2021(10):34-39.LIANG Y G, WANG Q, DING Q, et al. Measures for enhancing clinical research investigator capability building[J]. China Food Drug Adm Mag,2021(10):34-39.
[9] International Conference on Harmonisation E9 Expert Working Group. ICH Harmonised Tripartite Guideline. Statistical principles for clinical trials[J]. Stat Med,1999,18(15):1905-1942.
[10] 罗娟. 国际多中心临床试验在中国:专访中国抗癌协会临床肿瘤协作专业委员会主任委员吴一龙教授[J]. 中国新药杂志, 2014,23(19):2210-2212.LUO J. International multicenter clinical trials in China:an exclusive interview with Professor WU Yilong, chairman of the professional committee of clinical oncology cooperation of the China Anti-Cancer Association[J]. Chin J New Drugs,2014,23(19):2210-2212.
[11] OCHI N, KAWAHARA T, NAGASAKI Y, et al. Publication of lung cancer clinical trials in the Japanese Clinical Trial Registry[J]. Jpn J Clin Oncol,2018,48(11):995-1000.
