铜离子的光电化学可视化检测新方法
2022-05-20张楠胡佩文郭双铭王莹杨红
张楠,胡佩文,郭双铭,王莹,杨红
(南京农业大学理学院/江苏省农药学重点实验室,江苏 南京 210095)
随着工业的发展,铜离子(Cu2+)的污染问题日益严重。高浓度的Cu2+会破坏水中的生物再处理系统,降低天然水体的自净能力,其随食物链的积累也威胁着动物和人类健康[1-3]。我国现行《农田灌溉水质标准:GB 5084—2021》和《生活饮用水卫生标准:GB 5749—2006》规定水体中的Cu2+浓度不得超过7.8和15.6 μmol·L-1[4-5]。因此,发展针对铜离子快速、灵敏的定量方法具有重要意义。传统的铜离子检测方法主要包括原子吸收分光光度法(AAS)[6]、电感耦合等离子体原子发射光谱法(ICP-AES)[7]、紫外-可见分光光度法(UV-vis)[8]、荧光分析法(FL)[9-10]、电化学分析法[11-12]等。其中,光学分析方法技术较为成熟,但面临仪器价格昂贵、操作要求高等问题。电化学分析法价格低廉、灵敏度高,但易受到背景噪声的影响,且无法直接观测结果。光电化学(PEC)分析法是PEC过程与传统电化学分析法的高效融合,继承了电化学分析法优势,同时由于其激发信号(光)和检测信号(电)分属不同的能量形式,因此具有更低的背景信号;与光学方法相比,具有设备简单、价格低廉、便携化程度高的优势,近年来引起了广泛关注[13-15]。
电致变色是材料的光学属性(透过率、反射率或吸收率)在外加电场作用下发生稳定、可逆颜色变化的现象,目前该技术已经应用于智能建筑[16-17]、显示器[18]、电池[19]、电容器[20]等领域。将PEC技术与电致变色技术相结合,利用光电活性材料在光照下产生的光电压或光电流使电致变色材料发生颜色变化,可以作为PEC信号的显示窗口,达到PEC可视化检测的目的[21-23]。目前,此类分析模式仅有少量应用于人体疾病标志物检测中[24-26],但在环境分析领域还未见报道。基于此,本文开发了一种PEC-可视化分析方法,用于Cu2+的直观、灵敏检测。以具有高光电活性的CdS QDs/TiO2NPs为工作电极,具有电致变色性能普鲁士蓝(PB)为对电极,构建PEC-可视化检测平台。样品中的Cu2+可以与CdS QDs发生反应,使PEC信号猝灭,同时引起PB的颜色变化,得到可视化信号。其中,可视化信号可以作为现场筛查的快速半定量依据,PEC信号可以为后续进一步分析提供更准确的数据。该平台的建立,可以为Cu2+的直观、快速、准确检测提供新方法,在多种场景下具有潜在的应用前景。
1 材料与方法
1.1 主要仪器与试剂
1.1.1 主要仪器电极微观形貌使用JEOL(日本电子株式会社)JSM-7800F场发射扫描电镜(SEM)和JEOL JEM-2100F场发射透射电子显微镜(TEM)进行表征。紫外可见漫反射光谱使用PELambda 950分光光度计(珀金埃尔默仪器有限公司)测定。X射线光电子能谱使用Thermo Scientific K-Alpha测定。管式炉(TL1200)购自南京博蕴通仪器科技有限公司。PEC测试使用波长为410 nm的5 W LED灯作为激发光源,通过CHI660E 电化学工作站(上海辰华仪器公司)计时安培模式下进行测定(0.1 V vs Ag/AgCl)。PB电极照片使用智能手机拍摄,各通道色彩值通过Adobe Photoshop软件分析得到。
1.1.2 主要试剂巯基己酸(TGA)、氯化镉(CdCl2·xH2O)、聚二烯丙基二甲基氯化铵(20%,Mw 200 000~350 000)购自西格玛奥德里奇(上海)贸易有限公司;氢氧化钠、九水合硫化钠、盐酸、硫代硫酸钠、氯化钾、硫酸铜、硼酸、磷酸氢二钠、磷酸二氢钠、铁氰化钾、三氯化铁六水合物、氟钛酸铵均为分析纯。稻田水采集自南京农业大学牌楼教学科研基地稻田。FTO导电玻璃(KV-FTO-R15)购自珠海凯为光电科技有限公司。
不同浓度CuSO4溶液、磷酸盐缓冲液(PBS,pH7.4)均用纯净水配制而成。
1.2 试验方法
1.2.1 电极的制备及表征CdS QDs/TiO2NPs电极的制备。1)TiO2NPs电极的制备:使用液相沉积法制备TiO2NPs电极。100 mL烧杯中加入等体积的0.1 mol·L-1(NH4)2TiF6溶液和0.3 mol·L-1H3BO3溶液,超声混匀。将FTO导电玻璃导电面朝内,沿烧杯壁竖直摆放,25 ℃反应48 h后水洗3次,在管式炉中 500 ℃煅烧1 h。2)CdS QDs的制备:使用溶胶凝胶法合成CdS QDs。100 mL三颈瓶中加入50 mL 0.01 mol·L-1CdCl2溶液、250 μL巯基乙酸,磁力搅拌下通氮气30 min,期间用1 mol·L-1NaOH溶液调节混合液的pH值为11;加入5 mL 0.1 mol·L-1Na2S溶液,110 ℃加热回流4 h。冷却至室温后,加入55 mL纯净水混合均匀,4 ℃保存。3)CdS QDs/TiO2NPs电极的制备:通过静电吸附层层组装法得到CdS QDs/TiO2NPs电极。将TiO2NPs电极依次浸入2% PDDA(含0.5 mol·L-1NaCl)溶液10 min,取出后用纯净水清洗,再浸入CdS QDs溶液中10 min,取出后用纯净水清洗。重复上述步骤4次。
PB电极的制备。将0.3 g KCl、0.08 g K3[Fe(CN)6]溶于30 mL纯净水中得到溶液A。将0.04 g FeCl3溶于30 mL纯净水,滴加2滴浓HCl得到溶液B。均匀混合A、B溶液后,添加40 mL纯净水,得到普鲁士蓝电解液。以Ag/AgCl电极为参比电极,Pt电极为对电极,FTO为工作电极,在普鲁士蓝电解液中进行电沉积。参数设置为低电压0.4 V,高电压0.8 V,扫描速率100 mV·s-1,25个循环,得到PB电极。
1.2.2 光电化学可视化复合平台的搭建如图1所示:以CdS QDs/TiO2NPs为工作电极,Pt电极为对电极,Ag/AgCl电极为参比电极,分别在0.01 mol·L-1PBS溶液、含0.1 mol·L-1KI的PBS溶液和含0.1 mol·L-1Na2S2O3的PBS溶液中测定光电流,选择合适的电解液。以CdS QDs/TiO2NPs为工作电极,PB电极为对电极,Ag/AgCl电极为参比电极,在0.1 V电压下、选定的电解液中,观察在300 s光照和非光照条件下PB电极的变色情况。Cu2+浓度测定方法:在CdS QDs/TiO2NPs电极上分别滴加25 μL浓度为0、10-7、10-6、10-5、10-4和10-3mol·L-1的Cu2+溶液,25 ℃ 孵化30 min后,纯净水清洗3次。以清洗后的电极为工作电极,PB电极为对电极,Ag/AgCl电极为参比电极,0.1 mol·L-1Na2S2O3溶液为电解液,记录光照300 s的光电流,以及PB电极的颜色变化。
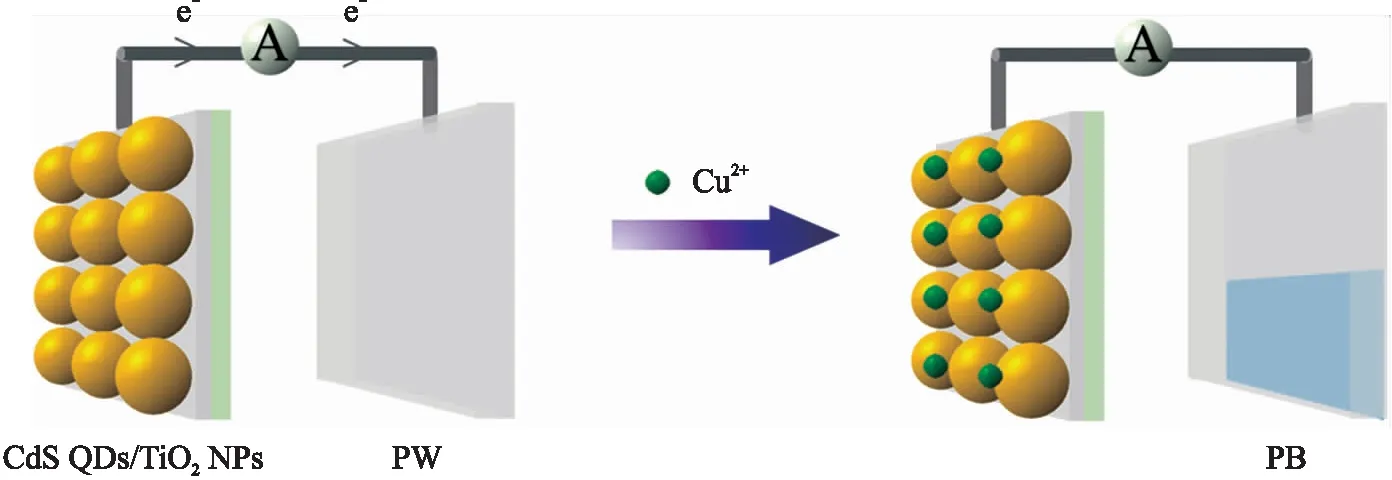
图1 PEC-可视化检测平台检测Cu2+机制示意图Fig.1 Schematic illustration of photoelectrochemical and visualized detection of Cu2+CdS QDs/TiO2 NPs为硫化镉量子点/二氧化钛纳米粒子复合电极,PW为普鲁士白,PB为普鲁士蓝。CdS QDs/TiO2 NPs is cadmium sulfide quantum dots,PW is Prussian white and PB is Prussian blue.
1.2.4 实际样品检测使用0.22 μm水相膜净化后的稻田水,分别配制0、10-6、10-5和10-4mol·L-1的Cu2+溶液,进行Cu2+的添加回收试验。
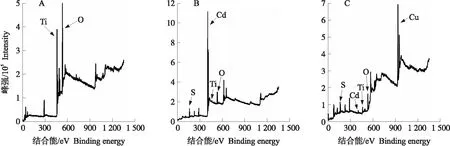
图2 TiO2 NPs电极在修饰前、后的X射线光电子能谱(XPS)Fig.2 X-ray photoelectron spectra(XPS)of TiO2 NPs electrode before and after modification A、B分别为CdS QDs修饰前、后TiO2 NPs电极的XPS表征;C为CdS QDs/TiO2 NPs电极在滴加10-3 mol·L-1 Cu2+后的XPS表征。A,B indicate XPS characterization of TiO2 NPs electrode before and after modification of CdS QDs,respectively;C indicates XPS characterization of CdS QDs/TiO2 NPs electrode after 10-3 mol·L-1 Cu2+ incubation.
2 结果与分析
2.1 CdS QDs/TiO2 NPs电极表征
用X射线光电子能谱(XPS)对修饰CdS QDs前、后的TiO2NPs电极进行表征,其光谱图和各元素的具体含量如图2和表1所示。可以看出,修饰CdS QDs前的TiO2电极分别在458.1和529.4 eV处有明显的尖峰,分别来自Ti和O,含量比例约为1∶2(27.58%和53.55%)。修饰CdS QDs后,162.1和404.1 eV处分别出现了2个新的峰,判断来自S和Cd,含量比例约为1∶1(23.12%和26.18%),分别与其化学组成相符。同时,原有的Ti峰和O峰的强度明显降低,证明了CdS QDs在TiO2NPs电极上成功修饰。
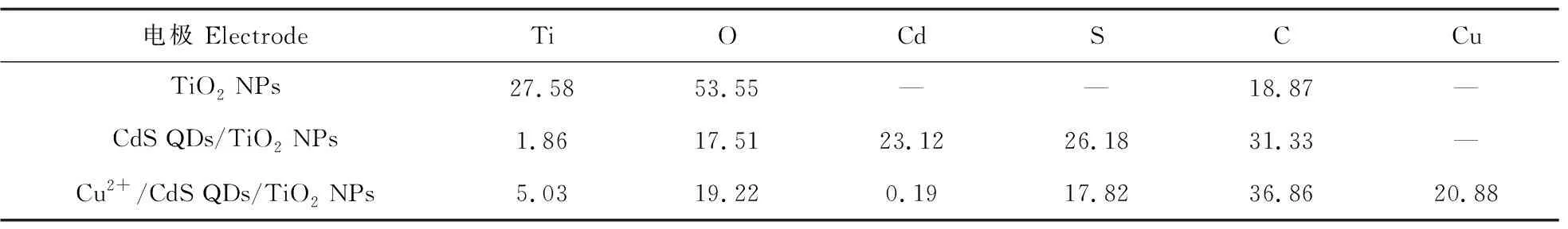
表1 TiO2 NPs电极在修饰CdS QDs前、后及CdS QDs/TiO2 NPs电极在滴加10-3 mol·L-1 Cu2+前、后表面元素的含量
使用透射电镜(TEM)和紫外可见吸收光谱(UV-vis)对CdS QDs进行表征(图3-A、B),可以看出,CdS QDs粒径约为5 nm,其溶液在502 nm前的可见光区有明显吸收。CdS QDs/TiO2NPs电极的扫描电镜(SEM)显示,液相沉积法制备的TiO2NPs直径约为20 nm,在FTO表面分布均匀,排列紧凑(图3-C);CdS QDs以三维网状的形态附着在TiO2电极上,形貌均一,覆盖率高,其颗粒与溶液态相比,有一定程度的团聚(图3-D)。
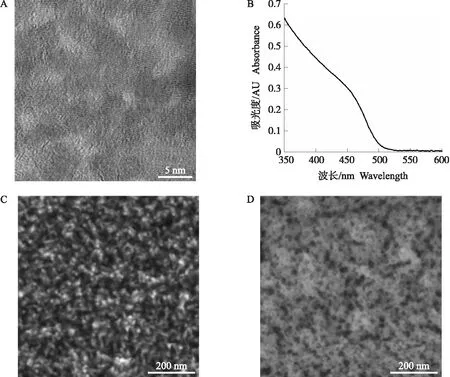
图3 CdS QDs/TiO2 NPs电极制备过程的形貌及光吸收表征Fig.3 Morphology and UV-vis absorption spectrum of the fabricated CdS QDs/TiO2 NPs electrode A、B分别为CdS QDs的TEM表征和UV-vis吸收谱;C、D分别为TiO2 NPs和CdS QDs/TiO2 NPs电极的SEM表征。A,B indicate TEM image and UV-vis absorption spectrum of CdS QD;C,D indicate SEM images of TiO2 NPs electrode and CdS QDs/TiO2 NPs electrode,respectively.
2.2 PB电极表征
通过循环伏安法制备的PB电极呈蓝色透明状,对其进行紫外-可见漫反射谱表征,可知该电极的吸收峰在697 nm处(图4-A)。通过SEM对其微观形貌进行考察,电沉积合成的PB电极表面相对平滑、均匀,无明显颗粒状(图4-B)。
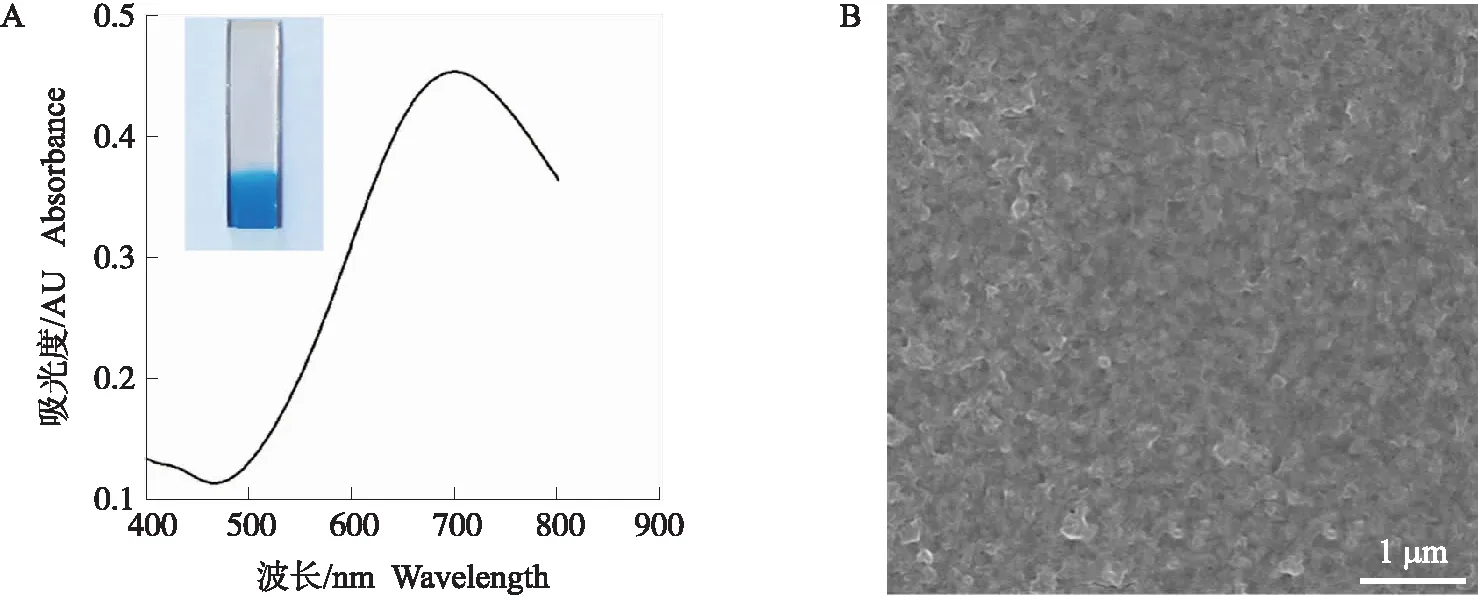
图4 PB电极的UV-vis漫反射吸收光谱(A)及 SEM表征图(B)Fig.4 UV-vis diffuse-reflectance spectrum(A)and SEM image of PB electrode(B)
2.3 条件优化与光电化学-可视化复合平台的搭建
以CdS QDs/TiO2NPs电极为工作电极,PB为对电极,Ag/AgCl电极为参比电极,分别在PBS溶液、含0.1 mol·L-1KI的PBS溶液和含0.1 mol·L-1Na2S2O3的PBS溶液中测定光电流,结果如图5-A所示,电极的光电流分别为8.7、23.4和51.9 μA;在0.1 mol·L-1Na2S2O3溶液中,光电流最大,因此后续测定选用含0.1 mol·L-1Na2S2O3的PBS溶液作为电解液。
在该溶液中,测定了修饰CdS QDs前、后TiO2电极的光电流变化,结果如图5-B所示。复合前光电流为5.8 μA,复合后光电流上升至52.0 μA。这是由于TiO2是宽禁带半导体,无法有效利用可见光,而 CdS QDs 作为窄禁带半导体,在可见光区有较大的吸收,且与TiO2NPs电极可以组成有效的异质结,加速光生电子的转移[27-28]。由于光电流是后续电致变色过程的驱动力,因此选用PEC响应更强的CdS QDs/TiO2NPs 电极作为后续工作电极。
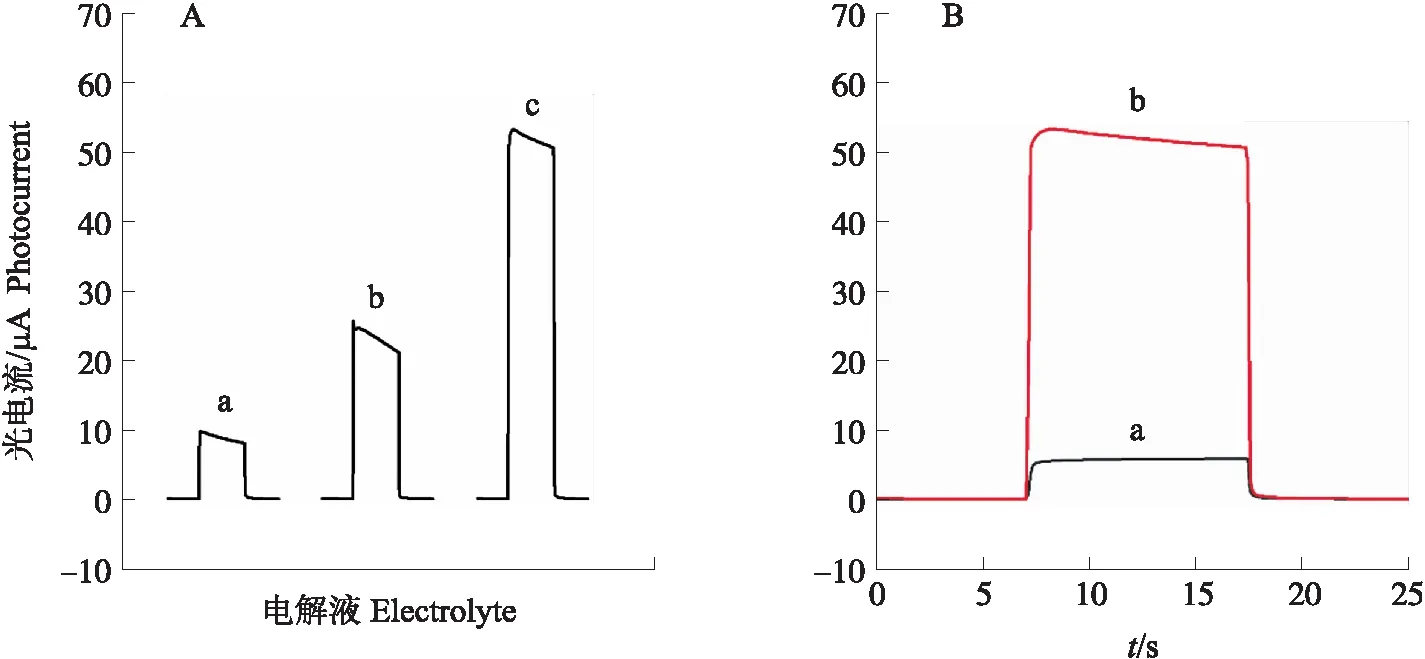
图5 电解液的优化及CdS QDs/TiO2 NPs电极制备过程的光电流变化Fig.5 Electrolyte optimization and photocurrent change of the working electrode A. CdS QDs/TiO2 NPs电极在PBS溶液(a)、含0.1 mol·L-1 KI的PBS溶液(b)和含0.1 mol·L-1 Na2S2O3的PBS溶液(c)中的光电流;B.TiO2 NPs电极(a)和CdS QDs/TiO2 NPs电极(b)在含0.1 mol·L-1 Na2S2O3的PBS溶液中的光电流。A. Photocurrent of CdS QDs/TiO2 NPs electrode in PBS(a),PBS containing 0.1 mol·L-1 KI(b),and PBS containing 0.1 mol·L-1 Na2S2O3(c);B. Photocurrent of TiO2 NPs electrode(a)and CdS QDs/TiO2 NPs electrode in PBS containing 0.1 mol·L-1 Na2S2O3(b).
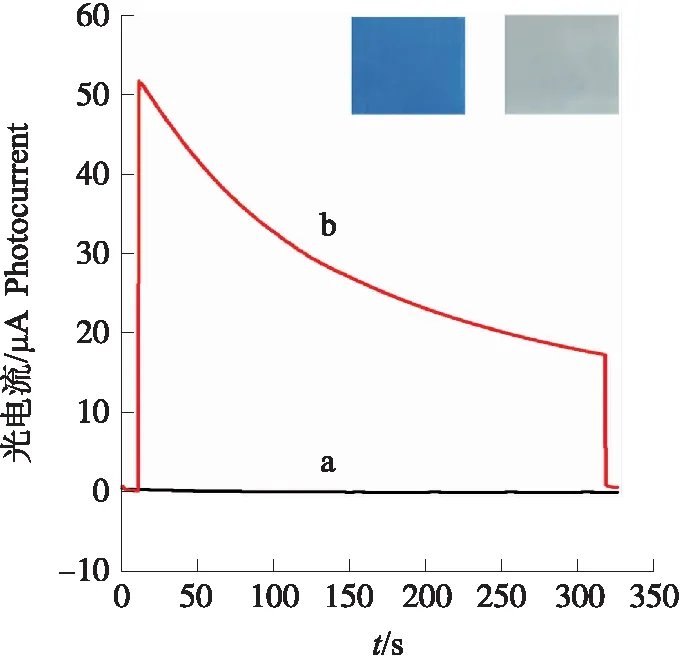
图6 PEC-可视化检测平台在410 nm光照前、后的信号变化Fig.6 Signal change of the PEC-visualized detection platform before and after 410 nm light irradiation a. 光照前;b. 光照后。PB电极的颜色变化(左侧光照前,右侧光照后)。a. Before light irradiation;b. After light irradiation. The color of PB electrode before(inset left)and after(inset right)410 nm light irradiation.
在优化条件下,以PB电极为对电极,Ag/AgCl电极为参比电极,410 nm入射光照射300 s,并以100 s处的光电流值作为记录标准,同时观察PB电极光照前、后的变色情况(图6)。CdS QDs/TiO2NPs电极在无光照条件下的光电流几乎为零,光照条件下光电流为32.6 μA。在该光电流的驱使下,PB电极可以达到褪色的效果。在这一过程中,PB被还原为PW,从而表现出无色透明状(公式1)[29-30]。而在非光照条件下,光电流为0,PB电极的颜色保持蓝色不变,表明PB电极可以作为工作电极的光电流的指示窗口,其颜色深浅可以作为光电流大小的直观表示。因此,完成了对PEC-可视化复合平台的搭建。
[FeⅢFeⅡ(CN)6]-+e-=[FeⅡFeⅡ(CN)6]2-
(1)
PB(蓝色) PW(无色)
2.4 光电化学-可视化平台检测铜离子
在CdS QDs/TiO2NPs电极的工作区域滴加10-3mol·L-1的Cu2+,记录滴加反应前、后的光电流变化(图7-A)。滴加Cu2+后,CdS QDs/TiO2NPs电极的光电流由32.6 μA下降至5.0 μA,猝灭率为84.6%。这是由于Cu2+与CdS QDs发生沉淀转化反应,生成溶度积更小的CuxS(pKsp=35.2)。新生成的CuxS在CdS QDs的禁带中引入了杂质能级,作为光生电子-空穴对的复合中心,从而阻断了 CdS QDs的光生电子向TiO2NPs传递,导致光电流的猝灭[31]。CuxS的形成,可以通过XPS谱图931.2 eV处的Cu峰(图3-C)及电极表面Cd、Cu元素含量变化(表1)得到佐证。
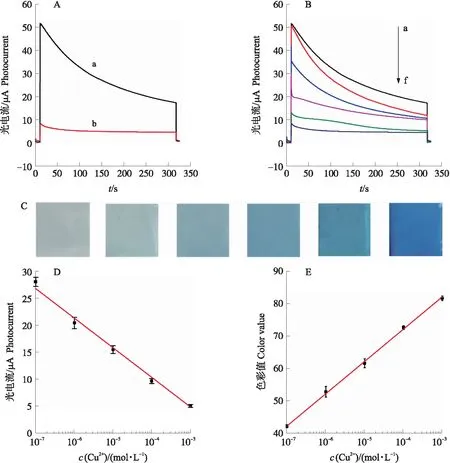
图7 PEC-可视化检测平台检测Cu2+Fig.7 Cu2+ analysis based on PEC-visualized detection platform A. 滴加10-3 mol·L-1 Cu2+前(a)、后(b)的光电流;B. 滴加0、10-7、10-6、10-5、10-4和10-3mol·L-1 Cu2+后(a—f)的光电流;C. 分别滴加0、10-7、10-6、10-5、10-4和10-3mol·L-1 Cu2+(从左至右)后PB电极的照片;D. 光电流值与Cu2+浓度的线性关系;E. PB电极照片中C通道色彩强度与Cu2+浓度的线性关系。A. Photocurrent of PEC-visualized detection platform before(a)and after(b)incubation of 10-3 mol·L-1 Cu2+;B. Photocurrent after incubation with 0,10-7,10-6,10-5,10-4 and 10-3mol·L-1 Cu2+(a-f);C. Digital photograph of PB electrode after incubation of 0,10-7,10-6,10-5,10-4 and 10-3 mol·L-1 Cu2+(from left to right);D. Linear relationship between photocurrent and Cu2+ concentration;E. Linear relationship between color value of PB electrode and Cu2+ concentration.
进一步改变滴加在电极表面的Cu2+浓度,记录产生的光电流(图7-B)。随着Cu2+浓度的增加,光电流逐渐减小,且其数值和Cu2+浓度的对数呈线性关系(图7-D),线性方程为I=-5.5×lg[c(Cu2+)]-11.6,线性相关系数R2=0.992,检测范围为10-7~10-3mol·L-1。使用3次测定空白样所得响应值的标准偏差3倍,带入上述线性方程,得检测限0.016 μmol·L-1,而我国现行《农田灌溉水质标准:GB 5084—2021》和《生活饮用水卫生标准:GB 5749—2006》规定水体中的Cu2+浓度阈值分别为7.8和15.6 μmol·L-1[4-5],本方法可以满足实际检测需求。
在获得PEC信号的同时,观察PB电极的颜色变化情况并用拍照记录(图7-C)。随着Cu2+浓度的增加,PB电极颜色逐渐加深。进一步使用Adobe Photoshop软件对照片中的电极区域的色彩进行数据化分析,在CMYK色彩模式下,C通道的色彩强度与Cu2+浓度的对数值呈线性关系(图7-E),线性方程为Cv=10.0×lg[c(Cu2+)]+112.0,线性相关系数R2=0.994。检测范围为10-7~10-3mol·L-1。即建立了Cu2+浓度的比色卡,实现了可视化检测。
2.5 选择性及干扰离子验证
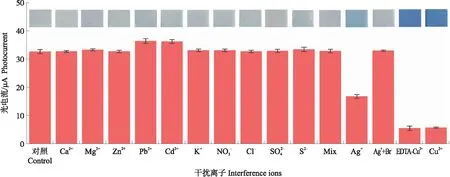
图8 PEC-可视化检测平台的抗干扰能力评价Fig.8 Selectivity performance towards Cu2+ 干扰离子依次为的混合溶液)、Ag+、(Ag++Br-)、(EDTA-Cu2+),所有离子(包括Br-和EDTA)浓度均为10-3 mol·L-1。Interference ions include of(Ca2+,Mg2+,K+),Ag+,(Ag++Br-),(EDTA-Cu2+). All the concentrations of the other ions are 10-3 mol·L-1.

图9 稻田水中Cu2+浓度的可视化检测结果Fig.9 Visualized signal of Cu2+ in paddy water从左至右Cu2+添加量依次为0、10-4、10-5和10-6 mol·L-1。The added concentration of Cu2+ from left to right is 0,10-4,10-5 and 10-6 mol·L-1.
2.6 稻田水中Cu2+浓度的测定
选用稻田水为基质,使用加入法对稻田水中的Cu2+浓度进行检测。首先通过可视化结果(图9)进行直观判断和初步筛查,可以看出颜色最深,即浓度最大的是左二样品;对照比色卡得出4个样品中Cu2+浓度依次约为0、10-4、10-5和10-6mol·L-1。结合PEC信号(表2)进一步分析可知,当基质中的Cu2+浓度为0、10-4、10-5和10-6mol·L-1时,回收率为92.3%~103.5%,相对标准偏差在4.7%~6.5%。该结果表明PEC-可视化复合平台可以实现以稻田水为代表的实际样品基质中Cu2+浓度的检测,可视化信号可以进行直观、快速判断,PEC信号能够提供更精确的检测结果。

表2 稻田水中Cu2+浓度的添加回收率Table 2 Spiked recoveries of Cu2+ in paddy water
3 结论
本文报道了一种新型PEC-可视化检测平台,实现了Cu2+浓度的直观、灵敏检测。在优化条件下,具有高光电活性的CdS QDs/TiO2NPs电极在可见光激发下产生的光电流可以驱动PB电极完全褪色,使PB电极作为PEC信号的可视化显示窗口。样品中的Cu2+可以与CdS QDs发生反应,猝灭光电流,同时使PB电极呈现出深浅不同的颜色变化。据此建立了比色卡,实现了Cu2+浓度的PEC-可视化双模式检测。其中,可视化信号作为直观的快速判断依据,适用于批量样品的筛查;PEC信号提供更精确的数据,便于进一步分析。该检测平台的建立,为Cu2+浓度的多场景检测提供了新的范式,也为未来多样化的环境污染物检测提供了有力借鉴。
