基于网络药理学探讨毛兰素抗肿瘤作用机制研究
2022-01-11梁若飞张亚兰唐晓平
梁若飞,张亚兰,向 月,唐晓平
(川北医学院附属医院神经外科1,病理科2,四川 南充 637002)
利用现代科技手段从传统中药中筛选新的广谱、高效的抗肿瘤药物已成为近年来科研工作者的研究热点。毛兰素(erianin)是从中药石斛中分离提取出来的单体,其化学名称是2-甲氧基-5-[2-(3,4,5-三甲氧基-苯基)-乙基]-苯酚(分子量为318.36)。目前已有研究发现[1-4],毛兰素对包括膀胱癌、鼻咽癌及肺癌等在内的多种肿瘤细胞表现出抗肿瘤作用。本研究以毛兰素为研究对象,利用网络药理学对其潜在作用靶点进行预测筛选并分析,一方面,希望为毛兰素的药理作用机制研究提供新思路,另一方面,为寻找毛兰素的潜在抗肿瘤机制提供参考。
1 材料与方法
1.1 毛兰素作用靶点预测 在Pubchem[5]查询毛兰素信息,打开相应的条目,下载毛兰素2D 结构,保存为“sdf”格式。将毛兰素2D 结构导入HT Docking 数据库中(https://www.cbligand.org/HTDocking/search_struct.php)进行基于蛋白结构特征的反向分子对接的潜在靶点的预测,选取Docking Score>7.8 靶点进行后续分析。
1.2 毛兰素作用靶点相关通路富集分析 排除非人靶蛋白后利用Uniprot[6]查询所获取的相关靶蛋白对应的基因名,进行检索和整理。运用Cytoscape 软件[7]中ClueGO 分析插件,对上述靶蛋白对应的基因信息进行KEGG 通路富集分析,设定阈值P<0.05。
1.3 蛋白质相互作用关系分析 将毛兰素治疗靶点信息上传至蛋白质相互作用网络分析网站Gene-MANIA[8],构建蛋白质相互作用网络。
1.4 统计学方法 通过Cytoscape 软件中ClueGO 分析插件对蛋白对应的基因信息进行KEGG 通路富集分析,统计检验采用超几何富集分析Enrichment(Two-sided Hypergeometric test),校正方法采用多重比较Bonferroni step down,当P<0.05 表示差异有统计学意义。
2 结果
2.1 毛兰素预测靶点信息分析 根据筛选条件,将毛兰素2D 结构导入HT Docking 数据库中,最终得到毛兰素2D 结构所对应的101 种人源潜在靶蛋白,见表1。
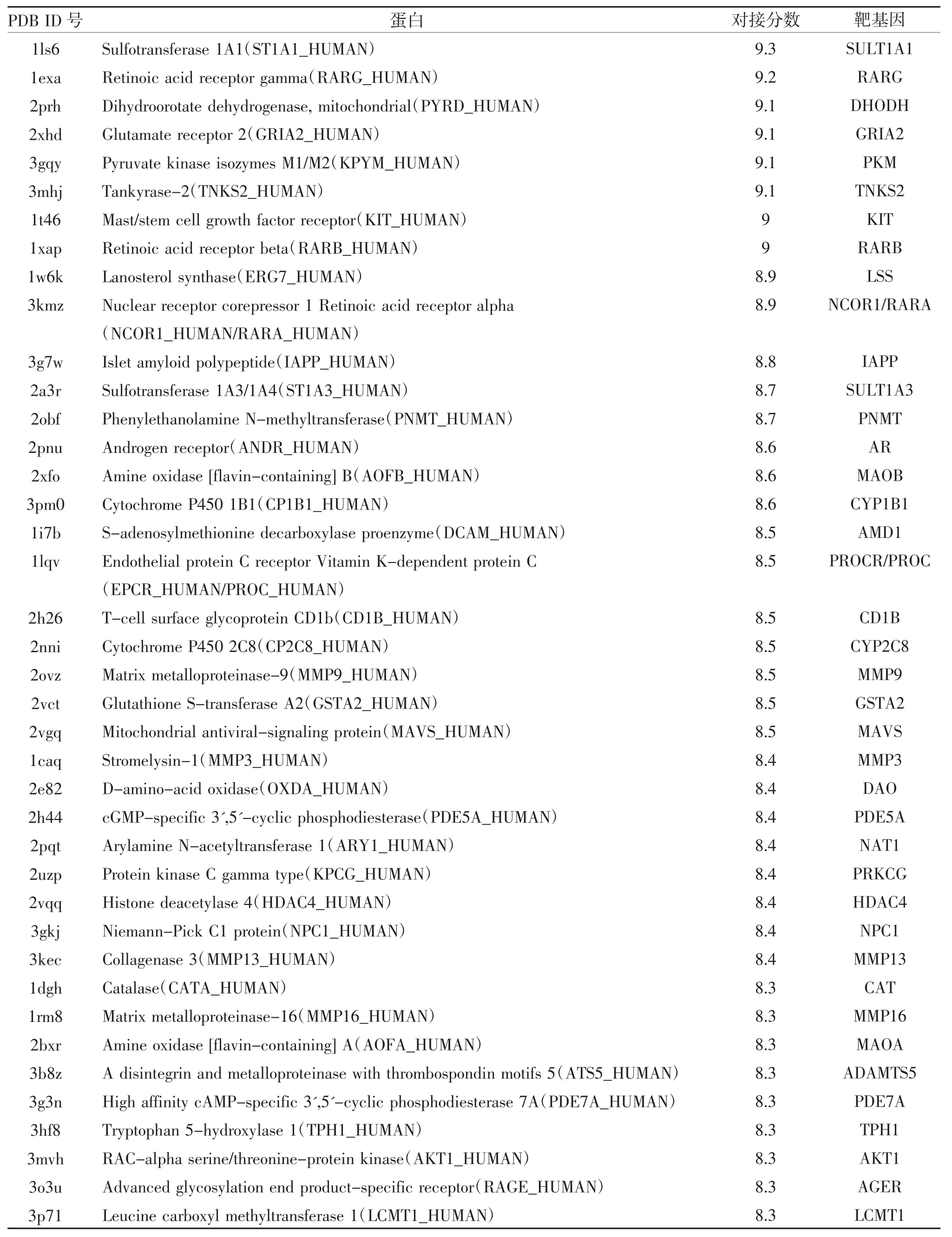
表1 毛兰素预测靶点信息

表1(续)
2.2 毛兰素作用靶点相关通路富集分析 运用Cytoscape 软件对将上述靶蛋白对应的基因信息进行KEGG 通路富集分析,结果显示毛兰素直接作用靶点参与13 条肿瘤相关通路,包括肿瘤通路、胶质瘤通路、前列腺癌通路、膀胱癌通路、胃癌通路、结直肠癌通路、胰腺癌通路、非小细胞肺癌通路、子宫内膜癌通路、癌症蛋白聚糖通路、癌症中心碳代谢通路、癌症胆碱代谢通路及急性髓性白血病通路,见表2、图1。

图1 毛兰素作用靶点KEGG 信号通路富集图

表2 毛兰素作用靶点KEGG 通路富集的基因情况
2.3 蛋白质相互作用关系分析 蛋白之间相互作用主要通过基因相关性、共享蛋白域、物理相关性、共定位、预测、蛋白共表达及通路表现出来。将毛兰素作用靶点信息上传至蛋白质相互作用网络分析网站GeneMANIA,构建蛋白质相互作用网络图,其中基因相关性占30.45%、预测占26.99%、共享蛋白域占15.69%、物理相关性占11.58%、共定位占5.99%、蛋白共表达占5.14%、通路占4.15%,见图2。

图2 毛兰素靶点蛋白交互作用图
3 讨论
中药单体一直是新药研发的重要来源,尤其在肿瘤药物研发方面。尽管近年来大量相关研究证实中药单体具有广泛的药理学和生物学活性,但如何快捷有效地寻找其潜在作用靶点及机制成为广大研究者们的困扰。中药往往具备多靶点、多途径、多环节的药理特性,目前虽然已有基因芯片等技术应用于中药靶点的筛选研究,但由于其价格相对较高且周期较长,在一定程度上限制了其在中药研究中的应用。然而,随着生物医学公共数据库的不断发展完善,网络药理学应运而生,其为阐明中药单体及复方的作用机制开辟了一条新途径[9-12]。网络药理学作为一门新兴学科,其主要是针对生物系统的网络进行综合分析,并选取特定的信号节点,从而进行多靶点药物分子设计[13-16]。运用网络药理学进行分析,不仅能够了解中药单体在不同疾病中的作用,而且也能了解其在同一种疾病中的多种作用机制,这大大节省了前期研究成本及时间。
近年来研究表明毛兰素具有一定的抗肿瘤作用。Zhu Q 等[1]研究发现,毛兰素能通过线粒体凋亡途径和JNK 途径抑制膀胱癌细胞的生长。Liu YT等[2]研究报道,毛兰素能通过ERK 途径诱导鼻咽癌细胞的凋亡。Zhang H 等[3]通过体内外实验发现毛兰素能抑制肺癌细胞的增殖,并将其细胞周期阻滞于G2/M 期。同时,Li M 等[17]研究发现,毛兰素能够阻止宫颈癌HeLa 细胞的生长,并诱导其发生凋亡和阻止其细胞周期于G2/M 期。Wang Y 等[18]研究发现,毛兰素能通过HRAS/PI3K/AKT 信号通路抑制胃癌的癌前病变进展。Sun Y 等[19]研究发现,毛兰素可以抑制结直肠癌细胞的生长并促进巨噬细胞介导的吞噬作用。Zhang X 等[20]通过体内外实验发现,毛兰素具有抗肝癌的作用,其机制主要与毛兰素对氧化应激介导的线粒体凋亡和免疫反应的调节有关。本研究利用网络药理学对毛兰素的潜在靶蛋白进行了虚拟筛选,结果显示毛兰素潜在作用靶蛋白共101 个。同时,进一步探讨了其KEGG 通路,其中有13 条通路与肿瘤相关。蛋白之间相互作用主要通过基因相关性、共享蛋白域、物理相关性、共定位、预测、蛋白共表达及通路表现出来。蛋白质相互作用网络分析显示,基因相关性占30.45%、预测占26.99%、共享蛋白域占15.69%、物理相关性占11.58%、共定位占5.99%、蛋白共表达占5.14%、通路占4.15%,表明毛兰素是一个潜在的通过多靶点治疗多种肿瘤的新的中药单体,其中AKT1 作为一种致癌基因,是AKT家族中的重要成员之一,在肿瘤细胞的增殖、侵袭、迁移等生物学过程中起着重要作用。而CDK6 作为一种调控细胞周期的重要因子,在多种恶性肿瘤中异常表达,与肿瘤的演进过程密切相关。本研究结果为后续毛兰素抗肿瘤实验研究提供了理论参考和指导方向。
综上所述,毛兰素通过AKT1、CDK6、AR、BRAF、CSF1R、DAPK1 等靶点发挥抗肿瘤效应,这些靶点参与13 条肿瘤相关通路,本研究为进一步深入探讨毛兰素抗肿瘤作用机制奠定了理论基础。
