高级别胶质瘤术后同步放化疗+替莫唑胺长周期辅助化疗的研究
2021-07-20龚巧英熊文敏吴新生彭世义李国庆
龚巧英 熊文敏 吴新生 彭世义 李国庆
间变型星形细胞瘤及胶质母细胞瘤统称为“高级别胶质瘤”,各个指南均推荐最大限度地安全切除肿瘤[1],术后结合放疗、化疗、电场[2]治疗等综合治疗方法[3]。手术切除是影响预后的重要因素[4-6]。术后复发概率高,主要复发模式为局部复发,约80%的复发病灶发生在原发灶周围2 cm之内。所以术后放疗可以提高高级别胶质瘤的疗效。术后开始放疗的时间与高级别胶质瘤的生存期明显相关,术后更早开始放疗,生存期更长[7]。局部放疗与全脑放疗的疗效相近,放射性中枢神经毒副作用明显降低[8]。目前对于新诊断的高级别胶质瘤均采用3D-CRT或IMRT技术进行局部放疗且多个研究发现更高剂量的放射治疗并不能改善术后患者的PFS和OS。应用放射外科或腔内后装加量与常规的外照射相比较并无任何生存优势,且放射性脑坏死的发生率明显升高[9-10]。目前对于高级别胶质瘤放疗剂量仍推荐60 Gy/30次左右。
STUPP方案[11-12]被美国NCCN指南、加拿大GBM共识、英国卫生与临床优秀成果研究所(NICE)以及澳大利亚成人胶质瘤临床诊疗指南推荐,目前被认为是新诊断的胶质母细胞瘤的标准治疗方案。但是高级别胶质瘤患者在完成标准STUPP方案后绝大部分仍会出现复发,那么延长辅助性化疗后对肿瘤是否能够更好的控制呢?
本文研究延长TMZ辅助性化疗的周期是否可以进一步提高高级别胶质瘤的疗效,患者的毒副作用能否耐受。
1 资料与方法
1.1 临床资料
2017年1月至2018年12月我院收治的具有完整随访信息的高级别胶质瘤患者45例,男性29例,女性16例,男女比例1.8∶1;发病年龄为14~71岁,中位年龄49岁,平均年龄49.7岁,所有病例均通过手术方式获得病理, 17例为间变性星形细胞瘤,28例为胶质母细胞瘤。
1.2 治疗
45例患者中24例接受颅脑肿瘤全切术,16例接受颅脑肿瘤部分切术,5例接受立体定向活检术;所有患者均在手术后4周左右开始接受术后放疗+同期替莫唑胺化疗;照射范围为原瘤床+1~2 cm,应用三维适形调强放疗技术,放疗剂量为64~60 Gy/30次,替莫唑胺75 mg/m2,qd×42天,随后每4周开始行替莫唑胺150~200 mg/m2,5/28 d的辅助化疗。
1.3 疗效评价
每1~3个月复查颅脑MRI平扫+增强及波谱分析。影像学出现可疑进展,可继续服用化疗密切观察,如后期明确为真性进展,逆推至可疑时间为复发时间。
1.4 辅助性化疗周期计数
辅助性化疗周期计数为同期放化疗后至肿瘤复发、患者无法耐受或拒绝继续服用为止。影像学检查确定为真性进展,逆推至可疑进展后服用的化疗周期数均不列入辅助性化疗周期计数。
1.5 随访方式
采用门诊随访、电话回访等方式随访,随访截止至2020年12月31日。
1.6 统计方法
应用SPSS 25.0软件进行统计分析,生存分析用Kaplan-Meier法绘制生存曲线,P<0.05为差异有统计学意义。
2 结果
45例患者中替莫唑胺辅助周期数为2~24个周期,24例辅助周期数≤6个周期的,21例辅助周期数>6个周期,18例辅助周期数≥9个周期,8例辅助周期数≥12个周期。中位周期数为6个周期,平均7.6个周期。其中11位患者在辅助性化疗期间出现肿瘤进展,虽然继续进行替莫唑胺化疗但肿瘤进展后化疗周期不计入辅助化疗周期数中。随访时间7.4~48个月,中位随访时间18.3个月。随访中34例患者发生进展,27例患者死亡,其中3例因非肿瘤原因死亡,使用Kaplan-Meier生存分析本研究中≤6个周期辅助性化疗的中位PFS为11.6个月,>6个周期辅助性化疗的中位PFS为18个月,P=0.001,有显著性差异(图1);≤6个周期辅助性化疗的中位OS为18.5个月,>6个周期辅助性化疗的中位OS为25.6个月,P=0.004,有显著性差异(图2);在其中对≤6个周期、6<化疗周期数≤9、>9个周期进行分层分析,≤6个周期的中位PFS为10.3个月,中位OS为18.5个月,6<化疗周期数≤9的中位PFS为14个月,中位OS为18.2个月,>9个周期的中位PFS为27.8个月,中位OS为27.5个月,P=0.001/0.002,均有显著性差异(图3,图4);13.3%(6/45)的患者出现Ⅲ度以上骨髓抑制,20%(9/45)的患者出现Ⅱ度骨髓抑制,4.4%(2/45)的患者出现感染,44.4%(20/45)的患者出现1度胃肠道反应。骨髓抑制主要是血小板减少和中性粒细胞减少,6例Ⅲ度以上的骨髓抑制5例出现在辅助性化疗的前6个周期,1例出现在第9个周期。

图1 高级别胶质瘤辅助周期数≤6与>6的PFS
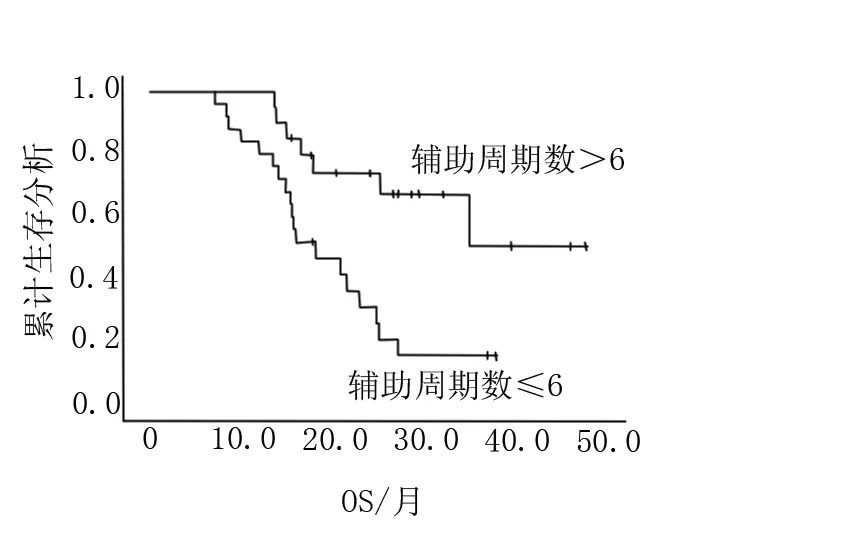
图2 高级别胶质瘤辅助周期数≤6与>6的OS

图3 高级别胶质瘤辅助周期数≤6个周期、6<化疗周期数≤9、>9个周期的PFS

图4 高级别胶质瘤辅助周期数≤6个周期、6<化疗周期数≤9、>9个周期的OS
3 讨论
高级别胶质瘤通过STUPP方案治疗后一年生存率65%远远超过传统化疗的一年生存率46%。但是高级别胶质瘤在完成标准STUPP方案后仍绝大部分会出现复发,那么延长辅助性化疗后是否可能提高高级别胶质瘤的PFS和OS呢。
Darliv A对于辅助性化疗6周期与≥9周期进行分析,6周期治疗组的死亡风险及疾病进展风险较≥9周期显著增加(P值=0.001和P值=0.03)[13]。本研究中≤6周期辅助性化疗的中位PFS为11.6个月,>6周期辅助性化疗的中位PFS为18个月,P值=0.001,有显著性差异;≤6周期辅助性化疗的中位OS为18.5个月,>6周期辅助性化疗的中位OS为25.6个月,P值=0.004,有显著性差异;那么是不是替莫唑胺辅助性周期化疗时间越长疗效越好呢?Hau P对于高级别胶质瘤接受至少12个周期一线替莫唑胺化疗的研究中发现,长周期替莫唑胺化疗的高级别胶质瘤中位肿瘤进展时间为14个月,较6周期化疗的中位肿瘤进展时间明显延长,仅少部分患者出现Ⅲ~Ⅳ级毒性反应[14]。本研究对≤6周期、6<化疗周期数≤9、>9周期进行分层分析,≤6周期的中位PFS为10.3个月,中位OS为18.5个月,6<化疗周期数≤9的中位PFS为14个月,中位OS为18.2个月,>9个周期的中位PFS为27.8个月,中位OS为27.5个月;可以看到6<化疗周期数≤9的PFS和OS虽然较≤6个周期的有提高,但是提高的并不多,但是周期数>9个周期的患者PFS和OS与其它两组的PFS和OS有非常明显的提高。本研究中有6例(13.3%)的患者出现III度以上骨髓抑制,5例发生在辅助性化疗的前6个周期,1例发生在第9周期,毒副作用与文献报道相似[13-14]。可以认为长疗程辅助性化疗毒副反应可以耐受。因此,对于替莫唑胺治疗有效且毒性可耐受的患者,可考虑延长替莫唑胺辅助化疗的治疗周期。
本研究中有11例患者在诊断肿瘤进展后继续使用替莫唑胺治疗2~11个周期,虽然不再纳入辅助性化疗计数,但是随访这些病例均分别获得了4~11个月的生存时间。提示长周期替莫唑胺辅助性化疗可以延长高级别胶质瘤的OS。
但是本研究病例数较小,可能有的患者在早期出现肿瘤复发影响了研究PFS和OS的客观性,能完成长周期的患者的PFS存在主观偏移。后续可设计前瞻性随机对照研究并征集更多的病例期望可以获得更加客观的效果。
