液质联用法同时测定干血斑中环孢菌素A、西罗莫司、他克莫司和依维莫司药物浓度
2021-02-03吴中豪龚子珊姜小梅许舒欣韩文念
吴中豪 龚子珊 姜小梅 许舒欣 韩文念 李 艳 汪 曣*
(1.天津大学,精密仪器与光电子工程学院,天津 300399;2.中科院苏州医工所天津工程技术研究院,天津300399)
1 引言
免疫抑制剂是一类可抑制机体异常免疫反应的药物,其在防治移植排斥、治疗超敏反应引起的疾病和自身免疫性疾病中占据着十分重要的地位,临床常用的免疫抑制类药物有环孢菌素A、西罗莫司、他克莫司、依维莫司、霉酚酸酯、糖皮质激素等[1]。这类药物的血药浓度与免疫抑制程度和肝肾毒性密切相关,它们大多表现出较高的药代动力学变异性,具有相对狭窄的治疗窗口和暴露-反应关系[2-4]。因此在临床应用时必须及时地监测其血药浓度,在保证治疗效果的同时应最大限度地减少排异反应及毒副作用[5]。目前该类药物的检测方法以LC-MS/MS法和免疫法(FPIA)为主,但是免疫分析法多以抗原抗体特异性结合为原理进行标记和筛选,在方法选择性和特异性方面会有很大区别,有时还会发生严重的交叉反应[6],而LC-MS/MS法由于其精密度、准确度及灵敏度方面的巨大优势,是目前药物检测的金方法。
在器官移植术后的药物治疗中,多次采集全血增加了患者的生理负担,也增加了门诊患者的单次门诊留院时间,而干血斑(Dried blood spots,DBS)采样技术具有微创、成本低、样本易于保存和运输等优势,非常适用于临床血药浓度检测[7]。目前多数DBS方法仅用于一种或两种免疫抑制剂的检测,这限制了DBS方法在高通量检测领域中的应用潜力。迄今为止,只有两份报告记录了LC-MS/MS方法在同时分析干血斑中4种免疫抑制剂方面的应用[8,9]。前者讨论了红细胞压积和免疫抑制剂浓度对回收率的影响,并进行了详细的方法学验证,但与其它3种药物的回收率相比(85.7%~98.8%),所建方法使得环孢菌素A的提取受血药浓度和红细胞压积影响较大,导致其在低浓度水平下的回收率异常高(121.3%)[8]。后者建立了稳定可行的免疫抑制剂检测方法,但4种药物的回收率较低(59.1%~80.0%),具有更高提取回收率的新方法有待进一步探索[9]。
本实验建立了一种同时定量检测DBS中环孢菌素A、西罗莫司、他克莫司和依维莫司的高通量LC-MS/MS方法,并根据美国FDA发布的《生物分析方法验证指南》[10]对方法的线性范围、定量限、提取回收率、精密度与准确度、残留效应和稳定性进行考察,根据欧洲EMA发布的《生物分析方法验证指南》[11]对基质效应进行考察,以确保方法的可靠性,旨在为临床免疫抑制剂的血药浓度监测提供良好的参考方法。
1 实验部分
1.1 仪器与试剂
API 4000型三重四极杆质谱仪,美国AB Sciex公司;岛津LC-20A液相色谱系统,日本岛津公司;5427R型高速冷冻离心机,德国Eppendorf公司;CE-7200A型超声波清洗机,东莞洁康超声波清洗机设备有限公司;VSD150-1A型氮吹仪,无锡沃信仪器制造有限公司;Milli-Q Advantage A10纯水仪,德国Merck Millipore公司。
环孢菌素A、西罗莫司、他克莫司、依维莫司、子囊霉素(环孢菌素A与他克莫司的内标)、西罗莫司-d3(西罗莫司氘代内标)和依维莫司-d4(依维莫司氘代内标)均购自加拿大Toronto Research Chemicals公司;甲醇、乙腈、甲酸均为色谱纯,美国Fisher Scientific公司;盐酸(分析纯),上海润捷化学试剂有限公司;乙酸铵、七水硫酸锌,美国Sigma-Aldrich公司;空白全血样本(EDTA抗凝不含待测药物的全血)来自健康志愿者;质控样本为实验室自制样本;干血滤纸片为Whatman 903号滤纸(批号:10538018),英国Whatman公司;实验用水为超纯水。
1.2 储备液和工作液的制备
分别用甲醇溶解环孢菌素A、西罗莫司、他克莫司和依维莫司标准品,制备成100μg/mL的标准品储备液(-20℃保存);分别精密吸取一定量的标准品储备液,混合后用甲醇依次稀释,制备成含环孢菌素A浓度分别为400、800、1600、2000、3200、6400、16000、20000ng/mL,含西罗莫司、他克莫司和依维莫司浓度分别为40、80、160、200、320、640、1600、2000ng/mL的4药混合系列标准品工作液,于4℃冰箱内保存备用。
分别用甲醇溶解子囊霉素、西罗莫司-d3和依维莫司-d4内标物,制备成100μg/mL的内标储备液(-20℃保存);分别精密吸取一定量的内标储备液,混合后用甲醇稀释,制备成含西罗莫司-d3浓度为350ng/mL,子囊霉素、依维莫司-d4浓度为100ng/mL的混合内标工作液,于4℃冰箱内保存备用。
1.3 标准曲线样品和质控样品的制备
精密吸取10μL标准品工作液分别添加到190μL空白全血中,涡旋混匀1min,室温放置30min后,制得含环孢菌素A浓度分别为20、40、80、100、160、320、800、1000ng/mL,含西罗莫司、他克莫司和依维莫司浓度分别为2.0、4.0、8.0、10、16、32、80、100ng/mL的“全血标准曲线样品”,室温下放置,当天使用;同时制备定量下限、低、中、高4个浓度水平的“全血质控样品”,其中环孢菌素A样本浓度分别为20、40、320、800ng/mL,西罗莫司、他克莫司和依维莫司样本浓度分别为2.0、4.0、32、80ng/mL,于4℃冰箱内保存。
精密吸取30μL全血样品(全血标准曲线样品、全血质控样品)垂直滴于Whatman 903滤纸的采样环中心,将滤纸转移至试管架上,室温过夜晾干后制得“DBS标准曲线样品”和“DBS质控样品”。其中,DBS标准曲线样品中环孢菌素A浓度分别为20、40、80、100、160、320、800、1000ng/mL,西罗莫司、他克莫司和依维莫司浓度分别为2.0、4.0、8.0、10、16、32、80、100ng/mL。定量下限、低、中、高浓度的DBS质控样品中环孢菌素A浓度分别为20、40、320、800ng/mL,西罗莫司、他克莫司和依维莫司浓度分别为2.0、4.0、32、80ng/mL。备用样品干燥后装入密封袋中,于-20℃冰箱内保存。
1.4 样品前处理
于DBS中心位置打孔取样直径8mm的圆形血斑,置于微量离心管中,加入290μL甲醇-乙腈(80∶20,v/v)提取液、10μL混合内标工作液和20μL盐酸溶液(0.05mol/L)。涡旋混匀后密封,50℃水浴下超声提取并孵化30min[12],随后在预置好的4℃高速冷冻离心机内14000g/min离心10min,转移上清液至自动进样器微量试管中,室温下氮气吹干,底物用80μL甲醇溶液涡旋复溶3min,离心5min(14000g/min),取上清液10μL进样检测。具体流程如图1所示。

图1 DBS样品前处理方法流程图
1.5 实验方法
1.5.1色谱条件
Shim-pack GIST-HP型C18色谱柱(100mm × 2.1mm,3μm),柱温60℃,流速0.9mL/min,进样量10μL,分析时间4.5min;流动相A为含有2mM乙酸铵和0.1%甲酸的水溶液,流动相B为含有2mM乙酸铵和0.1%甲酸的甲醇溶液;梯度洗脱:0~0.4min,40%B;0.4~2.2min,40%~100%B;2.2~3.0min,100%B;3.0~3.5min,100%~40%B;3.5~4.5min,40%B。
1.5.2质谱条件
采用电喷雾正离子电离(ESI+)和多反应监测(MRM)模式进行检测,电喷雾电压为4500V,离子源温度为300℃,气帘气、雾化气、辅助加热气压力分别为25psi、70psi、55psi;去簇电压为43~60V,碰撞室入口电压为11V,碰撞能为23~29eV,碰撞室出口电压为10~26V。
2 结果与讨论
2.1 色谱条件的优化
实验考察了甲醇-水、乙腈-水作为流动相时的影响,实验发现,对于同等浓度的分析物,甲醇-水作为流动相时得到的色谱图分离效果较好,其信号响应值和稳定性也较高。同时,在流动相中加入2mM的乙酸铵改善了分析物的峰形,加入0.1%甲酸提高了4种化合物的质谱响应值,降低了定量限。在此条件下,4种免疫抑制剂药物在4.5min内便可有效分离(如图2所示)。根据4种免疫抑制剂的亲脂特性,选取C18柱,考察了流速、柱温对分离效果和信号强度的影响,最终采用“1.5.1”的洗脱梯度,0.9mL/min的流速,以及60℃的柱温分析条件。
2.2 质谱条件的优化
在MRM模式下,采用手动优化方法,依次对去簇电压、碰撞室入口电压、碰撞能量、碰撞室出口电压、分析物及其内标的母离子和子离子等条件进行优化,最终确定的质谱分析条件如表1所示。

表1 4种免疫抑制剂及其内标的质谱分析条件
2.3 定量下限和标准曲线
使用已建立的LC-MS/MS分析方法测定3个浓度值接近检出限的DBS样品,每浓度进行6个样本分析,连续测定3个批次,通过分析各浓度样本测定结果的总变异系数(CV)和与理论值的偏差来确定方法的定量下限。根据2018年FDA发布的《生物分析方法验证指南》[10]要求,CV值应≤ 20%,偏差应在±15%以内。结果显示,环孢菌素A、西罗莫司、他克莫司和依维莫司的定量下限分别为20、2.0、2.0、2.0ng/mL,测定结果的偏差在-8.3%至8.6%之间,最大CV值为11.43%,方法满足FDA的指南要求。此结果与Koster[8]等人所报道方法的定量下限(环孢菌素A、西罗莫司、他克莫司和依维莫司的定量下限分别为20、1.0、1.0、1.0ng/mL)相近,可完全覆盖临床用药的低限浓度。4种免疫抑制剂的定量下限色谱图及分子结构式如图2所示。

图2 4种免疫抑制剂定量下限色谱图及分子结构式a.环孢菌素;b.西罗莫司;c.他克莫司;d.依维莫司
用所建方法测定“DBS标准曲线样品”中4种免疫抑制剂的浓度(8个质量浓度梯度),每一浓度进行双样本分析,记录色谱图。以各组分与其内标的峰面积比值(y)为纵坐标,各组分的浓度值(x)为横坐标,用加权(w=1/X2)最小二乘法进行回归计算。得到4种免疫抑制剂的线性范围、标准曲线方程、相关系数及定量下限如表2所示。

表2 4种免疫抑制剂的线性范围、标准曲线方程、相关系数和定量下限
2.4 提取回收率和基质效应
在对方法的提取回收率进行考察时,应准确知道打孔取样的DBS样品的负载血量,进而精确计算出空白对照样中应加入的待测物和内标的用量。D.H. Vu[13]等人报道了用红细胞压积为32%~38%的全血制备的直径8mm的血斑含血量约20μL。因此,本实验采用刚好可以覆盖8mm圆形滤纸片的20μL全血[14]来进行提取回收率和基质效应的验证。
用20μL的低、中、高3个浓度水平的“全血质控样品”制备DBS样品,每浓度进行6个样本分析,根据峰面积计算提取回收率。同时制备低、中、高3个浓度水平的纯溶液样品(溶剂为甲醇),每浓度进行3个样本分析,根据2011年EMA发布的《生物分析方法验证指南》[11]进行基质效应验证,通过计算4种免疫抑制剂在不同浓度水平下的内标归一化基质效应因子[11]及其CV值来评价基质效应。提取回收率和基质效应结果见表3。实验结果表明:方法具有较高的提取回收率,其中环孢菌素A为70.9%~76.4%;西罗莫司为81.7%~105.3%;他克莫司为105.4%~115.8%;依维莫司为89.1%~110.6%。本方法与Koster[8]等人的研究相比,可降低环孢菌素A药物的滤纸片色谱效应,使其在不同浓度下的提取回收率水平相当;方法的回收率比den Burger[9]等人的研究(环孢菌素A,59.1~65.9%;西罗莫司,65.8%~64.1%;他克莫司,78.6%~80.0%;依维莫司,64.1%~64.2%)要高,可实现对DBS样本中的4种免疫抑制剂进行更高效的提取。4种免疫抑制剂在低、中、高浓度水平下的内标归一化基质效应因子的CV值均<15%,基质效应满足EMA指南的相关规定[11]。

表3 4种免疫抑制剂的提取回收率和基质效应验证结果
2.5 精密度与准确度
用所建方法检测定量下限、低、中、高4个浓度水平的“DBS质控样品”,每浓度进行5个样本分析,连续测定3d。以当天的标准曲线计算DBS质控品浓度,以质控品测定结果来评估方法的精密度与准确度。结果如表4所示,4种免疫抑制剂的日内和日间精密度(CV)为1.9%~12.9%,准确度为-13.9%~8.6%。方法的精确度较高,结果满足FDA指南的相关要求[10]。

表4 4种免疫抑制剂的精密度与准确度验证结果
2.6 残留效应
用所建方法连续测定低浓度的“DBS质控样品”后,随行交替测定高、低浓度的DBS质控品,通过比较低浓度质控样品在第1次进样和后续进样的测定值来计算残留效应[15]。结果显示,环孢菌素A、西罗莫司、他克莫司和依维莫司的残留率分别为8.1%、-0.7%、-2.8%、-2.6%,残留效应均小于定量下限样本浓度的20%。
2.7 稳定性
选用-20℃保存3个月的储备液与新配储备液制备低、高(环孢菌素A浓度为40、800ng/mL,西罗莫司、他克莫司和依维莫司浓度为4.0、80ng/mL)2个质控品浓度的储备液样本,每浓度进行5个样本分析来考察储备液稳定性;选用低、中、高3个浓度水平的“DBS质控样品”,每浓度进行5个样本分析。其中,前处理后样品于20℃自动进样器中放置1d后进行分析来考察自动进样器稳定性,其余质控样品装入密封袋中,分别在不同温度条件(25℃、4℃、-20℃)下保存不同时间(5d、14d、21d)后进行分析来考察DBS样本稳定性。结果如表5所示,所有质控品浓度测定结果的准确度在-14.9%~14.2%之间,CV值均<14.2%,结果满足FDA指南的相关规定[10]。表明储备液于-20℃下至少可以稳定保存3个月,处理后样品在自动进样器内至少可以稳定保存1天,DBS样品在室温、4℃、-20℃条件下至少可以稳定保存5天、14天和21天。
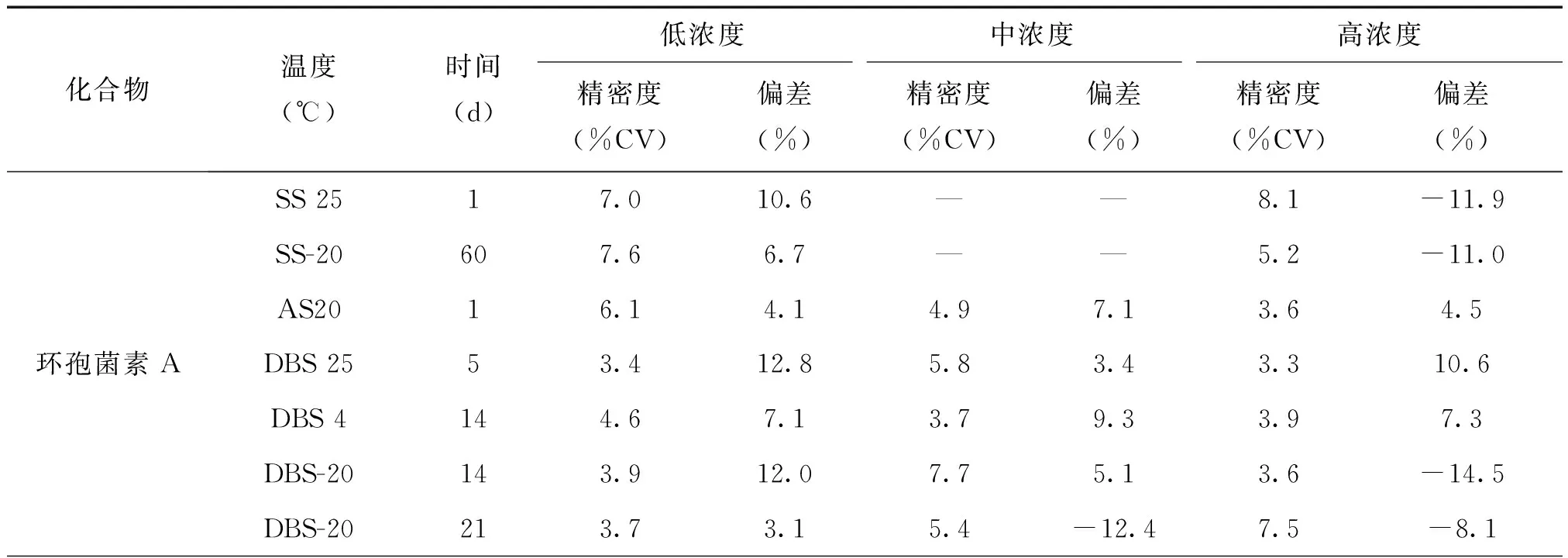
表5 4种免疫抑制剂的稳定性验证结果(n=5)
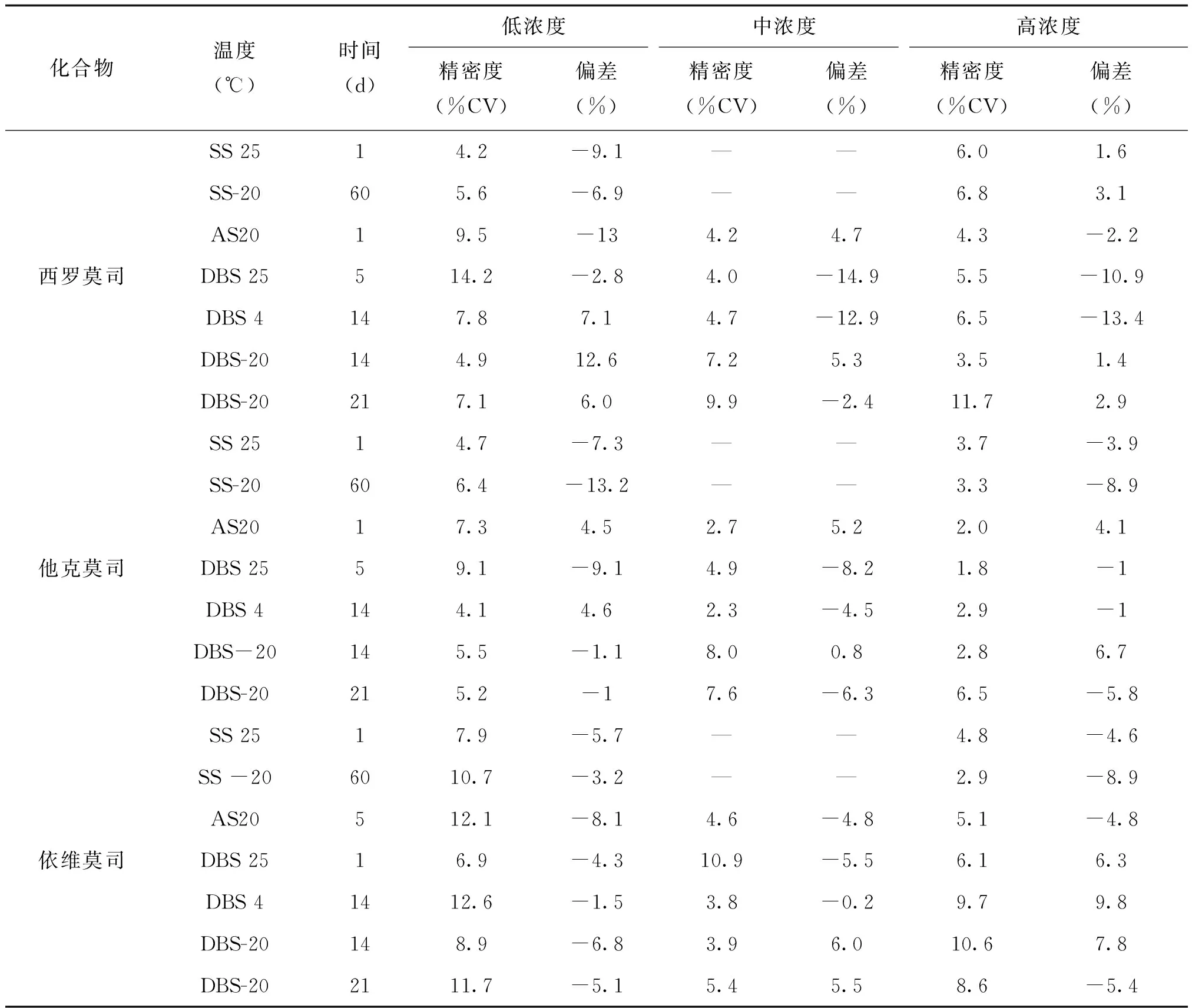
续表5
3 结论
本研究建立了一种高通量液相色谱-串联质谱法同时定量检测干血斑中环孢菌素A、西罗莫司、他克莫司、依维莫司的方法。通过对检测条件的优化,实现了对免疫抑制剂的高效、精准分析。样品前处理采用了甲醇-乙腈混合溶液提取和沉淀蛋白并结合氮气吹干和甲醇复溶的方式,使方法获得了较高的提取回收率(73.6%~110.8%)和较低的定量限。本方法具有快速、高效、准确度和精密度高、对病患友善、样本采集、储存和运输方便等优点,为临床免疫抑制剂的血药浓度监测提供了良好参考方法。
值得注意的是,红细胞压积可通过影响血液的黏稠度进而影响滴加到采血滤纸片上的血液的扩散。因此,与高红细胞压积的血液相比,单位体积的低红细胞压积的血液获得的干血斑会更大,这在打孔取样时,可能会对固定面积的DBS样品中的免疫抑制剂含量产生影响,进而造成分析误差。此外,红细胞压积也会影响血液在滤纸片上的渗透性,可能使得药物与滤纸片纤维之间的作用力发生变化,进而对方法的提取回收率造成影响。未来的研究可针对免疫抑制剂与滤纸片间的结合和提取机理进行深入探索,并考察和校正红细胞压积对本方法的影响。另外,本研究为满足方法建立和验证过程中需要大量样本的要求,选择了用移液枪吸取静脉全血滴加于滤纸片上制成DBS样本。日后的研究可采集真实病人样本,包括静脉全血、静脉全血DBS、指尖血DBS,来进行方法考察,全面比较不同采集方式的样本在该方法下所测得的免疫抑制剂药物浓度差异,探讨用指尖血DBS进行药物浓度测定来代替目前常规的用静脉全血进行药物浓度测定的可行性,将本方法真正应用于临床。
