电子自旋共振技术分析植物油氧化
2020-11-13刘其耸石丽花孙旭媛李进伟
刘其耸,石丽花,孙旭媛,李进伟
(1.烟台新时代健康产业有限公司,山东 烟台 264006; 2. 江南大学 食品学院,江苏 无锡 214122)
随着人民生活水平的不断提高,食用油脂具有更加广大的市场需求。而食用植物油热加工过程中的氧化反应对于油脂的风味、营养价值和健康均具有重要影响。油脂的氧化与自由基密切相关,可以说自由基的生成是油脂氧化进程开始的标志。充分了解食用植物油热加工过程中的氧化产物和关键控制点是实现氧化危害控制的核心。目前,油脂氧化主要集中在传统化学指标和氧化危害产物的分析方面,缺乏对热加工过程中氧化产物与自由基生成的定性定量研究。电子自旋共振(ESR)是一种直接检测和研究具有未成对电子的化合物的现代分析方法,其主要研究对象为自由基、双基或多基、具有奇数电子的原子以及含有单电子的分子等,并且已被广泛应用于油脂氧化过程中自由基含量的测定[1]。为此,本文采用ESR方法探究不同植物油在不同加热条件下自由基信号强度与油脂氧化的相关性,为进一步科学有效地表征油脂热氧化程度提供依据。
1 材料与方法
1.1 试验材料
未添加抗氧化剂的棕榈油、菜籽油、葵花籽油,上海益海嘉里有限公司;未添加抗氧化剂的冷榨亚麻籽油,内蒙古锡林郭勒盟红井源油脂有限责任公司;甲苯(分析纯)、N-叔丁基-α-苯基硝酮(PBN,纯度≥98%)、5,5-二甲基-1-吡咯啉氮氧化物(DMPO,纯度>97%),上海百灵威科技有限公司。
EL204电子天平,梅特勒-托利多仪器(上海)有限公司; EMXplus-10/12电子自旋共振波谱仪,德国布鲁克(Bruker)公司。
1.2 试验方法
1.2.1 植物油加热试验
将4种植物油置于煎炸锅中,分别在120、150℃和180℃条件下加热一定时间,定期取样,装入棕色瓶中,充氮气保护,置于-20℃冰箱中储藏备用。
1.2.2 自由基信号强度的测定
仪器参数:中心场强335.4 mT;扫描宽度10 mT;扫描时间40 s;分辨率1 024;微波强度20 mW;调制频率100 kHz;调制幅度0.1 mT;转换时间1.28 ms;时间常数20.48 ms;加热温度(393.15±1.00)K。
以溶于甲苯的DMPO或PBN为捕获剂。参照文献[2]按照过量添加原则将捕获剂配成100 mmol/L进行添加,以便及时捕获所有生成的自由基。将100 μL待测油样及20 μL捕获剂加入核磁管中振荡均匀。当谐振腔达到设定温度时放入核磁管。调节仪器处于最佳检测状态后开始检测,每隔5 min测定一次自由基谱图直至30 min,所有样品均在避光条件下进行检测。自由基谱图处理主要使用Sigma Plot 12.5软件以及ESR仪器的Xenon软件(Bruker,Germany),优化信噪比后,通过Xenon软件计算自由电子因子(g)值和超精细分裂常数,所得参数的精确度为3%[3]。ESR信号的强度,即低场下峰到峰的振幅,可由WINEPR软件程序确定[4]。
1.2.3 过氧化值的测定
过氧化值测定参照GB/T 5538—2005《动植物油脂 过氧化值测定》。
1.2.4 相关性分析
采用Pearson相关系数对植物油自由基信号强度与过氧化值进行相关性分析,数据以“平均值±标准差”表示3次平行试验结果。
2 结果与分析
2.1 不同植物油加热氧化过程中过氧化值的变化
油脂的氧化过程是较为复杂的动态反应过程,同时存在着氢过氧化物的形成与分解。4种植物油分别在120、150、180℃加热36 h,间隔4 h取样,测定其过氧化值变化,结果见图1。

图1 4种植物油不同温度加热氧化过程过氧化值变化
从图1可看出,120℃时4种植物油过氧化值随加热时间延长逐渐增加,说明氢过氧化物呈积累趋势。植物油的氧化是一个连续的过程,氢过氧化物在产生的同时伴随着部分分解,但是分解过程中产生的烷基自由基会使植物油的氧化反应循环下去而产生更多的氢过氧化物,氢过氧化物呈积累趋势,因而过氧化值随加热时间延长不断增大。对于150℃及180℃,植物油在加热过程中过氧化值呈现出波动增加的变化趋势,此时油脂中氢过氧化物的分解速率明显加快。加热初期产生的氢过氧化物是一种反应中间体,其形成速率取决于氧的可用性和温度,在常温下相对稳定[5]。此时植物油中的脂肪酸碳链并未断裂,然而氢过氧化物一旦形成后,容易分解成烷氧基,然后在金属存在或高温条件下,与—OOH相连的碳原子两边的键进一步发生断裂,形成醛、酮、酸、酯、醇和短链烃,当氢过氧化物达到一定含量时其分解速率将大于生成速率,从而导致氢过氧化物含量下降[6]。
2.2 植物油的电子自旋共振技术分析
2.2.1 自旋捕获剂的选择
脂质类自由基具有极短的半衰期,如烷氧自由基、超氧阴离子自由基和羟基自由基,检测时需要使用自旋捕获剂。针对本试验研究体系,首先对自旋捕获剂进行选择。图2为两种捕获剂及未添加自旋捕获剂时棕榈油150℃加热20 min的ESR本底信号。
由图2可以看出,PBN和DMPO均未产生自由基或干扰信号,且在未添加自旋捕获剂的情况下,棕榈油中几乎无法检测到任何自由基信号。因此,研究油脂热氧化过程自由基变化,需要加入适当的自旋捕获剂。
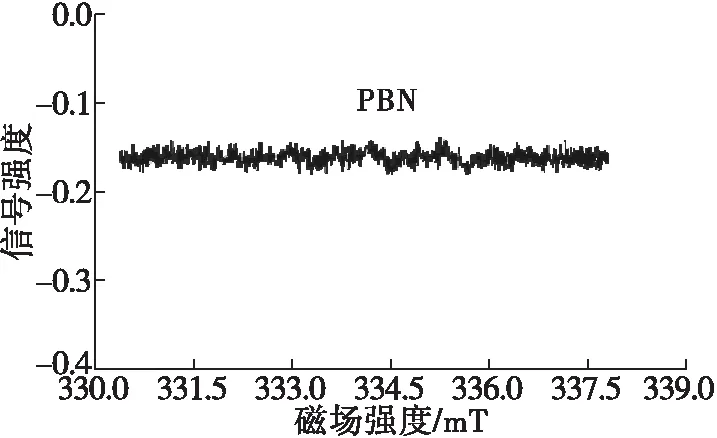
图3为150℃加热20 min时PBN和DMPO捕获下棕榈油中自由基的ESR谱图。
由图3(a)可以看出,用PBN捕获后所得自由基峰型为裂分的三重峰(即六重峰),测定其g值为2.007 0,接近自由电子g值(2.003 0),符合自由基的基本特性[7]。计算机拟合得到其超精细分裂常数αN=1.47 mT,αH=2.07 mT,为多种碳中心自由基相互叠加的结果。由于PBN捕获自由基加合物的谱图非常相似,所得谱图提供自由基信息较少,难以区分和判别自旋加合物的分子结构特征。
由图3(b)可以看出,与PBN相比,DMPO作为捕获剂时所得到的自由基ESR谱图明显更为复杂,呈现出多种自由基相互叠加的效果。由于DMPO捕捉自由基的动力学速率优于PBN[8],形成的各种自旋加合物的信号的β-H超精细耦合参数差异较大,因而更利于分析和鉴别体系中同时捕获到的几种分子结构不同的自由基。因此,DMPO是研究油脂热氧化过程的自由基变化和氧化途径合适的自旋捕获剂。

2.2.2 不同植物油加热氧化过程自由基信号强度的变化
图4为4种植物油在120、150、180℃加热氧化过程中的自由基信号强度变化。

由图4可知,新鲜植物油中自由基信号强度从高到低依次为亚麻籽油、葵花籽油、菜籽油、棕榈油。棕榈油和菜籽油在加热12 h前的自由基信号强度相近,说明二者氧化速率相近,均低于葵花籽油和亚麻籽油。12~36 h,菜籽油样品的自由基信号强度分别在0.67~1.83(120℃)、0.08~0.23(150℃)和0.09~0.36(180℃)之间,高于棕榈油的自由基信号强度。研究表明植物油脂肪酸组成对其氧化稳定性有很大影响[9],常见脂肪酸中亚麻酸(C18∶3)最容易氧化,其次是亚油酸(C18∶2)、油酸(C18∶1)。菜籽油富含不饱和脂肪酸C18∶1、C18∶2,棕榈油富含饱和脂肪酸棕榈酸(C16∶0),相同加热条件下,菜籽油更容易氧化,因而其自由基信号强度高于棕榈油。与棕榈油和菜籽油相比,葵花籽油的自旋加合物形成速率较高,葵花籽油样品的自由基信号强度随加热时间延长显著升高。180℃加热亚麻籽油的自由基信号强度的变化趋势与其他油不同。当在180℃加热时,亚麻籽油中自旋加合物的衰减速率高于其生成速率,导致自由基信号强度降低。这与Roman等[10]研究的动力学模型结果一致,较高的自由基信号强度会导致自旋加合物的衰减速率较高。
综上所述,脂质类自由基信号强度随着加热时间的延长而增加。这表明氧化程度与自由基加合物的量成正相关,可以使用自由基加合物的量作为参数评估在特定温度条件下植物油的热氧化程度。
2.3 自由基信号强度表征植物油热氧化
比较3种温度条件加热下4种植物油自由基信号强度与过氧化值之间的相关性,以评估ESR方法的准确度,结果见表1。

表1 自由基信号强度与过氧化值之间的相关性
由表1可知,在整个加热过程中,自由基信号强度与过氧化值呈线性关系,且二者为强相关(R2>0.83,P<0.05)。表明植物油在加热0~36 h的条件下,ESR可以预测油脂的氧化稳定性。这与Papadimitriou 等[11]的研究结果一致,其通过ESR测定橄榄油在70℃加热条件下PBN自旋加合物的量确定橄榄油的氧化诱导期,从而对橄榄油的氧化稳定性进行预测。
3 结 论
DMPO是研究油脂热氧化过程的自由基变化和氧化途径合适的自旋捕获剂,在相同加热温度下,植物油的自由基信号强度随着加热时间的延长而增加,自由基信号强度与过氧化值的相关性较强(P<0.05),故ESR方法可用于表征植物油的热氧化程度。
