不典型肺癌CT诊断与鉴别诊断
2020-10-22王守玉屈开新王庆龙骆华峰
王守玉 屈开新 王庆龙 骆华峰 高 翔 刘 伟
1.安徽省阜南县人民医院CT/MRI室,安徽阜南 236300;2.安徽省阜南县人民医院呼吸科,安徽阜南 236300
肺癌目前是全世界范围内癌症引起死亡的主要原因,在我国恶性肿瘤的死因中占首要地位[1],因此,肺癌的早期正确诊断非常重要,典型肺癌根据CT直接征象及间接征象容易诊断,但部分不典型肺癌容易漏诊,甚至误诊,让患者错过最佳治疗时机,影响患者治愈率、生存期,甚至给患者造成不可挽回的损失,因此,我们把近1年我科误诊、漏诊肺癌患者CT征象加以研究、总结,以便让大家对不典型肺癌能及时,准确做出诊断,让患者得到精准治疗。现报道如下。
1 资料与方法
1.1 一般资料
选取我院2018年1月~2019年12月18例经支气管镜活检,CT引导下穿刺活检及手术确诊的肺癌患者,其中男10例,女8例,年龄33~77岁,中位年龄50岁,临床症状有:不同程度咳嗽,咳痰,多数咳白色黏液痰,咯血,发热,胸闷,胸痛及呼吸困难等。实验室检查,包括血常规,肿瘤标志物5项指标检测[非小细胞相关抗原(CYFR21-1),癌胚抗原(CEA),糖类抗原125(CA125),糖类抗原153(CA153),神经元特异性烯醇化酶(NSE)]中的1项或多项呈阳性者10例。
1.2 CT检查方法
采用美国GE公司64排螺旋CT机(Optima 660),美国STELLANT高压注射器,扫描条件:管电压120kV,管电流100mA,层厚5mm,层间距5mm,螺距0.984,矩阵512×512,HRCT薄层重建层厚1.25mm,增强扫描采用非离子造影剂典帕醇30g(I)/100mL,用量1~1.5mL/kg,注射流率为3mL/s,用高压注射器经肘静脉经注入,延迟20~35s扫描,扫描范围从锁骨上区到肺底部。
1.3 评价方法
由1名高级职称及中级职称医师分成两组,双盲分析CT征象,拿出初步意见,然后汇总,意见不同时在一起讨论,最后均与临床联系,并与病理结果进行比较。
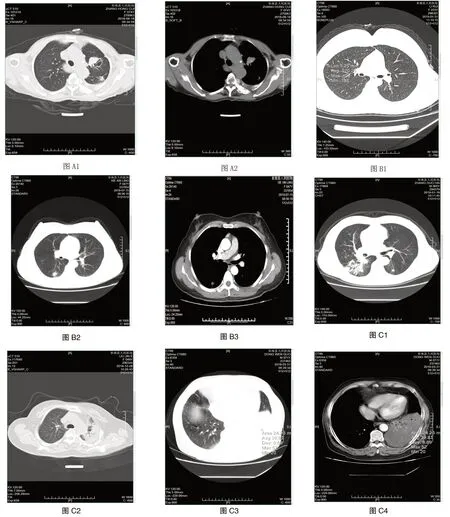
图A1-2含薄壁囊腔型肺癌;图A1肺窗,图A2与图A1系同一患者纵隔窗
2 结果
2.1 病灶在肺叶分布
右肺10例,其中上叶2例,中叶4例,下叶4例,左肺8例,其中上叶4例,下叶4例。
2.2 病灶病理细胞学分型
腺癌13例,鳞癌1例,小细胞癌 4例。
2.3 病灶CT征象分型
2.3.1 含薄壁囊腔型肺癌 如图A1 ~ 2示:左肺上叶见囊实性混杂密度影,周围见毛刺征,胸膜凹陷征,软组织成分内见点状钙化灶,穿刺活检病理证实为原位腺癌。
2.3.2 磨玻璃结节影(如图B1 ~ 3) 第一个病例((图B1)病灶位于右肺上叶近胸膜处,大小约7.3mm×5.2mm,边缘清晰,邻近胸膜稍增厚,手术后病理证实为原位腺癌。第2个病例(如图B2 ~ 3),病灶位于右肺下叶,大小约10mm×10.7mm,边缘见毛刺征、分叶征,胸膜凹陷征,本组3例,病灶与胸膜侧见局限性线条征改变,增强扫描结节实性部分轻度强化,穿刺活检病理证实为腺癌,因此,依据磨玻璃结节的密度、边缘分叶征,毛刺征,病灶与肺交界面清晰以及强化程度可对其良恶性做出明确判断。
2.3.3 肺炎型肺癌(如图C1 ~ 4) 本组病例CT表现:(1)大片状肺组织实变,内见空泡征,蜂窝征,本组10例(如图C1、C4);(2)空气支气管征,但支气管扭曲,狭窄,支气管分叉角度增大,本组5例(如图C2);(3)实变的肺组织在叶间裂处稍膨隆,增强扫描见血管集束征及血管造影征,局部肺组织轻度强化,CT值净增加8 ~ 20HU(如图C3 ~ 4)。
3 讨论
含薄壁囊腔型肺癌,是一种特殊类型肺癌,容易被忽视,文献报道[2-4]:其形成机制可能是:(1)细支气管壁上肿瘤,不断增大或侵润支气管壁,导致管腔逐渐狭窄,甚至闭塞,引起远端肺泡腔扩大、破裂、融合,形成囊腔;(2)肿块生长较快,中心组织缺血导致液化,坏死,经细支气管排出,形成薄壁囊腔;(3)肿瘤细胞沿着肺泡壁生长,肺泡壁破坏后相互融合形成薄壁囊腔;(4)患者原先患有支气管肺囊肿,肺结核空洞,肺大泡等含囊性病变基础上发生的肿瘤;(5)囊性病变周围的肺纤维结缔组织回缩、牵拉、导致空洞壁变薄。含薄壁囊腔的周围型肺癌CT表现:(1)囊壁厚薄不均,原因可能是囊壁上癌细胞浸润,以腺癌细胞为主,也可能是鳞癌、小细胞癌、大细胞癌等,肿瘤细胞破坏程度的不同导致了囊壁厚薄不均,囊腔内壁不光滑;(2)囊壁结节形成,猜想可能是肿瘤组织生长活跃的地方所致。囊腔的HRCT征象特点同样具备周围型肺癌特点,包括深分叶状、毛刺征、胸膜凹陷征、血管集束征等;文献报道[5]:囊腔内血管穿行征,就是囊腔内有血管穿行,猜测可能是因为肿瘤组织弹性纤维收缩、牵拉,导致局部囊腔出现裂隙,肺血管通过此处进入囊腔所致,且囊内无气液平面。本例囊腔型肺癌未见血管穿行征,仅见内侧软组织密度影及点状钙化灶,推测原因可能是在原有肺结核等基础病变上发生癌变可能,由于囊腔型周围型肺癌CT征象不典型,加之认识不足,一般没能引起医生的足够重视,容易导致漏诊、误诊发生[6]。
磨玻璃结节征:本组两例磨玻璃结节与肺组织交界面清晰,可能原因是肿瘤呈堆积性慢性生长或周围肺组织假包膜形成所致,相对于炎性病变则因炎性渗出,肺泡实质和间质局限性纤维化,故病灶与邻近肺组织分界不清[7],据祁闻等研究表明,边界模糊的磨玻璃结节诊断恶性病变的灵敏度及特异度比较低,分别为15.38%,36.36%;而具有清楚毛糙界面的磨玻璃结节诊断恶性病变的灵敏度及特异度较高,分别为51.92%,88.64%[8];第二例(图B2 ~ 3)病灶周围见分叶征,胸膜凹陷征及局限性线状影。分叶征形成病理基础可能是:(1)肿瘤边缘各部位肿瘤细胞分化程度差异,生长速度不同造成的;(2)肺的结缔组织间隔,包括进入肿瘤血管、支气管分支引起肿瘤生长受限,以及肿瘤内纤维组织的收缩,产生陷窝,从而形成分叶征。胸膜凹陷征形成病理基础可能是由于成纤维反应性收缩牵拉胸膜引起局部胸膜呈三角形或幕状凹陷形成。局限性线状影:见于肺内病变沿肺间质引向肺门或外围,如肺癌肿块与肺门之间或肿块与胸膜之间的细线状影[9]。
肺炎型肺癌:肺炎型肺癌(pneumonia type lung carcinoma,PTCL)是一种与普通肺炎链球菌肺炎CT表现相似的特殊类型肺癌,与常见普通肺炎不易区别,临床易误诊为普通型肺炎而错过最佳治疗时间[10],PTCL一般老年患者多见,临床症状以胸闷,咳嗽,咳痰,白色痰多见,大多数患者没有发热症状(少数合并细菌感染患者有发热及中性粒细胞升高病史),个人总结并参考文献报道[11],其CT征象及病理学基础为:(1)肺泡内的肿瘤细胞沿肺泡壁匍匐生长,随着肿瘤细胞增值浸润,肺泡腔逐渐缩小,同时癌细胞分泌大量黏液,并沿肺泡孔及细支气管蔓延、播散,CT表现为磨玻璃样改变;(2)PTCL支气管内大量纤维组织增生,引起支气管狭窄、扭曲、僵硬,甚至远端支气管截断,CT表现为:“枯树枝”征,蜂窝征,支气管分叉角度增大等;(3)细支气管由于肿瘤细胞浸润,可诱导新生异常肿瘤血管增生,导致血管结构异常,CT表现为血管集束征;本组病例实变肺组织内含气支气管扭曲、僵直、狭窄、不规则扩张及分叉角度增大(如图C1 ~ 2),这点与文献报道相似[12],PTCL支气管可呈多变性,如支气管管腔狭窄、扩张、狭窄与扩张共存等征象,而肺炎链球菌肺炎发病年龄较轻,临床症状主要为寒战、高热、咳黄色黏液痰,实验室检查血象升高,CT征象为大片实变影,其内可见空气支气管征,但含气支气管走行自然,不会出现狭窄、僵硬、截断等征象,且远端接近实变肺组织边缘甚至达胸膜下,这点可与PTCL鉴别[13],另外肺炎型肺癌患者除支气管改变外,临床咳大量白色泡沫状黏液痰,具有一定特征性[14]。
增强扫描:肺炎型肺癌见血管集束征及血管造影征,血管集束征CT 表现为一条或数条细小血管到达肿瘤边缘[15],形成机制主要是由于恶性肿瘤生长活跃,病灶内纤维组织增生牵拉邻近血管向肿瘤组织内集中所致,主要包括血管进入或穿过肿瘤组织,血管受牵拉向病灶移位,血管在病灶边缘截断三种情况。CT血管造影征:其形成机制可能是由于肿瘤细胞分泌大量黏液,加之血管树没有被肿瘤细胞破坏,故在增强时血管强化密度明显高于肿瘤组织,而大叶性肺炎的实变肺组织增强时呈明显均匀强化。
紧密结合临床:当CT怀疑肺炎时,而临床无高热病史,实验室检查与典型肺炎检测结果不相符,白细胞又无明显升高,再结合血清肿瘤标志物阳性,经过正规抗炎治疗无效或效果不佳时,应及早行纤维支气管镜检查或穿刺活检,以便明确诊断。
综上所述,当肺部病灶CT平扫见空泡征、蜂窝征、毛刺征、分叶征、胸膜凹陷征、支气管扭曲、狭窄、阻断、分叉角度增大,增强扫描见血管集束征及血管造影征,结合临床特征及肿瘤标志物检测阳性,大部分不典型肺癌能做出明确诊断,特殊疑难病例再进一步活检。
