高考无机化学工艺流程题解题指导
2019-11-08
无机化学工艺流程题是将化工生产中的生产流程用框图形式表现出来,并根据生产流程中有关的化学知识步步设问,是无机框图的创新。它以现代工业生产为基础,与化工生产成本、产品提纯、环境保护等相融合,考查物质的制备、检验、分离提纯等基本实验原理在化工生产中的实际应用,要求考生依据流程图分析原理,紧扣信息,抓住关键,准确答题。这类试题具有较强的实用性和综合性,能够充分考查考生的综合能力和学科素养,是近几年高考化学命题的常考题型,同时也是很多考生容易失分的题目。针对这种情况,笔者将自己多年来的高考备考经验进行了总结,对高考无机化学工艺流程题的解题思路和方法进行指导,希望对大家的复习备考能有所帮助。
一、无机化学工艺流程题的思维主线(如图1)
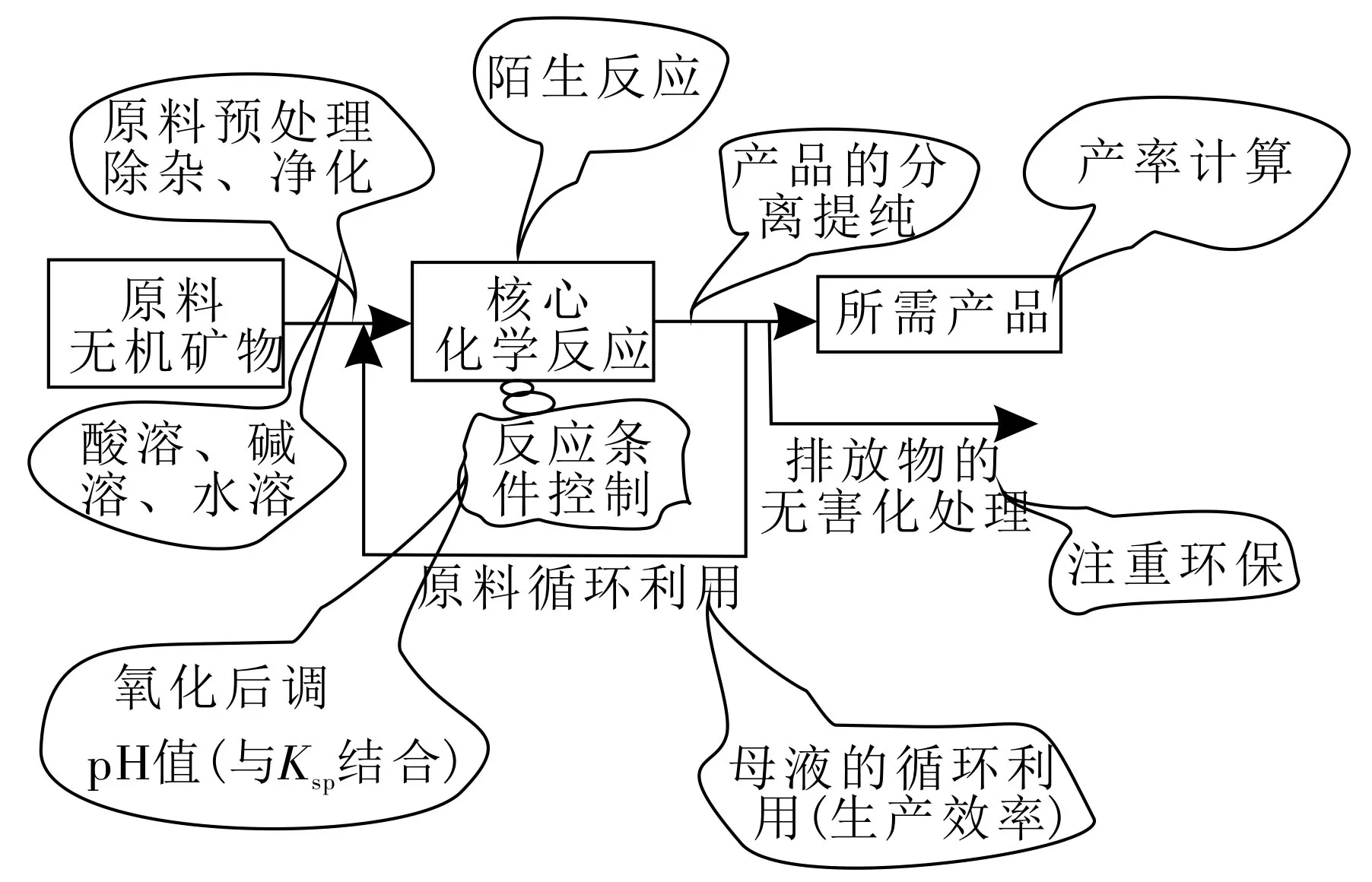
图1
此类试题多以金属矿物的加工为载体,综合考查无机元素及其化合物、化学反应原理和实验操作等,难度大,综合性强。流程图的规律:主线主产品,分支副产品,回头为循环。
二、工艺流程题分类突破
(一)以物质制备为目的的化工流程题
1.核心反应——陌生方程式的书写
关注箭头的指向:箭头指入→反应物,箭头指出→生成物。
(1)氧化还原反应:熟练应用氧化还原规律,判断产物并配平。
(2)非氧化还原反应:结合物质的性质和实际反应判断产物。
2.原料的预处理
预处理过程中涉及的几个概念的比较,如表1。

表1
(1)溶解:通常用酸溶,如用硫酸、盐酸、硝酸等。
(2)灼烧、焙烧、煅烧:改变结构,使一些物质能溶解,并使一些杂质高温下氧化或分解。
3.常用的控制反应条件的方法
(1)调节溶液的pH值:常用于使某些金属离子形成氢氧化物沉淀。调节pH值所需的物质一般应满足以下两点,一是能与H+反应,使溶液的pH值增大;二是不引入新的杂质。例如,若要除去Cu2+中混有的Fe3+,可以加入CuO、CuCO3、Cu(OH)2或Cu2(OH)2CO3等物质来调节溶液的pH值,不可加入NaOH溶液或氨水等。
(2)控制温度:根据需要升温或降温,改变反应速率或使平衡向需要的方向移动。
(3)趁热过滤:防止某物质降温时会析出。
(4)冰水洗涤:洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗。
例1(2016·全国卷Ⅰ,28题节选)NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺流程如下,请回答下列问题:

(1)NaClO2中Cl元素的化合价为___。
(2)写出反应步骤中生成ClO2的化学方程式:_____。
(3)电解所用的食盐水由粗盐水精制而成,精制粗盐水时,为除去其中的M g2+和C a2+,需要加入的试剂分别为___、__。
第二步:审流程,分块破题——拆分工艺流程。

第三步:看设问,结合题中的问题,回到工艺流程中找答案。
答案:(1)+3价 (2)2NaClO3+H2SO4+SO2==2NaHSO4+2ClO2(3)NaOH溶液Na2CO3溶液
(二)以分离提纯为目的的化工流程题
1.明确常用的提纯方法
(1)水溶法:除去可溶性杂质。
(2)酸溶法:除去碱性杂质。
(3)碱溶法:除去酸性杂质。
(4)氧化剂或还原剂法:除去还原性或氧化性杂质。
(5)加热灼烧法:除去受热易分解或易挥发的杂质。
(6)调节溶液的pH值法:如除去酸性溶液中的Fe3+等。
2.明确常用的分离方法
(1)过滤:分离难溶物和易溶物,根据特殊需要采用趁热过滤或者抽滤等方法。
(2)萃取和分液:利用溶质在互不相溶的溶剂里的溶解度不同提取分离物质,如用CCl4或苯萃取溴水中的溴。
(3)蒸发结晶:提取溶解度随温度变化不大的物质,如NaCl。
(4)冷却结晶:提取溶解度随温度变化较大的物质、易水解的物质或结晶水合物,如KNO3、FeCl3、CuCl2、CuSO4·5H2O等。
(5)蒸馏或分馏:分离沸点不同且互溶的液体混合物,如分离乙醇、甘油。
(6)冷却法:利用气体液化的特点分离气体,如合成氨工业采用冷却法分离平衡混合气体中的氨气。
例2(2016·全国卷Ⅲ,28题节选)以硅藻土为载体的五氧化二钒(V2O5)是接触法生产硫酸的催化剂。从废矾催化剂中回收V2O5,既避免污染环境又有利于资源的综合利用。废钒催化剂的主要成分如表2。

表2
以下是一种废钒催化剂回收工艺路线,请回答下列问题:

(1)酸浸时V2O5转化为VO2+,反应的离子方程式为___,同时V2O4转化成VO2+。废渣1的主要成分是___。
(2)氧化过程中欲使3mol的VO2+变为VO2+,则至少需要氧化剂KClO3___mol。

(1)酸浸时V2O5转化为VO+2,V元素的化合价不变,说明没有发生氧化还原反应,则反应的离子方程式为V2O5+2 H+==2 VO+2+H2O。由于SiO2与H2SO4不反应,故废渣1的主要成分为SiO2。(2)1molVO2+变为VO+2,V元素的化合价由+4价升高到+5价,转移1mol电子,1mol氧化剂KClO3被还原为KCl,Cl元素的化合价由+5价降低为-1价,转移6mol电子,故欲使3molVO2+变为VO+2,需氧化剂KClO3的物质的量至少为0.5mol。(3)酸浸并用KClO3氧化后的溶液中含有Fe3+、Al3+,在中和时生成Fe(OH)3、Al(OH)3沉淀,所以废渣2中含有Fe(OH)3、Al(OH)3。
答案:(1)V2O5+2H+==2VO+2+H2O SiO2(2)0.5 (3)Fe(OH)3、Al(OH)3
