奥曲肽联合前列地尔治疗肝硬化合并HRS疗效与安全性的Meta分析
2019-03-05石万红田瑞清胡苹苹梅昆有王峻峰
石万红 田瑞清 胡苹苹 梅昆有 王峻峰
肝肾综合征(hepatorenal syndrome,HRS)是终末期肝病中发现的功能性肾损伤的独特形式,主要发生在18%的失代偿肝硬化患者中[1]。导致内脏和全身性血管舒张和肾血管收缩的异常血流动力学改变,从而导致肾功能损害[2]。以前HRS有两种类型被确定, HRS 1型的特征是肾功能迅速恶化,不治疗的中位生存期约为2周;HRS 2型通常与难治性腹腔积液相关,进展相对较慢,生存期较长,平均中位生存期约6个月[3]。最近定义的HRS 3型是先天性疾病合并肾功能障碍和HRS 4型急性肝衰竭[3]。奥曲肽是人工合成的生长抑素8肽衍生物,其理化性质与生长抑素类似。奥曲肽可以下调循环中炎性介质,抑制其内毒素水平,具有保护细胞的作用,可能与减轻肝组织内质网应激反应机制有关[4]。前列地尔具有扩张血管,改善肾脏微循环,加强肾脏血流灌注,有效改善肾脏功能,还有抑制炎性反应、稳定溶酶体膜、保护肝细胞等功能[5]。鉴于肝硬化合并HRS的严重性,临床上迫切需要有效的药物干预来延长晚期肝硬化合并HRS患者的生存期,提高患者的生活质量。本研究主要对奥曲肽联合前列地尔治疗肝硬化合并HRS的疗效及安全性进行Meta分析,探讨联合用药的优越性,为临床药物治疗提供可靠依据。
资料与方法
1.检索策略:计算机检索PubMed、EMbase、Cochrane Library、中国知网、万方、维普及生物医学文献数据库(CBM)。检索时间从建库到2017年12月。中文检索词:肝硬化合并肝肾综合征,奥曲肽,前列地尔,前列腺素E1,治疗,随机对照试验;英文检索词:octreotide, sandostatin, octreotide acetate, octreotide acetate salt, alprostadil, PGE1 alpha, prostaglandin E1alpha, PGE1, Lipo PGE1, Prostaglandin E1, Liver cirrhosis, liver fibrosis, hepatic cirrhosis, cirrhosis of the liver, hepatorenal syndrome, HRS, treatment, therapy, randomized controlled trial。用以上检索词作为主题词或自由词,运用逻辑运算符制定检索式。通过人工检索部分纳入文献的相关参考文献,纳入所缺失的文献,有疑问或数据缺失的联系通讯作者。
2.纳入和排除标准:(1)纳入标准:①研究类型:国内外期刊公开发表的关于奥曲肽联合前列地尔治疗肝硬化合并肝肾综合征的随机对照试验(RCT)。文种限定中文和英文;②研究对象:所有肝硬化合并HRS患者均符合《慢性乙型肝炎防治指南(2015年版)》、《丙型肝炎防治指南(2015年更新版)》和《酒精性肝病诊疗指南》中的肝硬化诊断标准和2007年国际腹水俱乐部HRS诊断标准[6~9];③干预措施:治疗组采用治疗奥曲肽联合前列地尔治疗肝硬化合并HRS,对照组采用单用奥曲肽或者单用前列地尔或者常规用药治疗肝硬化合并HRS;④结局指标包括以下至少1种:临床总有效率、24h尿量、血肌酐(Scr)、尿素氮(BUN)、丙氨酸转氨酶(ALT)、总胆红素(TBiL)、心率(HR)、门静脉内径(DSV)、脾静脉内径(DPV)、平均动脉压(MAP)。(2)排除标准: ①原发性肾病或药物所致的急性肾损伤或肾衰竭或其他器质性肾病;②对奥曲肽或者前列地尔药物存在过敏者或精神异常者;③合并其他严重心脑血管系统性疾病者;④研究中的治疗组未进行奥曲肽联合前列地尔治疗肝硬化合并HRS的文献及分组或干预措施不明确的文献;⑤非RCT类文献,如回顾性研究、观察性研究、实验设计;⑥重复发表或资料不全的文献;⑦动物研究或细胞研究等非临床试验研究;⑧综述、文摘、病例报告、经验总结类文献;⑨未公开发表的研究;⑩无法获得全文的文献。

4.纳入文献的质量评价:根据Cochrane 协作网RCT评价手册的改良Jadad量表评估纳入研究的方法学质量,具体内容包括:①随机分配方法;②分配隐藏;③是否采用盲法;④撤出与退出;对于每项纳入的研究,按以上方面将纳入的文献分为3个等级[10]。A级:完全满足以上质量评价标准,提示低偏倚的可能性;B级:其中1条或多条质量评价标准部分满足或不清楚,提示中度偏倚的可能性;C级:其中1条或多条质量评价标准完全不满足,提示高度偏倚的可能性。其中低质量(1~3分)和高质量(4~7分)。

结 果
1.文献检索结果:通过计算机检索到74篇文献,通过剔除重复发表的文献及对照不符的文献,阅读题目及摘要后有14篇文献入选,进一步全文阅读后,最终有11篇文献入选[11~21]。11篇文献均为中文文献。文献发表时间为2012~2017年,包括肝硬化合并HRS患者人数为766例,其中治疗组386例,对照组380例。入选文献基本特征见表1,质量评价见图1。
2.临床总有效率:临床总有效率(%)=(显效例数+有效例数)/总例数×100%。①显效:治疗后患者24h尿量增加>1000ml,腰围、体质量减少>20%,Scr、ALT、BUN 和白蛋白等测得值恢复正常范围者;②有效:治疗后患者 24h 尿量增加>500ml,腰围、体重减少>10%,Scr、ALT 和 BUN 等测得值明显改善者;③无效,治疗后患者未达到治疗有效的标准者。10个研究均报道了显效、有效、无效例数及总有效率。异质性检验结果为P=0.98,I2=0%,无统计学异质性,故采用固定效应模型进行合并分析。结果显示, OR=3.65, 95%CI:2.52~5.28,P=0.000,两组比较差异有统计学意义,见图2[11~19,21]。
3.24h尿量:7篇文献均报道了治疗前后24h尿量的变化[11, 12, 14, 15, 17, 20, 21]。异质性检验结果为P=0.000,I2=96%,有统计学异质性,故采用随机效应模型进行合并分析。结果显示,MD=-480.35, 95% CI:-568.96~-391.73,P=0.000,两组比较差异有统计学意义,见图3。
4.Scr:9篇文献均报道了治疗前后Scr水平的变化[11, 12, 14~17, 19~21]。异质性检验结果为P=0.32,I2=13%,无统计学异质性,故采用固定效应模型进行合并分析。结果显示,MD=27.96, 95%CI:25.75~30.18,P=0.000,两组比较差异有统计学意义,见图4。

表1 纳入文献的基本特征
①临床总有效率;②24h尿量;③血肌酐(Scr);④尿素氮(BUN);⑤平均动脉压(MAP);⑥心率(HR);⑦门静脉内径(DSV);⑧脾静脉内径(DPV);⑨ALT;⑩TBiL

图1 方法学质量评价汇总图
5.BUN:7篇文献均报道了治疗前后BUN水平的变化[11, 12, 14, 15, 17, 20, 21]。异质性检验结果为P=0.84,I2=0%,无统计学异质性,故采用固定效应模型进行合并分析。结果显示,MD=4.08, 95%CI:3.18~4.97,P=0.000,两组比较差异有统计学意义,见图5。
6.ALT:4篇文献均报道了治疗前后ALT水平的变化[11, 12, 16, 19]。异质性检验结果为P=0.000,I2=96%,有统计学异质性,故采用随机效应模型进行合并分析。结果显示,MD=28.79, 95%CI:2.44~55.14,P=0.03,两组比较差异有统计学意义,见图6。
7.TBiL:3篇文献均报道了治疗前后TBiL水平的变化[11, 16, 19]。异质性检验结果为P=0.01,I2=76%,有统计学异质性,故采用随机效应模型进行合并分析。结果显示,MD=23.74, 95%CI:14.40~33.09,P=0.000,两组比较差异有统计学意义。
8.HR:3篇文献均报道了治疗前后HR的变化[15, 17, 21]。异质性检验结果为P=1.00,I2=0%,无统计学异质性,故采用固定效应模型进行合并分析。结果显示,MD=1.35, 95%CI:-0.30~3.00,P=0.11,两组比较差异无统计学意义。
9.DSV:3篇文献均报道了治疗前后DSV的变化[15, 17, 21]。异质性检验结果为P=1.00,I2=0%,无统计学异质性,故采用固定效应模型进行合并分析。结果显示,MD=1.16, 95%CI:0.68~1.63,P=0.000,两组比较差异有统计学意义。
10.DPV:3篇文献均报道了治疗前后DPV的变化[15, 17, 21]。异质性检验结果为P=0.94,I2=0%,无统计学异质性,故采用固定效应模型进行合并分析。结果显示,MD=1.28, 95%CI:0.77~1.78,P=0.000,两组比较差异有统计学意义。
11.MAP:2篇文献均报道了治疗前后MAP的变化[17, 21]。异质性检验结果为P=1.00,I2=0%,无统计学异质性,故采用固定效应模型进行合并分析。结果显示,MD=-1.70, 95%CI:-3.46~0.06,P=0.06,两组比较差异无统计学意义。
12.发表偏倚分析:以效应指标比值比为横坐标,以比值比对数标准误为纵坐标绘制倒漏斗图(图7),结果显示漏斗图左右对称性较好,提示本研究纳入的文献不存在明显的发表偏倚。对漏斗图进行Eegger′s检验,结果显示,t=2.07,P=0.072,漏斗图对称性较好,发表偏倚得到有效控制(表2)。

图2 两组临床总有效率的Meta分析森林图
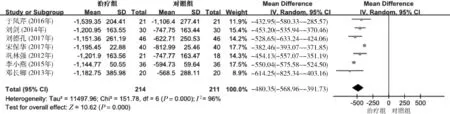
图3 两组治疗后24h尿量的Meta分析森林图

图4 两组治疗后Scr水平的Meta分析森林图

图5 两组治疗后BUN水平的Meta分析森林图

图6 两组治疗后ALT水平的Meta分析森林图

图7 两组患者临床总有效率的漏斗图
讨 论
肝硬化合并HRS的发病机制复杂,HRS预后差,2周内病死率高达80%[22]。据估计,大约有40%的肝硬化和腹腔积液患者5年内发展为HRS,50%的住院患者出现肝硬化并发症,并且一般在几天内发展为肾损伤[22]。因此,急切需要药物临床干预挽救患者生命。奥曲肽保留了天然生长抑素的药理活性,且半衰期长,能明显减少内脏血流量,改善有效循环血量,并且能减少血管紧张素和肾素的分泌,降低门脉压力以及具有抗损伤和保护肝细胞的作用[23]。前列地尔的主要成分是前列腺素E1,具有很强的扩血管作用,可靶向性的作用于肝肾血管,降低门静脉压力,改善高动力循环,促进肝细胞再生和肝功能恢复;提高血浆胶体渗透压,增加有效循环血量;降低内毒素、血栓素、白三烯等缩血管物质对肾血管的作用,并可扩张肾血管,加强缓激肽的扩血管作用,增加肾血流量,改善肾功能[24]。据相关报道,前列地尔所致的不良反应常发生在用药前3天,主要有静脉炎、皮疹、瘙痒、皮肤红肿、头晕、头痛、心慌、胸闷、心悸、腹泻、腹痛、四肢疼痛、四肢肿胀等[25]。
研究表明,奥曲肽联合前列地尔治疗肝硬化合并HRS具有更好的治疗效果,但是缺乏足够的循证医学证据。本研究纳入11个RCTs,总样本量766例,其中联合用药组386例,对照组380例。Meta分析结果显示,奥曲肽联合前列地尔治疗肝硬化合并HRS能提高患者临床总有效率,同时改善其肝肾功能指标,如显著降低患者ALT、TBiL、DSV、DPV水平及提高治疗后患者的24h尿量,差异有统计学意义(P<0.05);但对HR和MAP无影响,差异无统计学意义(P>0.05)。然而,对TBiL、HR、DSV、DPV和MAP的Meta分析中,TBiL、HR、DSV和DPV的纳入文献仅有3篇,MAP纳入的文献仅有2篇,因此,纳入的文献及样本量不足,结果可能存在一定的偏倚。所有文献中,联合用药组仅3例出现恶心和1例出现面部潮红的不适[13, 15];而对照组2例出现面部潮红不适[15]。所有患者耐受性较好、未停药。漏斗图显示所有研究左右基本对称,表明本研究不存在发表偏倚。进一步采用Egger′s检验显示,t=2.07,P=0.072,说明本研究不存在发表偏倚。纳入的所有研究中,除了24h尿量、ALT和TBiL的结局指标异质性较大外(I2>75%),其他结局指标均不存在较大的异质性(I2<25%)。异质性来源可能为患者的病情、病程、疗程、给药剂量和常规治疗方案等方面存在差异。但各研究指标的结果均提示联合用药比单用药具有更好的临床治疗有效性。
本研究存在一定的局限性,在全面检索了中英文权威数据库的情况下,严格按照纳入排除标准,纳入的文献全部为中文文献,未检索到相关的外文文献,文献质量不高,质量等级多为C级。所有纳入研究未详细介绍分配隐藏方法,导致研究结果具有一定的局限性。虽然Egger′s检验显示本研究纳入的文献不存在明显的发表偏倚,但在所有文献中,只有孟娜娜的研究提到了双盲,刘德孔和刘剑的研究按随机数字表法的分配,李小燕、于凤芹和巩林强的研究按入院顺序或按治疗用药分配,分配方式不合理。其余的研究中只提到了随机,未详细说明采用具体方法。对ALT、TBiL、MAP、HR、DSV、DPV评价时,纳入的文献数量较少,样本量小,且疗程不均一。特别是24h尿量、ALT、TBiL存在较大的统计学异质性,且严格遵照其纳入排除标准异质性均不能消除。因此,有必要更多关注国内外相关文献来完善系统评价。
综上所述,奥曲肽联合前列地尔能明显提高肝硬化合并HRS患者的临床总有效率,改善其肝肾功能,降低ALT、TBiL、Scr、BUN水平及提高患者治疗后24h尿量。并且可减小患者的DSV和DPV,但对MAP和HR无影响。虽然个别研究报道了不良反应的发生,但仍不能忽视联合治疗中的不良反应。因此,奥曲肽联合前列地尔治疗肝硬化合并HRS的疗效及安全性还需进一步大样本、多中心、高质量、双盲、随机对照试验来加以验证。
