磁固相萃取结合高效液相色谱检测农田灌溉水中4种苯甲酰脲类农药
2019-01-22贾叶青念琪循冀欠欠徐厚君王曼曼王学生郝玉兰
贾叶青,念琪循,张 磊,冀欠欠,徐厚君,王曼曼,王学生,郝玉兰
(华北理工大学 公共卫生学院 河北 唐山 063210)
苯甲酰脲类农药(Benzoylurea pesticides,BUs)是一种高效的昆虫生长调节剂,具有杀虫率高,杀虫谱宽,残留量低等特点,广泛应用于粮食、蔬菜、水果等病虫害防治[1]。然而,BUs农药的广泛使用容易造成农田土壤及灌溉水污染,进而经渗透或蒸发等途径进入环境水系中。已有学者在农田灌溉水、河水以及湖水等环境水系中检测到虱螨脲、氟铃脲等BUs的存在[2-3]。虽然目前相关部门并未制定环境水中BUs的限量标准,但研究发现,水栖生物特别是甲壳类(虾、蟹幼体)对BUs存在敏感反应。美国环境保护局已将部分苯甲酰脲类农药定为Ⅲ类毒性或Ⅳ类毒性的中等毒性农药[4]。由于BUs种类较多,本文以4种常用的BUs作为目标物,对农田灌溉水中的BUs残留进行分析,以期为该类农药的合理使用和环境安全评价提供数据。
目前,BUs的分析方法主要包括高效液相色谱-紫外检测、高效液相色谱-串联质谱检测等方法[5-6]。但鉴于实际水样的基底成分复杂,且BUs往往处于痕量水平,因此,有效、简单且快速的前处理技术是决定分析方法准确度和灵敏度的关键。目前,BUs分析常用的前处理方法包括液液萃取、固相萃取及纤维固相微萃取等[6-8]。
磁性固相萃取技术(MSPE)是一种新型固相萃取技术,其通过施加外部磁场以实现吸附剂与样品溶液的快速分离。相比于传统的前处理方法,MSPE的操作简单,样品分析速度快,且避免了填充柱的背压高等问题。金属-有机骨架(MOFs)是以有机配体中的氧原子和氮原子连接无机金属离子形成的多孔晶体材料,具有比表面积大、孔道可调控等特性,在吸附分离方面具有明显优势[9-11]。将MOFs引至磁性固相萃取技术,一方面可利用磁性纳米粒子的超顺磁特点,使其在外部磁场作用下与样品溶液快速分离;另一方面可充分发挥MOFs较强的吸附性能,以达到高效富集痕量物质的目的。2005年,法国Férey等[12]率先采用Cr(Ⅲ)与对苯二甲酸键合而成MIL-101,该材料呈立方结构,比表面积达4 000 m2/g以上,在水及有机溶剂中具有优良的稳定性,被广泛用于吸附、催化等领域[13-14]。2014年,Huang等[15]制备了功能化复合材料Fe3O4-NH2@MIL-101,该材料中MIL-101对BUs的苯环结构具有较强的π-π共轭作用;而Fe3O4-NH2的加入则提高了材料在水中的分散性,增加了材料与BUs的接触面积,进一步提高了吸附效率;且BUs本身具有强疏水性,易从水溶液中吸附分离。
基于此,本研究将Fe3O4-NH2@MIL-101复合材料作为磁固相萃取介质,结合高效液相色谱-紫外法,发展了一种简便、快速检测农田灌溉水中4种BUs残留的分析方法。
1 实验部分
1.1 仪器与试剂
Agilent 1260高效液相色谱,配有紫外检测器(美国Agilent公司);100 mL水热合成反应釜(天津凯易达仪器设备销售有限公司);JEM-2800F聚焦离子束-电子束双束电镜(美国FEI仪器有限公司);Nicolet-6700傅立叶变换红外光谱分析仪(美国Thermo公司);XRD-6100型X射线衍射仪(日本岛津公司);LDJ 9600-1型振动样品磁强计(美国LDJ电子仪器公司);DZF-6020型真空干燥箱(上海博讯实业有限公司);LC-36热风循环烘箱(上海旦顺实业有限公司)。
九水合硝酸铬、对苯二甲酸、1,6-己二胺(分析纯,上海阿拉丁试剂有限公司);甲醇(MeOH)、乙腈(ACN)(色谱纯,美国Fisher公司);丙酮(DMK)、乙酸乙酯(EA)、无水乙酸钠、六水合氯化铁、乙二醇、N,N-二甲基甲酰胺(DMF)、无水乙醇(分析纯,天津光复试剂有限公司);实验用水为超纯水。
4种BUs标准品:氯吡脲、氟幼脲、虱螨脲(纯度≥98%,国家标准物质资源共享平台),氟铃脲(纯度≥98%,上海阿拉丁试剂有限公司),用乙腈配制成1 mg/mL标准储备液,于4 ℃储存待用。
1.2 样品采集
样品采集自河北省唐山市曹妃甸区不同农田灌溉水出水口,水样分析之前经0.45 μm的滤膜过滤以除去悬浮颗粒。
1.3 磁性金属有机骨架吸附材料的制备与表征
将0.65 g六水合氯化铁分散于20 mL乙二醇中,加入1.3 g无水乙酸钠,超声混匀后,加入5 mL 1,6-己二胺,于50 ℃下搅拌均匀。将混合溶液转移至聚四氟乙烯内衬反应釜中,置于预先加热至190 ℃的烘箱中反应10 h。反应釜在烘箱中冷却至室温,所得产物用水和无水乙醇洗涤,60 ℃真空干燥12 h后,得到Fe3O4-NH2。
将2 g九水合硝酸铬和0.83 g对苯二甲酸溶于15 mL水中,磁力搅拌3 h后,超声10 min,再加入0.1 g Fe3O4-NH2和5 mL水。将反应溶液转移至聚四氟乙烯内衬反应釜中,220 ℃下反应18 h。冷却至室温,施加外部磁场将产物与反应介质分离,经DMF、乙醇和水清洗产物,100 ℃下真空干燥过夜,得到Fe3O4-NH2@MIL-101磁性吸附剂。
对制备的Fe3O4-NH2@MIL-101磁性吸附剂进行表征:采样扫描电子显微镜、红外光谱及X射线衍射考察Fe3O4-NH2@MIL-101的表面形貌、基团和晶体结构,通过振动样品磁强计考察吸附剂的磁性强弱。
1.4 高效液相色谱分析条件
色谱柱为Agilent EC-C18(4.6 mm×150 mm,4 μm),采用梯度洗脱方式,流动相A为水,B为乙腈,洗脱程序为:0~5 min,B由40%线性增加至65%;5~7 min,B由65%线性增加至80%,7~12 min,B保持80%至分析结束。流速为1 mL/min,检测波长为260 nm,柱温22 ℃,进样量10 μL。
1.5 磁性固相萃取流程
称取22 mg磁性吸附剂Fe3O4-NH2@MIL-101加至100 mL水样中,吸附15 min后,施加外部磁场将吸附剂与样品溶液分离,弃去上清液。采用0.5 mL甲醇对BUs进行洗脱,充分振荡3 min后磁分离,重复3次后合并洗脱液,氮吹浓缩后用甲醇定容至1 mL,待测。
2 结果与讨论
2.1 Fe3O4-NH2@MIL-101的表征
对Fe3O4-NH2@MIL-101进行扫描电镜分析(SEM),可观察到Fe3O4纳米粒子均匀地附在MIL-101表面(图1A),表明二者已成功复合。对吸附剂的磁强度进行考察,得到Fe3O4-NH2@MIL-101吸附剂的磁化饱和度值为27.7 emu·g-1(图1B),表现出较强磁性,能够在外加磁场作用下与样品溶

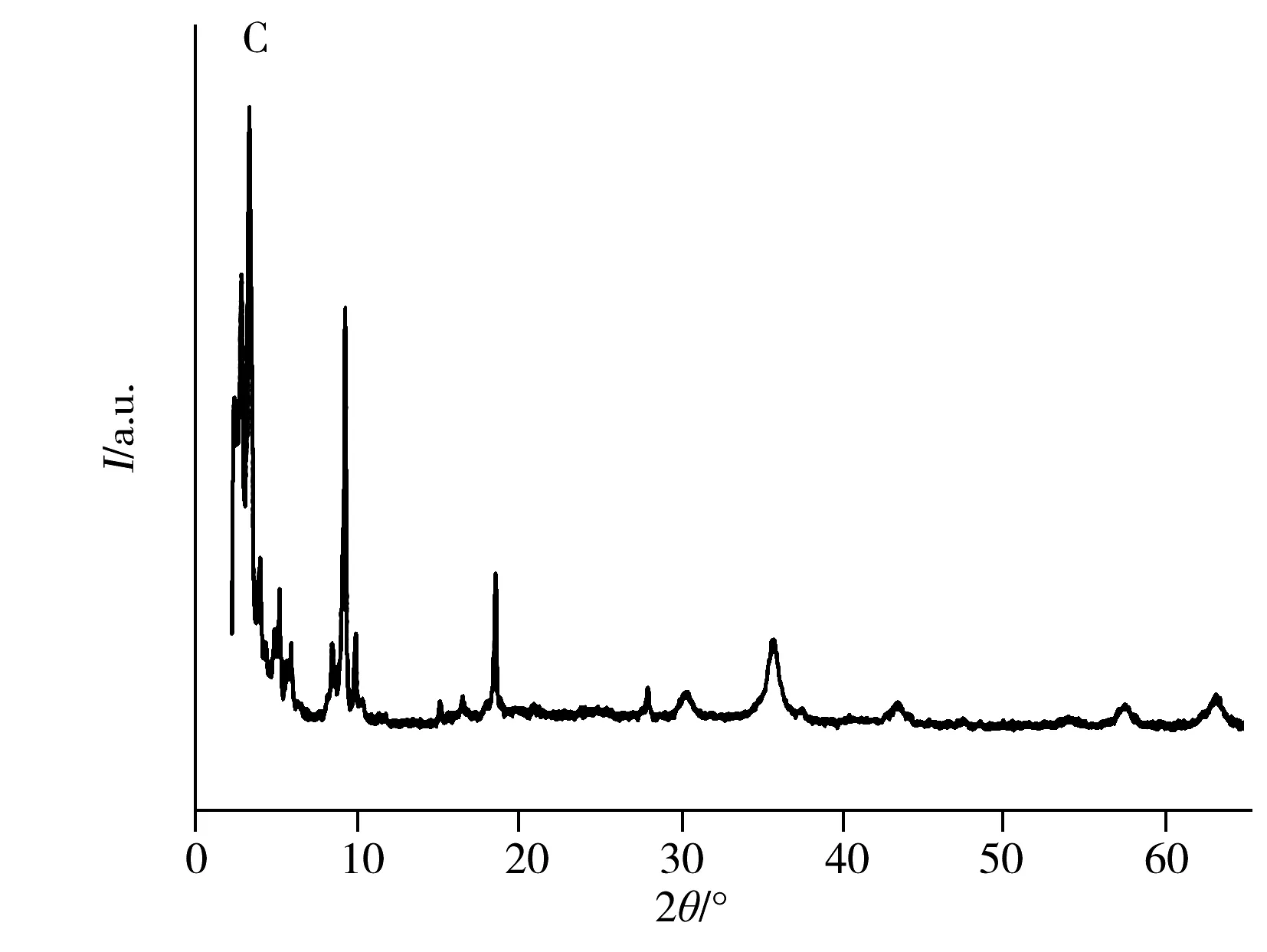
液快速分离。采用X射线晶体衍射进一步鉴别材料的晶体结构,可观察到衍射图中保留了Fe3O4-NH2的6个特征峰和MIL-101的2个特征峰(图1C),表明该复合材料由Fe3O4-NH2和MIL-101组成,与文献一致[13]。为了进一步验证复合材料的构成,对其进行红外光谱(FT-IR)分析(图1D),可观察到在3 415 cm-1处出现典型的—OH和—NH伸缩振动峰,1 506 cm-1和1 690 cm-1处的吸收峰可归属为有机配体对苯二甲酸中—COOH的不对称拉伸,578 cm-1处的吸收峰则由Fe—O键伸缩振动引起,这些特征峰说明了Fe3O4-NH2和MIL-101的存在。
2.2 磁性固相萃取条件的优化
吸附和洗脱过程是影响磁固相萃取效果的关键,因此实验对吸附剂用量、吸附时间等吸附条件,以及洗脱溶剂种类与体积等洗脱条件进行了优化。优化过程采用100 mL混合标准水溶液进行实验,其中氯吡脲的质量浓度为10 μg/L,氟幼脲、氟铃脲、虱螨脲的质量浓度均为30 μg/L。所有实验均平行3次。
2.2.1吸附条件的优化吸附剂的用量和时间决定了前处理过程的效率和成本。实验考察了吸附剂用量分别为16、18、20、22、24 mg,吸附时间分别为12、13、14、15、16 min时,对4种BUs萃取效率的影响,结果显示,随着磁性吸附材料用量的增加和吸附时间的延长,4种BUs的吸附效率也随之提高。当吸附剂用量为22 mg,吸附时间为15 min时,吸附效率达到最高,继续增加吸附用量和吸附时间,吸附效率保持稳定。图2A为吸附剂用量对BUs萃取效率的影响。后续实验选择最佳吸附剂用量为22 mg,最佳吸附时间为15 min。
离子强度和pH值也会影响萃取效率。在溶液中分别加入不同浓度(0%、0.5%、1.0%、1.5%、2.0%,m/v)NaCl调节离子强度,以考察离子强度对萃取效率的影响。结果显示,4种BUs的吸附效率随着NaCl浓度的增加而增加,当NaCl浓度达到1.5%时,吸附效率最好,继续增加NaCl浓度,吸附效率逐渐降低。实验确定NaCl的最佳浓度为1.5%。另外,在pH 2.0~8.0范围内探讨了溶液pH值对吸附效率的影响。由图2B可以看出,BUs的吸附效率在pH 5.0时达到最大,因此实验选择pH值为5.0。
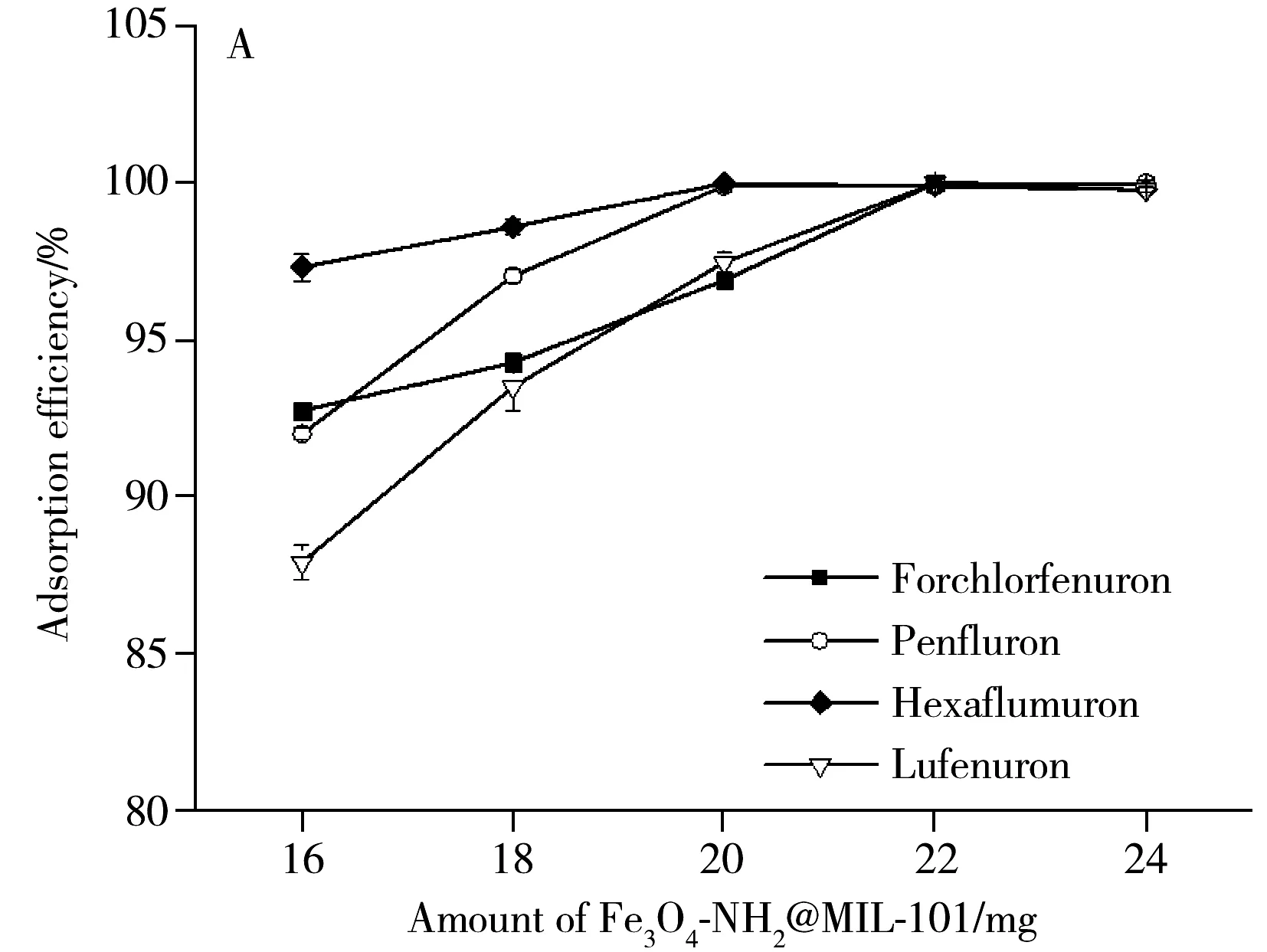

图3 洗脱溶剂种类对BUs洗脱效率的影响Fig.3 Effect of eluent type on elution efficiencies of BUs
2.2.2洗脱条件的优化考察了甲醇、乙腈、丙酮和乙酸乙酯4种溶剂对BUs的洗脱效果,结果显示,甲醇的洗脱效率达到85%(图3),明显高于其他3种溶剂,因此实验选择甲醇作为洗脱溶剂。
实验同时考察了不同洗脱时间(1、3、6、9、12 min)及洗脱体积(0.5 mL、0.5×2 mL、0.5×3 mL、0.5×4 mL、0.5×5 mL)对BUs洗脱效率的影响。结果表明,当洗脱时间为9 min,洗脱体积为0.5×3 mL时的洗脱效率最佳。
2.3 方法验证
在优化实验条件下,配制了一系列BUs的标准工作溶液,以峰面积(y)对BUs质量浓度(x,mg/L)作图。如表1所示,氯吡脲在0.010~1.0 mg/L范围内,氟幼脲和氟铃脲在0.015~3.0 mg/L范围内,虱螨脲在0.030~3.0 mg/L范围内,线性关系良好,相关系数均大于0.999 5。氯吡脲、氟幼脲、氟铃脲、虱螨脲的检出限(LOD,S/N=3)分别为0.03、0.05、0.05、0.09 μg/L,定量下限(LOQ,S/N=10)分别为0.10、0.17、0.17、0.30 μg/L。

表1 基于Fe3O4-NH2@MIL-101磁固相萃取4种BUs的分析特征量Table 1 Analytical performance data for 4 BUs by Fe3O4-NH2@MIL-101 based MSPE technique
对实际农田灌溉水样进行3个水平的加标回收实验,4种物质的加标浓度见表2,所有实验平行3次,计算方法的加标回收率与相对标准偏差(RSD)。由表2可知,4种BUs的回收率为81.7%~95.4%,方法的日内和日间RSD分别为2.2%~6.8%和4.7%~9.4%。

表2 Fe3O4-NH2@MIL-101磁性固相萃取灌溉水中BUs的回收率及相对标准偏差(RSD)Table 2 Recoveries and RSDs obtained in the determination of BUs from spiked irrigation water samples by using Fe3O4-NH2@MIL-101 as sorbent
2.4 实际样品的分析
在最优实验条件下,对5份农田灌溉水样品中的BUs进行萃取和分析,5份样品均未检出BUs。对样品进行加标回收实验,加标浓度为1.0 mg/L氯吡脲和3.0 mg/L氟幼脲、氟铃脲、虱螨脲,图4为空白样品(A)、样品加标后未经MSPE(B)和经MSPE(C)处理的色谱图,由图4B、C可见,4种BUs经Fe3O4-NH2@MIL-101吸附剂MSPE处理后,能够得到有效富集,富集倍数达100倍。

2.5 与文献方法对比
将本方法与文献报道的其他前处理技术结合高效液相色谱检测BUs的结果进行对比(见表3)。结果显示,在回收率与检出限相当的情况下,本方法所需的吸附剂用量少,吸附时间仅需15 min,且只需在外加磁场作用下即可完成对目标物的萃取,无需过滤和离心,方法快速、简单。

表3 本方法与其他前处理技术结合高效液相色谱对BUs检测的比较Table 3 Comparison with this work and the reported techniques for determination of BUs in various samples using HPLC
a:multiple monolithic fiber solid-phase microextraction,b:solid-phase extraction,c:thin film microextraction;*:no data
3 结 论
本研究将Fe3O4-NH2@MIL-101用于固相萃取水中BUs的残留,结合高效液相色谱-紫外检测,发展了一种简单、快速检测农田灌溉水中BUs残留的分析方法。Fe3O4-NH2@MIL-101磁性萃取充分利用了MIL-101的吸附能力,以及磁性固相萃取操作简单的优势,使其在外部磁场作用下可迅速分离目标物,从而避免了离心、过滤等操作。方法操作简单、快速,为水中BUs的前处理方法提供了新选择。
