热解条件对CuCe-O/γ-Al2O3催化性能的影响
2018-11-03张传驹李明航谈冠希靳广洲
张传驹,李明航,谈冠希,苗 杰,靳广洲
(北京石油化工学院 化学工程系 燃料清洁化及高效催化减排技术北京市重点实验室,北京 102617)
随着人们环保意识的逐渐增强和全球环保法规的日益苛刻,大气污染物(如CO,NOx)的治理引起了政府和广大学者的关注[1-5]。而在炼油行业的催化裂化再生过程中会产生大量的CO,故需要加入CO助燃剂进行控制。目前CO助燃剂的研究大部分集中在Pt,Pd等[6-9]具有良好的CO催化性能的贵金属上,但由于贵金属资源匮乏,价格昂贵,影响其应用的经济性。以价格低廉且具有良好的催化氧化活性的非贵金属取代贵金属Pt,Pd催化剂已成为当今的一种趋势。非贵金属中的过渡金属(Cu,Mn,Co,Fe等)[10-14]在氧化还原反应中被人们广泛研究,但受它们自身结构的限制,单一组分非贵金属的氧化还原反应活性明显低于相应的Pt,Pd等贵金属。稀土元素氧化物如CeO2存在Ce4+和Ce3+的可逆性转换,具有独特的储存和释放氧的能力[15-16],但CeO2作为氧化还原催化剂单独使用时活性较差。CeO2与CuO按某种比例组合后却表现出很好的协同效应,在CuO-CeO2两相共生共存体系中,CeO2在二相共生过程中微调了CuO的结构,引起CuO相晶胞体积增大和Cu2+物种被还原为低价Cu+物种并产生相应的氧空位,使得CuO的氧化还原活性大幅度提高,可媲美于贵金属催化剂[17]。
本工作采用柠檬酸络合法制备了CuCeO/γ-Al2O3催化剂,通过控制热解过程中环境的含氧量和热解温度,探索了在柠檬酸热解过程中热解条件对CuO-CeO2二相共生共存性能的影响。
1 实验部分
1.1 试剂
Cu(NO3)2·3H2O,Ce(NO3)3·6H2O:AR,国药集团化学试剂有限公司;柠檬酸:CP,北京化工厂;γ-Al2O3:工业级,山东铝业公司。
1.2 催化剂的制备
采用柠檬酸络合法制备CuCe-O/γ-Al2O3试样。金属氧化物负载量为12.50%(w),按Cu/Ce摩尔比为7∶3配制Cu2+和Ce3+的混合溶液,加入适量柠檬酸混合均匀,静置过夜。按饱和浸渍法将混合液浸渍到γ-Al2O3载体上,搅拌、陈化,在烘箱中110 ℃低温下干燥。将烘干后的试样放到管式炉中热解2 h,热解气氛分别为15%(φ)空气+ 85%(φ)N2、30%(φ)空气+70%(φ)N2的混合气,热解温度分别为200,230,245 ℃。将热解后的试样在N2气氛、580 ℃下于管式炉中钝化2 h,所得试样标记为 CuCe-O/γ-Al2O3-x%Air-y℃,x表示热解时空气的体积百分含量,y表示热解温度。
1.3 表征方法
试样相分析在日本理学公司D/Max-2600/PC型强力转靶X射线衍射仪上进行,工作条件为:CuKα射线,管电压40 kV,管电流100 mA,石墨单色器,闪烁计数器,入射狭缝1°,接收狭缝0.3 mm,扫描速度2(°)/min,步宽0.02,扫描范围2θ=8°~80°。
H2-TPR分析在泛泰仪器公司FINESORB-3010型程序升温化学吸附仪上进行,在石英试样管中装入(100±0.1)mg试样(40~60目),在Ar气流中于400 ℃下预处理40 min,然后降至室温,用5.0%(φ)H2/95.0%(φ)Ar吹扫30 min,至检测器基线稳定,由室温开始程序升温至700 ℃并稳定30 min,升温速率为10 ℃/min,热导池检测器。
试样的比表面积测定在北京金埃谱科技有限公司的V-Sorb 2800TP型比表面积及孔径分析仪上进行,N2吸附法。
试样的形貌特征在FEI公司的Quante 400F型场发射扫描电子显微镜上进行,工作电压为20 kV。将试样研磨,使试样颗粒均匀后再进行测定。
1.4 催化剂的性能评价
催化剂的CO氧化性能评价在连续固定床微反装置上进行。催化剂的装填量为(20±0.1)mg,反应气组成(φ)为:CO 6.00%,O23.64%,He为平衡气,反应气态空速90 000 h-1;将(20±0.1)mg试样与200 mg石英砂混合,然后将混合物装入用石英棉支撑的石英管反应器中,用精度±0.1 K的铠装热电偶控制反应床层温度。催化剂在He流中100 ℃下预处理1 h,然后转为反应气进行反应。反应尾气用北京北分瑞利分析仪器有限公司的SP-3420A型气相色谱仪进行检测,5A分子筛柱,TCD检测。每个反应点取5次结果的平均值计算催化剂对CO氧化性能的转化率。CO氧化的转化率X计算见式(1)。

式中,A1和A2分别为催化剂反应前后CO的积分峰面积。
2 结果与讨论
2.1 XRD表征结果
γ-Al2O3及30%(φ)空气 +70%(φ)N2的热解气氛中不同热解温度下制备的CuCe-O/γ-Al2O3试样的XRD谱图见图1和图2。从图1和图2可 看 出,2θ= 19.580°,31.936°,37.603°,39.491°,45.788°,60.457°,66.761°处的衍射峰分别归属于γ-Al2O3的(111),(220),(311),(222),(400),(511),(440)晶面的衍射(JCPDS 29-0063),为典型的γ-Al2O3的特征谱(JCPDS 29-0063)。 在 30%(φ) 空 气 + 70%(φ)N2弱氧气氛中,200 ℃热解温度制备的CuCe-O/γ-Al2O3试样的XRD谱图中归属于γ-Al2O3的晶相峰保持完好,在 2θ= 28.555°,56.335°处出现了归属于CeO2的(111)晶面和(311)晶面的衍射峰,未发现明显CuO的晶相峰,表明制备的CuCe-O/γ-Al2O3中CuO呈高度分散状态,没有形成明显的CuO晶体,在XRD谱图中观测不到归属于CuO的晶相峰出现。从图2还可看出,将热解温度提高至230 ℃和245 ℃制备的CuCe-O/γ-Al2O3试样的XRD谱图没有明显变化,表明热解温度基本不影响活性组分的物相结构及分散状态。
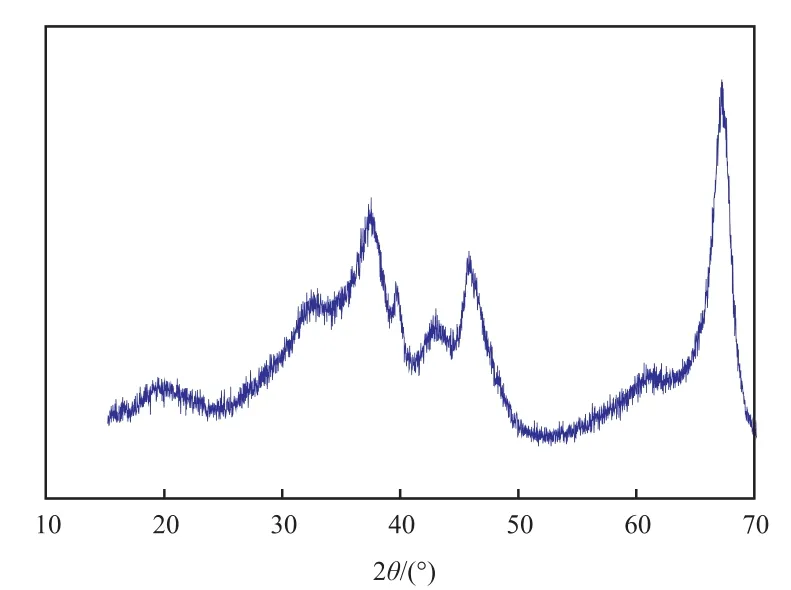
图1 γ-Al2O3的XRD谱图Fig.1 XRD pattern of γ-Al2O3.
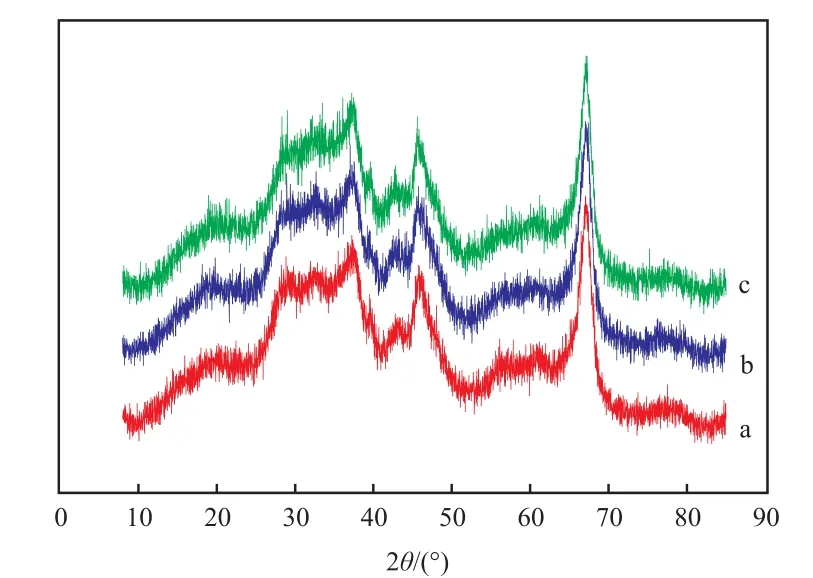
图2 30%(φ)空气+ 70%(φ)N2热解气氛中不同热解温度下制备的CuCe-O/γ-Al2O3试样的XRD谱图Fig.2 XRD patterns of CuCe-O/γ-Al2O3 samples prepared at different temperatures in 30%(φ)air+70%(φ)N2 atmosphere.
230 ℃热解温度下,不同热解气氛制备的CuCe-O/γ-Al2O3试样的XRD谱图见图3。由图3可看出,在230 ℃热解温度下,100%(φ)空气富氧气氛,30%(φ)空气+ 70%(φ)N2弱氧气氛及15%(φ)空气+ 85%(φ)N2弱氧气氛中热解制备的CuCe-O/γ-Al2O3试样物相中除归属于 γ-Al2O3的XRD特征峰外,也出现了归属于CeO2(111)晶面和(311)晶面的衍射峰,观测不到归属于CuO的特征衍射峰。表明改变热解气氛基本不影响活性组分的物相结构及分散状态。
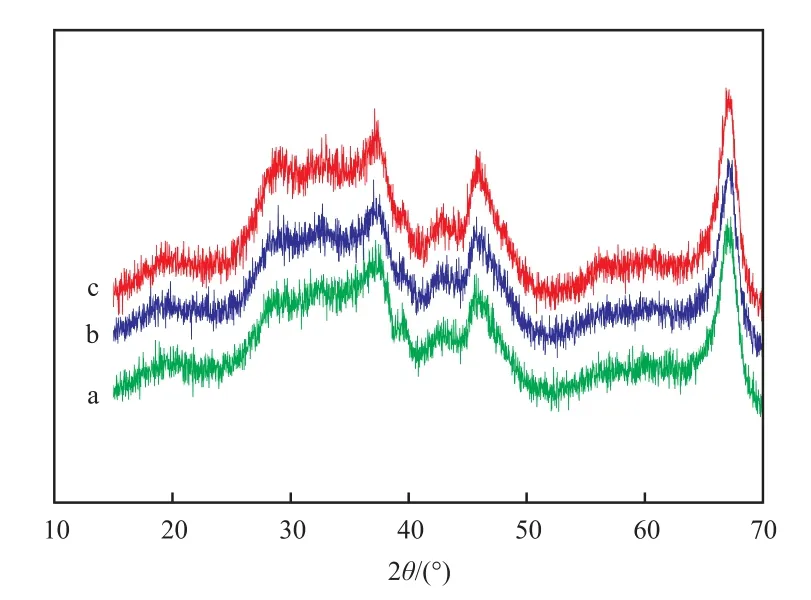
图3 230 ℃下不同热解气氛制备的CuCe-O/γ-Al2O3试样的XRD谱图Fig.3 XRD patterns of CuCe-O/γ-Al2O3 samples prepared in different atmospheres at 230 ℃.
2.2 H2-TPR表征结果
230 ℃热解温度下,不同热解气氛中制备的CuCe-O/γ-Al2O3试样的H2-TPR表征结果见图4。
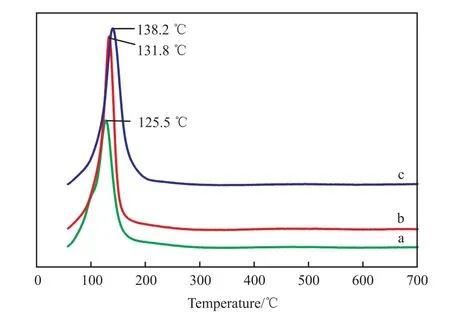
图4 230 ℃温度下不同热解气氛制备的CuCe-O/γ-Al2O3试样的H2-TPR谱图Fig.4 H2-TPR profiles of CuCe-O/γ-Al2O3 samples prepared in different atmospheres at 230 ℃.
从图4可看出,在230 ℃热解温度下,100%(φ)空气热解气氛中制备的CuCe-O/γ-Al2O3试样的H2-TPR还原温度峰值位于138.2 ℃,30%(φ)空气+ 70%(φ)N2弱氧气氛中热解制备的CuCe-O/γ-Al2O3试样的H2-TPR还原温度降至131.8 ℃,下降了6.4 ℃,15%(φ)空气+85%(φ)N2气氛中热解制备的CuCe-O/γ-Al2O3试样的H2-TPR还原温度降至125.5 ℃,下降了12.7 ℃。Ce(NO3)3和Cu(NO3)2的柠檬酸溶液中,每个柠檬酸分子可机会均等地络合一个Ce3+和一个Cu2+,或2个Ce3+或2个Cu2+,形成存在于水中的柠檬酸金属络合物。将此柠檬酸络合液浸渍在γ-Al2O3载体上,经低温烘干脱除水分后,柠檬酸金属络合物均匀分布在γ-Al2O3载体上。热解过程中,柠檬酸会迅速分解为H2O和CO2,同时爆发式析出所有的Cu2+和Ce3+,形成Cu或Ce的氧化物,并相互均匀地混合。此时的铜氧化物为CuO,而铈氧化物由于柠檬酸络合的是Ce3+,热解时析出速度过快,Ce3+未能全部氧化为Ce4+,最初形成的铈氧化 物 为且Ce3+占较大的比例。此时一方面从环境的空气中获得部分氧,使部分Ce3+氧化为Ce4+,另外由于CuO与氧化铈颗粒细小且分布均匀并紧密接触,因此氧化铈还可以从CuO获取部分氧,使部分Ce3+转化为Ce4+,相应的Cu2+转换成Cu+,同时也会伴随着相应氧空位的产生[18-20]。热解气氛中氧气含量直接影响到Ce3+/Ce4+变价过程中Ce3+从CuO中获取氧的趋势,热解气氛中氧气含量的减少,使铈氧化物从环境中获取氧受到限制,增强了CuO/CeO2两相间的相互作用,加剧了Ce3+从CuO中获取氧的趋势,使CuO相中Cu+增多,氧空位也增多,形成了具有非完整结构的表相提高了氧化铜的氧化还原能力[17]。随着热解气氛中氧气含量的减少,制备的CuCe-O/γ-Al2O3试样的H2-TPR还原峰温度逐渐向低温区偏移,与100%(φ)空气热解气氛相比,15%(φ)空气+85%(φ)N2热解气氛中制备的CuCe-O/γ-Al2O3试样的H2-TPR还原温度下降了12.7 ℃。
15%(φ)空气+85%(φ)N2热解气氛中,不同热解温度制备的CuCe-O/γ-Al2O3试样的H2-TPR表征结果见图5。从图5可看出,在15%(φ)空气+85%(φ)N2弱氧气氛中,230 ℃热解温度下制备的CuCe-O/γ-Al2O3试样的H2-TPR还原温度降至125.5 ℃。与之相比,200 ℃热解温度下制备的CuCe-O/γ-Al2O3试样的H2-TPR还原温度位于127.0 ℃,上升了1.5 ℃,而245 ℃热解温度下制备的CuCe-O/γ-Al2O3试样的H2-TPR还原温度升至128.2 ℃,升高了2.7 ℃。在弱氧气氛下热解时,Ce3+从CuO相中夺取氧导致部分Cu2+变为Cu+的几率增大。当热解温度为230 ℃时,柠檬酸分解较为充分,CuO/CeO2两相的相互作用达到最佳,此时Ce3+最大限度地从CuO中获取氧,使得Cu+/Cu2+的相对含量达到最大,制备的CuCe-O/γ-Al2O3试样的H2-TPR还原温度降至最低。当热解温度降至200 ℃时,由于热解温度较低柠檬酸分解不够完全,会有部分积碳残余,影响CuO/CeO2两相的相互作用,此时Ce3+不能最大限度地从CuO中获取氧,引起制备的CuCe-O/γ-Al2O3试样的H2-TPR还原温度有所上升。当热解温度升高到245 ℃时,过高的热解温度反而加强了Ce3+从热解气氛中夺取氧的能力,从而减弱了CuO/CeO2两相间的相互作用,引起Cu+/Cu2+的相对含量减小,制得试样的H2-TPR还原温度明显升高。
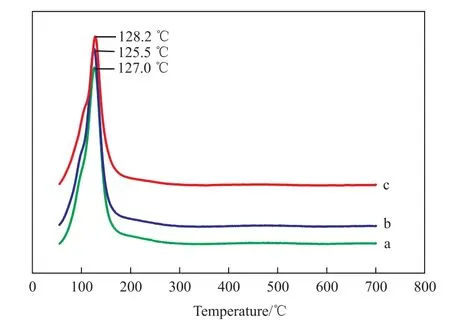
图5 15%(φ)空气+85%(φ)N2热解气氛中不同热解温度制备的CuCe-O/γ-Al2O3试样的 H2-TPR 谱图Fig.5 H2-TPR profiles of CuCe-O/γ-Al2O3 samples prepared at different temperatures in 15%(φ)air+85%(φ)N2 atmosphere.
2.3 BET表征结果
230 ℃热解温度下,不同热解气氛中制备的CuCe-O/γ-Al2O3试样的BET表征结果见表1。从表1可看出,实验用γ-Al2O3载体的比表面积为152 m2/g。由于金属活性组分峰负载,制备的CuCe-O/γ-Al2O3试样的比表面积明显下降。对比表1可以看出,230 ℃热解温度下制备的CuCe-O/γ-Al2O3试样的比表面积随热解气氛中氧含量的增大略有提高。改变热解气氛,增大热解气氛中的氧含量,有利于减少柠檬酸热解过程中部分积碳的残余,从而有利于增大其比表面积,但整体差异相对较小。热解 气氛 中 氧 含 量 增 大 对从环境气氛中获得部分氧使部分Ce3+氧化为Ce4+的几率增大,从而影响从CuO获取部分氧使相应的Cu2+转换成Cu+的几率减小,形成具有非完整结构的表相的几率减小,相应产生的氧空位亦减少,不利于氧化铜的氧化还原能力的提高。综合考虑,在230 ℃热解温度下,以15%(φ)空气+85%(φ)N2弱氧的热解气氛较为适宜。
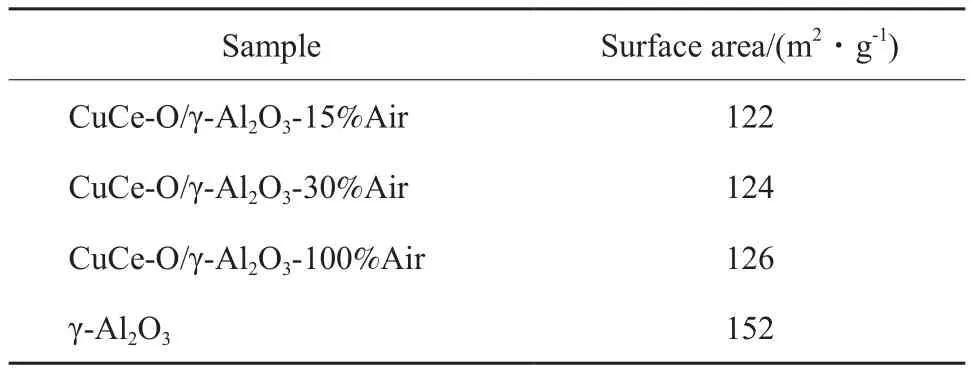
表1 230 ℃下不同热解气氛制备的CuCe-O/γ-Al2O3试样的比表面积Table 1 BET surface areas of CuCe-O/γ-Al2O3 samples prepared in different atmospheres at 230 ℃
15%(φ)空气+85%(φ)N2弱氧气氛中,不同热解温度下制备的CuCe-O/γ-Al2O3试样的BET表征结果见表2。从表2可看出,在15%(φ)空气+85%(φ)N2弱氧气氛中制备的CuCe-O/γ-Al2O3试样的比表面积随热解温度的升高略有增大,但差异化相对较小。考虑到热解温度升高对Ce3+从热解气氛中夺取氧的能力的影响,结合相应的H2-TPR还原温度的数据,在15%(φ)空气+85%(φ)N2弱氧的热解气氛中,选用230 ℃热解温度较为适宜。

表2 15%(φ)空气+85%(φ)N2热解气氛中不同热解温度制备的CuCe-O/γ-Al2O3 试样的比表面积Table 2 BET surface areas of CuCe-O/γ-Al2O3 samples prepared at different temperatures in 15%(φ)air+85%(φ)N2 atmosphere
2.4 SEM表征结果
230 ℃热解温度下,不同热解气氛中制备的CuCe-O/γ-Al2O3试样的SEM表征结果见图6。

图6 230 ℃温度下不同热解气氛制备的CuCe-O/γ-Al2O3试样的SEM照片Fig.6 SEM images of CuCe-O/γ-Al2O3 samples prepared in different atmospheres at 230 ℃.
从图6可看出,与相应的γ-Al2O3载体相比,CuCe-O/γ-Al2O3-15%Air-230 ℃试样的形貌没有大的变化,金属活性组分在γ-Al2O3载体上分散状态较好,表明230 ℃热解温度下,改变热解气氛未对CuCe-O/γ-Al2O3-15%Air-230 ℃试样的形貌产生大的影响。
2.5 CO氧化反应实验结果
在连续固定床微反装置上考察了15%(φ)空气+85%(φ)N2气氛中和30%(φ)空气+70%(φ)N2气氛中不同热解温度下制备的CuCe-O/γ-Al2O3试样CO氧化活性的反应结果见表3。由表3可看出,相同热解气氛中不同热解温度下制备的CuCe-O/γ-Al2O3试样在同一反应温度下催化氧化CO的反应转化率不同,其中,230 ℃热解温度下制备的CuCe-O/γ-Al2O3试样的催化氧化CO活性最高,与H2-TPR表征结果相一致,进一步验证了15%(φ)空气+85%(φ)N2气氛即弱氧气氛中,230 ℃热解温度下,柠檬酸分解较充分,CuO/CeO2两相的相互作用达到最佳,此时Ce3+最大限度地从CuO中获取氧,使得制备的CuCe-O/γ-Al2O3试样的H2-TPR还原温度降至最低,催化氧化CO活性达到最高。
230 ℃热解温度下,不同热解气氛制备的CuCe-O/γ-Al2O3试样CO氧化活性的结果见表4。
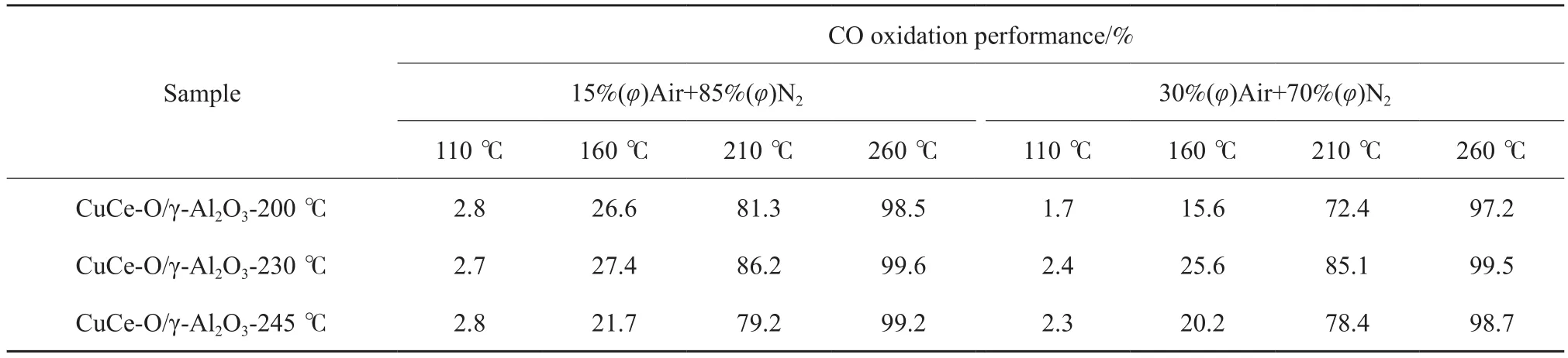
表3 15%(φ)空气+85%(φ)N2气氛和30%(φ)空气+70%(φ)N2气氛中不同热解温度下制备的CuCe-O/γ-Al2O3试样的CO氧化性能Table 3 CO oxidation performances of CuCe-O/γ-Al2O3 samples prepared in 15%(φ)air+85%(φ)N2 and 30%(φ)air+70%(φ)N2 at different temperatures
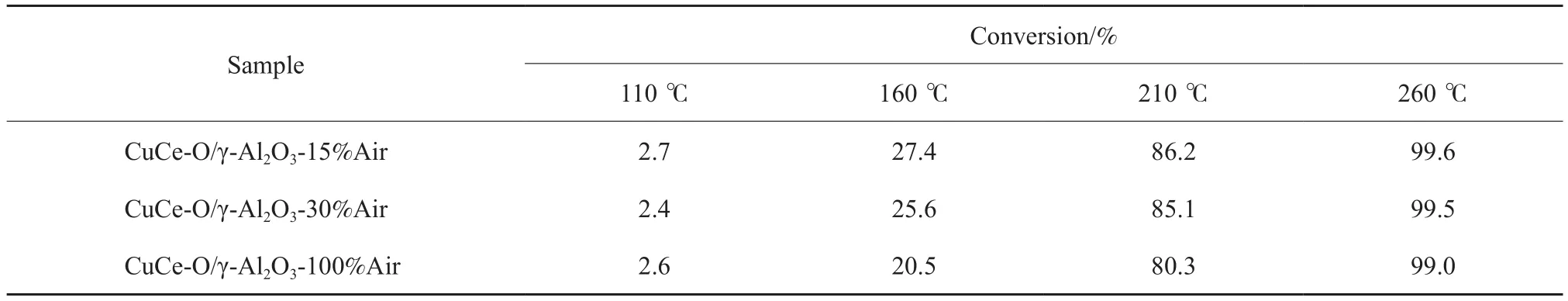
表4 230 ℃温度下不同热解气氛制备的CuCe-O/γ-Al2O3试样的CO氧化性能Table 4 CO oxidation performances of CuCe-O/γ-Al2O3 samples prepared in different atmospheres at 230 ℃
由表4可看出,230 ℃热解温度下,热解气氛为15%(φ)空气+85%(φ)N2弱氧气氛中制备的CuCe-O/γ-Al2O3试样催化氧化CO活性最高,热解气氛为100%(φ)空气富氧气氛中制备的CuCe-O/γ-Al2O3试样催化氧化CO活性最差,与H2-TPR表征结果相一致,更进一步验证了弱氧气氛中,230 ℃热解温度下,制备的CuCe-O/γ-Al2O3试样的H2-TPR还原温度最低,催化氧化CO活性达到最高。
3 结论
1) 制 备 的 CuCe-O/γ-Al2O3试 样 中 CuO 在γ-Al2O3载体表面上呈高度分散状态,改变热解温度、热解气氛基本不影响活性组分的物相结构及分散状态。
2)弱氧气氛热解使CuO/CeO2两相的相互作用达到最佳,加剧了Ce3+从CuO中获取氧的趋势,提高了氧化铜的氧化还原能力,相应的H2-TPR还原峰温度向低温区偏移。
3)230 ℃热解温度下,热解气氛为15%(φ)空气+85%(φ)N2弱氧气氛中制备的CuCe-O/γ-Al2O3试样具有优良的CO氧化性能。
