氯气与水反应实验的设计及相关教学探讨
2018-06-09李振雯秦浩正
李振雯 秦浩正


摘要: 巧妙利用三颈烧瓶、气球、一次性注射器、一次性塑料滴管和笔式酸度计等常用仪器,设计氯气与水反应的完全密闭、不会造成氯气泄漏的新实验装置。该装置装配简单,现象明显,用于教学中能够使学生根据酸度计的读数变化规律分析可逆反应历程,探寻达到化学平衡状态的特征,完成知识目标的同时,发展创新思维,培养实验能力。
关键词: 氯气与水反应; 化学平衡; 可逆反应; 实验改进
文章编号: 1005-6629(2018)4-0069-04 中图分类号: G633.8 文献标识码: B
“化学平衡”是化学中平衡理论体系的核心,是学习电离平衡、水解平衡等的必备基础知识,对深入理解其他平衡具有重要的理论指导意义。由于实际教学中很难找到合适的方法使学生直接感受化学平衡的建立过程,沪科版教材补充氢气与碘单质的可逆反应,直接呈现反应物和生成物浓度随时间变化的数据,用以说明可逆反应不能进行到底[1]。可逆反应存在化学平衡,多数教师在教学时仅限于宏观性质的讲解,学生对化学平衡的学习多为机械记忆,没有进行太多的思维活动,很难理解并掌握这一概念,因此该内容一直是化学教学的重点和难点[2~3]。笔者认为有必要通过实验帮助学生探讨反应达到平衡状态的过程与特征,通过宏观的实验现象解释微观反应历程,建立坐标图像模型,发展学生思维,帮助其理解与掌握知识[4]。
1 实验选择
在学习该内容之前,学生已经知道二氧化硫催化氧化、工业合成氨、二氧化碳与水、氯气与水的反应是可逆反应,了解影响化学反应速率的因素,故在此基础上可以深入探索可逆反应与化学平衡。在上述反应中,笔者选择有色气体氯气和水的反应作为本节知识学习的载体,巧妙利用气球和医用注射器,使反应装置密闭;用笔式酸度计测定溶液pH变化情况,酸度计读数变化表示溶液中H+(生成物)的含量变化,解决反应现象不明显的问题;实验结束后,用NaOH溶液吸收残余氯气,防止污染,体现绿色化学的思想。
2 实验改进
2.1 改进原理
氯气与水的混合体系中同时存在氯气的溶解平衡、氯气与水反应的化学平衡和次氯酸的解离平衡,溶于水的部分氯气与水发生反应生成HCl和HClO,此时氯气与水反应的化学平衡与次氯酸的解离平衡同时存在且相互影响[5]。
25℃时,Ka(HClO)=2.95×10-8,根据范特霍夫方程可求得0℃时,Ka(HClO)=2.39×10-8;当体系中溶液pH<6.0时,两温度下,该溶液体系中HClO的各型体分布分数δHClO=[H+]/([H+]+Ka)≈1, δClO-≈0,即在此狀态下可忽略HClO的解离过程,反应生成的HClO完全以HClO分子的形式存在,溶液中[Cl-]=[HClO],可认为溶液中氯离子和次氯酸分子的浓度等于反应生成的氢离子浓度。因此,笔者通过测量溶液pH便能够得到溶液中H+浓度,并推测出反应Cl2+H2OH++Cl-+HClO的正反应生成物(Cl-、 HClO)的浓度。
2.2 实验药品与装置
2.2.1 实验药品与仪器
氯气、蒸馏水、冰块、氢氧化钠溶液;250mL三颈烧瓶、1000mL烧杯、笔式酸度计、硅胶塞、一次性塑料滴管、50mL医用注射器若干、气球、秒表
2.2.2 实验装置
实验装置如图1所示。三颈烧瓶三口分别用作通入氯气(A)、插入笔式酸度计(B)、注入氢氧化钠溶液(C)。A处用针筒通入氯气,针头下端插入一个一次性塑料滴管作为内导管,可将氯气直接通入蒸馏水中,使反应物充分接触,同时起防倒吸的作用;B口用气球密封,通入氯气之后,利用气球的张力使体系内的总压强基本保持不变,为该实验创造了一个近似恒压的条件。实验结束后,C口用针筒注入NaOH溶液吸收残余氯气。将250mL三颈烧瓶放在1000mL大烧杯中,便于在实验过程中观察烧瓶内溶液与气体的颜色,同时在实验二中作为容器盛装冰水混合物。
图1 氯气与水的反应实验装置图
整个装置简易且完全密闭,不会造成氯气泄漏,在课堂中既适合作为演示实验,又适合学生分组实验。
2.3 实验过程与数据记录
实验一:
(1) 用针筒分别收集50mL氯气[6],30mL 1mol/L氢氧化钠溶液,并将针头扎入软木塞中密封备用;
(2) 按图1装置组装仪器,三颈烧瓶中盛100mL蒸馏水;
(3) 检查装置的气密性: 用一次性医用注射器通过三颈烧瓶的A口通入50mL空气,通入之后一直按压注射器不松手,发现B口处气球鼓起,若2~3分钟内气球不瘪下去,则该装置气密性良好;
(4) 记下B处笔式酸度计读数,将收集满Cl2的针筒插在三口烧瓶A处的针头上,迅速通入Cl2,能够发现B处气球鼓起,然后瘪下去。此过程中,一位实验者手持秒表从通入氯气时开始计时,观察并报出酸度计的读数(每秒报一次),另一位实验者记录数据,根据所得数据绘制溶液的pH-t趋势图。
实验二:
(1) 在大烧杯中盛装冰水混合物,使三颈烧瓶内的液面完全浸入冰水中,一位实验者手持秒表从体系接触冰水混合物之时开始计时,观察并报出酸度计的读数(每秒报一次),另一位实验者记录数据,根据所得数据在上述图像中继续绘制溶液的pH-t趋势图;
(2) 反应结束后,在C处扎入盛有氢氧化钠溶液的针筒,将NaOH溶液注入三颈烧瓶中,吸收残余氯气。
2.4 数据收集与处理
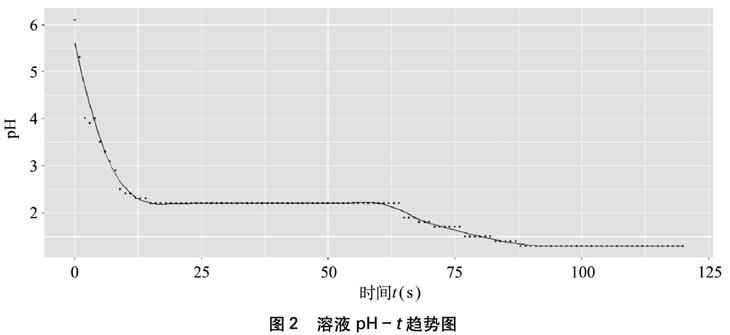
笔者进行了一组实验并记录数据如表1、表2所示。实验一从通入氯气时开始计时,在第60s开始实验二操作,每隔1s记录一次酸度计的读数,两实验酸度计读数分别记为pH-1、 pH-2,并运用R语言统计软件绘制pH-t趋势图如图2所示。
装置中A口处接一次性塑料滴管作为内导管,可将氯气直接通入水中,氯气与水充分接触,发生可逆的化学反应。在通入氯气之后,体系中该可逆反应正反应的反应物浓度大于逆反应的反应物浓度,正反应速率大于逆反应速率,即溶液中氢离子的生成速率大于消耗速率,因此溶液pH迅速下降。从t=0s时刻起,逆反应的反应物浓
表1 实验一过程中溶液pH记录(水起始温度T=21℃,室温T′=18℃)
表2 实验二过程中溶液pH记录(60s时三颈烧瓶浸入冰水中,冰水T=0℃,室温T′=18℃)
图2 溶液pH-t趋势图
度逐渐升高,正反应的反应物浓度逐渐降低,逆反应速率增大而正反应速率减小,正逆反应速率的差值逐渐减小,氢离子的生成量与消耗量的差值逐渐减小,因此,溶液中pH-t趋势图从t=0s时刻起先急速下降,后缓慢下降;t=15s时,正反应速率与逆反应速率相等,溶液pH不变,可视为该反应达到化学平衡状态。
t=60s时,将三颈烧瓶浸入冰水混合物中,由于氯气与水的正反应是放热反应,降低体系温度,平衡正向移动,此过程中,溶液pH又呈现先快速下降后缓慢下降的趋势;t=88s时,溶液pH再次保持不变,说明该反应在此状态下重新建立新的化学平衡。
当反应达到上述两个平衡状态时,三颈烧瓶中均能看到未反应的黄绿色气体——氯气,说明该反应是可逆反应,反应不能进行到底。
3 实验在教学中的应用
本实验可用于有关“化学平衡”的教学中,将难以直接观察的可逆反应通过酸度计的读数反映出来,根据酸度计的读数变化规律分析该可逆反应的反应历程,寻求反应达到化学平衡状态的四个特征——①动: 动态平衡;②等: v(正)=v(逆)≠0;③定: 各组分含量保持不变;④变: 改变影响平衡的因素,平衡发生移动,并在该条件下建立新的平衡。
4 实验优点
4.1 装置简单,实验易操作
该实验用到的三颈烧瓶、针筒、酸度计、气球、一次性塑料滴管等均为实验室常用仪器,可在课前搭建好,各准备两针筒氯气(一筒备用)、兩筒氢氧化钠溶液(一筒备用),课堂中只需将氯气注入三颈烧瓶中即可,不受条件限制,适合一般学校课堂。
4.2 现象明显,实验耗时短
通氯气的针头下接一次性塑料滴管,作为导管直接将氯气通入水中,使反应物充分接触,反应现象明显,通入氯气后即可观察到酸度计示数的变化,半分钟左右pH计读数不再变化,此过程溶液pH呈现明显的变化趋势,即先迅速下降,再缓慢下降最终保持不变,整个实验2~3分钟即可完成。
4.3 可做进一步改进
该实验用于探究可逆反应达到化学平衡状态的特征,是化学平衡第一课时的内容,笔者选取笔式酸度计而未使用DIS传感系统,是为了让学生体验完整的科学探究过程,培养学生的探究能力[7]。在接下来的有关平衡移动的教学中,可继续利用该装置,将酸度计换成传感探头(H+传感器,Cl-传感器,Cl2传感器,压强传感器等)可由计算机直接呈现出相关物理量随时间变化的图像。
5 小结
本研究设计的氯气与水反应的实验装置,装配简单,操作方便,现象明显,且实验过程中不会造成氯气泄漏,绿色安全。将其用于有关“化学平衡”的教学中,对教材中很难用实验表征的知
识内容加以补充,拓展了教材的思想与内涵,突出了实验的基础作用。学生在此过程中观察、搜集证据,基于证据建立坐标图像模型,由此分析可逆反应的反应历程,参与寻求特征与概念的形成,在完成知识目标的同时,培养搜集证据、分析处理数据的能力,促进自身“证据推理与模型认知”、“科学探究与创新意识”[8]等化学学科核心素养的发展。
参考文献:
[1]姚子鹏主编.高级中学课本·化学(高一年级第二学期)(试用本)(第1版)[M].上海.上海科学技术出版社,2007: 45~46
[2][3]任丽曼.高中生化学平衡学习困难的因素分析[D].上海: 上海师范大学硕士学位论文, 2010.
[4]唐红珍.高中化学定量实验能力培养的教学策略[J].化学教学, 2017,(6): 49~52.
[5]张映明.氯气与水的歧化反应是可逆反应[J].化学教学, 2015,(2): 91~94.
[6]李猛,王世存.氯气制备及性质实验一体化设计[J].化学教学, 2016,(8): 63~65.
[7]薛青峰.基于问题导引图示教学法的实践与反思[J].化学教学, 2017,(6): 57~59.
[8]杨海艳.高中化学教材非实验内容实验化的探索[J].化学教学, 2016,(2): 72~74.
