特异质型药物性肝损伤病因评估及生物标志物的研究进展
2017-09-16王春红邹正升
孙 颖,谢 欢,王春红,邹正升
特异质型药物性肝损伤病因评估及生物标志物的研究进展
孙 颖,谢 欢,王春红,邹正升
特异质型药物性肝损伤是少数特异性体质人群发生的药物性肝损伤。对于疑似特异质型药物性肝损伤的诊断,目前主要依靠排他性诊断, 临床中易被误诊或漏诊。近年来对于特异质型药物性肝损伤的病因评估及生物标志物的研究取得了一定的进展。 本文主要针对目前特异质型药物性肝损伤的病因评估方法及具有应用前景的诊断生物标志物的研究进展进行总结,为今后特异质型药物性肝损伤诊断提供思路。
特异质型药物性肝损伤;病因;生物标志物
药物性肝损伤(drug induced liver injury,DILI)是最常见和最严重的药物不良反应之一,部分患者甚至出现肝衰竭而危及生命。 按病程,DILI可分为急性DILI和慢性DILI。按发病机制,DILI可分为固有型DILI(intrinsic DILI, InDILI)和特异质型DILI(idiosyncratic DILI, iDILI)(图1)。InDILI是由药物本身或其代谢产物直接引起的肝损伤,其肝损伤呈剂量依赖性,即应用剂量越大,肝损伤也越重。iDILI是少数特异性体质的人群发生的DILI,临床上的DILI通常是指iDILI。由于难以预测机体对药物的特异质反应,因此对于疑似iDILI患者的诊断主要依靠排他性诊断。Roussel Uclaf因果关系评估法(Roussel Uclaf causality assessment method, RUCAM)量表是目前
1 iDILI的病因评估方法
1.1 RUCAM评分 iDILI的临床表现缺乏特异性,其病因极易与其他肝脏疾病病因混淆,导致iDILI的诊断十分困难。20世纪90年代前,对于DILI,尤其是iDILI,没有很好的诊断工具。1993年修改完善的 DILI评估方案RUCAM(也称为Danan方案)对于建立DILI诊断至关重要[1],可用来判断肝损伤是否由药物所引起。RUCAM是常用的急性DILI的诊断评估方案,但对于难以进行诊断的病例,则需要专业的肝脏病理学家对肝活检组织进行鉴别以排除其他肝脏疾病,这严重影响了iDILI的诊断水平,使iDILI易被误诊或漏诊。因此寻求敏感性和特异性较高的iDILI的生物标志物,对于提高iDILI的预测和诊断的准确性具有重要的临床意义。 本文主要针对目前iDILI的病因评估方法及具有应用前景的生物标志物的研究进展进行综述。目前国际上对DILI因果关系评估最为常用的方法,被认为是设计合理、要素全面、诊断准确率较高的DILI诊断工具。RUCAM评分考虑到用药史、临床特征、危险因素、伴随用药、排除非药物性肝损伤、药物肝毒性信息、药物再激发反应 7方面内容,共计14分,根据评分结果将药物与肝损伤的因果相关性进行分级,并进一步确定DILI的可能性。评分≤0分可排除DILI,1~2分为不太可能,3~5分为可能,6~8分为很可能,>9分为极可能[1]。但是RUCAM中的部分评分标准界定含糊,评分项目复杂,临床操控性差,更不适用于可疑慢性DILI 的病因评估,在除外其他肝损伤病因的评分中甚至需要专业的肝脏病理学专家协助完成。且当患者在发生DILI前曾服用多种药物时,更是无法通过RUCAM鉴定出由哪种药物导致的肝损伤(表1)。
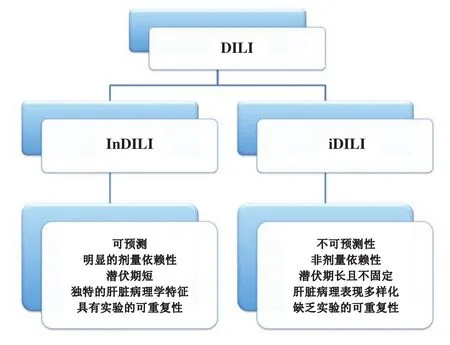
图1 InDILI及iDILI的临床特点Figure 1 Clinical characteristics of InDILI and iDILI
1.2 细胞模型在iDILI病因评估中的应用

表1 RUCAM的评分组成及其临床意义Table 1 The composition and clinical significance of RUCAM
1.2.1 肝细胞样细胞模型 部分iDILI患者在发病前并非仅服用一种药物,确定何种药物为致病药物,评价可疑药物与肝损伤的相关性,一直是令临床医师及患者困惑的问题。不同年龄、性别、生理病理状况、种族及遗传因素等的个体差异均可影响药物在体内的代谢过程,同时也是影响药物不良反应发生的重要因素。如能建立一种基于个体化的DILI检测系统,可针对易感人群或iDILI患者筛选出致病药物,将会对指导用药的安全性具有重要的临床意义。iDILI损伤的靶器官为肝脏,通过肝细胞研究疾病的致病因素是最为直接的方法,然而来自iDILI患者的原代肝细胞不易获得,且体外培养细胞生物学特性不够稳定,因此限制了对iDILI的致病因素的研究。不过,目前发现可以通过单核细胞来源的肝细胞样(monocyte derived hepatocyte-like, MH)细胞模型从一组药物中鉴定出致病药物,该方法有望成为体外研究iDILI致病药物的工具。MH 细胞具有供体特异性肝细胞的特征,能够呈现较好的ALT、CYP3A4的活性及凝血因子分泌的功能,该细胞内的细胞色素P450能够介导对乙酰氨基酚对肝细胞的毒性损伤;体外培养4周,MH细胞仍具有良好的稳定性;MH细胞除了保留细胞供体细胞色素P450活性和细胞毒性的特异性,还保留了性别特异性,可作为长期研究肝细胞毒性、药物代谢和药物相互作用的体外模型。Benesic等[2]通过体外分离培养iDILI患者MH细胞并进行不同药物对肝细胞毒性的研究,细胞毒性的强弱通过乳酸脱氢酶的释放水平来评估。研究结果表明采用MH细胞鉴定iDILI患者较 RUCAM评分具有更高的敏感性和特异性,当iDILI患者的MH细胞暴露于致病药物时更易受损[3-4]。图 2例举了MH细胞的毒性鉴定方法。图中选用的病例为1例急性iDILI患者,该患者发病前曾服用3种药物,分别为舒尼替尼、苯丙香豆素和二甲双胍,药物对MH细胞毒性(以乳酸脱氢酶的释放水平评估)采用蜘蛛网图进行分析。分析结果显示舒尼替尼组MH细胞呈现出明显的肝毒性,而苯丙香豆素和二甲双胍组均未出现MH细胞受损[5]。
MH细胞在iDILI的诊断和鉴别诊断中具有更好的敏感性和特异性,可以鉴别出患者对何种药物产生不良反应,在评估暴露药物与iDILI因果关系中具有重要的作用,这是RUCAM评分所不能实现的。MH细胞是iDILI病因诊断研究的新方向,有助于寻找更多关于iDILI 预测、风险评估和预后转归等方面的生物标志物。
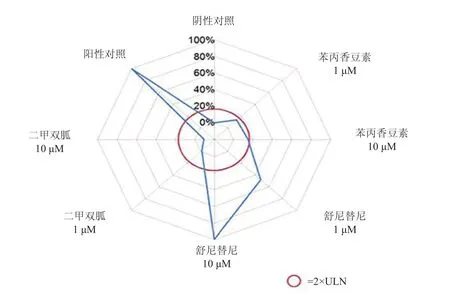
图2 药物对MH细胞的毒性鉴定方法Figure 2 Identification method of MH cell toxicity by drug
1.2.2 THP-1细胞系 在药物引起的超敏反应中,免疫系统可能是药物作用的重要靶点。提高临床前期的预测能力对于预防药物不良反应的发生十分重要。Galbiati等[6]利用THP-1 细胞系(人急性单核细胞白血病细胞系),IL-8分泌能力以及CD86、CD54的表达水平对高敏人群临床前期的免疫状态进行安全性评估。将THP-1细胞经过药物处理24 h后进行IL-8分泌水平及CD86分子表达水平的检测(图3)。如果IL-8分泌和/或CD86的表达达到检测标准, 则说明该药物为致敏药物,如果未出现上述结果,可通过以下3种方式之一判断结果:①继续培养3 h,检测IL-8 mRNA水平,结果达到检测标准,说明该药物为致敏药物,否则为非致敏药物;②继续培养48 h,如果IL-8分泌和/或CD86的表达达到检测标准, 则说明该药物为致敏药物,否则为非致敏药物;③继续培养24 h,了解CD54分子的表达情况,如达到检测水平,则证实为致敏药物,否则为非致敏药物。该方法有助于体外早期发现可能引起超敏反应的药物,从而避免易感人群出现药物不良反应。
2 iDILI生物标志物
2.1 常用的生物标志物 ALT、AST、ALP及TBIL是DILI检测的传统方法。虽然这些标志物对于iDILI的检测不特异,但却可以在疾病的早期发生变化,是目前DILI临床分型的重要依据。DILI 按照R值水平[R值=(ALT实测值÷ALT正常上限) /(ALP 实测值÷ALP正常上限)]可以分为3型:肝细胞损伤型、胆汁淤积型和混合型[7-8]。肝细胞损伤型:ALT≥3×ULN,且R≥5;胆汁淤积型:ALP≥2×ULN,且 R≤2;混合型:ALT≥3×ULN,ALP≥2×ULN,且 2<R<5。在服药的过程中如果仅出现肝功能轻微异常时,这种肝损伤通常是可逆的,或是存在其他原因(如脂肪肝),不应考虑是iDILI 所致。国际DILI专家组认为DILI诊断的肝功能界值应符合以下指 标: ① ALT ≥ 5×ULN; ② ALP ≥ 2×ULN ;③ALT≥3×ULN 且TBIL≥2×ULN[9]。最后一条即为Hy’s法则[10]。美国FDA对Hy’s法则作出进一步解释,认为DILI患者肝损伤不应该具有显著的胆汁淤积的特征,应是一种肝细胞的损伤。符合该法则的DILI患者约10%有死亡或肝移植的风险,这一观点已经被大规模的队列研究所证实[11-12]。但也有数据显示在ALP>2ULN的DILI患者中,如符合Hy’s定律同样不能降低发生急性肝衰竭的风险[13]。如果iDILI确诊后30~60 d内TBILI及ALP仍持续升高,预示患者病情可能将发生慢性化。除了ALT、ALP及TBIL,AST对于评价iDILI 的预后亦十分重要。当iDILI患者出现AST显著升高,伴有AST/ALT比值超过1.5时,也提示该患者具有不良的预后[12-13]。
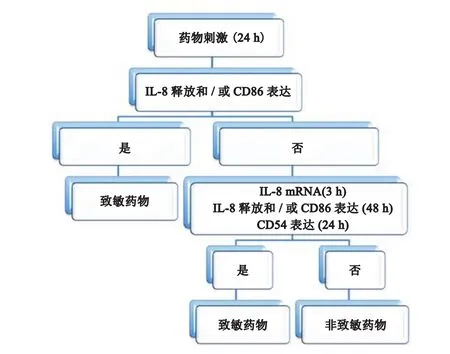
图 3 药物致THP-1细胞活化的分析流程Figure 3 Flow diagram of analysis for drug-induced activation of THP-1 cells
2.2 具有潜力的iDILI生物标志物 尽管传统的肝功能检测在iDILI的诊断中发挥重要的作用,但由于缺乏足够的特异性和敏感性,使其在临床应用中受到一定的限制。随着对检测手段研究的不断深入,目前发现比较有潜力的能够反应早期肝损伤的生物标志物还包括谷氨酸脱氢酶(glutamate dehydrogenase, GLDH),高迁移率族蛋白1(high mobility group box-1 protein, HMGB1),角蛋白18(keratin18, K18),苹果酸脱氢酶(malate dehydrogenase, MDH)等,它们主要是反应肝细胞坏死的生物标志物。
2.2.1 GLDH GLDH是一种线粒体酶,主要存在于肝脏,该酶较ALT及AST更具有组织特异性。健康人体内GLDH处于较为稳定的水平,不受性别及年龄影响。当循环血液中的GLDH升高时提示肝细胞坏死,伴有线粒体膜的完整性受到破坏和线粒体功能受损。各种原因所致的肝损伤,包括过量服用对乙酰氨基酚,GLDH与ALT均可显著升高,二者具有较好的相关性,但GLDH在预测肝毒性方面不如ALT敏感。
2.2.2 HMGB1 HMGB1的主要生物学功能是与DNA结合。核内HMGB1与特定结构的染色质DNA 结合,通过影响靶序列的结构,参与DNA的重组、修复、基因转录调控、细胞复制及分化成熟等生命活动。 HMGB1可以通过高乙酰化的免疫细胞主动分泌或通过炎性反应中的坏死细胞被动释放至胞外介导炎症反应。HMGB1的促炎活性,主要通过Toll样受体和晚期糖基化终产物受体介导信号转导,它可作为一种晚期炎症介质参与炎症性疾病的发病过程,也可作为一种免疫“预警信号”调控机体的免疫反应。 因此体内HMGB1水平可以反映细胞的坏死程度以及经乙酰化修饰的活化免疫细胞的状态[14-16],在预测肝损伤时较ALT更为敏感[17]。
2.2.3 K18 角蛋白是角质细胞中的主要骨架蛋白,主要功能是维持上皮组织的完整性及连续性。K18是角蛋白家族中的一员。与HMGB1相似,全长K18也是由坏死细胞被动释放的。但在细胞凋亡过程中因细胞结构重排,K18在半胱天冬酶的介导下裂解为角蛋白的片段蛋白(caspasecleaved cytokeratin-18, ccCK-18),并不断释放入血液。因此血清中全长K18和 ccCK-18的水平可以作为细胞凋亡和坏死的生物标志物。目前无论是HMGB1还是K18均被认为是血液中较ALT更为灵敏的肝损伤的生物标志物,通常在ALT水平升高前即可显著升高[18]。
2.2.4 MDH MDH是参与三羧酸循环的一种酶,主要催化L-苹果酸脱氢变成草酰乙酸。MDH广泛存在于线粒体中,其血清活性主要与肝脏和心脏损伤有关,在评估肝损伤的严重程度时比AST升高更有意义。但因MDH的组织特异性较差,其血清水平易受肝外组织受损的影响[19]。
2.2.5 MicroRNA MicroRNA(miRNA)是一类长约20~24个核苷酸的非编码小RNA,在调节基因表达的过程中发挥重要作用。miRNA在体液中相对稳定,当器官受损时被释放入血液,因此外周循环中的miRNA有望成为iDILI的生物标志物。在对乙酰氨基酚诱导的急性肝损伤小鼠模型中, miRNA-122和miRNA-192在小鼠血清中显著升高;而在对乙酰氨基酚所致急性肝损伤患者的血清中miRNA-122和miRNA-192亦显著升高,而miRNA-122与ALT的峰值水平呈正相关,但与凝血酶原时间无相关性。miRNA-122在非对乙酰氨基酚所致急性DILI患者中同样随着ALT水平的升高而呈上升趋势。与ALT相比,miRNA-122更具肝脏特异性,较ALT更为敏感[20]。但是目前研究尚未能确定 miRNA-122在iDILI诊断中的界值,有待深入探讨。
2.2.6 外泌体 外泌体是指包含了复杂 RNA 和蛋白质的小膜泡,主要为来源于细胞内溶酶体微粒内陷形成的多囊泡体,经多囊泡体外膜与细胞膜融合后释放到胞外基质中。近年来外泌体作为一种潜在的DILI生物标志物备受关注。在肝细胞坏死或凋亡后,外泌体能够被动的进入到血液、尿液等多种体液中,通过研究iDILI过程中外泌体内的肝脏特异性mRNAs(如白蛋白、纤维蛋白原、结合珠蛋白等)以及肝脏富集的miRNA 对于早期诊断iDILI,最大程度地减少药物对人体的不良反应具有重要的临床意义,但这些标志物在iDILI中的应用仍须广泛深入地研究及验证。
3 通过GWAS确定的与iDILI相关的HLA易感基因
3.1 药物与HLA的相互作用 人类白细胞抗原(human leukocyte antigen, HLA)在DILI发病中发挥着重要的作用[21],药物可能通过多种方式与HLA发生相互作用。在肝细胞中药物作为半抗原与细胞表面或循环中的蛋白质共价结合形成药物蛋白复合体。当肝细胞死亡后该复合体便从肝细胞中释放出来,并被抗原递呈细胞——巨噬细胞所吞噬,经过加工处理后通过HLA-II分子表达于巨噬细胞表面,被CD4+T细胞的TCR 受体识别,从而活化CD4+T细胞;药物蛋白质复合体也可以通过肝细胞的MHC-I类分子表达于肝细胞表面,进而使肝细胞受到体内CD8+T细胞的免疫攻击。部分药物也可通过改变HLA分子的肽结合槽结构,使其更易结合至HLA分子上,或与HLA分子或T细胞受体结合,进而活化药物特异性T细胞,导致免疫介导的肝损伤[22]。
3.2 与iDILI相关的HLA易感基因 随着人类基因组研究的快速发展,越来越多的证据显示iDILI患者的个体遗传可能决定了机体对药物产生有效、有害、还是致命的反应。全基因组关联分析(genome-wide association studies, GWAS)为 iDILI病因评估的一个新方向,通过在人类全基因组范围内找出存在的序列变异,从中筛选出与iDILI相关的单核苷酸多态性。现有研究显示利用GWAS已发现大量的HLA-I和HLA-II的等位基因与DILI的关联性。希美加群是一种直接凝血酶抑制剂,由于其严重的肝毒性,目前已被撤市。临床试验显示,接受本品治疗的患者有出现严重肝损害的不良反应的风险。研究还发现该药导致的肝毒性与HLA-DRB1*0701密切相关,服用药物后ALT 异常的患者体内HLA-DRB1*0701 频率明显高于对照组。希美加群在北欧人群中引起ALT 升高的发生率明显高于亚洲人群,这可能与HLADRB1*0701 等位基因在北欧人群中的携带率明显高于亚洲人群有关[23],而希美加群代谢产物与HLA-DRB1*0701 相关肽类分子结合后,可引起T 细胞介导的免疫反应,进而导致DILI 的发生。非甾体抗炎药罗美昔布是选择性COX-2 抑制剂,临床上被用于治疗关节炎和急性疼痛,同样因其严重的肝毒性而被撤市。研究显示罗美昔布引起的DILI与 HLA-DRB1密切相关[24]。而抗生素中的氟氯西林、阿莫西林-克拉维酸、米诺环素所致的DILI分别与HLA-B*5701,HLA-DQB1*0602及HLA-B*35∶02密切相关。另有研究发现部分乳腺癌患者在接受拉帕替尼(酪氨酸激酶抑制剂)治疗后会发生iDILI。HLA-DQA1*0201及HLADQB1*0701可能是拉帕替尼引起iDILI的易感基因位点。上述HLA分子的存在可导致特定药物的肝损伤,而携带HLA-A*33∶01基因的人群则具有发生胆汁淤积型或混合型DILI的风险[25]。
4 结论与展望
iDILI是一种较为复杂的疾病,其临床症状、病理特征均缺乏特异性,目前诊断仍然依靠排他性诊断。寻求单一的实验室诊断方法,简化疑似iDILI的诊断过程,始终是临床医生和科研工作者追求的目标,但是迄今为止仍无可靠的生物标志物用于常规iDILI的诊断[26]。RUCAM评分是目前应用较为广泛、认可度比较高的用于诊断疑似iDILI的工具,但对于慢性iDILI却不适用。未来的研究应着眼于寻求替代或辅助RUCAM评分的生物标志物,而这种生物标志物应具有药物特异性、反应敏感性及使用方便性的特点。 面对大量具有潜在肝毒性的药物和差异万千的iDILI易感者,开发一种或一组能够适用于所有iDILI患者早期诊断的生物标志物,不仅有助于降低 iDILI易感人群发病的风险,同时对于提高临床用药的安全性,实现治疗的个体化的指导具有重要的临床应用价值,但也对临床医师和研究人员均提出了巨大的挑战。
[1] Danan G, Benichou C. Causality assessment of adverse reactions to drugs--I. a novel method based on the conclusions of international consensus meetings: application to drug-induced liver injuries[J].J Clin Epidemiol, 1993, 46(11):1323-1330.
[2] Benesic A, Rahm NL, Ernst S, et al. Human monocyte-derived cells with individual hepatocyte characteristics: a novel tool for personalized in vitro studies[J]. Lab Invest, 2012, 92(6):926-936.
[3] Benesic A, Gerbes AL. Drug-induced liver injury and individual cell models[J]. Dig Dis, 2015, 33(4):486-491.
[4] Benesic A, Leitl A, Gerbes AL. Monocyte-derived hepatocyte-like cells for causality assessment of idiosyncratic drug-induced liver injury[J]. Gut, 2016, 65(9):1555-1563.
[5] Kullak-Ublick GA, Andrade RJ, Merz M, et al. Drug-induced liver injury: recent advances in diagnosis and risk assessment[J].Gut, 2017, 66(6):1154-1164.
[6] Galbiati V, Papale A, Kummer E, et al. In vitro models to evaluate drug-induced hypersensitivity: potential test based on activation of dendritic cells[J]. Front Pharmacol, 2016, 7:204.
[7] Chalasani NP, Hayashi PH, Bonkovsky HL, et al. Practice Parameters Committee of the American College of Gastroenterology:ACG clinical guideline: the diagnosis and management of idiosyncratic drug-induced liver injury[J]. Am J Gastroenterol,2014,109(7):950-966.
[8] Hayashi PH, Fontana RJ. Clinical features, diagnosis, and natural history of drug-induced liver injury[J]. Semin Liver Dis, 2014,34 (2):134-144.
[9] Aithal GP, Watkins PB, Andrade RJ, et al. Case definition and phenotype standardization in drug-induced liver injury[J]. Clin Pharmacol Ther, 2011, 89(6):806-815.
[10] Zimmerman HJ. The spectrum of hepatotoxicity[J]. Perspect Biol Med, 1968, 12(1):135-161.
[11] Navarro VJ, Barnhart H, Bonkovsky HL, et al. Liver injury from herbals and dietary supplements in the U.S. drug-induced liver injury network[J]. Hepatology, 2014, 60(4):1399-1408.
[12] Bjornsson E, Olsson R. Outcome and prognostic markers in severe drug-induced liver disease[J]. Hepatology, 2005, 42(2):481-489.
[13] Robles-Diaz M, Lucena MI, Kaplowitz N, et al. Use of Hy's law and a new composite algorithm to predict acute liver failure in patients with drug-induced liver injury[J]. Gastroenterology,2014, 147(1):109-118.
[14] Kubes P, Mehal WZ. Sterile inflammation in the liver[J].Gastroenterology, 2012, 143(5):1158-1172.
[15] Scaffidi P, Misteli T, Bianchi ME. Release of chromatin protein HMGB1 by necrotic cells triggers inflammation[J]. Nature,2002, 418(6894):191-195.
[16] Bonaldi T, Talamo F, Scaffidi P, et al. Monocytic cells hyperacetylate chromatin protein HMGB1 to redirect it towards secretion[J].EMBO J, 2003, 22(20):5551-5560.
[17] Antoine DJ, Dear JW, Lewis PS, et al. Mechanistic biomarkers provide early and sensitive detection of acetaminophen-induced acute liver injury at first presentation to hospital[J]. Hepatology,2013, 58(2):777-787.
[18] Antoine DJ, Williams DP, Kipar A, et al. High-mobility group box-1 protein and keratin-18, circulating serum proteins informative of acetaminophen-induced necrosis and apoptosis in vivo[J].Toxicol Sci, 2009, 112(2):521-531.
[19] Schomaker S, Warner R, Bock J, et al. Assessment of emerging biomarkers of liver injury in human subjects[J]. Toxicol Sci,2013, 132(2):276-283.
[20] Reis H, Wohlschlager J, Hagemann S, et al. (Cleaved) CK18 serum and tissue expression levels differentiate acute HCV reinfection from acute rejection in liver allografts[J]. Liver Int, 2015,35(3):905-913.
[21] Grove JI, Aithal GP. Human leukocyte antigen genetic risk factors of drug-induced liver toxicology[J]. Expert Opin Drug Metab Toxicol, 2015, 11(3):395-409.
[22] Kindmark A, Jawaid A, Harbron CG, et al. Genome-wide pharmacogenetic investigation of a hepatic adverse event without clinical signs of immunopathology suggests an underlying immune pathogenesis[J]. Pharmacogenomics J, 2008, 8(3):186-195.
[23] Gibert M, Sanchez-Mazas A. Geographic patterns of functional categories of HLA-DRB1 alleles: a new approach to analyse associations between HLA-DRB1 and disease[J]. Eur J Immunogenet, 2003, 30(5):361-374.
[24] Singer JB, Lewitzky S, Leroy E, et al. A genome-wide study identifies HLA alleles associated with lumiracoxib-related liver injury[J]. Nat Genet, 2010, 42(8):711-714.
[25] Nicoletti P, Aithal GP, Bjornsson ES, et al. Association of liver injury from specific drugs, or groups of drugs, with polymorphisms in hla and other genes in a Genome-Wide Association study[J].Gastroenterology, 2017, 152(5):1078-1089.
[26] 李保森,孙颖. 药物性肝损伤的研究现状及存在问题[J]. 传染病信息,2013,26(5):263-265.
(2017-07-29收稿 2017-08-08修回)
(本文编辑 闫晶晶)
Advance of causality assessment and biomarker of idiosyncratic drug-induced liver injury
SUN Ying, XIE Huan, WANG Chun-hong, ZOU Zheng-sheng*
Diagnostic and Treatment Center for Non-Infectious Liver Diseases, 302 Military Hospital of China, Beijing 100039, China SUN Ying, XIE Huan and WANG Chun-hong are the first authors who contributed equally to the article
The onset of idiosyncratic drug-induced liver injury (iDILI) is rare. The diagnosis for iDILI mainly depends on exclusive diagnosis of the suspected iDILI cases. It’s easy to be misdiagnosed or missed in clinical practice. Recent researches focusing on the causality assessment and the diagnostic biomarkers in iDILI have got some progressions. In this article, we summarize recent advances in the causality assessment and the potential diagnostic biomarkers of iDILI, which will provide evidence for the diagnosis of iDILI in the future.
iDILI; causality; biomarker
R595.3
A
1007-8134(2017)04-0203-06
10.3969/j.issn.1007-8134.2017.04.005
国家自然科学基金资助项目(81641065)
100039 北京,解放军第三〇二医院非感染性肝病诊疗与研究中心(孙颖、谢欢、邹正升);053000,衡水市第三人民医院肝三科(王春红)
前三位作者对本文有同等贡献,均为第一作者
邹正升,E-mail: zszou302@163.com
*Corresponding author, E-mail: zszou302@163.com
