原发性肝癌诊疗规范(2017年版)更新解读
2017-09-16王春平陆荫英黄加干李因茵高旭东杨永平
王春平,任 波,陆荫英,黄加干,李因茵,曾 珍,杨 斌,高旭东,杨永平
原发性肝癌诊疗规范(2017年版)更新解读
王春平,任 波,陆荫英,黄加干,李因茵,曾 珍,杨 斌,高旭东,杨永平
2017年6月中华人民共和国国家卫生和计划生育委员会发布了基于循证医学证据的《原发性肝癌诊疗规范(2017年版)》。新版规范对肝细胞癌(hepatocellular carcinoma, HCC)的诊断、分期和治疗均进行了更新。本文现就更新内容进行描述和阐释。
癌,肝细胞;诊断;治疗;规范
原发性肝癌是目前我国第4位常见恶性肿瘤及第3位肿瘤致死病因,严重威胁我国人民的生命和健康[1-2]。《原发性肝癌诊疗规范(2011年版)》已发布6年,随着国际上肝癌的临床和基础研究不断深入和发展,中国在影像学、外科手术、放化疗技术以及索拉非尼等靶向治疗方面都取得了新进展,为此中华人民共和国国家卫生和计划生育委员会再次组织专家对2011年版诊疗规范进行修订,于2017年6月26日发布了《原发性肝癌诊疗规范(2017年版)》[3]。该规范首次采用牛津循证医学中心2011版证据等级划分标准,引入临床循证医学证据级别,对肝细胞癌(hepatocellular carcinoma,HCC)的诊断、分期和治疗均进行了更新,现就新版规范的更新部分进行解读。
1 凸显了影像学技术进展在肝癌诊断及肿瘤全面评估中的价值
新版规范中,肝癌诊断所依据的影像学检查由原来的2项(动态增强CT、动态增强MRI)增加到4项,即动态增强CT、动态增强MRI、超声造影(contrast enhanced ultrasound, CEUS)和肝细胞特异性对比剂普美显动态增强MRI。新版规范明确肯定了新增加的CEUS和普美显动态增强MRI在肝癌诊断中的价值。
常规超声筛查可以早期敏感地检出肝内可疑占位性病变,准确鉴别是囊性或实质性占位,并可观察肝内或腹部有无其他相关转移灶。彩色多普勒血流成像不仅可以观察病灶内血供,也可明确病灶与肝内重要血管的毗邻关系,为临床治疗方法的选择及手术方案的制定提供重要信息。实时CEUS技术可以揭示肝肿瘤的血流动力学改变,帮助鉴别和诊断不同性质的肝肿瘤,凭借实时显像和多切面显像的灵活特性,在评价肝肿瘤的微血管灌注和引导介入治疗方面具有优势。
普美显为肝细胞特异性对比剂,可被肝细胞摄取并随胆汁经胆管排泄。静脉注射后随血流进入肝脏后可被肝细胞特异性吸收,吸收率可达50%,从而使得肝细胞在注射普美显约20 min后(肝胆期)产生增强效果,没有或者仅有很少功能性肝细胞的病灶,比如囊肿、血管瘤、转移瘤和HCC,由于无法累积普美显,因此没有增强效果。这样无强化的病灶与强化的正常肝细胞间产生明显对比,更加容易发现病灶,尤其可提高≤1.0 cm肝癌的检出率和对肝癌诊断及鉴别诊断的准确性[4-6],同时为有肝细胞功能的良性病变如结节再生性增生、局灶性结节性增生与高分化肝癌的鉴别提供了良好的诊断方法。
近年来核医学影像技术迅速发展,新版规范也更加具体肯定了正电子发射计算机断层成像(positron emission tomography/CT, PET/CT)在肿瘤全面评估以及放射治疗靶区设计中的贡献。新版规范明确指出氟-18-脱氧葡萄糖(18F-FDG)PET/CT全身显像的优势:①对肿瘤进行分期,通过1次检查能够全面评价淋巴结转移及远处器官的转移(证据等级1);②再分期,因PET功能影像不受解剖结构的影响,可准确显示解剖结构发生变化后或者是解剖结构复杂部位的复发转移灶(证据等级2);③疗效评价,对于抑制肿瘤活性的靶向药物,疗效评价更加敏感、准确(证据等级2);④指导放疗生物靶区的勾画、穿刺活检部位(证据等级2);⑤评价肿瘤的恶性程度和预后(证据等级2)。碳-11标记的乙酸盐(11C-acetate)或胆碱(11C-choline)PET显像,可提高对高分化肝癌诊断的灵敏度,与18F-FDG PET/CT显像具有互补作用。
2 肝癌的临床诊断标准及路线图更加简洁、清晰,操控性强
新版规范中,血清AFP和肝脏超声检查仍是早期筛查的主要手段,建议高危人群每隔6个月进行至少1次检查。且AFP仍然作为肝癌临床诊断路线中的参考指标。然而新版规范关于AFP在肝癌的临床诊断标准中的作用与《原发性肝癌诊疗规范(2011年版)》有1处明显不同,即在高危人群中,若发现肝内直径≤2 cm结节,动态增强MRI、动态增强CT、CEUS及普美显动态增强MRI 4项检查中至少有2项显示肝癌典型特征,则可做出肝癌的临床诊断,摒弃了《原发性肝癌诊疗规范(2011年版)》中同时要求AFP≥400 ng/L超过1个月,或≥200 ng/L持续2个月,排除妊娠、生殖胚胎癌和活动性肝病的条件。从而使肝癌临床诊断更加简洁,易于操作。
肝癌的临床诊断标准如下。
第一,有乙型肝炎或丙型肝炎,或者有任何原因引起肝硬化者,至少每隔6个月进行1次超声及AFP检测,发现肝内直径≤2 cm结节,动态增强MRI、动态增强CT、CEUS及普美显动态增强MRI 4项检查中至少有2项显示有动脉期病灶明显强化、门脉或延迟期强化下降的“快进快出”的肝癌典型特征,则可做出肝癌的临床诊断;对于发现肝内直径>2 cm的结节,则上述4种影像学检查中只要有1项有典型的肝癌特征,即可临床诊断为肝癌。
第二,有乙型肝炎或丙型肝炎,或者有任何原因引起肝硬化者,随访发现肝内直径≤2 cm结节,若上述4种影像学检查中无或只有1项检查有典型的肝癌特征,可进行肝穿刺活检或以每2~3个月密切的影像学随访确立诊断;对于发现肝内直径>2 cm的结节,上述4种影像学检查无典型的肝癌特征,则须进行肝穿刺活检以确立诊断。
第三,有乙型肝炎或丙型肝炎,或者有任何原因引起肝硬化者,如AFP升高,特别是持续增高,应该进行上述4种影像学检查以确立肝癌的诊断,如未发现肝内结节,在排除妊娠、活动性肝病、生殖胚胎源性肿瘤以及消化道癌的前提下,应该密切随访AFP水平以及每隔2~3个月1次的影像学复查。肝癌诊断路线图见图1。
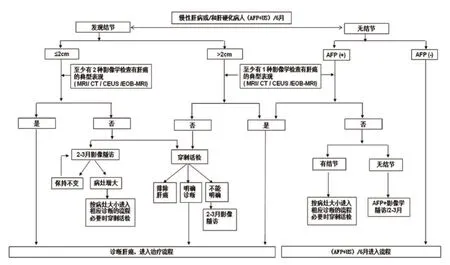
图1 肝癌诊断路线图[3]Figure 1 Diagnostic algorithm for hepatocellular carcinoma[3]
3 正式提出肝癌病理诊断规范
新版规范中未再提出肝癌病理诊断金标准一词,病理诊断须与临床证据和患者检查情况相结合。与《原发性肝癌诊疗规范(2011年版)》比较,新版规范正式、详尽地提出肝癌病理诊断规范,由标本处理、标本取材、病理检查和病理报告等部分组成。
3.1 标本处理要点 ①手术医生应在病理申请单上标注送检标本的部位、种类和数量,对手术切缘和重要病变可用染料染色或缝线加以标记;②尽可能将肿瘤标本在离体30 min以内完整送达病理科切开固定;③10%中性福尔马林溶液固定12~ 24 h。
3.2 标本取材要点 采用“7点”基线取材法(图2),在肿瘤的12 点、3点、6点和9点位置上于癌与癌旁肝组织交界处取材按1∶1取材;在肿瘤内部至少取材 1 块;对距肿瘤边缘≤1 cm(近癌旁)和>1 cm(远癌旁)范围内的肝组织分别取材1块。“7点”基线取材法的目的是为提高微血管侵犯(microvascular invasion, MVI)和卫星结节分布数量、范围等肝癌生物学特征的准确性。
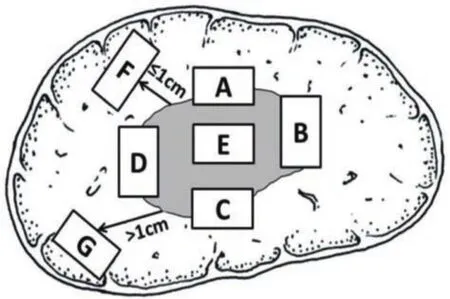
图2 肝肿瘤标本基线取材部位示意图[3]Figure 2 Pathologic specimen cutting sites for liver tumors[3]
3.3 病理检查中重视MVI的检出 MVI是指在显微镜下于内皮细胞衬覆的脉管腔内见到癌细胞巢团,以门静脉分支为主(含包膜内血管)(证据等级1);病理分级方法:M0,未发现 MVI;M1(低危组),≤5 个 MVI,且发生于近癌旁肝组织;M2(高危组),> 5 个MVI,或MVI发生于远癌旁肝组织。MVI是评估肝癌复发风险和选择治疗方案的重要参考依据,应作为常规病理检查指标(证据等级2)。
3.4 规范病理报告重点描述内容 由大体标本描述、显微镜下描述、免疫组化检查结果、典型病理照片及病理诊断名称等部分组成。此外,还可附有与肝癌克隆起源、药物靶点检测、生物学行为评估以及预后判断等相关的分子病理学检查结果,提供临床参考。
4 依据中国的具体国情及实践积累,提出了中国的肝癌分期及相应的治疗方案
肝癌分期对预后的评估、合理治疗方案的选择至关重要。国际上已有多个不同的肝癌分期标准,如:巴塞罗那临床肝癌分期、TNM分期、日本肝病学会分期、亚太肝病学会分期等,各类分期在临床实践上侧重不同,难以统一。巴塞罗那临床肝癌分期因将肿瘤因素、患者一般情况、肝功能情况、门脉高压情况与治疗原则联系起来,并且具有循证医学高级别证据的支持,在国际范围内被广泛采用。但是,国内不少外科医师认为巴塞罗那临床肝癌分期与治疗策略对于手术指征控制过严,提出应当根据中国肝癌的异质性、肝癌患者的临床特征和中国肝癌手术切除的大量临床实践建立中国的肝癌分期系统。新版规范依据中国的具体国情及临床实践积累,依据患者的全身状况、肝功能情况、肝外转移、血管侵犯、肿瘤数目、肿瘤大小等特征将肝癌进行分期,分期方案包括7期:Ia期、Ib期、IIa期、IIb期、IIIa期、IIIb期、IV期,同时基于不同分期优化选择治疗方案,形成了一套适合我国肝癌患者的肝癌分期和治疗选择系统。中国肝癌临床分期及治疗路线见图3。
与中国肝癌分期相对应的治疗方案选择上有以下显著变化。
第一,适当扩大肝癌手术切除及局部消融的适应证,并重视联合治疗。新版规范指出外科治疗仍是根治肝癌的主要方法,肝脏储备功能良好的Ia期、Ib期和IIa期肝癌是手术切除的首选适应证。在部分IIb期(肿瘤数目较多,≥4个)和IIIa期(伴有血管侵犯)肝癌患者中,手术切除有可能获得比其他治疗方式更好的效果(证据等级1),但需更为谨慎的术前评估,设计细致的手术方案,须充分考虑联合消融、肝动脉化疗栓塞治疗(transcatheter arterial chemoembolization, TACE)、放疗及全身治疗等方法以提高手术切除疗效。局部消融是作为手术切除之外的另一种根治性治疗选择。其最佳适应证:单个肿瘤直径≤5 cm;或肿瘤结节不超过3个、最大肿瘤直径≤3 cm;无血管、胆管和邻近器官侵犯以及远处转移的患者(证据等级1)。新版规范适当扩大了局部消融肝癌的适应证,对单个较大(>5 cm)的肝癌(Ib期)可采取局部消融和/或联合TACE的治疗手段。对于不能手术切除的直径3~7 cm的单发肿瘤或多发肿瘤,可联合TACE(证据等级1)。局部消融方法有多种,如射频、微波、冷冻消融及无水酒精等,应当根据各消融技术的优势,结合肿瘤的大小及位置选择最适合的局部消融方法。
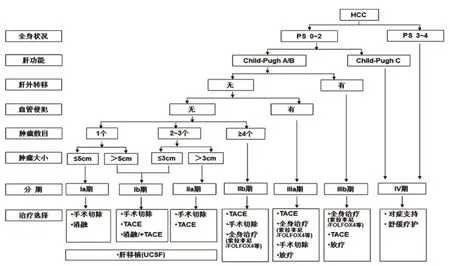
图3 中国肝癌临床分期及治疗路线[3]Figure 3 Hepatocellular carcinoma staging system and treatment allocation in China[3]
第二,推荐了现阶段肝癌肝移植标准。肝移植作为肝癌根治性治疗手段之一,尽管国内已有多家单位和学者陆续提出了不同的肝癌肝移植标准,但尚未统一,仍须多中心协作研究以获得高级别的循证医学证据。经专家组充分讨论,新版规范推荐采用美国加州大学旧金山分校(UCSF)标准作为现阶段我国肝癌肝移植的标准,因此新版规范对肿瘤数目≥4 个(IIb期)的治疗选择中未列入肝移植。
第三,系统治疗时间前移。新版规范关于肝癌的全身治疗中仍然将分子靶向药物索拉非尼列为首位,明确指出:迄今为止,索拉非尼仍然是惟一获循证医学证据最高,且得到批准治疗晚期肝癌的分子靶向药物,可用于肝功能Child A、B级的患者(证据等级1),而且将全身治疗如索拉非尼等提前到IIb期(肿瘤数目≥4个)。
第四,增加禁忌应用TACE的肾功能障碍标准。TACE被认为是肝癌非手术治疗的最常用方法之一(证据等级1),多作为手术治疗和消融治疗以及放疗的联合治疗手段应用。新版规范在介入治疗禁忌证中增加了肾功能障碍标准,即肌酐>2 mg/dl或者肌酐清除率<30 ml/min的患者禁忌应用TACE。
第五,肯定了晚期肝癌的放射治疗效果。不管是外放射治疗,还是放射性粒子植入的内放射治疗,新版规范中指出放疗对伴有门静脉/下腔静脉癌栓或肝外转移的IIIa期、IIIb期肝癌可改善症状,延长生存期。
第六,引入循证医学依据,重视局部加局部治疗和局部联合全身治疗。
5 新版诊疗规范明确指出了全身治疗的疗效评估标准
对于化疗患者,仍然采用Recist 1.1标准,可同时参考血清学肿瘤标记(AFP)以及肿瘤坏死程度的变化,一般在治疗期间每6~8周进行影像学评估,同时通过动态观察患者的症状、体征及治疗相关不良反应进行综合评估。鉴于索拉非尼、TACE治疗很少能改变肿瘤大小,故建议采用以肿瘤血管生成和密度改变为基础的修改后实体瘤疗效评价标准(mRecist标准)。mRecist标准是以“存活肿瘤”为对象,能够更加客观地评估索拉非尼、TACE治疗的疗效。对于免疫治疗的评价,可参照irRC(immune-related response criteria)标准。
6 总 结
以最高级别的循证医学证据为基础,以已发表的重要文献为依据,更新修订、精炼突出重要的以及新的诊疗相关内容,与国际接轨,形成具有中国特色的《原发性肝癌诊疗规范(2017年版)》,其出台有非常重要的现实意义,相信在新版规范的指引下,各种治疗方法的应用将更加规范,局部加局部治疗和局部联合分子靶向药物为首的全身治疗将不断发展。但是肝癌诊治的真实世界仍面临种种挑战,肝癌的精准治疗仍有待突破,免疫治疗已进入精确、联合、多样化的时代,如何根据患者的具体病情,制定最佳的个体化治疗方案仍须要在新规范的基础上不断总结临床经验,开展多中心的随机对照临床和基础研究,进一步完善肝癌诊疗规范。靶向药物联合免疫治疗或将成为未来治疗晚期肝癌的方向。
[1] Torre LA, Bray F, Siegel RL, et al. Global cancer statistics, 2012[J].CA Cancer J Clin, 2015, 65(2):87-108.
[2] Chen W, Zheng R, Baade PD, et al. Cancer statistics in China,2015[J]. CA Cancer J Clin, 2016, 66 (2):115-132.
[3] 中华人民共和国国家卫生和计划生育委员会. 原发性肝癌诊疗规范(2017 年版)[J].传染病信息,2017,30(3):111-127.
[4] Zeng MS, Ye HY, Guo L, et al. Gd-EOB-DTPA-enhanced magnetic resonance imaging for focal liver lesions in Chinese patients: a multicenter, open-label, phase III study[J].Hepatobiliary Pancreat Dis Int, 2013, 12(6):607-616.
[5] Ichikawa T, Saito K, Yoshioka N, et al. Detection and characterization of focal liver lesions: a Japanese phase III,multicenter comparison between gadoxetic acid disodiumenhanced magnetic resonance imaging and ontrast-enhanced computed tomography predominantly in patients with hepatocellular carcinoma and chronic liver disease[J]. Invest Radiol, 2010,45(3):133-141.
[6] Chen CZ, Rao SX, Ding Y, et al. Hepatocellular carcinoma 20mm or smaller in cirrhosis patients: early magnetic resonance enhancement by gadoxetic acid compared with gadopentetate dimeglumine[J]. Hepatol Int, 2014, 8(1):104-111.
[7] Lencioni R, de Baere T, Soulen MC, et al. Lipiodol transarterial chemoembolization for hepatocellular carcinoma: a systematic review of efficacy and safety data[J]. Hepatology, 2016,64(1):106-116.
(2017-08-14收稿 2017-08-20修回)
(本文编辑 闫晶晶)
Diagnosis and treatment guidelines for hepatocellular carcinoma(2017 Edition): an update and interpretation
WANG Chun-ping, REN Bo, LU Yin-ying, HUANG Jia-gan, LI Yin-yin, ZENG Zhen, YANG Bin, GAO Xu-dong, YANG Yong-ping*Center of Therapeutic Research for Hepatocellular Carcinoma, 302 Military Hospital of China, Beijing 100039, China
The National Health and Family Planning Commission of the People's Republic of China published evidencebased clinical practice guidelines on diagnosis, treatment and management of hepatocellular carcinoma (V2017) in June 2017. In this guidelines, the diagnosis, staging, and treatment of hepatocellular carcinoma are updated. This article briefly describes and interprets only new or changed recommendations.
carcinoma, hepatocellular; diagnosis; treatment; standard
R735.7
A
1007-8134(2017)04-0193-05
10.3969/j.issn.1007-8134.2017.04.003
首都临床特色应用研究与成果推广课题(Z161100000516173);院长基金课题(YNKT2010003)
100039 北京,解放军第三〇二医院肝脏肿瘤诊疗与研究中心(王春平、陆荫英、黄加干、李因茵、曾珍、杨斌、高旭东、杨永平),麻醉科(任波)
杨永平,E-mail: yongpingyang@hotmail.com
*Corresponding author, E-mail: yongpingyang@hotmail.com
