HPLC考察头孢克洛颗粒的有关物质
2017-06-24顾晓红
顾晓红
(苏州市药品检验检测研究中心,江苏 苏州 215104)
HPLC考察头孢克洛颗粒的有关物质
顾晓红
(苏州市药品检验检测研究中心,江苏 苏州 215104)
目的:建立头孢克洛颗粒中头孢克洛有关物质检查的方法。方法:采用高效液相色谱法(HPLC),C18色谱柱;以pH 4.0的0.78%磷酸二氢钠为流动相A,pH 4.0的0.78%磷酸二氢钠-乙腈(55∶45)为流动相B;检测波长220 nm;流速1.0 mL/min;线性梯度洗脱。结果:该方法稳定性RSD为0.44%,平均回收率99.1%,相对标准偏差(RSD)为0.52%,8个厂家的8批样品测定结果均满足要求。结论:该方法专属性好,灵敏度高,可作为测定头孢克洛颗粒有关物质的方法。
高效液相色谱法;头孢克洛颗粒;有关物质
头孢克洛是第二代口服广谱头孢菌素,临床用于治疗敏感菌所致的呼吸道、泌尿道和皮肤、软组织感染及中耳炎等[1]。头孢克洛颗粒在《中华人民共和国药典》(2015年版)未收载有关物质检查项,主要考虑颗粒的辅料成分比较复杂,对检查结果可能会有干扰,但考虑到其在储存和生产过程中易产生杂质,影响安全性和有效性[2],因此对头孢克洛颗粒进行有关物质考察是有必要的。本次考察主要参照头孢克洛原料及干混悬剂有关物质的测定方法[3-5],以下是本次考察说明:①《中华人民共和国药典》(2015年版)二部和《欧洲药典》(EP9.0)及《美国药典国家处方集》(USP39-NF34)中头孢克洛有关物质测定方法均采用线性梯度洗脱,前两者方法相同,均以主要杂质对照δ-3异构体考察系统适用性,与后者方法有所差别,《中华人民共和国药典》(2015年版)二部要求头孢克洛在23 min左右出峰,USP39-NF34则要求23~29 min,实际出峰时间更接近《中华人民共和国药典》的规定,在USP39-NF34规定范围内;②《中华人民共和国药典》(2015年版)二部有关物质测定方法为自身对照法,本次考察为便于计算采用头孢克洛对照品的主成分对照外标法;③本次考察拟定的限度参考了《中华人民共和国药典》(2015年版)二部头孢克洛干混悬剂有关物质检查的限度。
1 仪器与试剂
采用岛津LC-20AD高效液相色谱仪;Mettler XS105电子分析天平;头孢克洛对照品(含量95.3%,批号:130481-201205);头孢克洛δ-3异构体对照品(批号:130494-201204,购自中检院);头孢克洛颗粒:8个企业(A-H)各选择一批样品;辅料:羧甲基淀粉钠、聚乙烯吡咯烷酮K30、蔗糖、乳化桔子香精,由某企业提供。乙腈为色谱纯;磷酸二氢钠为分析纯。
2 实验方法
2.1 色谱条件
色谱柱:Phenomenex C18(4.6 mm×250 mm,5 μm),流动相A为0.78%磷酸二氢钠(用磷酸调节pH至4.0),流动相B为0.78%磷酸二氢钠(pH 4.0)-乙腈(55∶45),检测波长220 nm,流速1.0 mL/min,进样体积20 μL,线性梯度洗脱。见表1。
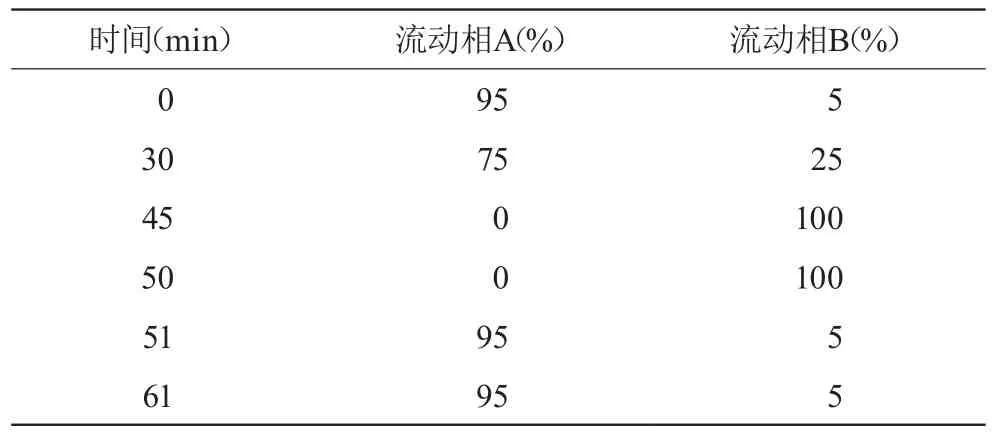
表1 梯度洗脱表
2.2 溶液配制
溶剂为0.27%磷酸二氢钠溶液(pH 2.5)。
2.2.1 对照品溶液 取头孢克洛对照品25 mg,置50 mL量瓶中,用溶剂溶解制成500 μg/mL的溶液。
取头孢克洛δ-3-异构体对照品25 mg,置25 mL量瓶中,用溶剂溶解制成1000 μg/mL的溶液。
精密移取上述两种对照品溶液各5 mL,置100 mL量瓶中,用溶剂制成分别约含25 μg/mL和50 μg/mL的混合溶液。
2.2.2 供试品及自身对照溶液 取样品适量(约相当于头孢克洛50 mg),置10 mL量瓶中,用溶剂溶解并稀释至刻度,摇匀,取续滤液作为供试品溶液;精密量取1 mL,至100 mL量瓶中,用溶剂稀释至刻度,摇匀。
2.2.3 空白辅料溶液 取颗粒空白辅料适量(相当于头孢克洛50 mg的颗粒辅料),置10 mL量瓶中,用溶剂稀释至刻度,摇匀。
3 结果与讨论
3.1 专属性实验
3.1.1 系统适应性实验 空白辅料、混合对照和供试品溶液的HPLC色谱图见图1。头孢克洛保留时间24.6 min,头孢克洛与头孢克洛δ-3-异构体峰分离度9.7,头孢克洛峰拖尾因子0.98,理论板数按头孢克洛峰计算为89695。已获得的辅料峰不干扰主峰,同时与杂质峰完全分离, 各杂质峰与主峰完全分离,本方法系统适应性符合检测要求。

图1 空白辅料、混合对照、供试品溶液HPLC图
3.1.2 破坏实验 ①酸破坏产物的制备:取A企业样品适量(约相当于头孢克洛50 mg),置10 mL量瓶中,加1 mol/L盐酸适量浸润,静置1 h,用1 mol/L氢氧化钠中和后加溶剂溶解并稀释至刻度,摇匀,滤过,取续滤液即得。②碱破坏产物的制备:取A企业样品适量(约相当于头孢克洛50 mg),置10 mL量瓶中,用1 mol/L氢氧化钠适量浸润,立即用1 mol/L盐酸溶液中和后加溶剂溶解并稀释至刻度,摇匀,滤过,取续滤液即得。③氧化破坏产物的制备:取A企业样品适量(约相当于头孢克洛50 mg),置10 mL量瓶中,用30%过氧化氢适量浸润,静置1 h,加溶剂溶解并稀释至刻度,摇匀,滤过,取续滤液即得。④光破坏产物的制备:取A企业样品适量(约相当于头孢克洛50 mg),置10 mL量瓶中,置4500 lx强光下照射5天,加溶剂溶解并稀释至刻度,摇匀,滤过,取续滤液即得。⑤热破坏产物的制备:取A企业样品适量(约相当于头孢克洛50 mg),置10 mL量瓶中,105℃烘箱中放置1 h,加溶剂溶解并稀释至刻度,摇匀,滤过,取续滤液即得。
破坏试验结果表明,在强酸、强碱中主成分全部降解破坏,氧化后在6.8 min,10.8 min处有较大破坏产物,热破坏也增加了几个小的杂质峰,光照对峰影响较小。综上所述,强酸、强碱和强氧化对头孢克洛颗粒的性质影响很大,同时表明本色谱系统破坏产物与主成分峰完全分离。
3.2 精密度试验
取“2.2.2”项下的供试品溶液,连续进样6次,峰面积测得结果为122915296,122917960,123546606,123836596,124030541,1241345421,RSD为0.44%,结果表明,本法进样精密度良好。
3.3 检出限试验
取“2.2.1”项下的对照溶液,用溶剂逐级稀释制成系列浓度进样检测,当信噪比为3∶1时,头孢克洛的最低检测限度为0.25 ng左右,头孢克洛δ-3-异构体的最低检测限度为1 ng左右。
3.4 稳定性试验
取“2.2.2”项下供试品溶液及其自身对照溶液,分别于0,2,4,6,12,24,36 h进样,记录色谱图,主峰峰面积无明显的降解。结果表明该溶液在室温条件下稳定性良好,不过为避免温度影响,USP39-NF34明确规定,样品液在室温条件下应2 h内进样,冰箱保存条件下在20 h内应进样。
3.5 线性试验
精密称取头孢克洛对照品12.5 mg,置50 mL量瓶中,加溶剂溶解并稀释至刻度,摇匀,再分别精密量取1.0,1.5,2.0,2.5,3.0 mL,置10 mL量瓶中,加溶剂稀释至刻度,摇匀,作为头孢克洛对照品系列浓度溶液。取上述溶液进样。以峰面积A为纵坐标,浓度C(μg/mL)为横坐标,进行线性回归。头孢克洛在25~75 μg/mL内,与峰面积呈良好的线性关系,线性回归方程:
A=31999C+21142,
相关系数r=0.9999。
精密称取δ-3头孢克洛对照品20 mg,置20 mL量瓶中,加溶剂溶解并稀释至刻度,摇匀,分别精密量取0.5,1.0,1.5,2.0,3.0 mL,置20 mL量瓶中,加溶剂稀释至刻度,摇匀,作为δ-3头孢克洛对照品系列浓度溶液。取上述溶液进样。以峰面积A为纵坐标,浓度C(μg/mL)为横坐标,按最小二乘法进行线性回归。δ-3头孢克洛浓度在25~150 μg/mL内,与峰面积呈良好的线性关系,线性回归方程:
A=35782C+36433,
相关系数r=0.9999。
3.6 准确度试验
精密称取A企业样品适量(约相当于头孢克洛50 mg),置10 mL量瓶中,加入δ-3头孢克洛对照品0.8,1.0,1.2 mL,用溶剂溶解并稀释至刻度,摇匀,滤过。分析结果见表1,可见该方法的准确度良好。
3.7 样品测定
共考察不同厂家的供试品8批,结果见表2。

表1 有关物质回收率结果(n=6)

表2 头孢克洛颗粒有关物质检测结果
4 结论
参照《中华人民共和国药典》(2015年版)二部头孢克洛干混悬剂有关物质检查项下要求[1],8批样品均在限度范围内,即单个杂质峰面积均小于对照溶液主成分峰面积的2倍(2.00%),各杂质峰面积和均小于对照溶液主成分峰面积的3倍(3.00%),本实验建立的HPLC方法真实反映了市场上头孢克洛颗粒的质量情况,该方法专属性好,灵敏度高,可作为检测头孢克洛颗粒有关物质的方法,对进一步提高头孢克洛颗粒的标准具有积极意义,更保证了药品使用的安全性和有效性。
[1]国家药典委员会.中华人民共和国药典(2015年版)二部[S].北京:中国医药科技出版社,2015:258-261.
[2]刘海涛,张寒,王俊秋,等.北京地区市售头孢克洛胶囊质量评价[J].首都医药,2011,18(12):48-49.
[3]李蔷薇,李强,邓俊丰,等.HPLC法测定头孢克洛原料中杂质C的研究[J].中国抗生素杂志,2015,40(8):599-602.
[4]向世英,林波,梁振益.头孢克洛干混悬剂中有关物质的研究[J].化学分析计量,2009,18(1):44-47.
[5]傅小英,郑悦,田增光,等.头孢克洛胶囊有关物质考察[J].解放军药学学报,2013,29(3):244-246.
本文编辑:张钰
Determination of Relevant Substances in Cefaclor Granules by HPLC
Gu Xiao-hong
(Suzhou Research Center for Drug Control and Detection, Jiangsu Suzhou 215104, China)
Objective:To establish a method for determination of cefaclor-related substances in cefaclor granules. Methods:HPLC was adopted by using a C18column, serving 0.78% sodium dihydrogen phosphate (pH 4.0) as the mobile phase A and 0.78% sodium dihydrogen phosphate (pH 4.0)-acetonitrile (55∶45) as the mobile phase B. The detection wavelength was 220 nm, while the flow rate was 1.0 mL/min. Linear gradient elution was adopted. Results:The RSD in stability test was 0.44%. The average recovery was 99.1% with a RSD of 0.52%. All the determination results of eight batches of samples from eight manufacturers were satisfied. Conclusion:The method is specific and sensitive, which may be for the determination of cerfaclor-related substances in cefaclor granules.
HPLC; Cefaclor Granules; Related Substances
R917
A
10.3969/j.issn.2096-3327.2017.04.009
2017-02-03
顾晓红,女,硕士,主管药师。研究方向:药品质量检验。E-mail:callmegxh@126.com
