EDTA络合滴定法持续测定铁矿石中钙和镁研究
2015-11-26洪达峰
洪达峰
摘要:EDTA络合滴定法是测定铁矿石中钙和镁的主要方法之一,对于计算铁矿石中的氧化镁和氧化钙含量有着重要作用。对铁矿石中铜、铅、锌、镍、锰等干扰元素进行处理后,在PH值=10的氨水-氯化铵溶液中,以酸性铬兰K-萘酚绿B为指示剂,利用EDTA络合滴定法测定钙、镁的合量;随后另取一份样品容液加入适量氢氧化钾溶液,将PH值调至13左右,以钙试剂为指示剂,用同样的方法测定钙含量,将钙镁合量减去钙量来计算镁含量。采用此方法对铁矿标准样品中氧化钙、氧化镁进行了多次平行测定,测定值与认定值相符,测定结果的相对标准偏差(RSD)在1.1%~3.0%(n=6)之间,加标回收率范围在98%~104%。
关键词:EDTA络合滴定法;铁矿石;钙镁含量
铁矿石中的氧化钙和氧化镁含量一般在w(B)为0.χ%~χ%之间,通常采用络合滴定和原子吸收光谱法进行测定。原子吸收法测定钙、镁的步骤虽较为简便,对低含量的钙、镁有较高的准确性,但钾、钠等元素对测定结果影响较大[3],同时因為钙、镁元素的灵敏度很高,采用换次灵敏线方法并不能达到测定高含量钙镁的目的[4]。而采用络合滴定方法测定时,以使用六次甲基四胺-铜试剂来分离干扰离子的方法应用较多,缺点是分析流程繁杂,需多次沉淀分离,同时因生成氢氧化物沉淀,对钙、镁离子有一定的吸附,致使结果偏低。
本实验是采用盐酸溶矿,以消除矿石中的硫化物,然后加入氢氟酸以去除矿石中的硅,利用硫化钠和铜试剂来将铁矿石中的铜、锌、镍、锰等元素化为沉淀物,达到分离钙镁目的,再利用盐酸羟胺来消除剩余少量锰元素的干扰,其他残余的金属离子使用三乙醇胺等来掩蔽。然后分别利用不同溶液和指示剂得到钙镁合量及钙含量,并通过加减法得到镁元素的单独含量,在持续测定中,需要保证测定结果相同于原子吸收光谱法(AAS)为止[1]。
1.EDTA络合滴定法的实验方法
1.1滴定剂准备
EDTA络合滴定法是以络合反应为基础的方法,其借助的滴定剂主要是多金属有较强络合能力的氨羧络合剂。
在对铁矿石中金属金属离子的络合反应中,所有的滴定剂主要有以下几种:(1)新配置的氢氧化钠溶液,浓度分别为200g/L和500g/L,要在密封条件下用塑料瓶保存。(2)新配置的200g/L氢氧化钾溶液,保存条件与氢氧化钠相同。(3)酸类:1.15g/mL的氢氟酸、1.42g/mL的硝酸和1.67g/mL的高氯酸;1+1的盐酸。(4)PH值为10的氨水~氯化铵溶液,制取方法为:在200ml纯水中加入67.5g氯化铵并搅拌,在此过程中加入570ml氨水,然后加纯水至1000ml定容。(5)(1+4)的三乙醇胺溶液。(6)10g/L的L-半胱氨酸溶液和盐酸羟胺。(7)试剂类溶液:30g/L的铜试剂溶液;100g/L的硫化钠溶液;氧化钙标准溶液,取纯度优级的碳酸钙1.7848g置于玻璃杯中,加入盐酸少量进行溶解后煮沸,以除去其中的二氧化碳,冷却后转移到刻度为1000ml的容量瓶中,加入纯水至刻度;氧化镁标准溶液,取光谱纯的氧化镁1.0000g置于玻璃杯中,其制作步骤与氧化钙相同,得到浓度为1mg/mL的标准溶液。(8)指示剂类:酸性铬兰K-萘酚绿B,分别取酸性铬兰K和萘酚绿B各1.0g,将其与100g硫酸钾混合搅匀后研磨,其中硫酸钾需要事先进行1~2h烘干处理,烘烤温度为105℃,保存采用磨口瓶;钙试剂,分别取2-羟基-3-萘酸0.20g和硫酸钾20g,将两者混合搅匀研磨后用磨口瓶保存。(9)EDTA标准溶液制备与标定:制备,精确称量EDTA 7.446g,将其置于1000ml纯水中溶解,得到浓度为0.02mol/L的标准溶液;标定,分别取氧化钙和氧化镁标准溶液各25.00ml共同置于容量为250ml的锥形瓶中,并向其中加入纯水25ml,再分别取盐酸羟胺0.2g、三乙醇胺溶液5ml、氢氧化钾溶液10ml、L-半胱氨酸溶液4ml以及钙指示剂0.08~0.1g,在试剂加入过程中,都需要在搅拌均匀后开始下一种试剂的加入,当混合溶液表现出纯蓝色时,即为EDTA标准溶液标定值。
1.2 EDTA络合滴定测定铁矿石中钙和镁的实验方法
在测定实验中,需要先将铁矿石中其它金属离子进行掩蔽,然后测定钙镁合量,再次测定钙含量,并据此得到镁含量的值,因此,在实验中,需要分三个步骤进行,具体如下:
1.2.1其它金属离子的掩蔽处理 精确称量铁矿石测定样品0.5000g,将其置于容量为250ml的聚四氟烧杯中,然后向其中加入盐酸(1+1)20ml,将烧杯放在电热板上加热数分钟,以使样品充分溶解;在此过程中,还需分别加入氢氟酸5~8ml、硝酸3~5ml,待烧杯被加热近干时,再取高氯酸5ml加入其中,等到出现高氯酸白烟并持续3~4min后,将烧杯取下,并将烧杯内物质转移到同容量的玻璃烧杯中持续加热,直到不再出现白烟为止。再次向冷却后的玻璃杯中加入盐酸(1+1)10ml和纯水20ml,通过加热使其中的盐类充分溶解后静置冷却;向其中加入纯水少量,并加入氯化铵5g,加热至沸腾状态后滴入氢氧化钠溶液,其滴入量以出现轻微的氨气味和氢氧化物沉淀为止。然后对溶液进行搅拌,并在此过程中添加100g/L的硫化钠溶液5ml,利用加热板将其加热到沸腾,随即冷却到室内温度状态;最后将得到的溶液转移到事先加入了铜试剂溶液5ml的250ml容量瓶中,加入纯水至刻度并过滤,去除最先流出的10~15ml左右的溶液;抽取过滤后溶液50ml二份,分别置于250ml的锥形瓶中。
1.2.2钙镁总含量的测定 取以上得到的1份滤液,依次向其中添加盐酸羟胺0.2g、三乙醇胺溶液(1+4)5ml、浓度为10g/L的L-半胱氨酸溶液4ml和PH=10的氨水-氯化铵溶液10ml以及性铬兰K-萘酚绿B指示剂0.08~0.1g,在加入过程中,每种试剂都需要做搅匀处理,最后用EDTA标准液进行滴定,当出现纯蓝色时就可以停止。
1.2.3钙含量测定及镁含量计算 (1)钙含量测定:取另一份滤液,向其中依次加入盐酸羟胺0.2g、三乙醇胺溶液(1+4)5ml、浓度为10g/L的L-半胱氨酸溶液4ml和浓度为200g/L的氢氧化钾溶液10ml以及性铬兰K-萘酚绿B指示剂0.08~0.1g,其余条件与钙镁含量测定步骤相同。(2)氧化钙、氧化镁含量计算:
w(CaO)=(V1-V0)*T/m*100%;
式中:w(CaO)为氧化钙的质量分数,%;
V1为滴定试样溶液消耗的EDTA标准溶液体积,mL;
V0为滴定试样空白溶液消耗的EDTA标准溶液体积,mL;
T为EDTA标准溶液对氧化钙的滴定度,g/mL;
m为测定氧化钙所用的试样质量,g。
w(MgO)=(V1-V0)*T/m*100%-w(CaO)×0.7187;
式中:w(MgO)为氧化镁的质量分数,%;
w(CaO)为氧化钙的质量分数;
V1为滴定试样溶液中钙、镁合量消耗的EDTA标准溶液体积,mL;
V0为滴定试样空白溶液中钙、镁合量消耗的EDTA标准溶液体积,mL;
T为EDTA标准溶液对氧化镁的滴定度,g/mL;
m为测定钙、镁合量所用的试样质量,g;
0.7187为氧化钙换算为氧化镁的因数。
2.EDTA络合滴定法的理论分析
2.1其它干扰离子的排除
在铁矿石中,会给钙、镁测定造成干扰的主要有铜、铁、锌、铅、锰、镍等金属离子,所以,为保证测定准确,必须对其进行排除。根据这些金属离子特性,可以将其置于微氨条件中,利用铜试剂和硫化钠,将其分别转变为络盐和硫化物沉淀,消除其干扰。同时,为保证指示剂不会被痕量金属离子干扰出现结果偏高问题,特别采用了盐酸羟胺、三乙醇胺溶液和L-半胱氨酸溶液进行掩蔽,起到消除干扰的作用[2]。
2.2指示剂的选用原理
采用酸性铬兰K-萘酚绿B作为指示剂,是由于其测定结果不会手微量Fe3+影响,而在铁矿石中,Fe3+很难被完全掩蔽,因此,酸性铬兰K-萘酚绿B有较强的实用性。
3.样品分析
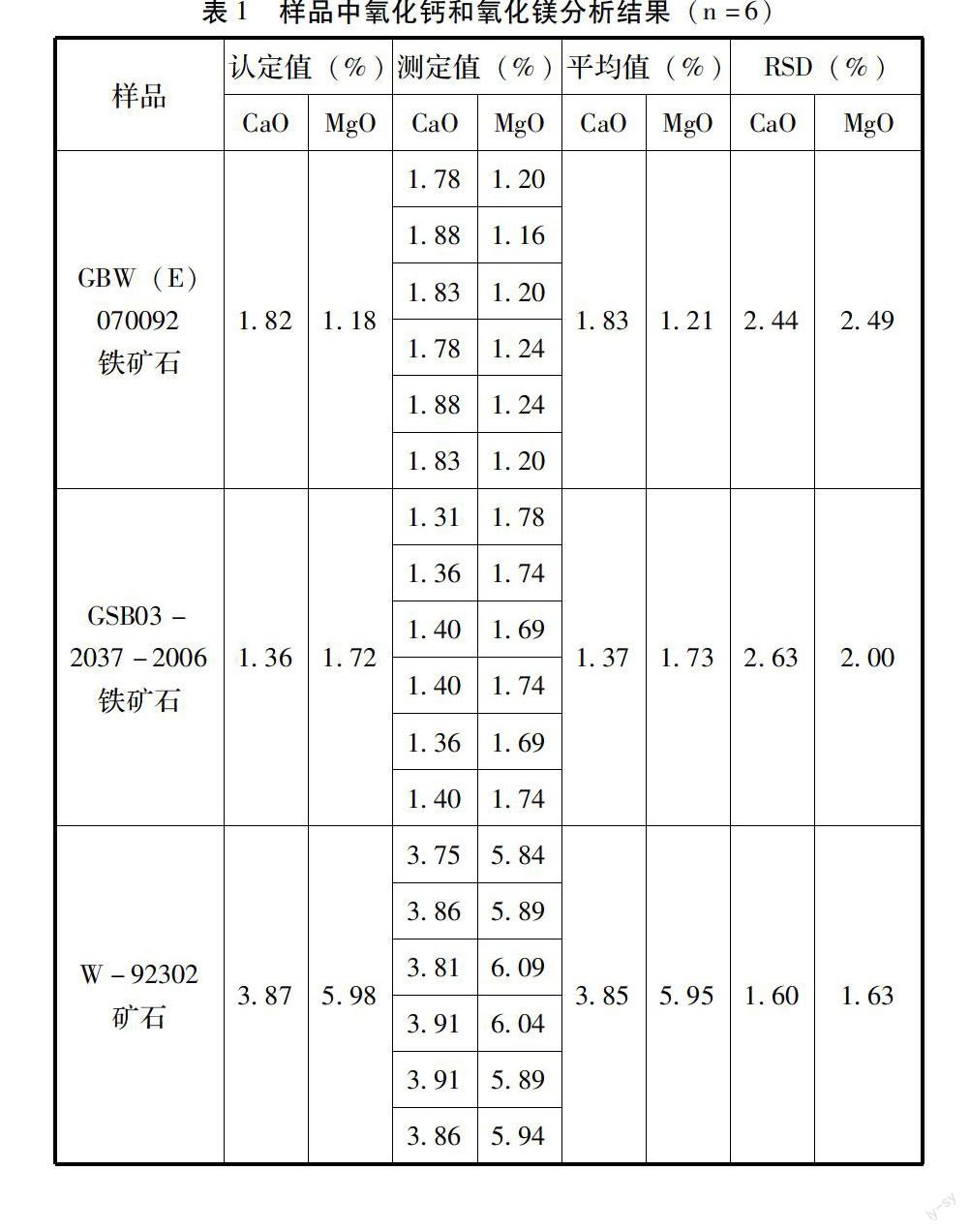
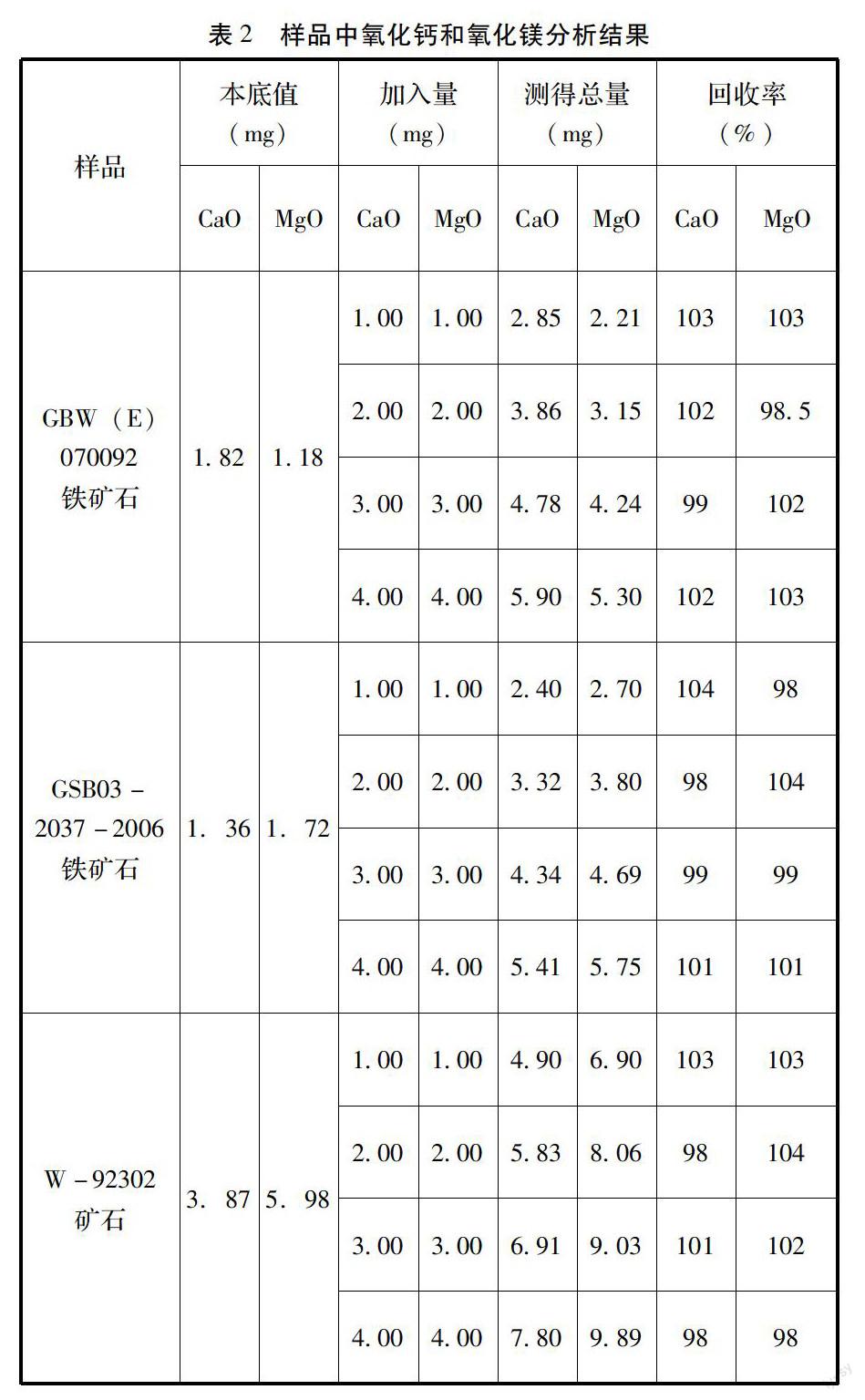
按照实验方法对不同的铁矿标准样品进行了多次平行滴定,测定结果见表1。为了检验本方法的准确度,按照实验方法进行了回收率试验,结果见表2。
4.小结
综上所述,在测定铁矿石中的钙和镁时,需要利用矿样中金属离子特性,在微氨条件下,通过硫化钠和铜试剂使其变为沉淀物,同时采用掩蔽剂进一步消除其它金属离子干扰,再使用EDTA络合滴定法来测定铁矿石中钙和镁含量,测定结果的相对标准偏差(RSD)在1.1%~3.0%(n=6)之间,加标回收率范围在98%~104%。
参考文献:
[1]赵树宝.EDTA络合滴定法测定铁矿石中钙和镁[J].冶金分析,2009,11:76-80;
[2]张建珍,樊晓红,薛丽华.EDTA络合滴定法连续测定铁矿石中钙和镁[J].冶金分析,2011,08:74-78;
[3]董启太.原子吸收分光光度法测定铁矿中氧化钙、氧化镁.山西冶金,2003,01:35-37;
[4]孫伟,李俊伟,邢宇,郭丽娜.巧用原子吸收光谱干扰测定高含量钙镁.科技论坛,2008第12期;
[5]《岩石矿物分析》(第二分册) 地质出版社 2011年2月第1版
