住院患者药物性肝损伤病因分析及熊去氧胆酸协同治疗疗效观察
2015-08-12王震凯王少东杨妙芳路又可汪芳裕
施 慧,魏 娟,王震凯,王少东,杨妙芳,路又可,刘 炯,汪芳裕
住院患者药物性肝损伤病因分析及熊去氧胆酸协同治疗疗效观察
施慧,魏娟,王震凯,王少东,杨妙芳,路又可,刘炯,汪芳裕
【摘要】目的观察熊去氧胆酸协同治疗药物性肝损伤(DILI)患者的临床疗效,分析我院引起DILI的药物种类及其发生比例。方法纳入我院200例药物性肝损伤患者,分析引起DILI的药物种类。将患者分成两组,对照组给予异甘草酸镁、谷胱甘肽和多烯磷酯酰胆碱中的1~3种药物治疗,对伴有高胆红素血症者加用腺苷蛋氨酸;治疗组在对照组治疗的基础上,加用熊去氧胆酸,两组疗程均为4 w,观察治疗后肝功能变化和临床疗效。结果本组引起DILI的首位药物是免疫抑制剂(34.0%),其次为中药(28.5%),其后依次为抗生素(13.0%)、抗结核药物(7.5%)、抗肿瘤化疗药(7.5%)和解热镇痛药(4.5%);治疗组在肝功能改善方面明显优于对照组(P<0.01),尽管两组患者肝功能均有明显改善。结论引起我院住院患者DILI的最常见的药物为免疫抑制剂,可能与我院开展器官移植较多有关。熊去氧胆酸在甘草酸制剂等的基础上可以较快地改善DILI患者肝功能。
【关键词】药物性肝损伤;诱发药物;熊去氧胆酸;中药
药物性肝损伤(drug-induced liver injury,DILI)是指药物本身和(或)其代谢产物引起的肝脏损伤。DILI是常见的肝病之一,其发病率约为(1/100 000~1/10 000)暴露患者年(PYE)[1],仅次于病毒性肝炎、脂肪性肝病(乙醇和非乙醇性)[2]。它是发达国家急性肝衰竭的首要病因[3,4]。药物性肝损伤是影响人类健康的一大因素,是药物通过上市批准时遇到的重要问题,也是已上市药物退出市场的主要原因。目前,报道已有1000余种药物可引起DILI,几乎涉及各类药物。本文分析了我院住院患者诱发DILI的常见药物和熊去氧胆酸的治疗作用。
1 对象与方法
1.1研究对象回顾2010年10月~2014年5月在我院住院的200例DILI患者(导致肝损伤的药物有中药、抗病毒药、抗感冒药、抗肿瘤药、免疫抑制剂、降脂药等)。用药后发生的血生化学检测异常,表现为血清丙氨酸氨基转移酶(ALT)或直接胆红素升高至正常值上限2倍以上;或血清天冬氨酸氨基转移酶(AST)、碱性磷酸酶(ALP)、总胆红素(TB)同时升高,且其中至少有1项升高至正常值上限2倍以上。由于DILI发病机制具有复杂性、多样性,发病时间存在很大差异,临床表现亦多种多样,各诊断标准都存在其优缺点及局限性,临床诊断缺乏金标准,诊断量表也仅能作为参考。在现有的诊断标准不尽完善的情况下,目前DILI的诊断主要依靠排除法,详细询问用药史和用药过程中监测肝功能是诊断的关键,实验室检查可有助于与其他肝病鉴别诊断。本研究药物性肝损伤的诊断标准主要依据2007年由中华消化专业委员会拟定的《急性药物性肝损伤诊治建议(草案)》进行[5]。DILI的诊断基于以下几点:(1)药物暴露出现在肝损伤发生前,首剂用药至发生肝损伤的时间在5~90天内;(2)停药后血异常升高指标迅速恢复;(3)排除其他病因或疾病所致的肝损伤;(4)再次服用该药后又出现肝损伤指标明显异常。符合以上诊断标准的(1)+(2)+(3),或符合前三项中的2项,加上第(4)项,即诊断为DILI。本研究将土三七所致的肝损伤排除在外,因考虑其所致的肝损伤为特殊类型。诊断分型参照医学科学国际组织委员会(CIOMS)推荐的DILI分型标准分为3型[6],即(1)肝细胞型:ALT≥3 ULN和R≥5;(2)淤胆型:ALP≥2 ULN和R≤2;(3)混合型:ALT≥3 ULN,ALP≥2ULN和2<R<5,[R=ALT(ULN)/ALP (ULN)]。排除肝炎病毒、人类免疫缺陷病毒、酒精性肝病、脂肪性肝病、自身免疫性肝病、肝硬化等其它肝病。对有可疑其他原因所致的肝损伤,则检测受试者的肝功能及其可能引起肝功能改变的病因,如病毒性肝炎、脓毒症引起的淤胆、乙醇性、自身免疫性、胆源性疾病、血流动力学异常性、代谢紊乱、恶性肿瘤、肝脏手术或外伤等。同时也排除非肝因素引起的肝脏生化试验异常,如Dubin-Johnson综合征、先天性非溶血性黄疸、心肌梗死、肌病、充血性心力衰竭、全身炎性反应、营养不良等。常规进行超声、CT、MRI检查。根据饮酒史来判断有无酒精性肝炎。根据高血压病史判断有无缺血性肝脏疾病。
1.2检测常规ELISA法检测传染性疾病感染标志物[英科新创(厦门)公司];采用间接免疫荧光法或免疫印迹法检测抗核抗体(ANA)等十四项自身免疫性疾病标志物(欧蒙公司)。
1.3治疗方法停用一切可疑导致肝功能损伤的药物,休息,避免劳累和油腻饮食,加强营养。将患者分成两组。对照组应用保护肝细胞药物:给予异甘草酸镁(天晴甘美,正大天晴药业股份有限公司)0.32 g静脉滴注,1次/d,谷胱甘肽(泰特,意大利福斯卡玛公司)1.8 g静脉滴注,1次/d、多稀磷脂酰胆碱注射剂(易善复,赛诺菲安万特公司)697.5 mg静脉滴注,1 次/d,选择以上三种或两种。对有明显胆红素升高(血清TBIL大于171 μmol/L)者,则加用腺苷蛋氨酸注射剂(思美泰,雅培公司)1 g静脉滴注,1次/d;治疗组在对照组基础上加用熊去氧胆酸胶囊(UDCA,优思弗,德国霍克药厂)250 mg口服,3次/d。两组均治疗4 w,对4 w后仍有ALT和AST大于2 ULN者,则继续应用上述药物,直至血生化指标正常后改为口服给药,维持疗效至停药。
1.4统计学方法应用SPSS17.0软件进行统计分析。计量资料以(x±s)表示,采用t检验,P<0.05为差异有统计学意义。
2 结果
2.1一般资料对照组84例,男50例,女34例。年龄17~74岁,平均年龄(46.9±10.3)岁。肝细胞型25例,淤胆型27例,混合型32例;治疗组116例,男56例,女60例。年龄18~86岁,平均年龄(50.5±9.7)岁。肝细胞型38例,淤胆型35例,混合型43例。
2.2引起DILI的药物分类本组患者因免疫抑制剂引起的肝功能异常为最多,因中药引起的肝功能异常为其次,其他包括抗生素、抗结核药物、抗肿瘤化疗药物、解热镇痛药等(表1)。
2.3两组患者治疗前后血生化指标变化情况在治疗4w后,治疗组患者血TBiL、ALT、AST、ALP、γ-GT水平与对照组比较,差异有统计学意义(P<0.01,表2)。

表1 200例DILI患者诱发药物分类
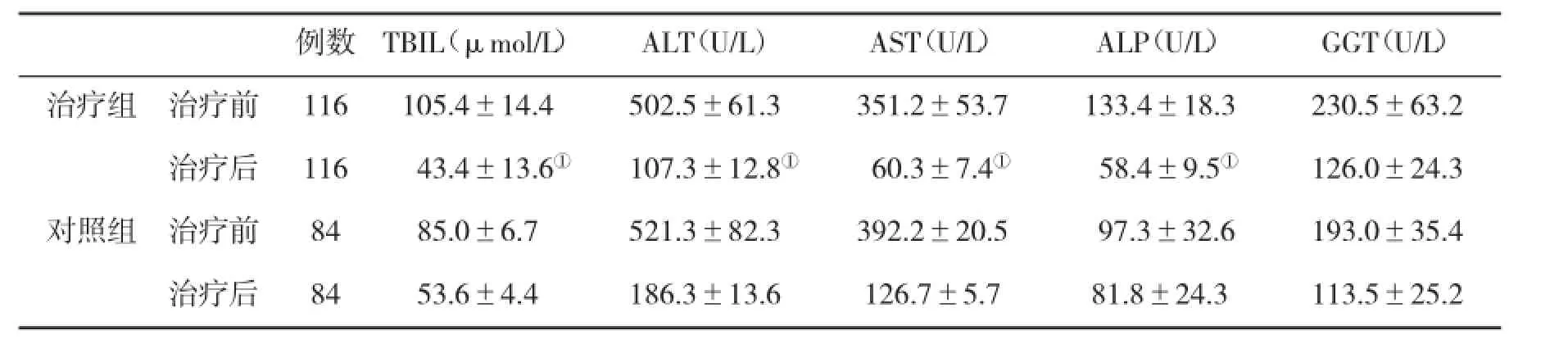
表2 两组治疗前后肝功能指标(x±s)变化的比较
3 讨论
近年来,DILI发生率呈上升趋势,在急性肝衰竭患者中,13%~15%由药物引起[7,8]。越来越多的患者也将药物副作用作为药物选择的首要考虑问题,这就对医生用药带来更大的考验。药物所引起的肝损伤,一般有两类反应,一类是直接肝毒性,是可预测的;另一类是因个体免疫反应情况及遗传因素不同对药物反应不同,难以预测。既往有基础肝病的患者更容易引起药物性肝损害的发生[9]。
在本研究中,引起DILI的首位药物是免疫抑制剂,其次为中药,后面依次为抗生素、抗结核药物、抗肿瘤化疗药、解热镇痛药等。在欧美,药物性肝损害最常见的病因是抗生素、心血管药物和中枢神经系统用药[10],亚洲则是中药和食品添加剂位列第一、二位[11]。国内报道,位居第1位的是中药制剂,第2位是抗生素[12]或激素[13],但本组药物性肝损伤的疾病谱有所不同,免疫抑制剂所占比例最大。由于我院肾病患者多,免疫抑制剂使用量大。本研究不包含在门诊就诊的轻度肝功能损害患者,实际在门诊这类因免疫抑制剂所致的肝损害患者数量仍有很多。此类药物的使用常常是两种同时服用,比如吗替麦考酚酯联合他克莫司,或雷公藤联合百令胶囊等组合,或在此基础上加用激素或抗真菌药物。本研究将有些合并使用的免疫抑制剂和中成药物的病例纳入免疫抑制剂所引发的的药物性肝损害中,因而有可能人为地使免疫抑制剂所致的肝损害比例增加。有文献报道,由中草药引起的肝损伤比例有逐年上升的趋势,为21.5%~37.7%[14]。中药所致肝损伤甚至多于西药[15]。本研究将土三七所致肝损伤的2例排除,该2例患者均发生了肝功能衰竭[16],最终死亡,考虑该病例使用激素或CRRT治疗或可致判断药物的作用有误,且发生的肝小静脉闭塞症的病理学改变较为特殊。中药引起的肝损伤比例较大的原因是受我国传统观念的影响,多数国人认为中药天然而安全,而中药的副作用往往被忽视。市面上还有一些私人中医诊所,开具一些所谓秘方,甚至连具体用药都不明示。目前,抗生素的使用仍然有一部分是根据个人经验选择,其种类有医生个人习惯的差别[17],所引起的肝功能损害也应引起重视。抗结核药物引起的肝功能损害日益得到重视[18],往往我们在使用抗结核药物同时就使用保肝药物服用,故我院抗结核药物治疗后的药物性肝损害发病率低于抗生素所致肝损害的发病率。
本研究所有病例均无死亡,大部分病例在治疗2周后就可以得到明显好转,在治疗4周后虽有部分患者未能达到生化学上的完全缓解,但都获得了明显改善。有研究认为TBiL、AST水平和DILI类型与患者预后具有明显的相关性,而性别、年龄、ALT、γ-GT、ALP与预后相关性不大[19]。在本研究的治疗组患者中,可以看到TBiL、ALT、AST、ALP下降较对照组明显,考虑为UDCA能促进胆汁酸排泄及抑制细胞凋亡。在本研究中,药物性肝损害所致的胆红素升高最高达232.6 μmol/L,因出现黄疸的药物性肝损害预后较差(病死率在10%左右),因此对TBiL大于171 μmol/L的病例除了使用UDCA外,还加用了腺苷蛋氨酸降低胆红素,确保快速降低胆红素水平。2011年有一项研究表明,在重症DILI患者中使用UDCA是安全有效的[20]。UDCA是人体合成的内源性胆汁酸,较鹅去氧胆酸的亲水性更高而对细胞无毒,有免疫调节和抑制炎症作用。大量体内外试验表明,UDCA是细胞保护剂,可解毒、抑制过氧化物的产生、保护肝细胞线粒体结构[21,22]。根据Kaplowitz[23]提出DILI的发病机制,该病由“上、下游”事件和3个主要连续步骤组成:“上游”事件强调药物引起初始肝细胞损伤,“下游”事件泛指发生在线粒体中非特异的细胞损伤途径和细胞保护途径间的失衡。3个主要连续步骤:(1)内源性途径;(2)外源性途径;(3)直接损伤线粒体功能,触发细胞凋亡或坏死。在联合使用UDCA时发挥了对线粒体的保护作用,减少肝细胞的坏死,并且对下游事件的发生起到一定的抑制作用,从而促进TBiL、ALT、AST、ALP等的下降。UDCA是安全有效的治疗DILI的药物,联合运用时对于肝功能的改善有增效作用。
【参考文献】
[1] StephensC,LucenaMI,AndradeRJ.Geneticvariationsin drug-induced liver injury(DILI):resolving the puzzle.Front Genet,2012,16(11):253-253.
[2] NathwaniRA,KaplowitzN.Drughepatotoxicity.ClinLiver Dis,2006,10(2):207-217.
[3]Devarbhavi H,Dierkhising R,Kremers WK,et al.Single-center experience with drug-induced liver injury from India:causes,outcome,prognosis,and predictors of mortality.Am J Gastroenterol,2010,105:2396-2404.
[4]Au JS,Navarro VJ,Rossi S.Review article:Drug-induced liver injury-its pathophysiology and evolving diagnostic tools.Aliment Pharmacol Ther,2011,34:11-20.
[5]中华消化专业委员会.急性药物性肝损伤诊治建议(草案).中华消化杂志,2007,27(11):765-767.
[6] Bagheri H,Michel F,Lapeyre-Mestre M,et al.Detection and incidence of drug-induced liver injuries in hospital:a prospective analysis from laboratory signals.Br J Clin Pharmacol,2000,50:479-484.
[7]Aithal GP,Watkins PB,Andrade RJ,et al.Case definition and phenotype standardization in drug-induced liver injury.Clin Pharmacol Ther,2011,89:806-815.
[8] Au JS,Navarro VJ,Rossi S.Review article:drug-induced liver injury-its pathophysiology and evolving diagnostic tools.Aliment Pharmacol Ther,2011,34:11-20.
[9]李晨,辛绍杰,游绍莉.中草药致肝损害研究进展.实用肝脏病杂志,2013,16(6):278-281.
[10]García-Cortés M,Lucena MI,Pachkoria K,et al.Evaluation of naranjo adverse drug reactions probability scale in causality assessment of drug induced liver injury.Aliment Pharmacol Ther,2008,27:780-789.
[11]Takikawa H,Murata Y,Horiike N,et al.Drug induced liver injury in Japan:An analysis of 1676 cases between 1997 and 2006.Hepatol Res,2009,39:427-431.
[12]魏傲,石小枫.药物性肝损害344例临床分析.现代医药卫生,2010,26:3528-3530.
[13]Xu HM,Chen Y,Xu J,et al.Drug-induced liver injury in hospitalized patients with notably elevated alanine aminotransferase.World J Gastroenterol,2012,18(41):5972-5978.
[14]中华医学会消化病分会肝胆疾病协作组.全国多中心急性药物性肝损伤住院病例调研分析.中华消化杂志,2007,27(7):439-442.
[15]苏尊玮,廖宗琳.中药与西药所致药物性肝损伤的临床对比分析.实用肝脏病杂志,2009,12(2):137-138.
[16]Fontana RJ,Watkins PB,Bonkovsky HL,et al.Drug-induced liver injury network(DILIN)prospective study:rationale,design and conduct.Drug Saf,2009,32:55-68.
[17]FontanaRJ,SeeffLB,AndradeRJ,etal.Standardizationof nomenclature and causality assessment in drug-induced liver injury:summary of a clinical research workshop.Hepatology,2010,52:730-742.
[18]Kato H,Horita N,Miyazawa N,et al.Risk factors for liver injury with an elevated serum bilirubin concentration caused by antituberculous drugs.Intern Med,2013,52(19):2209-22014.
[19]滕光菊,孙颖,常彬霞,等.418例药物性肝损害临床特征及预后分析.肝脏,2013,18:11-14.
[20]Wree A,Dechêne A,Herzer K,et al.Steroid and ursodesoxycholic acid combination therapy in severe drug-induced liver injury.Digestion,2011,84(1):54-59.
[21]周健,刘黎,黄丽雯,等.牛磺熊去氧胆酸治疗非酒精性脂肪肝疗效观察.实用肝脏病杂志,2014,17(1):80-81.
[22]Anwar S,Jawad H,Sawsan S.A study of the effect of Nigella sativa(Black seeds)in isoniazid(INH)-induced hepatotoxicity in rabbits.Indian J Pharmacol,2012,44(6):678-682.
[23]Kaplowitz N.Idiosyncratic drug hepatotoxicity.Nat Rev Drug Discov,2005,4:489-499.
(收稿:2014-05-30)(本文编辑:陈从新)
第一作者:施慧,女,34岁,医学硕士,住院医师。E-mail:bena0923@163.com
DOI:10.3969/j.issn.1672-5069.2015.01.009
作者单位:210000南京市 南京军区南京总医院消化内科
通讯作者:汪芳裕,E-mail:wangf65@yahoo.cn
Common agents in patients with drug-induced liver injury and observation of therapeutic efficacy of ursodeoxycholic acid Shi Hui,Wei Juan,Wang Zhenkai,et al.Department of Gastroenterology and Hepatology,Nanjing General Hospital,Nanjing Military Area Command,Nanjing 210000,Jiangsu Province,China
【Abstract】Objective To investigate the common agents related to drug-induced liver injury(DILI)in our hospitalized patients and to observe the clinical efficacy of ursodeoxycholic acid in treatment of patients with DILI. Methods Two hundred patients with DILI were recruited in this study and the common agents were analyzed. The patients were divided into two groups.Patients in control group received magnesium isoglycyrrhizinate,glutathione and polyene phosphatidylcholine(one,two,and all or any combination of them)for four weeks.Ademetionine was given when hyperbilirubinemia appeared.The patients in observation group received additionally ursodeoxycholic acid for four weeks at the base treatment in the control.Results The leading agents in our patients with DILI were immunosuppressive agents(34.0%),followed by traditional Chinese medicin(28.5%),and other common agents were antibacterial(13.0%),antitubercular agents(7.5%),chemotherapeutics(7.5%),and antipyretic analgesics(4.5%).Liver function improved in both groups after four week treatment,while the efficacy was superior in ursodeoxycholic acid-treated patients(P<0.01).Conclusion Immunosuppressive agents are the main causes of DILI in our hospitalized patients,and the ursodeoxycholic acid could improve the efficacy of basic treatment such as glycyrrhizin in patients with DILI.
【Key words】Drug-induced liver injury;Common agents;Ursodeoxycholic acid;Traditional Chinese medicine
