Zn/Al-LDH和Zn/Mo-LDH及其改性产物的制备和吸附性能
2014-10-10田宏燕王月辉梁力曼王少飞
田宏燕,牛 奎,王月辉,梁力曼,王少飞,方 明
(河北科技师范学院化学工程学院,河北秦皇岛,066600)
随着染料合成、印染、纺织等工业废水的不断排放,染料造成的环境污染愈发严重。为了解决有机染料对环境造成的污染问题,许多国家已经投入了大量人力和财力进行环境治理。染料废水处理常用的脱色方法有吸附脱色、混凝脱色、化学氧化脱色、超滤膜脱色等多种方法[1,2]。其中吸附法因具有选择性吸附某些化合物的特性而在废水处理领域占有重要的地位[3],常用吸附剂有活性炭、树脂、矿物、废弃物(如炉渣等)等。但是,由于活性炭处理成本较高,微孔树脂吸附容量低,大孔树脂对大分子染料的亲合力差,其它类树脂的吸附能力也受到染料废水中无机盐的影响[4];矿物、废弃物虽然有较好的吸附处理效果,但吸附饱和后的产物处理又是一个亟待解决的难题,因此,开发新型高效吸附材料是一个重要的研究方向[5,6]。水滑石(Hydrotalcite,简称HT)又称为层状双金属氢氧化物 (Layered double hydroxide,LDH),它们是一类由带正电荷层和层间填充带负电荷的阴离子所构成的层状化合物,经焙烧以后的水滑石类材料以层状双金属氧化物(Layered double oxides,简称LDO)形式存在。因其可以自由调变层板电荷和层取代元素,使得水滑石及其焙烧形态的应用涉及多个学科领域,在环境污染治理中主要作为催化剂[7]和吸附剂(离子交换剂)[8]加以应用,并展现出良好应用前景[9]。本研究采用共沉淀法以硝酸锌、硝酸铝、氯化钼和尿素为原料,在水浴加热条件下制备出锌铝、锌钼层状双金属氢氧化物(LDH),并通过焙烧、改性制得了相应的双金属氧化物及其一系列衍生物。对所得产物在亚甲基蓝溶液中的吸附性能进行了对比研究,以期使其在污水处理中得到实际应用奠定理论基础。
1 材料与方法
1.1 实验仪器与试剂
硝酸锌(Zn(NO3)2·6H2O),硝酸铝(Al(NO3)3·9H2O),氯化钼(MoCl5),尿素(H2NCONH2),癸二酸(C10H18O4),辛二酸(C8H14O4),己二酸(C6H10O4),亚甲基蓝(C16H18ClN3S),以上药品均为分析纯。
傅里叶变换红外光谱仪,日本岛津FTIR-8900;X射线衍射仪(XRD),日本理学DMAX2500PCX,角度为2°~60°,转速10°/min;透射电子显微镜(TEM),日本日立7650;热重分析测试仪(TG),德国NETZSCHSTA409PC/PG。
1.2 实验方法
1.2.1 LDH 的制备 按M2+与M3+的摩尔比为2.33∶1 称取硝酸锌(Zn(NO3)2·6H2O,0.023 1 mol),硝酸铝(Al(NO3)3·9H2O,0.009 9 mol)或氯化钼(MoCl5,0.009 9 mol),尿素(H2NCONH2,0.5 mol),放入1 L的烧杯中加入2次蒸馏水制成1 L混合溶液,放入90℃的水浴锅中,在剧烈搅拌的条件下反应进行12 h,将烧杯从水浴锅中取出,陈化12 h,抽滤洗涤,至滤出液pH值为7,将滤出物放入干燥箱中,在60℃下干燥12 h,取出用研钵研为粉末,得到Zn/Al-LDH和Zn/Mo-LDH。
1.2.2 产品的处理 将适量制备的Zn/Al-LDH和Zn/Mo-LDH样品盛在坩埚中,放入马弗炉中由室温升温至500℃,焙烧3 h,得到相应的焙烧产物,记为Zn/Mo-LDO。将焙烧产物在干燥器中冷却至室温。称取适量的脂肪酸(己二酸、辛二酸、癸二酸),放入200 mL的2次蒸馏水中,搅拌溶解。再按脂肪酸与交换前体的质量比2∶1称取定量焙烧产物,放入制好的有机酸溶液中搅拌制成浆液(均匀的悬浮液),在水浴锅中升温至80℃,搅拌反应8 h,陈化12 h,抽滤洗涤,至滤出液pH值为7,滤出物于60℃干燥12 h,取出用研钵研磨为粉末,得到改性产物。样品通过X射线衍射(XRD)、红外射线(IR)、透射电子显微(TEM)、热重(TG)等手段来表征。
2 结果与讨论
2.1 LDH 的TG分析
Zn/Mo-LDH有2个质量损失阶段(图1)。第1质量损失阶段较为明显,对应于110~280℃之间,由失去表面吸附水和层间结构水引起的,此时仍保持层状结构,质量损失为18%,即受热后Zn/Mo-LDH晶体质量减轻,质量分数为0.72;第2质量损失阶段对应于290~490℃之间,此时水滑石的结构被破坏,层间的OH-基团及层板羟基和层间的CO2-3分别以H2O和CO2的形式失去。质量损失为2%,即质量分数为0.92(图1)。
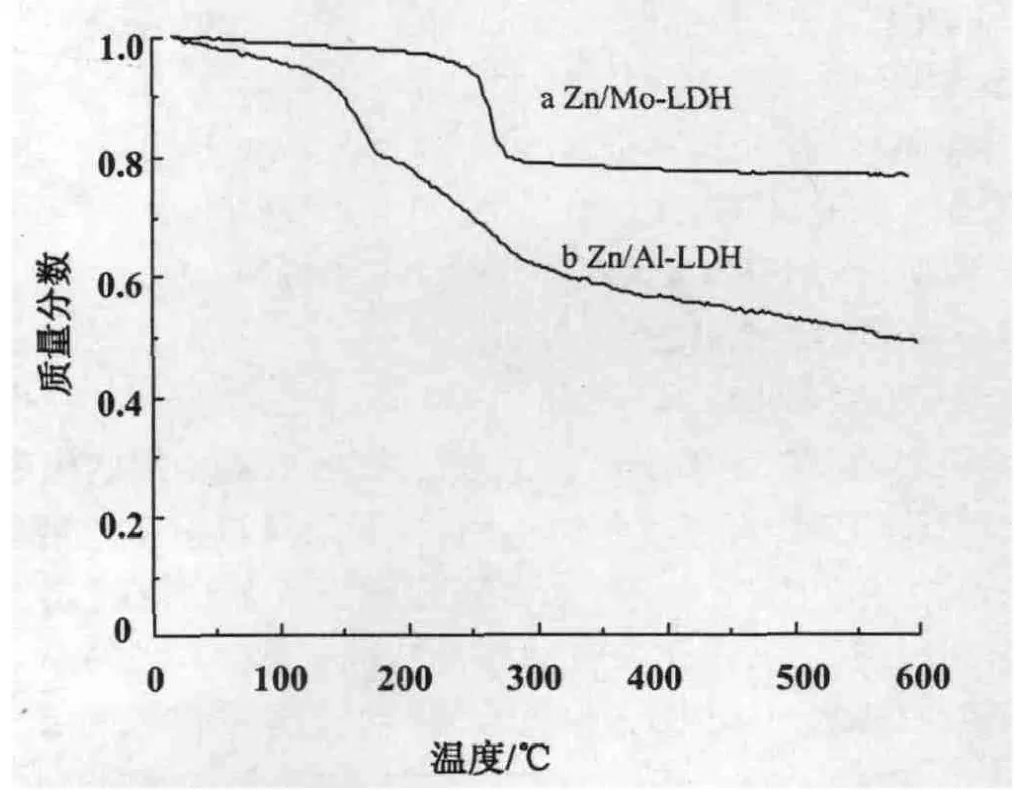
图1 Zn/Mo-LDH和Zn/AL-LDH的TG曲线
Zn/Al-LDH也有2个相似的质量损失阶段。第1质量损失阶段对应于80~175℃之间,由失去表面吸附水和层间结构水引起,此时仍保持层状结构,质量损失约16.0%,即质量分数约为0.84(图1);第2质量损失阶段对应于190~460℃之间,此时水滑石的结构被破坏,层间的OH-基团及层板羟基和层间的分别以H2O和CO2的形式失去,质量损失为25.0%,即质量分数约为0.75。
比较可知,Zn/Mo-LDH中的水、OH-及在Zn/Al-LDH中在相对更高的温度下才会失去,说明高价LDH与层间水分子的氢键作用更强,层状结构更为稳定。
2.2 LDH改性前后XRD分析
Zn/Al-LDH和Zn/Mo-LDH改性前后的XRD在低角度的衍射峰比较尖锐,高角度的衍射峰较弱,并出现成倍数关系(图2,图3),有规律的特征衍射峰,体现了其层状结构的存在,衍射峰峰形窄而尖锐且具有良好的对称性及强度,表明样品的结晶度良好(图2和图3的a曲线),其对应的Zn/Al-LDH层间距为d=0.77 nm,Zn/Mo-LDH的层间距为d=0.73 nm。经500℃焙烧后,表征层状结构的特征衍射峰已经消失,出现了ZnO和Al2O3混合氧化物的特征衍射峰。表明500℃焙烧后的产物已经完全失去了层状结构,层间的和H2O已经完全失去,成为Zn-Al或Zn-Mo复合氧化物(图2和图3的b曲线)。
考察LDH插层产物的晶面衍射峰位置是否向低2θ角度发生位移,通常是判断有机高分子或离子是否插入层状主体层间的有力证据之一。图2中的a,c,d,e曲线分别为Zn/Al-LDH,Zn/Al-己二酸,Zn/Al-辛二酸,Zn/Al-癸二酸的XRD谱图。与a曲线相比,其他3条曲线的晶面衍射峰向低2θ角发生明显的位移,其各衍射峰所对应的层间距也由 d=0.77 nm 变为 0.83,1.07,1.26 nm。图 3 的 a,c,d,e曲线中Zn/Mo-LDH改性前后衍射峰位置也发生了明显偏移,层间距由改性前d=0.73 nm变为0.82,1.07,1.27 nm。改性后产物特征衍射峰为对称性良好的高强度尖锐峰形,表明插层后的LDH分子结构依然保持良好的层状结构规整性,同时可知随着直链脂肪酸的长度的增长,改性后LDH的层间距呈现递增趋势。
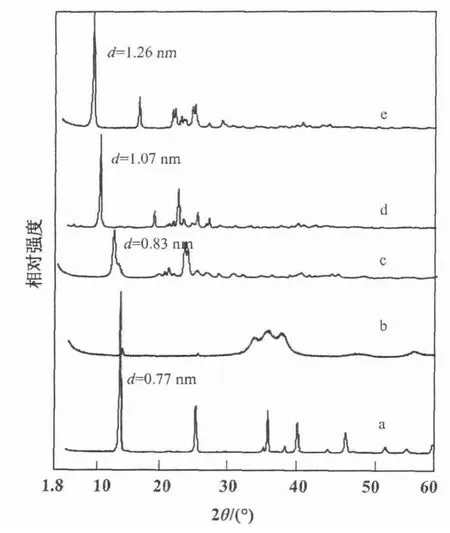
图2 Zn/Al-LDH及其焙烧产物改性产物的XRD图谱
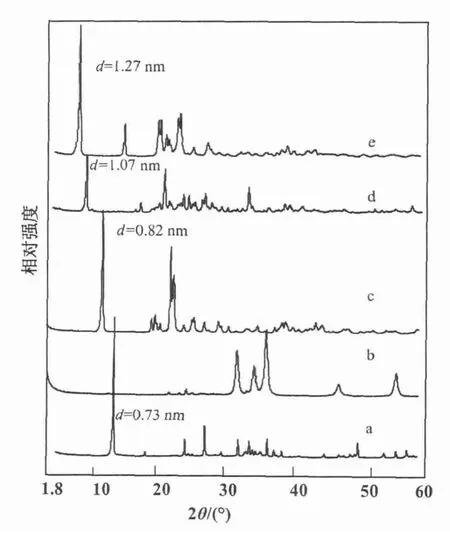
图3 Zn/Mo-LDH及其焙烧产物改性产物的XRD图谱
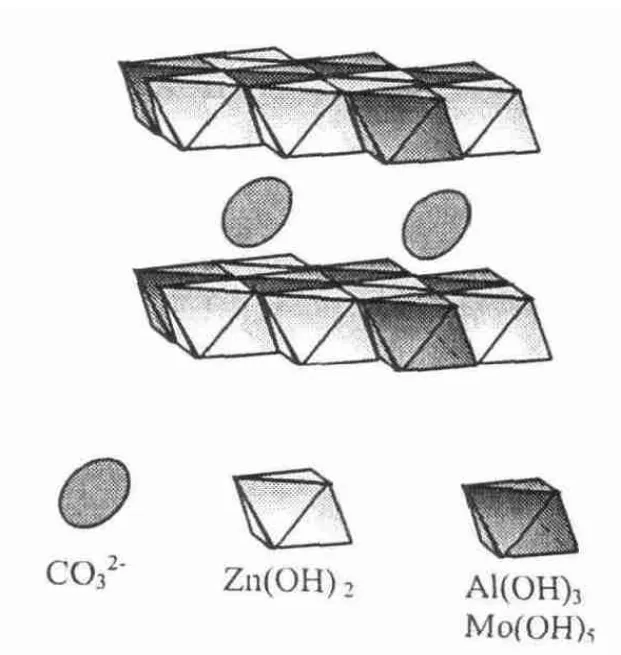
图4 Zn/Al-LDH和Zn/Mo-LDH结构
2.3 LDH改性前后IR分析
对Zn/Al-LDH和Zn/Mo-LDH改性前后产物进行IR分析,结果表明,在3 400 cm-1处附近存在吸收峰为层状氢氧化锌铝或氢氧化锌钼中羟基的氢键伸缩振动峰,与自由态的羟基(~3 600 cm-1)相比,层间水分子可能与层间阴离子和(或)层板羟基之间发生氢键作用,因此吸收峰向低波数位移。1 600 cm-1处附近的弱吸收峰为H2O中羟基的弯曲振动峰,说明合成的层状氢氧化锌铝中有羟基和水分子的存在,在 1 300 cm-1处附近的吸收峰为中C-O的不对称伸缩振动峰,与碳酸钙中碳酸根吸收峰位置(1 429 cm-1)相比,吸收峰向低波数发生位移,表明层间插入的碳酸根离子与层间水分子间存在着强的氢键作用。
结合Zn/Al-LDH和Zn/Mo-LDH的热重分析以及XRD图谱分析,可知其构型分别由Zn-Al或Zn-Mo的氢氧化物八面体构成层板结构,层内以及层间含有H2O分子,层间阴离子由组成(图4)。
2.4 LDH改性前后TEM分析
改性前后Zn/Al-LDH呈规则的正六边形层状结构,Zn/Mo-LDH呈不规则层状结构(图5),其有机酸改性产物都整体或部分插入层状结构中,其结果与XRD及IR分析所得结论相符。
2.5 层状双金属氢氧化物(LDH)的吸附性能
2.5.1 吸附试验 测定10种不同吸附剂在0.25~4.00 h内室温下对质量浓度为30 mg/L的亚甲基蓝溶液的吸附量。取1组(10个)具塞锥形瓶,编号为1~10,向其中加入质量浓度为30 mg/L的亚甲基蓝溶液(C0),再向各锥形瓶中各加入质量为0.05 g的固体吸附剂(Zn/Al-LDH,Zn/Al-己二酸,Zn/Al-辛二酸,Zn/Al-癸二酸,Zn/Al-LDO,Zn/Mo-LDH,Zn/Mo-己二酸,Zn/Mo-辛二酸,Zn/Mo-癸二酸,Zn/Mo-LDO)。将具塞锥形瓶放入恒温水浴振荡器中震荡0.5 h后离心分离取上清液测定其吸光度,根据所得上清液吸光度,从标准曲线中读取各上清液的亚甲基蓝的平衡质量浓度(Ce)。计算得各吸附后溶液的平衡质量浓度Ce,求出各吸附剂的脱色率为[(C0-Ce)/C0]×100%。
2.5.2 LDH改性前后及LDO吸附性能 在较长的时间范围内(2.75 h),Zn/Al-LDH及其焙烧产物和改性产物的吸附率按Zn/Al-LDO,Zn/Al-癸二酸,Zn/Al-LDH,Zn/Al-辛二酸,Zn/Al-己二酸的顺序依次减小(图6)。同时,随着直链脂肪酸长度的增长,改性后LDH的吸附能力与层间距一样呈现递增趋势。
在一定时间范围内(0.9 h),Zn/Al-LDH及其焙烧产物和改性产物的吸附率按Zn/Mo-LDH,Zn/Mo-癸二酸,Zn/Mo-辛二酸,Zn/Mo-己二酸,Zn/Mo-LDO的顺序依次减小(图7)。同时可以得出结论,随着直链脂肪酸的长度增长,改性后LDH的吸附能力与层间距一样呈现递增趋势。Zn/Al-LDO,Zn/Al-癸二酸,Zn/Mo-LDH,Zn/Mo-癸二酸均能够达到较高的脱色率。
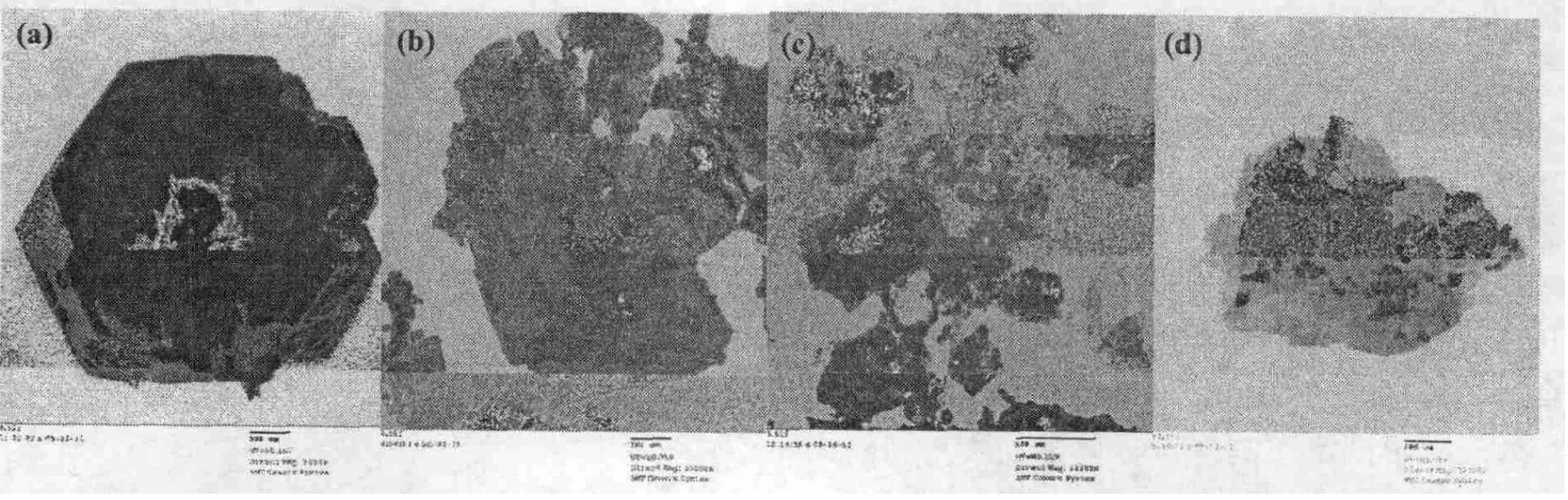
图5 Zn/Al-LDH和Zn/Mo-LDH改性前后透射电镜照片
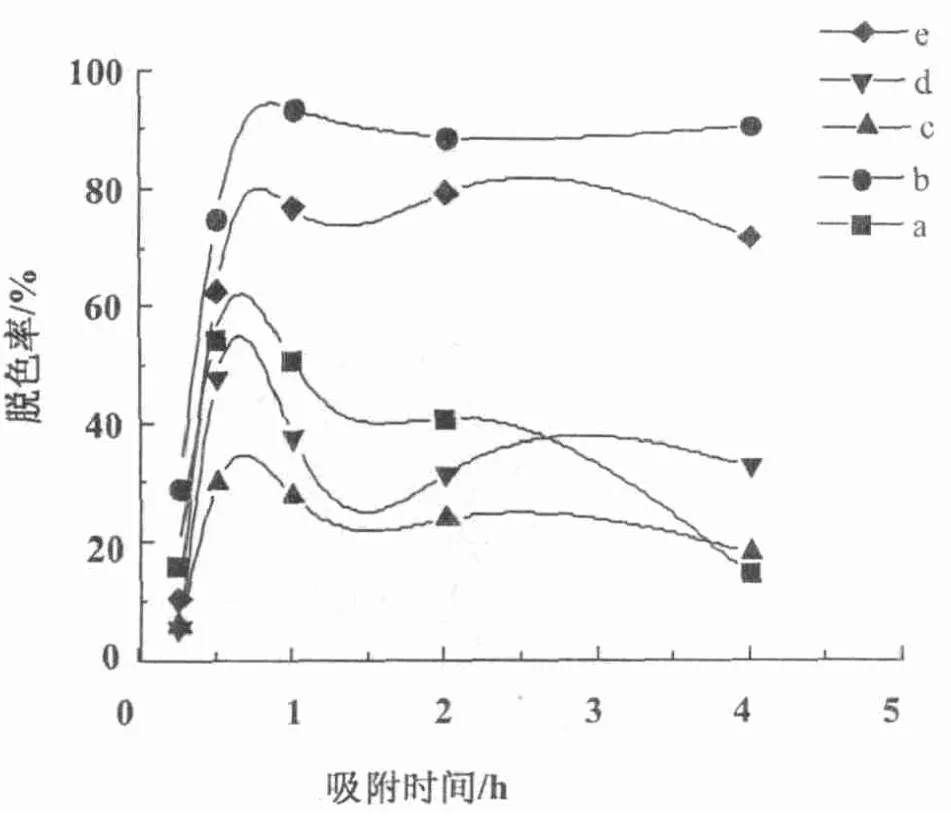
图6 Zn/Al-LDH及其焙烧产物和改性产物的 吸附时间-脱色率曲线
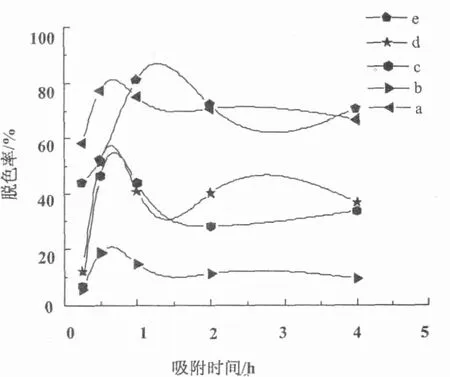
图7 Zn/Mo-LDH及其焙烧产物和改性产物的 吸附时间-脱色率曲线
2.5.3 吸附时间对脱色率的影响 测量各吸附剂最佳吸附时间及其脱色率,可知Zn/Al-LDO,Zn/Al-癸二酸,Zn/Mo-LDH,Zn/Mo-癸二酸均能达到较高的脱色率(80%以上),而这4种吸附剂中Zn/Al-LDO的脱色率最大,达94.5%,而Zn/Mo-LDH的最佳吸附时间最短,为0.66 h(表1)。
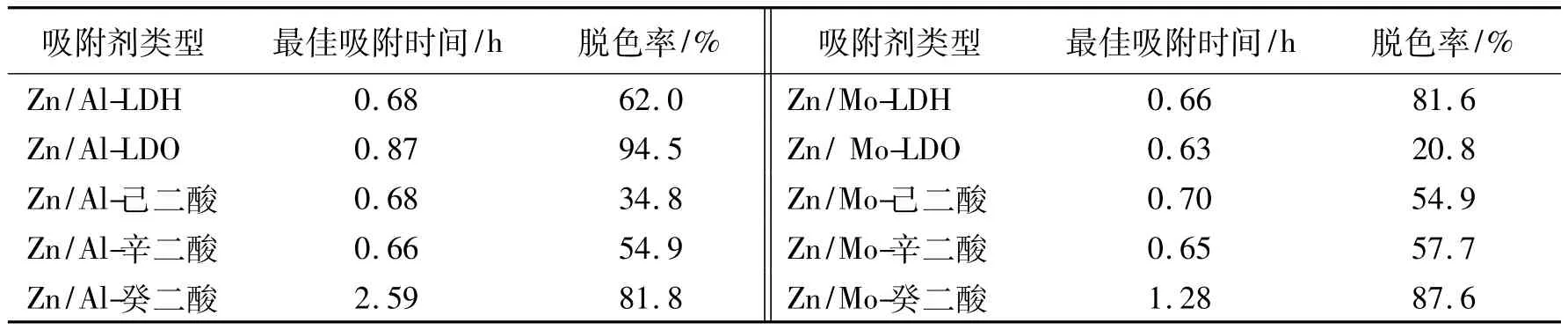
表1 各吸附剂的最佳吸附时间及其吸附率
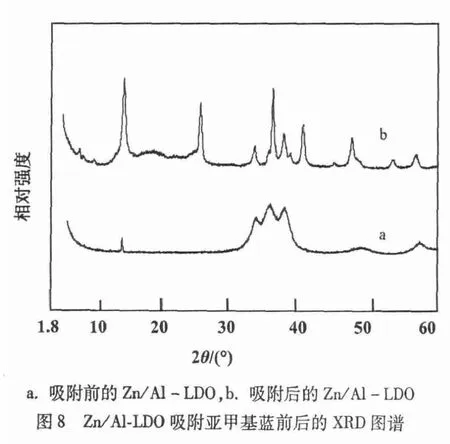
2.5.4 吸附原理分析 水滑石对亚甲基蓝的吸附主要是通过层板上的正电荷与碱性染料的亚甲基蓝之间的静电作用实现的。这也从一定程度上解释了高价的Zn/Mo-LDH比Zn/Al-LDH对亚甲基蓝的吸附更加迅速的原因。其中吸附效率最高的Zn/Al-LDO吸附后出现了层状结构的特征衍射峰(图8),说明吸附过程中使得Zn/Al-LDO由金属氧化物变成了水滑石的层状结构,这一现象正是利用了水滑石的记忆效应。
3 结 论
用共沉淀法制得了多价金属锌钼水滑石(Zn/Mo-LDH),并成功地用有机酸(己二酸,辛二酸,癸二酸)对其进行了改性。XRD,IR,TEM的表征结果表明,所制得的锌钼水滑石及其改性产物具有较为良好的晶体结构。同时发现,随着直链脂肪酸的长度增长,改性后LDH的层间距呈现递增趋势。
通过吸附试验证实高价金属锌钼水滑石对碱性染料的吸附快速高效。除癸二酸改性Zn/Mo-LDH外,其他几种改性后Zn/Mo-LDH及Zn/Al-LDH的脱色率均小于改性前的脱色率,Zn/Mo-LDH-癸二酸的脱色率高于Zn/Mo-LDH及其他改性产物的脱色率,但其所需要最佳吸附时间较长。高价金属水滑石作为阴离子吸附剂具有很高的研究价值。
[1]姚铭,杜莉珍,王凯,等.合成水滑石治理水体阴离子染料污染研究[J].环境科学学报,2005,25(8):1 034-1 040.
[2]王立秋,王海增.层状氢氧化镁铝对阴离子染料的脱色性能研究[D].青岛:中国海洋大学,2006.
[3]王昕.水滑石类吸附剂的研究进展[J].化工时刊,2007,21(11):67-75.
[4]胡静,吕亮.焙烧水滑石对Cr(VI)的去除性能研究[J].化工时刊,2007,21(6):32-33.
[5]王立秋,王海增,李冬梅,等.水滑石对水溶性染料活性深蓝 ST-2GLN脱色性能研究[J].矿物学报,2007,27(2):115-120.
[6]牛向楠,朱洪涛,赵毅.水滑石类材料的制备及在水污染治理中的应用[J].电力科技与环保,2010,26(4):29-32.
[7]Vaocari A.Clays and catalysis a promising future[J].Applied Clay Science,1999,14(4):161-198.
[8]Foranoa C,Costantinob U,V Prévota,et al.Chapter 14.1-Layered Double Hydroxides(LDH)[J].Developments in Clay Science,2013,5:745-782.
[9]杨一青,刘从华,张莉,等.水滑石及类水滑石材料的合成及催化应用新进展[J].炼油与化工,2008(l):9-11.
