单剂量口服奥美沙坦酯片在中国健康志愿者体内的药代动力学研究
2014-10-08胡玉钦刘建芳侯艳宁
于 洋,胡玉钦,刘建芳,侯艳宁
高血压病是常见的心血管疾病,控制血压及预防其并发症是治疗的主要目的[1-2]。奥美沙坦酯是一种非肽类抗高血压药,通过选择性拮抗血管紧张素Ⅱ受体(AT1)发挥作用,该药口服吸收快、半衰期长,每日一次给药,患者依从性好,且药物相互作用少、不良反应发生率低、耐受性良好[3-5]。研究表明,奥美沙坦酯在欧洲人体内具有良好的药代动力学特性,年龄、性别和肝肾功能等因素对药代动力学的影响较小[6-7]。国内有关奥美沙坦酯人体药动学的报道多为临床生物等效性研究,奥美沙坦酯给药剂量均为20 mg,未见其他剂量下中国人口服给药的药代动力学资料[8-10]。本文采用高效液相色谱-质谱法(high performance liquid chromatography mass spectrography,HPLC-MS)测定健康志愿者口服奥美沙坦酯后血浆中奥美沙坦的浓度,研究奥美沙坦酯片单次口服给药在中国健康志愿者体内的药代动力学特征,为临床应用该药提供依据。
1 材料与方法
1.1 仪器与试药 Agilent 1100高效液相色谱-质谱联用仪(含二元输液泵、在线脱气机、自动进样器、柱温箱,配MSD四极杆质谱检测器)及A.09.01化学工作站(美国Agilent公司)。奥美沙坦酯片(北京万生药业有限责任公司,批号:20040101,规格20 mg/片)。试验所用试剂除甲醇(色谱纯)外均为市售分析纯,空白人血浆购自解放军白求恩国际和平医院血库。
1.2 受试对象 本试验共入选30名志愿者,其中29名参加并完成本试验,男15名,女14名;年龄(23.43±2.21)岁,体重(61.24±7.33)kg,身高(1.69±0.08)m。受试者于试验前进行病史询问和体格检查,心电图、胸透、肝肾功能、血尿常规等均正常。试验前2周及试验期间未服用其他任何药物,试验期间禁烟酒及含咖啡因的饮料。受试者了解试验目的、方法、意义以及可能发生的不良反应后,签署知情同意书。
1.3 方法 采用随机、开放试验设计。试验方案经医院伦理委员会批准后实施。受试者随机分配至3个奥美沙坦酯剂量组,低剂量组10名,男5名,女5名,单次口服剂量为20 mg;中剂量组10名,男5名,女5名,单次口服剂量为40 mg;高剂量组9名,男5名,女4名,单次口服剂量为80 mg。受试者于试验前1 d进食清淡晚餐后禁食10 h过夜,于试验当日清晨空腹口服给药(温开水250 ml送服)。服药后2 h内禁饮水,试验期间统一进食标准餐。受试者分别于服药前及服药后 0.5、1、2、3、4、6、8、12、24、36、48、60 及72 h 取静脉血 5 ml,肝素抗凝,离心分离血浆后于-20℃冷冻保存备用。
1.4 血药浓度检测 受试者血浆样品中奥美沙坦浓度以本实验室建立的LC-MS法测定[11]。血浆样品采用固相萃取法处理,过程为:取待测样品1 ml,依次加入甲醇和内标工作液(浓度为0.25 μg/ml的替米沙坦甲醇溶液)各100 μl,涡旋混匀后离心,上样至活化、平衡后的固相萃取小柱(OASIS HLB 3cc,美国Waters公司),先用5%甲醇溶液洗脱杂质,再用2 ml甲醇洗脱,洗脱液在60℃水浴中通氮气流吹干,残渣用流动相100 μl溶解后进行LC-MS分析。LC-ESI+-MS检测方法条件参照文献[11]方法,定量分析采用选择离子监测(SIM)方式,奥美沙坦和内标替米沙坦选择监测的离子分别为m/z 447.2 和 m/z 515.3,质谱扫描时间均为 0.64 s。
1.5 数据处理和统计分析 房室模型判断采用DAS 2.0药代动力学软件进行拟合,统计距法计算该药在不同给药剂量时主要药代动力学参数,其中血药浓度峰值(Cmax)和达峰时间(tmax)均为实测值。采用SPSS 11.5统计软件,计量资料以均数±标准差(±s)表示,采用线性回归分析对Cmax和曲线下面积(AUC)值与剂量进行线性相关分析,各组间其他参数比较采用方差分析,α=0.05为检验水准。
2 结果
2.1 血药浓度检测 上述试验条件下,奥美沙坦的保留时间为6.7 min,内标替米沙坦为8.6 min,血浆基质中的内源性物质对待测物和内标均无干扰。奥美沙坦与内标峰面积的比值在1~3000 ng/ml范围内呈良好的线性关系,最低定量浓度为1 ng/ml。低浓度(3 ng/ml)、中浓度(100 ng/ml)、高浓度(2400 ng/ml)3个质控样品的日内和日间相对标准差(RSD)均 <13.3,准确度为 -2.4%~0.9%。受试者单剂量口服奥美沙坦酯片20、40和80 mg后平均血药浓度-时间曲线见图1,结果显示3个剂量组的血药浓度-时间曲线随剂量增加而递增。
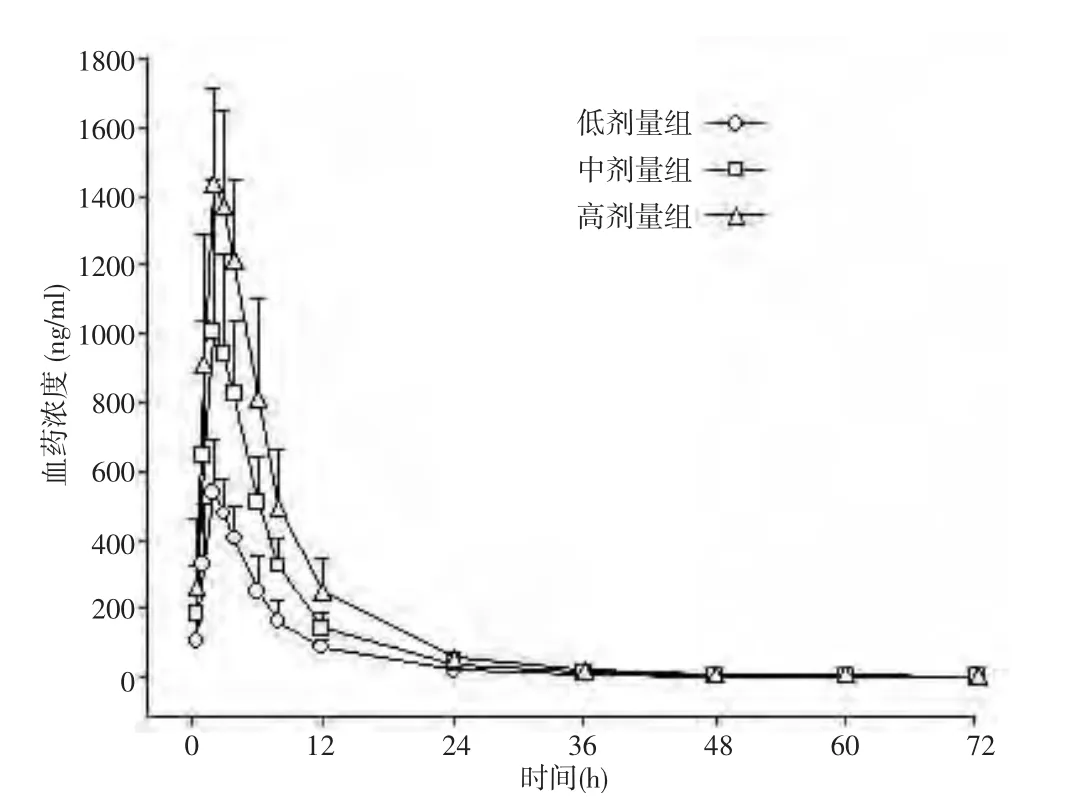
图1 3个剂量组健康受试者口服奥美沙坦酯片后平均血药浓度-时间曲线
2.2 药代动力学特征 受试者单剂量口服奥美沙坦酯片20、40和80 mg后体内过程符合二房室模型,Cmax、AUC值与给药剂量呈显著正相关(r=0.80,r=0.87,P <0.01)。3 个剂量组 tmax、半衰期(t1/2)和平均驻留时间(MRT)比较差异均无统计学意义(P>0.05),高剂量组表观清除率(Cl/F)显著高于低、中剂量组,差异均有统计学意义(P<0.05),见表1。
2.3 安全性 试验期间所有受试者均未主诉不适、未发生不良反应,耐受性较好。
表1 3个剂量组健康受试者口服奥美沙坦酯片后主要药代动力学参数(±s)
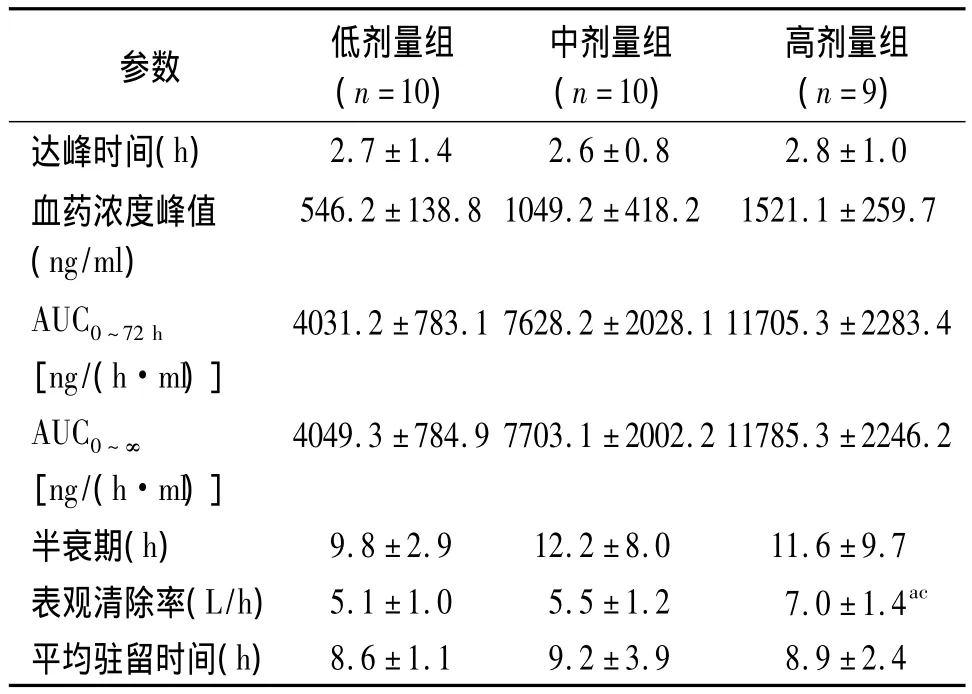
表1 3个剂量组健康受试者口服奥美沙坦酯片后主要药代动力学参数(±s)
注:AUC为曲线下面积;低剂量组为单剂量口服奥美沙坦酯片20 mg/d,中剂量组为40 mg/d,高剂量组为80 mg/d;与低剂量组比较,aP<0.05,与中剂量组比较,cP<0.05
参数 低剂量组(n=10)中剂量组(n=10)高剂量组(n=9)2.7 ±1.4 2.6 ±0.8 2.8 ±1.0血药浓度峰值(ng/ml)达峰时间(h)546.2 ±138.8 1049.2 ±418.2 1521.1 ±259.7 AUC0~72 h[ng/(h·ml)]4031.2 ±783.1 7628.2 ±2028.1 11705.3 ±2283.4 AUC0~∞[ng/(h·ml)]4049.3 ±784.9 7703.1 ±2002.2 11785.3 ±2246.2 8.6 ±1.1 9.2 ±3.9 8.9 ±2.4半衰期(h) 9.8 ±2.9 12.2 ±8.0 11.6 ±9.7表观清除率(L/h) 5.1 ±1.0 5.5 ±1.2 7.0 ±1.4ac平均驻留时间(h)
3 讨论
奥美沙坦酯设计为其活性代谢物——奥美沙坦的前体药物,母药经口服后可迅速转化为奥美沙坦,通过拮抗AT1受体,松弛血管平滑肌,发挥降压作用[12]。此外,奥美沙坦还能抑制血管紧张素转换酶活性,下调升高的血管紧张素Ⅱ水平,保护心血管系统重构[13]。近年来,有关奥美沙坦对糖尿病的疗效、高剂量下的治疗作用及与其他药物联合应用的临床研究也取得许多进展[14-15]。
研究表明,确切的降压效果和良好的药代动力学特性使奥美沙坦酯在临床广泛应用具有广阔的前景[14,16]。奥美沙坦酯的推荐起始剂量为 20 mg或更低,日最高剂量为40 mg/d,但部分临床试验中每日最大剂量可达80 mg[6-7]。本试验结果显示,健康受试者口服20~80 mg奥美沙坦酯后母药在体内迅速转化为活性代谢物——奥美沙坦,3个剂量组受试者体内过程均符合二房室模型。此外,健康人口服给药后奥美沙坦血药浓度平均2.7 h达峰值,平均消除t1/2约为11.2 h,Cmax和 AUC与剂量呈正相关,在20~80 mg剂量范围内表现出良好的线性关系。上述结果与国外研究结果相似[6-7],表明口服奥美沙坦酯的人体药代动力学的种族差异较小。从试验结果中还可发现,受试者口服奥美沙坦酯的主要药代动力学参数Cmax和AUC的变异较大,说明该药存在较大的个体差异,提示临床应用该药时宜监测血药浓度,针对不同个体制定适宜的临床用药方案。高剂量组 Cl/F值为(7.0±1.4)L/h,高于低、中剂量组,也可能与受试者的个体差异有关。
[1] 陈业泰,李东,李伟,等.中青年官兵高血压病患者的临床特征及其干预措施[J].空军医学杂志,2013,29(2):100-101.
[2] 王婷,罗丹,马红雨.飞行员高血压的危险因素分析研究[J].空军医学杂志,2012,28(2)70-71,75.
[3] Warner G T,Jarvis B.Olmesartan medoxomil[J].Drugs,2002,62(9):1345-1353.
[4] Brousil J A,Burke J M.Olmesartan medoxomil:an angiotensin Ⅱ-receptor blocker[J].Clin Ther,2003,25(4):1041-1055.
[5] Gardner S F,Franks A M.Olmesartan medoxomil:the seventh angiotensin receptor antagonist[J].Ann Pharmacother,2003,37(1):99-105.
[6] von Bergmann K,Laeis P,Puchler K,et al.Olmesartan medoxomil:influence of age,renal and hepatic function on the pharmacokinetics of olmesartan medoxomil[J].J Hypertens Suppl,2001,19(1):S33-S40.
[7] Schwocho L R,Masonson H N.Pharmacokinetics of CS-866,a new angiotensin II receptor blocker,in healthy subjects[J].J Clin Pharmacol,2001,41(5):515-527.
[8] 张小丽,于洋,侯艳宁,等.奥美沙坦酯胶囊的人体药动学及生物等效性[J].中国医院药学杂志,2007,27(5):622-624.
[9] 蒋娟娟,田蕾,黄一玲,等.奥美沙坦酯片人体生物等效性研究[J].中国新药杂志,2007,16(12):976-978,984.
[10] 杨武云,李珍,唐世新,等.奥美沙坦酯片在健康人体内的药动学[J].药学服务与研究,2009,9(5):367-369.
[11] 于洋,侯艳宁,刘建芳,等.固相萃取结合HPLC-MS法测定人血浆中奥美沙坦的药物质量浓度[J].中国药学杂志,2006,41(20):1592-1593,1600.
[12] Giles T D,Robinson T D.Effects of olmesartan medoxomil on systolic blood pressure and pulse pressure in the management of hypertension[J].Am J Hypertens,2004,17(8):690-695.
[13] Fernandes Santos C,de Souza Mendonca L,Mandarim de Lacerda C A.Favorable cardiac and aortic remodeling in olmesartan-treated spontaneously hypertensive rats[J].Heart Vessels,2009,24(3):219-227.
[14] Destro M,Preti P,D'Ospina A,et al.Olmesartan medoxomil:recent clinical and experimental acquisitions[J].Expert Opin Drug Metab Toxicol,2009,5(9):1149-1157.
[15] Deeks E D.Olmesartan medoxomil/amlodipine/hydrochlorothiazide fixed-dose combination in hypertension[J].Drugs,2011,71(2):209-220.
[16] El Gamal M I,Anbar H S,Chung H J,et al.Discovery of olmesartan hexetil:a new potential prodrug of olmesartan[J].Bioorg Med Chem Lett,2013,23(5):1347-1350.
