柠檬精油的化学成分分析及其抗氧化活性研究
2014-09-11侯小桢邓其海邹利运
秦 轶 侯小桢 章 斌 邓其海 丁 心 邹利运
(1.广东中兴绿丰发展有限公司,广东 河源 517000;2.韩山师范学院生物学系,广东 潮州 521041)
柠檬是芸香科柑橘属水果,在全球范围内均有栽培;其果肉富含VC和矿物质,有极佳的食疗功效,如预防糖尿病、风湿性关节炎等[1]。近年来,中国柠檬种植面积不断扩大,产量逐渐增加,市售的柠檬制品种类也日益丰富,包括有柠檬果酒、柠檬果醋、柠檬干片等[2-4]。柠檬加工过程产生的皮渣等废弃物,富含挥发性精油、果胶、色素、黄酮类化合物等功能性成分[1,5],如对其加以高值化综合开发与利用,在减小对污染环境的同时,也可获得良好的经济效益。
植物精油是重要的植物源次生代谢物,是从植物的果皮、花、叶、茎、根、全草或果实等部位提取的一种挥发性油状液体物质;具有独特的清香和天然、安全无毒等特点[6],且含具有抗氧化、抑菌等性能的生理活性成分,应用前景十分广阔。目前,有关柠檬精油的研究[7-10]多见于提取与组分检测等方面;本研究拟采用冷压法从柠檬果皮中提取精油物质并检测其化学组成;同时对其在油脂抗氧化与清除自由基方面的性能进行研究,旨在为柠檬精油的应用提供参考。
1 材料与方法
1.1 材料与设备
柠檬果皮精油(LEO):采用冷压法提取,广东中兴绿丰发展有限公司;
花生油、猪油:市售。
对氨基苯磺酸、盐酸萘乙二胺、柠檬酸钠、盐酸、亚硝酸钠、硫酸钠、无水乙醇、乙醚、氯仿、冰乙酸、碘化钾:分析纯,广州化学试验厂;
可溶性淀粉、二甲胺、碳酸钠、α-萘胺、硫代硫酸钠、酚酞、柠檬酸、磷酸氢二钠、氢氧化钠、过氧化氢:分析纯,广东西陇化工有限公司;
BHT、VC、VE、PG、TBHQ:食品级,河北百味生物科技有限公司;
气质联用仪:TRACE GC-MS型,美国Finnigan公司;
紫外可见分光光度计:UFJ-7200型,上海尤尼科仪器有限公司;
冷压榨离心分离机:HH-2型,上海精科实业有限公司;
pH计:PHS-3C型,上海雷磁仪器厂;
电热恒温水浴锅:HH-2型,常州华普达教学仪器有限公司;
紫外分析仪:WFH-203型,上海精科实业有限公司;
旋转蒸发仪:RE-52型,上海亚荣生化仪器厂;
电子分析天平:AUW120型,日本岛津公司。
1.2 试验方法
1.2.1 GC—MS检测分析条件
(1)色谱条件[11]:色谱柱为 DB-1(30m×0.25mm,0.25μm),载气为高纯氦气(99.999%),流速为1mL/min,分流比为40∶1,进样口温度220℃,进样量0.1μL。柱温从50℃以3℃/min升温至220℃,保持2min。
(2)质谱条件[11]:传输线温度220 ℃,EI离子源,电子能量70eV,离子源温度230℃,m/z 扫面范围29~400amu。
1.2.2 超氧阴离子(O-2·)生成抑制能力的测定 用乙醇配制2,4,6,8,10mg/mL的柠檬精油、TBHQ溶液、VC溶液各5mL为样品溶液。取0.05mol/L的 Tris—HCl(pH=8.2)缓冲液3mL于试管中,(25±0.5)℃水浴平衡20min后,加入0.1mL上述配制好的各浓度样品液,然后立即加入7mmol/L的邻苯三酚0.3mL,振荡使之充分反应4min后,加入10mol/L HCl 1mL终止反应,在420nm 处测定吸光度(A1),平行测定3次,按式(1)计算抑制率[12]:
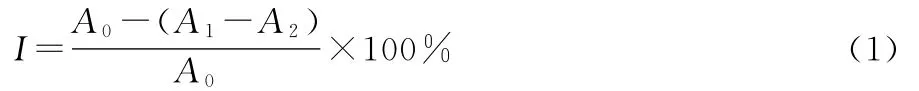
式中:
I——抑制率,%;
A0——以0.1mL蒸馏水代替样品液的吸光度;
A1——样品组的吸光度;
A2——用0.3mL蒸馏水代替邻苯三酚的吸光度。
1.2.3 OH·自由基清除能力的测定 在一系列50mL容量瓶中加入0.4mmol/L结晶紫溶液1.5mL、1.0mmol/L的FeSO4溶液2.0mL、2.0mmol/L的 H2O2溶液1.0mL,调pH 4.0,定容并静置30min,580nm处测吸光度;同时测定不加H2O2时的吸光度,及在上述反应体系中加H2O2之前加入LEO溶液和VC溶液的吸光度,按式(2)计算羟自由基清除率[13,14]:

式中:
R1——羟自由基清除率,%;
A——加H2O2溶液所测的吸光度;
A0——不加H2O2时所测的吸光度;
A1——加H2O2之前加VC和LEO反应液的吸光值。
1.2.4 食用油脂过氧化值(POV)和酸价值(AV)的测定
分别取0.02%BHT、0.02%PG和0.02%LEO各加入50.00g猪油和50.00g花生油,搅拌均匀,置于60℃电热恒温烘箱,每24h交换其在烘箱中的位置,并做空白对照试验,每隔2d取样测定过氧化值和酸价;测定和计算方法按GB/T 5538—2005《动植物油脂过氧化值测定》和 GB/T 5009.37—2003《食用植物油卫生标准的分析方法》的规定进行。
1.2.5 对NaNO2清除率和亚硝胺阻断率的测定
(1)NaNO2标 准 曲 线 的 绘 制[15]:分 别 准 确 吸 取5μg/mL亚硝酸钠标准液 0.00,0.20,0.40,0.60,0.80,1.00,1.50,2.00,2.50mL 于50mL 比 色 管,加 入2mL 0.4%对氨基苯磺酸溶液,混匀,静置3~5min后,加入1mL 0.2%盐酸萘乙胺溶液,用水稀释至刻度,摇匀,静置15min后,于波长540nm处测吸光度;同时以蒸馏水为空白,绘制标准曲线,得标准曲线的回归方程y=0.008 7x-0.000 6。
(2)对 NaNO2清除率的测定[15]:将0.5mol/L的柠檬酸钠—盐酸缓冲液(pH 3.0)5.0mL置于10mL容量瓶中,加入100mg/kg的NaNO2溶液1mL,再分别加入一定量的VE、VC和LEO,定容至刻度,37℃下反应1h。取1mL反应液于50mL容量瓶中,加入0.4%对氨基苯磺酸溶液2mL,0.2%盐酸萘乙胺溶液1mL,摇匀放置15min后,以蒸馏水为参比液,于540nm处测吸光度值,依据标准曲线,按式(3)计算NaNO2清除率。

式中:
R2——NaNO2清除率,%;
A0——不加 VE、VC、LEO的空白试验的吸光值;
Ax——不同用量 VE、VC、LEO的反应液的吸光值。
(3)对亚硝胺阻断率的测定[15]:量取1%VE、1%VC和1%LEO 溶液各0.1,0.2,0.3,0.4,0.5,0.6,0.7,0.8mL 于25mL比色管中,加入pH 3.0的柠檬酸—磷酸氢二钠缓冲液10mL,1mmol/L NaNO2溶液1.0mL和1mmol/L 二甲胺溶液1.0mL,稀释至刻度并于37℃恒温水浴1h。然后吸取1.0mL上述反应液至50mL烧杯,加入0.5%Na2CO3溶液0.5mL,于紫外分析仪上照15min;取出后加入1%对氨基苯磺酸1.5mL,0.1% α-萘胺1.5mL和蒸馏水0.5mL,静置15min,525nm波长下测吸光度,同时测定以去离子水代替亚硝酸钠标液的空白试验吸光度,及以去离子水代替VE、VC和LEO的空白试验吸光度。按式(4)计算亚硝胺阻断率:
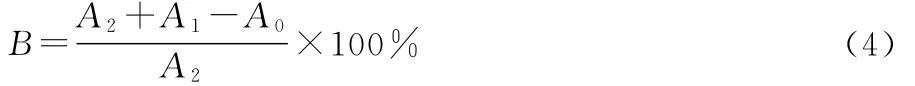
式中:
B——亚硝胺阻断率,%;
A0——空白试验的吸光值;
A1——以去离子水代替亚硝酸钠标液的空白试验吸光值;
A2——以去离子水代替VE、VC和LEO的空白试验吸光值。
2 结果与分析
2.1 柠檬果皮精油成分分析
按1.2.1条件经GC—MS分析采集图谱,得LEO挥发性成分色谱图见图1,分析鉴定出的LEO化学组分见表1。由表1可知,LEO中共有23种化合物被鉴定出,占精油总含量的95.43%,其中相对含量较高的组分主要为dl-柠檬烯(47.53%)、γ-萜品烯(11.19%)、α-蒎烯(5.38%)、α-松油醇(4.09%)、Z-柠檬醛(4.07%)、E-柠檬醛(3.99%)等。
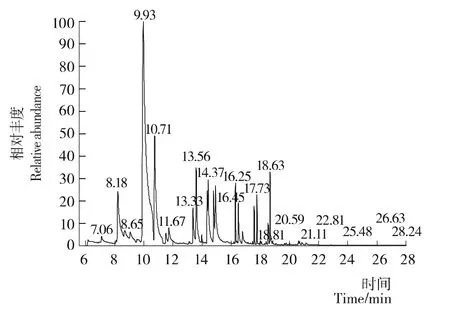
图1 LEO挥发性成分色谱图Figure 1 Chromatorgram map of volatile compounds of lemon peel essential oil
2.2 柠檬果皮精油的自由基清除效果
2.2.1 清除羟自由基(OH·)作用 羟基自由基具有极强的氧化能力,可破坏机体组织中的糖类、蛋白质、核酸等物质而引起氧化性损伤。VC具有较强的还原能力,可与OH·发生氧化还原反应而降低其危害;同时,LEO中的萜烯类化合物含有不饱和键,亦可被OH·氧化而对其起到一定的清除效用[16]。由图2可知,LEO和VC对OH·的清除效果均随其浓度增大而逐渐增强,且分别在0.4,0.3μg/mL时趋于平缓,清除率可分别高达95.14%和98.51%;同时,可能是由于LEO中所含的萜烯类化合物相对含量不高,以致LEO对OH·的清除效果在试验浓度下略低于同浓度的VC。
2.2.2 抑制超氧阴离子(O-2·)生成作用 抗氧化剂可通过基于H原子转移法(即抗氧化剂通过提供H原子淬灭自由基)和基于电子转移法(即抗氧化剂通过转移电子使自由基被还原)清除O-2·[17]。由图3可知,VC和LEO对O-2·的抑制效果均随浓度增大而逐渐增强,其中VC抑制作用的增幅相对较小,抑制率稳定在83%~89%;LEO在10mg/mL用量 下 的 抑 制 率 达 到 最 大 ,为6 1.3 5% 。对 比 明 显 的 是TBHQ的抑制率随其浓度增大而呈下降趋势(这与陈莹[17]的研究结论一致),且逐渐与LEO的清除作用接近;造成这一结果的可能原因是由于TBHQ主要是通过4位羟基给O-2·自由基提供氢原子而达到清除效果,但具体作用机制仍需进一步探讨。

表1 冷压法所提LEO的挥发性成分Table 1 Volatile components of LEO extracted by cold-pressing method
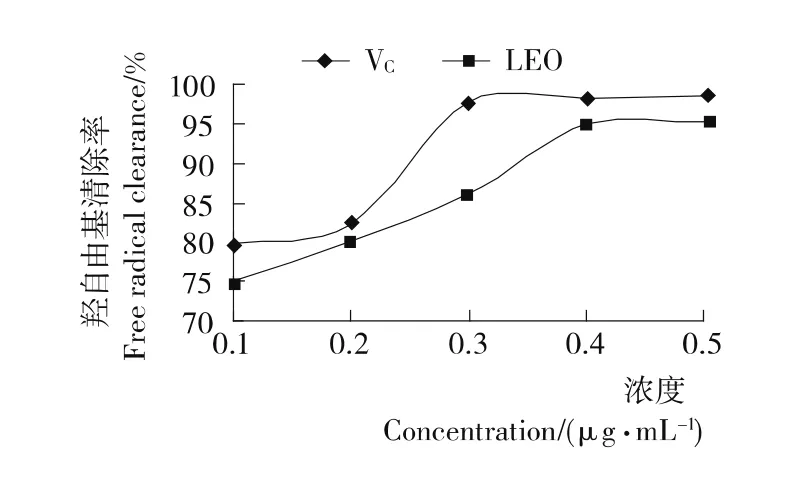
图2 VC和LEO清除·OH能力Figure 2 Ability of VCand LEO to remove·OH
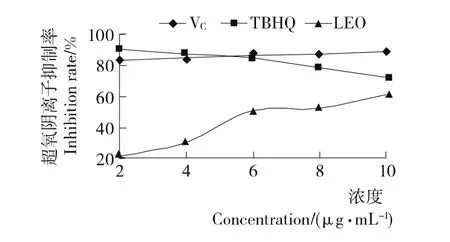
图3 VC、TBHQ和LEO清除O-2·能力Figure 3 Ability of VC,TBHQ and LEO to remove O-2·
2.3 对食用油脂的抗氧化作用
由图4和图5可知,LEO对食用油脂有一定的抗氧化效果,且总体的抗氧化能力较BHT和PG差。LEO对油脂的抗氧化效果有两方面的综合作用:①LEO含有的萜烯类化合物可消耗部分氧而减缓油脂的氧化进程[18,19];②LEO在60℃高温下因逐渐挥发,导致其抗氧化能力迅速下降;且LEO在高温作用下可部分水解产生游离脂肪酸,使油脂体系中的总游离脂肪酸含量较其它试验组略高,一定程度上加快了总油脂体系的氧化进程[18,19]。
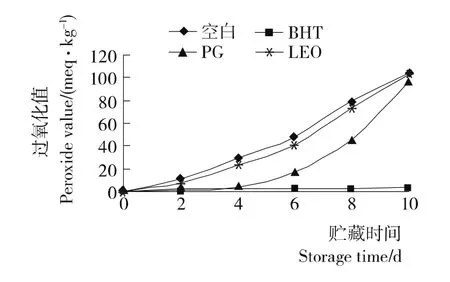
图4 猪油在不同抗氧化剂作用下的POV值Figure 4 POV of lard under different antioxidants
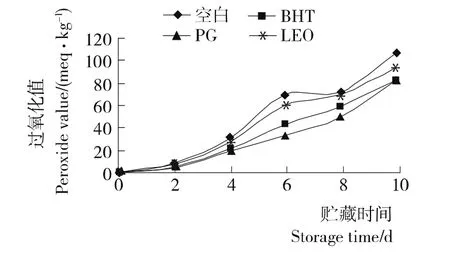
图5 花生油在不同抗氧化剂作用下的POV值Figure 5 POV of peanut oil under different antioxidants
2.4 清除NaNO2和阻断亚硝胺生成的作用
2.4.1 对NaNO2的清除作用 亚硝酸钠是肉制品加工中的常用发色剂,过量使用会引起食物中毒;还可在肠胃中与胺结合成强致癌物质亚硝胺[20]。其分子中—NO2基团所含的N为中间化合态,既具氧化性也有还原性;VC等抗氧化剂有较强的供氢活性,可将亚硝酸盐分子中—NO2基团所含的N还原为—NH+4,以达到清除效果降低其潜在毒性危害[21]。
由图6可知,VE、VC和LEO对亚硝酸钠均有明显的清除作用,且清除率均随其用量增加而迅速增大,当用量超过0.1g/mL时,三者的清除效果趋于平缓上升;LEO用量增至0.7g/mL时,对亚硝酸钠的清除效果与VE、VC接近,达87.50%。
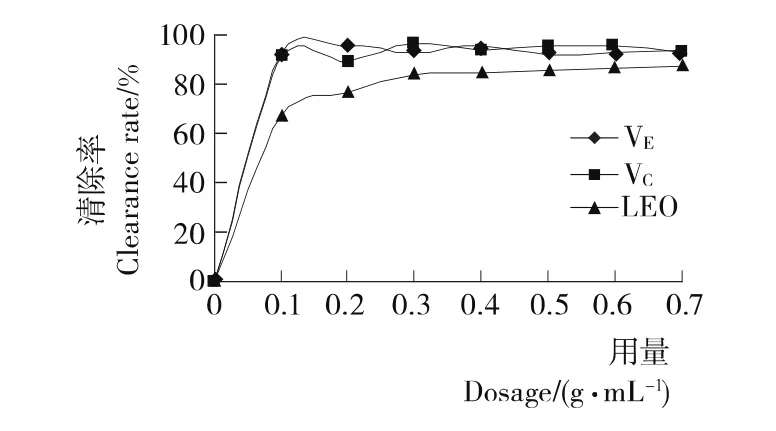
图6 VE、VC和LEO清除NaNO2效果Figure 6 Effect of VE,VC,LEO to remove NaNO2
2.4.2 对亚硝胺生成的阻断作用 亚硝胺是一类广泛存在于啤酒和熏腊食品中的化学污染物,可引起强烈的致癌、致畸和致突变作用;VC等抗氧化活性物质可与胺竞争性结合亚硝酸盐,从而阻断亚硝胺的产生[20]。由图7可知,VE、VC和LEO对亚硝胺的阻断作用呈随用量增大而增强的剂量—效应关系,且LEO的阻断效果明显低于VE与VC;在试验浓度范围内,LEO的最大阻断率可达56.91%。
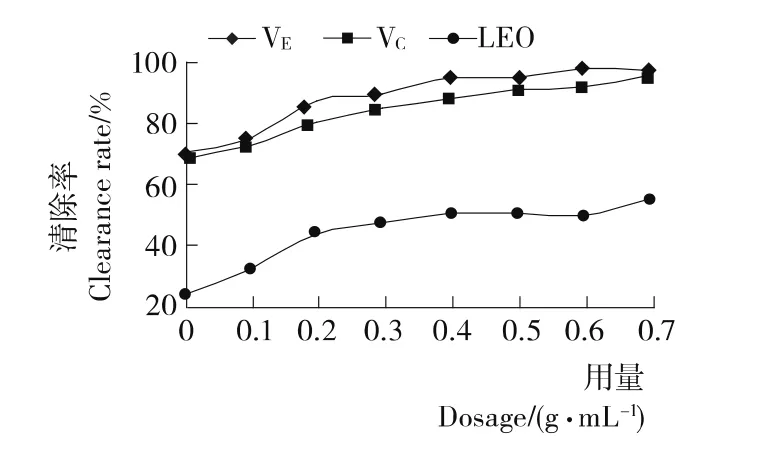
图7 VE、VC和LEO阻断亚硝胺效果Figure 7 Effect of VE,VC,LEO to block nitrosamine
3 结论
(1)柠檬果皮精油中共有23种化合物被鉴定出,占精油总含量的95.43%;含量较高的主要组分为dl-柠檬烯(47.53%)、γ-萜品烯(11.19%)、α-蒎烯(5.38%)、α-松油醇(4.09%)、Z-柠檬醛(4.07%)和 E-柠檬醛(3.99%)等。精油得率及其化学组成受提取方法等因素影响而有一定差异,为进一步优选柠檬精油提取的工艺条件与合理利用其香气资源,后续需继续开展冷压法与其它提取方法对精油化学成分影响的比较研究。
(2)合成抗氧化剂具有潜在毒性作用,开发理化性质稳定、已成行业发展趋势。因此,对清除OH·和O-2·自由基及延缓油脂货架期有较好抗氧化作用的柠檬精油不失为良好的来源之一。
(3)亚硝酸盐是肉制品加工中常用的发色剂,但过量使用可引起人体的致癌、致畸等毒性危害;如何降低其在肉制品中的残留量和寻求等效的替代物已成为行业普遍关心的热点问题。LEO对亚硝酸钠清除作用(清除率可达87.50%,远高于芹菜籽精油[22]、芫荽茎叶精油[23]和佛手柑精油[24]等)和亚硝胺阻断作用(清除率可达56.91%)的试验结果可为其在香肠等肉制品加工中的实际应用提供借鉴。
1 龚晓,张有捷,李赤翎,等.几种柑橘类水果功能性营养物质测定与比较分析[J].食品与机械,2012,28(2):36~39.
2 谢林,张泗淮,王平先.柠檬酒的研制[J].酿酒科技,2002(2):94.
3 王毅,刘学文,伍学明,等.柠檬果醋醋酸发酵工艺的研究[J].食品研究与开发,2011,32(1):75~78.
4 范兰娣.冻干柠檬片生产工艺的研究[J].食品科技,2009,34(5):54~56.
5 付复华,李忠海,单杨,等.柑橘皮渣综合利用技术研究进展[J].食品与机械,2009,25(5):178~184.
6 章斌,秦轶,邓其海,等.柠檬果皮精油的应用研究进展[J].食品研究与开发,2013,34(21):119~122.
7 A Verzera,P Dugo,L Mondello,et al.Extraction technology and lemon oil composition[J].Italian Journal of Food Science,1999,11(4):361~370.
8 Yoshiaki Miyake,Masanori Hiramitsu.Isolation and extraction of antimicrobial substances against oral bacteria from lemon peel[J].Journal of Food Science and Technology,2011,48(5):635~639.
9 Fausto Gironi,Marco Maschietti.Continuous countercurrent deterpenation of lemon essential oil by means of supercritical carbon dioxide:Experimental data and process modelling[J].Chemical Engineering Science,2008,63(3):651~661.
10 廖玉琴,包清彬,李松柏,等.柠檬精油提取工艺的优化及其GC—MS分析[J].食品与机械,2012,28(1):186~189.
11 赵文红,黄桂颖,陈悦娇,等.柠檬果皮精油挥发性成分的GC—MS分析[J].食品工业科技,2009,30(12):113~115.
12 刘婷,厍文波,王婷,等.水蒸气蒸馏和超临界萃取薰衣草精油抗氧化作用研究[J].时珍国医国药,2009,20(12):3 035~3 037.
13 林燕如,丁利君.番石榴叶中黄酮类物质提取及其抗氧化性研究[J].现代食品科技,2007,23(10):58~61.
14 索金玲,彭秧,张纵圆,等.石榴叶总黄酮提取工艺及体外抗氧化性研究[J].生物技术,2009,19(1):63~65.
15 梁英岳,傅亮,孙颖莺,等.模拟胃液条件下红豆多肽清除亚硝酸盐及阻断亚硝胺合成的研究[J].食品与发酵工业,2010,36(4):40~44.
16 谢田伟.枇杷花黄酮与精油的提取及其性质分析研究[D].福建:集美大学,2012.
17 陈莹.抗氧化剂的抗氧化活性评价方法研究[D].江苏:江南大学,2012.
18 侯滨滨,李悦.柑橘类精油对食用油脂的抗氧化研究[J].食品研究与开发,2010,31(11):234~236.
19 张薇薇.高压电场和抗氧化剂处理对油脂抗氧化作用效果评价[D].山西:山西农业大学,2013.
20 赵二劳,王晓妮,张海容,等.山楂清除亚硝酸盐及阻断亚硝胺合成的研究[J].食品与发酵工业,2006,32(10):29~31.
21 黄苇,李远志,赵玲华,等.消除梅菜中亚硝酸盐的方法研究[J].中国调味品,2003(6):22~25.
22 陆占国,张怀涛,李伟.芹菜籽精油成分以及清除亚硝酸钠作用研究[J].化学与黏合,2008,30(6):38~40.
23 陆占国,郭红转,李伟.索氏法提取芫荽茎叶精油和成分解析以及清除亚硝酸钠作用[J].食品科学,2007,28(5):29~32.
24 章斌,侯小桢,饶强,等.佛手精油的超声提取及清除亚硝酸钠作用研究[J].食品研究与开发,2011,32(12):43~47.
