体部伽玛刀图像引导技术的发展
2014-06-24付东山黎维娟
付东山,黎维娟
江苏瑞尔医疗科技有限公司,江苏 无锡 214109
体部伽玛刀图像引导技术的发展
付东山,黎维娟
江苏瑞尔医疗科技有限公司,江苏 无锡 214109
体部立体定向放射治疗(SBRT)是立体定向放射外科(SRS)技术和临床应用的自然延伸,是一种在精确图像引导下的大剂量低分次的放射治疗方法。体部伽玛刀是中国自主研发的创新放疗设备,把伽玛射束治疗从头部延伸至体部。在近15年的技术发展和临床实践中,体部伽玛刀沿用了传统的体部框架定位模式,由于缺少足够定位精度,限制了其作为SBRT设备在临床上的广泛使用。近年来,图像引导定位技术开始应用于体部伽玛刀,将为体部伽玛刀SBRT规范治疗开启崭新一页。本文介绍了体部伽玛刀图像引导定位的原理、方法、试验和初步应用。
体部伽玛刀;图像引导放射治疗;体部立体定向放射治疗;立体定向放射外科;锥形束CT;X射线立体平面成像;二维-三维图像配准
0 前言
图像引导放射治疗(Image Guided Radiation Therapy, IGRT)是近十几年来逐步发展起来的肿瘤放射治疗新技术[1],它通过先进的影像设备及图像处理方法对患者靶区在治疗前进行精确定位、在治疗中进行实时定位跟踪,实现对肿瘤的精确放射治疗,降低对肿瘤周边正常组织及关键器官的损伤。图像引导技术是现代新兴精确放射治疗的基石,如立体定向放射外科(SRS)、体部立体定向放射治疗(SBRT)以及图像引导调强放疗(IG-IMRT)。
ASTRO和ACR对SBRT定义为以单次或少次对体部靶区进行非常精确的高剂量投射[2]。AAPM TG 101报告也描述了SBRT区别于其它治疗方法的主要特点[3]:高剂量(每次6~30 Gy),低分次(1~5次),毫米级边缘,精确定位。不论采用何种影像定位技术,kV级或MV级(EPID)的X射线平面成像,kV级或MV级的CT成像,SBRT和SRS对定位精度的要求一样严格,剩余摆位误差应≤1 mm[4]。随着IGRT技术不断进步,SBRT得到了越来越普遍的临床实践,大量临床数据肯定了SBRT在肺、肝、肾、胰腺、前列腺和脊椎肿瘤的治疗效果[5]。然而SBRT是一种仍在发展中的治疗方法,现有临床研究多集中在肺部肿瘤,还需更多适应症的临床实践和更丰富的临床证据,来证明SBRT相比其他方法的理论优势[6]。为了避免低分次大剂量可能出现的临床风险,医务人员要接受特殊SBRT临床操作流程培训,医学物理师要严格把关,实施质量保证[7]。
早期SRS头部伽玛刀源于1951年瑞典神经外科专家Leksell提出的立体定向放射治疗的设想,采用立体定向定位装置和多源射束准直聚焦,单分次将非常大的适形剂量投放到定义好的病变靶区[8-9]。斯坦福大学神经外科医生Adler教授,从头部伽玛刀的临床优势和缺陷中获得启发,创立了无立体定位框架SRS概念,并在90年代成功研发了CyberKnife系统(Accuray Inc., Sunnyvale, CA)[10-11]。CyberKnife结合图像引导、现代机器人和小型化直线加速器技术,实现了精确图像引导下的SRS,可低分次(1~5)治疗不同大小的肿瘤。早期CyberKnife只适用于头颈部各种肿瘤治疗,随着脊椎影像定位跟踪技术的发展,其临床应用延伸到脊椎肿瘤治疗[12],进而成为全身神经放射外科手术系统。伴随着体部肿瘤影像定位及呼吸运动跟踪技术的进一步成熟和成功应用,临床应用范围扩展到肺、肝、胰腺、前列腺等体部肿瘤治疗,实现了从头部SRS到体部SBRT的自然发展,从而实现了全身SBRT[13],。另一个全身SRS、SBRT系统Novalis(BrainLAB Inc. Feldkirchen, Germany),在2001开始应用于头部和脊椎肿瘤治疗[14-15],已得到广泛临床应用。CyberKnife和Novalis不仅能实施治疗分次间(interfraction)定位,还可在治疗中(intrafraction)对靶区运动进行定位跟踪,提供整个治疗过程中的靶区位置精度。CyberKnife和Novalis具备很强的图像引导和实时运动跟踪功能,是非常有效的SBRT治疗设备,是SBRT技术发展和临床实践的先驱。
在Leksell发明的静态头部伽玛刀技术基础上,经过学习、消化、局部创新,我国于1995年自主研发设计了第一台旋转式头部伽玛刀,又进一步开展了体部伽玛刀的技术研究,并于1998年成功研发了第一台多源旋转聚焦式OUR-QGD型体部伽玛刀[16],随后又研发了多种型号体部伽玛刀,并相继投入临床使用。体部伽玛刀治疗采用了传统的体部框架定位方式,难以严格控制和保证定位精度。精度的不确定性,极大地限制了体部伽玛刀适应症的范围,也给治疗剂量和分次的规划带来了难度。体部伽玛刀作为一种SBRT设备,要能实施符合SBRT要求和规范的治疗,精确图像引导定位是必不可缺的[2-3]。图像引导定位替代或结合体部框架定位,是大部分体部伽玛刀放疗医生和物理师长期以来所期待的。近年来,我国借鉴国际上IGRT技术发展经验,开展了适合于体部伽玛刀的图像引导定位技术研发,目前已与两种型号体部伽玛刀结合使用,并开始进入临床试验。本文将介绍此项图像引导放疗定位系统的技术原理、实施方法、试验结果。
1 图像引导定位技术比较
放疗图像引导技术主要包括kV级锥形束CT(CBCT)、MV级螺旋CT、kV级X射线立体平面成像、EPID、Ultrasound、MRI。而两种主流技术是CBCT三维成像和X射线立体平面成像。CBCT技术应用于Varian和Elekta生产的系列IGRT机型,如RapidArc、TrueBeam、Synergy、VMAT;而X射线立体平面成像技术应用于CyberKnife和Novalis系统。
CBCT技术采用由X线源和平板探测器组成的机载X线成像设备,绕加速器机架中心点旋转一圈或一定弧度,在不同旋转角度产生锥形线束、采集二维透视图像,通过对多个二维图像的快速三维重建得到CBCT图像。然后,利用CBCT图像与治疗计划CT图像的三维-三维(3D-3D)图像配准,得到患者或靶区的位置偏移。通过移动治疗床来调整病人位置,达到治疗前精确定位的目的。其优点:三维图像可提供更全面的体内解剖结构信息;可对部分软组织进行直接图像配准定位,并且必要时可进行非刚性图像配准;根据每分次CBCT,观察判断肿瘤大小变化,如发现肿瘤大小发生变化,可对后续分次治疗做适当的计划调整。缺点:成像剂量大,单次成像剂量是X射线立体平面成像技术的近2个数量级[17];定位过程所需时间较长,需数分钟;定位后无法再做另一次CBCT验证剩余摆位误差,在必要时需要辅助定位系统作最后位置验证;无法在治疗中对病人位置变化和肿瘤运动移位进行验证。
X射线立体平面成像技术采用kV级X射线交角透视成像,对患者的内部解剖结构或外部植入金属标记进行两个方向的透视成像,取得两个二维透视图像,利用两个二维透视图像和治疗计划CT图像的二维-三维(2D-3D)图像配准,计算出患者或靶区的位置偏移,由此在治疗前通过移动治疗床来调整患者摆位。然后可多次重复上述定位过程,校正、验证剩余摆位误差,直到最终剩余摆位误差达到要求。优点:单次成像剂量一般<5 mGy,远小于CBCT成像剂量[17];定位时间较短,单次定位只需数十秒钟,整个定位过程一般只需1~2 min;每个分次可进行多次位置校正、验证,保证最后剩余摆位误差达到临床要求;在治疗过程中,可不断地验证病人位置移动,如果结合红外呼气运动跟踪技术,则能实时地定位跟踪胸腹部肿瘤运动。缺点:二维透视成像只提供了有限的体内解剖结构信息,在图像上较难分辨软组织和靶区;2D-3D图像配准一般利用骨骼解剖标记或外部植入的金属标记。
X射线立体平面成像和CBCT都可提供6个自由度的定位结果,包括3个平移和3个转角,比较两种不同方法的定位精度是必要的。NovalisTx系统同时结合了两套图像引导系统:BrainLAB的X射线立体平面成像定位系统ExacTrac和Varian的CBCT定位系统OBI,为精度比较研究提供了一个理想平台。Ma J对头部人体模型以及18例颅内肿瘤患者进行了定位精度比较研究[18],比较两种方法定位所获得的剩余摆位误差的差别,用平方根均差RMS表示,人体模型比较结果:平移RMS<0.5 mm,转角RMS<0.2°;患者比较结果:平移RMS<1.5 mm,转角RMS<1.0°。Chang Z对脊椎人体模型以及16例脊椎肿瘤患者进行了类似研究[19],人体模型比较:平移RMS<1.0 mm,转角RMS<1.0°;患者比较:平移RMS<2.0 mm,转角RMS<1.5°。上述比较研究可发现,ExacTrac与CBCT有可比较的定位精度。
采用X射线立体平面成像定位技术的CyberKnife系统针对不同部位肿瘤,设计了不同定位跟踪方法,6D Skull Tracking System、Xsight Spine Tracking System、Xsight Lung Tracking System、Fiducial Tracking System分别适用于头部、脊椎、肺部和其他部位。通过人体模型对各种方法的精度研究表明[20-23],定位精度:平移RMS<0.5 mm,转角RMS<0.5°;通过人体模型胶片测试的整机系统靶点精度<1.0 mm。Fürweger C采集了用Xsight Spine Tracking System连续单次治疗260例脊椎病人数据,研究剩余摆位误差及治疗中不断验证的靶区位置,结果显示:在95%情况下,靶区位置精度<1 mm[24]。CyberKnife图像引导定位跟踪系统,具有满足SRS和SBRT治疗对高精度的要求。2008年Sahgal A对4种IGRT设备( CyberKnife、Novalis,、TomoTherapyHiArt和Elekta Synergy)用于脊椎SBRT治疗的精度进行了分析比较:发现CyberKnife具有最好的interfraction和intrafraction定位跟踪精度[25]。
综上所述,X射线立体平面成像是一种很有效的IGRT定位技术,具有以下特点:① 精度高;② 成像剂量低;③定位时间短;④ 能进行治疗前病人定位和治疗中靶区运动跟踪。另外,现代的质子/重离子加速器放疗设备也普遍采用了立体平面成像定位技术,作为其严格控制靶点精度的重要手段[26]。
2 体部伽玛刀图像引导技术及其应用
2.1 原理和方法
X射线立体平面成像技术的核心是2D-3D图像配准。在IGRT、图像引导外科手术(Image-Guided Surgery, IGS)和图像引导微创治疗(Image-Guided Minimally Invasive Therapy, IGMIT )等技术领域,已有大量关于2D-3D图像配准方法的研究和应用。两个商业IGRT系统CyberKnife和Novalis的成功研发和广泛临床应用,使这种配准技术的研究达到了登峰造极的境界[27]。2D-3D图像配准利用在线获取的一个或两个二维X射线投影图像和之前产生的一个三维CT(或MRI)图像,根据图像相似性测量原理[28],找到病人体内靶区(Target)或体内感兴趣区(ROI)在两个不同时间的位置变化,首先根据具体临床应用的X射线成像系统几何尺寸,从三维CT获得数字重组透视图像(Digitally Reconstructed Radiograph, DRR),把2D-3D图像配准转化为X射线图像与DRR的二维-二维(2D-2D)图像配准。通过复杂的图像处理和配准算法,计算两个投影面上的二维配准结果,然后经过二维到三维几何转换,得到在病人三维坐标系上6个自由度的配准结果,即3个方向平移和3个方向转角。
本文介绍的图像引导定位系统(Image-Guided Positioning System, IGPS)采用X射线立体平面成像技术。系统结构和成像设备组成如图1所示,通过由计算机软件控制两组由kV级X射线管、高压发生器、非晶硅平板探测器和曝光控制器组成的成像系统,对患者的内部解剖结构或外部植入金属标记进行两个方向的X射线透视投影,实时地采集一对X射线透视图像。IGPS软件系统组成如图2所示,数据库接受由放疗系统TPS通过Ethernet传输的病人DICOM数据,包括CT图像和定位参考点;计划软件处理CT图像,生成DRR图像,选择图像配准ROI;定位软件生成DRR图像库,控制成像设备实时采集X射线图像,进行2D-3D图像配准,计算病人位置偏移,输出定位结果(3个平移和3个转角),并传输给放疗系统控制台。
用一个盆腔肿瘤病人定位过程中采集的图像作为例子,图3描述了图像配准的流程和结果。TPS根据靶区位置定义了图像配准参考点,IGPS定义以配准参考点为中心的图像配准ROI,同时生成以配准参考点为中心的DRR图像。IGPS采集到X射线图像后,对左右投影图像进行独立的2D-2D图像配准,用DRR上的ROI(黄色)作为配准参考区域,在X射线图像中找到相应的被配准ROI(紫色)。被配准ROI相对于配准参考ROI的位置偏移,即为图像配准结果,被配准ROI相对于配准参考ROI的位置显示在X射线图像上。根据配准结果,校正X射线图像位置,并与DRR图像重叠,可用分割方块目视检查图像配准的准确性。

图1 IGPS系统成像结构和设备组成
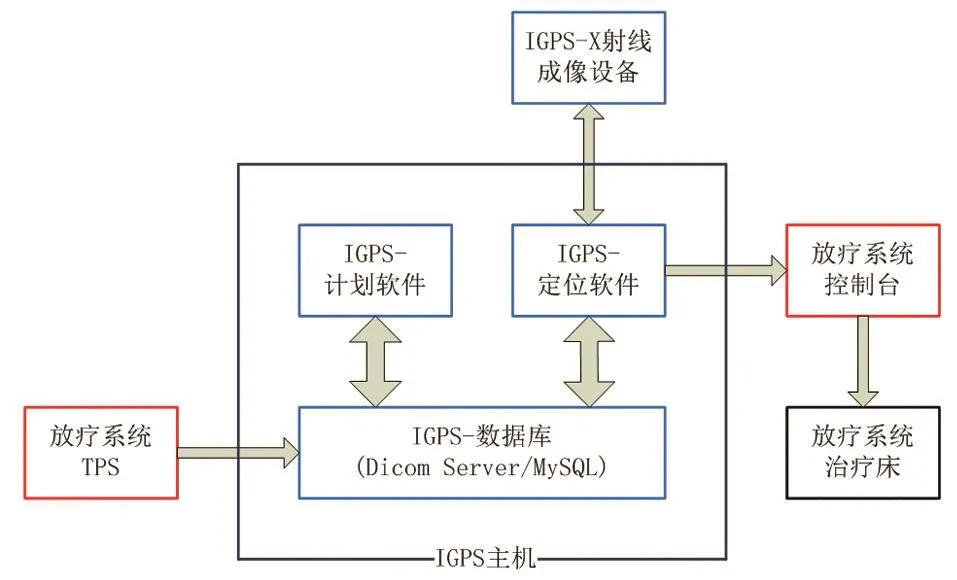
图2 IGPS软件系统组成
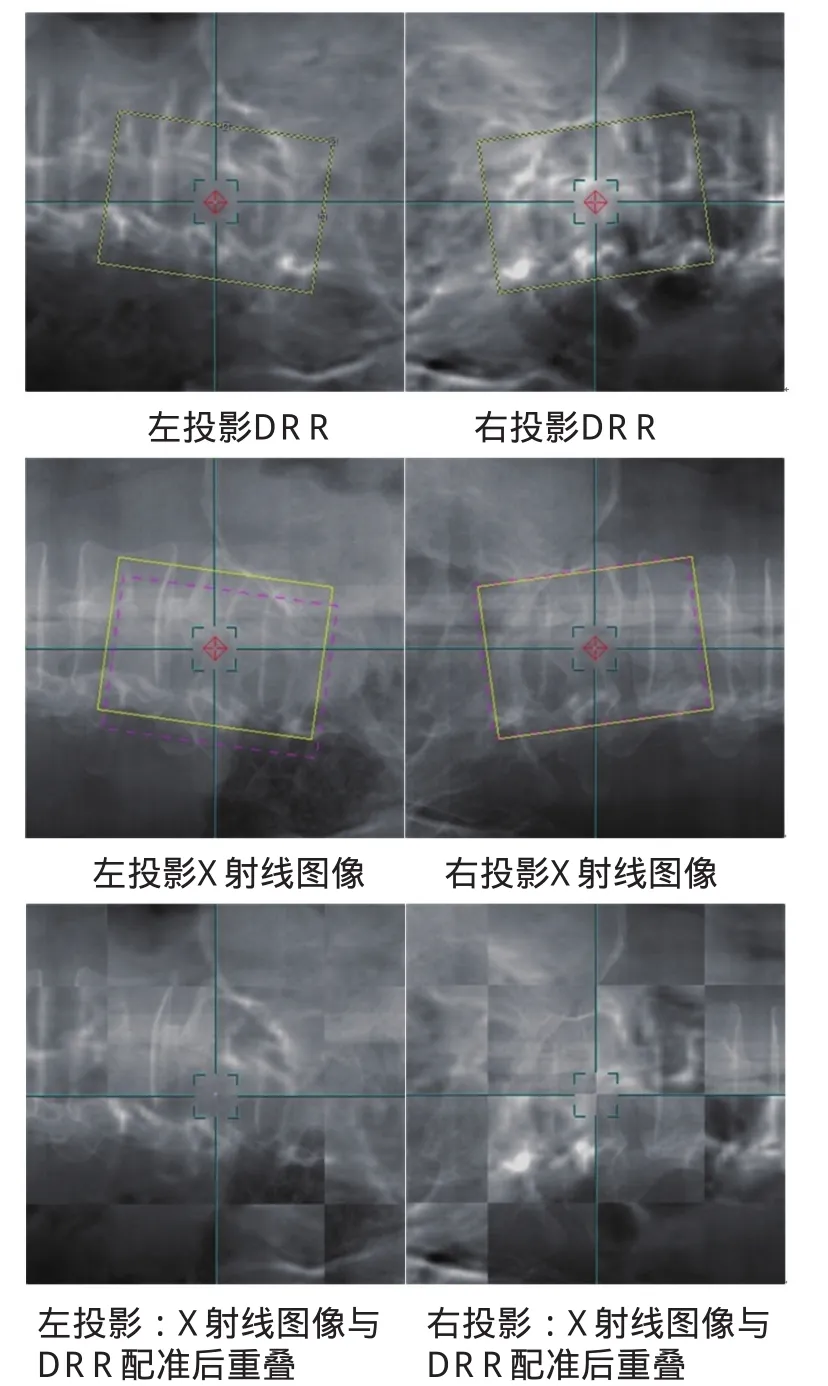
图3 图像配准的过程和结果
2.2 与体部伽玛刀系统结合
根据不同类型体部伽玛刀的机械结构特点,可选择IGPS成像几何,优化IGPS与伽玛刀系统的结合。IGPS首先实现了与深圳市海博科技有限公司研发生产的SGS-I+型体部伽玛刀的对接,见图4。由于SGS-I+自身机械结构的特点,其内部无足够空间容纳IGPS成像硬件,为此IGPS放置于伽玛刀机身外部前侧。两个X射线管固定在从伽玛刀机体前侧延伸出来的悬臂上,平板探测器安装固定于地面,形成对称的双投影交角成像几何,两X射束中心线交叉于定位中心点。IGPS在定位中心点完成病人定位,然后通过移动治疗床,把病人推进到治疗中心点,即伽玛刀聚焦中心点。
IGPS也实现了与深圳市奥沃医学新技术发展有限公司生产的OUR-QGD型体部伽玛的对接,见图5。OUR-QGD为开放式的机械结构,提供了足够内部空间安装成像设备。两个X射线管悬挂固定在从伽玛刀机体两侧延伸出来的机架上,两个平板探测器安装固定于地面,两X射束中心线交叉的定位中心点在伽玛刀聚焦中心点的正下方。在定位中心点完成病人定位后,向正上方移动治疗床,把病人移到治疗中心点位置。
结合后的图像引导体部伽玛刀系统(IGRT-GK),借助带仿真肿瘤的仿真人体模型,进行严格的系统校准和整机靶点精度测试。系统校准是精确测量IGPS定位中心点和伽玛刀聚焦中心点的实际空间距离,用人体模型胶片靶点精度测试方法来确定。在重复测试靶点精度的过程中,不断修正空间距离,直到靶点精度<1.0 mm。完成系统校准后,继续重复几次靶点精度测试,得到具有足够统计性的整机靶点精度。
2.3 初步试验结果
IGPS已安装在SGS-I+体部伽玛刀上,完成了系统对接和测试工作。人体模型精度测试结果显示:IGPS定位精度<0.5 mm,整机靶点精度<1.0 mm。临床使用后,采集并分析了10个病例数据,比较了体部框架定位和IGPS图像引导定位所得的剩余摆位误差。10个患者接受了SGS-I+体部伽玛刀7~10分次放射治疗,每个分次治疗前,先用体部框架定位,再用图像引导定位,记录剩余摆位误差,每个患者分次间剩余摆位误差是变化的,结果见图6。体部框架定位后的剩余摆位误差范围约10 mm,然而图像引导定位后的摆位误差远<1 mm,极大地提高了定位精度。
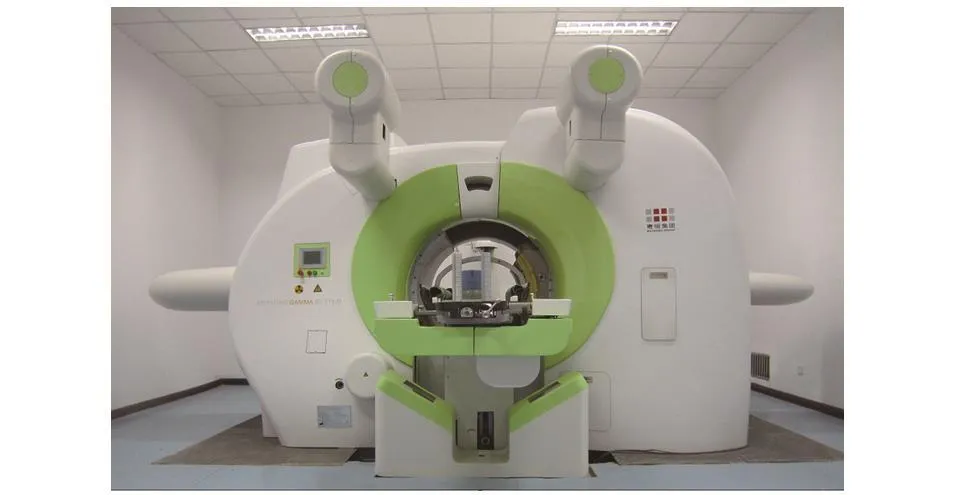
图4 IGPS与SGS-I+体部伽玛型刀的结合
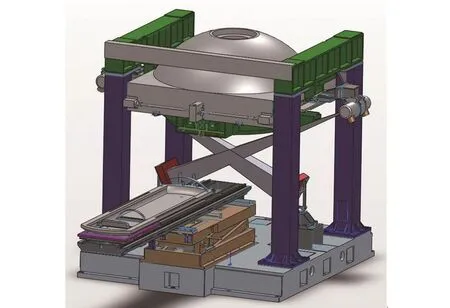
图5 IGPS与OUR-QGD型伽玛刀的结合

图6 剩余摆位误差比较
3 总结
图像引导技术是现代精确放射治疗的基石,在高精度保证下,SBRT大剂量低分次治疗才是安全有效的。基于X射线立体平面成像技术的IGPS,通过与SGS-I+体部伽玛刀的结合,形成图像引导体部伽玛刀。整机系统靶点精度好于1 mm,病人剩余摆位误差<1 mm,满足SBRT临床规范的要求,是一种很有潜力的SBRT设备。图像引导体部伽玛刀的成功研发和使用,解决了多年来用体部框架定位无精度保证带来的困惑,是国产体部伽玛刀技术发展的一个里程碑,将为其进一步推广使用起到积极作用。
[1] Xing L,Thorndyke B,Schreibmann E,et al.Overview of imageguided radiation therapy[J].Medical Dosimetry,2006,31(2):91-112.
[2] Potters L,Kavanagh B,Galvin JM,et al.American Society for Therapeutic Radiology and Oncology (ASTRO) and American College of Radiology (ACR) practice guideline for the performance of stereotactic body radiation therapy[J].Int J Radiat Oncol Biol Phys,2010,76:326-332.
[3] Benedick SH,Yenice KM,Followill D,et al.Stereotactic body radiation therapy:The report of AAPM Task Group 101[J]. Medical Physics,2010,37(8):4078-4101.
[4] Klein EE,Hanley J,Bayouth J,et al.Task Group 142 report: Quality assurance of medical accelerators[J].Medical Physics, 2009,36(9):4197-4212.
[5] Martin A,Gaya A.Stereotactic body radiotherapy: a review[J]. Clinical Oncology,2010,22(3):157-172.
[6] Tipton K,Launders JH,Inamdar R,et al.Stereotactic Body Radiation Therapy:Scope of the Literature[J].Annals of Internal Medicine,2011,154:737-745.
[7] Saw CB,Bao S,Li S.A review on the technical and dosimetric aspects of stereotactic body radiation therapy (SBRT) [J].Journal of Radiation Oncology,2012,1:317-322.
[8] Leksell L.The stereotactic method and radiosurgery of the brai[J]. ActaChir.Scand,1951,102:316-319.
[9] Leksell L.Stereotactic radiosurgery[J].Journal of Neurology, Neurosurgery & Psychiatry,1983,46:797-803.
[10] Adler JR Jr,Chang SD,Murphy MJ,et al.The Cyberknife:A Frameless Robotic System for Radiosurgery[J].Stereotactic Functional Neurosurgery,1997,69:1-4.
[11] Adler JR Jr,Murphy MJ,Chang SD,et al.Image-guided robotic radiosurgery[J].Neurosurgery,1999,44:1299-1307.
[12] Ryu SI,Chang SD,Kim DH,et al.Image-guided hypo-fractionated stereotactic radiosurgery to spinal lesions[J].Neurosurgery, 2001,49(4):838-846.
[13] Coste-ManièreÈ,Olender D,Kilby W,et al.Robotic whole body stereotactic radiosurgery:Clinical advantages of the CyberKnife integrated system[J].Int J Med Robot Comput Assist Surg,2005,1:28-39.
[14] YinFF,Ryu S,Ajlouni M,et al.A technique of intensitymodulated radiosurgery (IMRS) for spinal tumors[J].Medical Physics,2002,29(12):2815-2822.
[15] Yan H,Yin FF,JK.A phantom study on the positioning accuracy of the Novalis Body system[J].Medical Physics,2003,30(12):3052-3060.
[16] 夏廷毅,康静波.体部肿瘤伽玛刀治疗学[M].北京:人民卫生出版社,2009:57-59.
[17] Murphy MJ,Balter J,Balter S,et al.The management of imaging dose during image-guided radiotherapy:report of the AAPM Task Group 75[J].Medical Physics,2007,34(10):4041-4063.
[18] Ma J,Chang Z,Wang Z,et al.ExacTrac X-ray 6 degree-offreedom image-guidance for intracranial non-invasive stereotactic radiotherapy:Comparison with kilo-voltage cone-beam CT[J]. Radiotherapy and Oncology,2009,93(3):602-608.
[19] Chang Z,Wang Z,Ma J,et al.6D image guidance for spinal non-invasive stereotactic body radiation therapy:Comparison between ExacTrac X-ray 6D with kilo-voltage cone-beam CT[J].Radiotherapy and Oncology,2010,95(1):116-121.
[20] Fu D,Kuduvalli G.A fast,accurate,and automatic 2D-3D image registration for image-guided cranial radiosurgery[J].Medical Physics,2008,35:2180-2194.
[21] Anthony KH,Fu D,Cotrutz C,et al.A study of the accuracy of CyberKnife spinal radiosurgery using skeletal structures tracking[J].Neurosurgery,2007,60:147-156.
[22] Fu D,Kahn R,Wang B,et al.Xsight Lung Tracking System:A fiducial-less method for respiratory motion tracking. In Robotic radiosurgery:Treating Tumors that Move with Respiration. Edited by:Urschel HC,Kresl JJ,Luketich JD,Papiez L,Timmerman RD[M].Berlin:Springer-Verlag,2007:265-282.
[23] Antypas C,Pantelis E.Performance evaluation of a CyberKnife® G4 image-guided robotic stereotactic radiosurgery system[J]. Physics in Medicine and Biology,2008,53(17):3697-4718.
[24] Fürweger C,Drexler C,Kufeld M,et al.Patient motion and targeting accuracy in robotic spinal radiosurgery: 260 singlefraction fiducial-free cases[J].International Journal of Radiation Oncology Biology Physics,2010,78(3):937-945.
[25] Sahgal A,Larson DA,Chang EL,et al.Stereotactic body radiosurgery for spinal metastases:a critical review[J].International Journal of Radiation Oncology Biology Physics,2008,71(3):652-665.
[26] Mori S,Zenklusen S,Knopf AC.Current status and future prospects of multi-dimensional image-guided particle therapy[J].Radiological Physics Technology,2013,6(2):249-272.
[27] Markelj P,Tomazevic D,Blikar B,et al.A review of 3D/2D registration methods for image-guided interventions[J].Medical Image Analysis,2012,16(3):642-661.
[28] Penney GP,Weese J.A comparison of similarity measures for usein 2D-3D medical image registration[J].IEEE Trans.Med.Imaging, 1998,17(4):586-595.
Development of Image Guidance Techniques of Body Gamma Knife
FU Dong-shan, LI Wei-juan
Jiangsu Ruier Medical Technology Co., Ltd., Wuxi Jiangsu 214109, China
Stereotactic body radiation therapy (SBRT) derives naturally from stereotactic radiosurgery (SRS) technology and clinical application. Under very precise image guidance, SBRT delivers a very large dose to a well-def i ned target in a small number of fractions. Body gamma knife is an innovative radiotherapy device that was independently conceptualized and designed in China, which extends Gamma-beam therapy from head to body. For nearly fi fteen years of technology development and clinical practice, body gamma knife has been following the traditional body frame positioning mode, whose lack of position precision prevents the knife’s widespread application as a SBRT equipment. However, in recent years, image guidance technique begins to be applied in body gamma knife, which would initiate a new phase for its standard SBRT practice. This paper mainly introduces the principles, methods, experiments and preliminary results of an image-guided positioning system used in Body Gamma Knife.
body Gamma knife; image-guided radiation therapy (IGRT); stereotactic body radiation therapy (SBRT); stereotactic radiosurgery (SRS); cone beam computed tomography (CBCT); X-ray stereoscopic planar imaging; 2D-3D image registration
R741.05
A
10.3969/j.issn.1674-1633.2014.10.002
1674-1633(2014)10-0004-05
2014-03-05
2014-05-09
作者邮箱:dongshan_fu@hotmail.com
