有限元技术在心动脉支架设计中的应用
2013-12-18
上海康德莱企业发展集团医疗器械有限公司(上海,201803)
近10年来冠脉支架已经在介入手术中得到了较为广泛的应用,它可以获得较大的内腔尺寸、比较好的长期开放性和临床效果,但是支架植入后再狭窄率仍超过20%[1]。主要原因在于:支架的应用中一开始就受到"大一点好"这一思想的影响,希望通过大的支架即刻膨胀来获得好的应用效果,不太注意支架设计和材料的影响[2]。但是大量的动物实验和临床应用均表明,不同的支架设计之间确实存在差别[3-6]。其主要原因在于支架的植入会造成血栓及血管损伤[7],而支架设计不同所造成的损伤也不同,从而能够影响再狭窄[8]。因此,支架设计越来越受到重视。
有限元法(finite element method ,FEM)最早出现于20世纪60年代,当时是用来解决航天领域的结构问题,后期逐步扩展到了热传递、流体力学、运动学以及电磁场等方面。自二十世纪七十年代被应用于医学领域以来,显示出了极大的优越性,目前已经被应用到心动脉支架领域。本文综述了有限元技术在支架设计中的研究进展,并提出了支架优化设计的方向。
1 有限元法在支架设计中的应用
复杂形状是很难通过常规的方法获得其分析结果,因此引入有限元之类的数字化分析方法是非常必要的。有限元分析法通过网格化将复杂的区域划分成相互连接的小而简单的区域(单元),通过单元之间的应力、应变传递可以获得整体的应力、应变结果,从而可以方便的对复杂的机械问题进行求解[9]。换句话说,有限元技术首先是对每一个小的单元求解,然后将其正确组合以获得整体的求解结果,而不是直接对整体求解。有限元分析中的网格化、生成单元及相互连接的节点、定义边界条件被称为问题的离散化。将材料特性赋予有限元模型,施加载荷并约束边界条件,就可进行有限元的分析计算。通过后处理程序,即可获得应力、应变结果,从而可以对各种性能进行预测及分析。
目前,全球使用的支架设计超过100种,它们在支架类型、尺寸、网孔形状、网孔间连接等方面均存在较大差别,且由于支架本身形状的复杂性以及与血管或病变接触的复杂性,常规的方法也很难获得所需要的结果。因此,有限元技术被认为是进行支架设计成本最低,且最适合的工具。利用有限元技术可以模拟支架膨胀[10]、弹性回缩[11]、球囊-支架接触分析[12]、支架-血管接触分析[13]、支架-斑块-血管接触分析[14]等,从而确定支架、血管及斑块的应力情况以及支架对血流情况的影响等。它可以很方便的改变支架形状进行重新分析,以比较不同设计之间的区别,进而进行优化设计。
目前支架的主要材料有316L不锈钢与 NiTi合金二种。316L的力学行为比较常见,有限元技术可以方便的对其性能进行模拟;而NiTi合金由于其加载过程中应力诱发马氏体转变,出现奥氏体与马氏体两相混合的过渡区,性能发生较大变化,其卸载曲线既不是沿着加载曲线,也不是沿着传统的斜率为弹性模量的卸载曲线,而是存在一定的滞后区(如图1所示),这就为有限元模拟带来很大的困难。随着有限元技术的不断发展,相关材料模型的不断完善,使得对镍钛合金材料的模拟成为可能。目前能够模拟NiTi合金的有限元软件主要有ABAQUS (Hibbit Karlsson & Sorenses Inc.)与ANSYS (ANSYS.Inc.)。有限元分析中常用的材料常数如表1所示(由于各个公司的球囊性质差别较大,其参数未列入表中)。
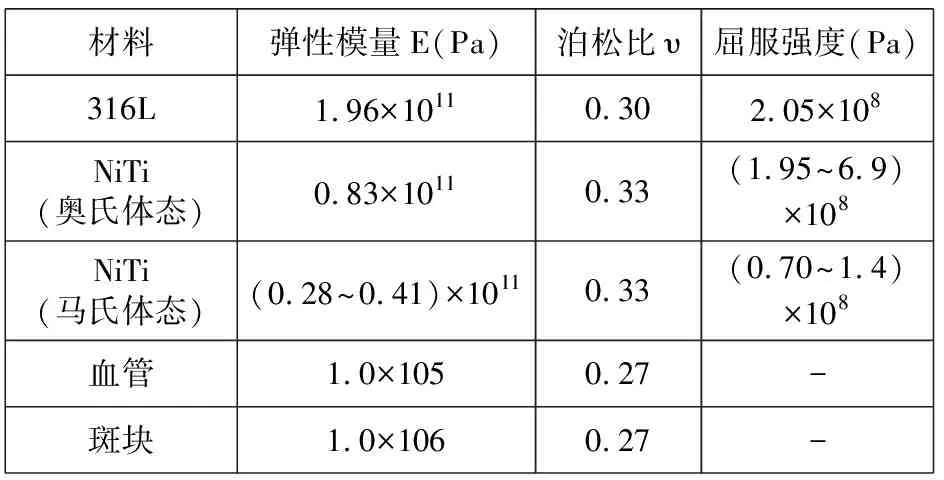
表1 有限元分析中的材料常数Tab.1 Parameters of materials used in FEM
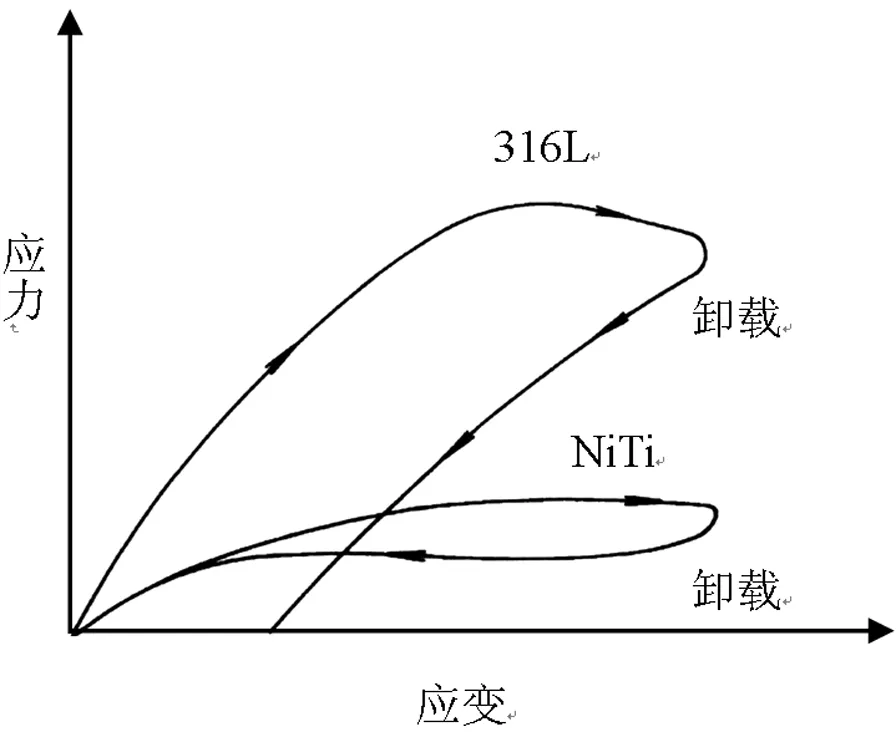
图1 NiTi与316L的应力-应变曲线Fig.1 Stress-Strain Curves of NiTi and 316L
2 国内外研究现状
由于支架的变形量较大涉及到塑性变形(材料非线性),另外,球囊与支架以及支架与斑块或血管之间的接触(状态非线性)均属于结构非线性领域,有限元技术对于结构非线性问题具有较强的处理能力,为支架分析及优化提供了一种非常方便的工具。但是需要注意的是:并不是所有的有限元软件均适合进行支架的非线性分析,由于支架外形及接触环境的复杂性,对软件及处理器的要求均较高。目前在支架的有限元分析中被广泛采用的是ABAQUS、ANSYS与ADINA(ADINA R & D Inc.)等。
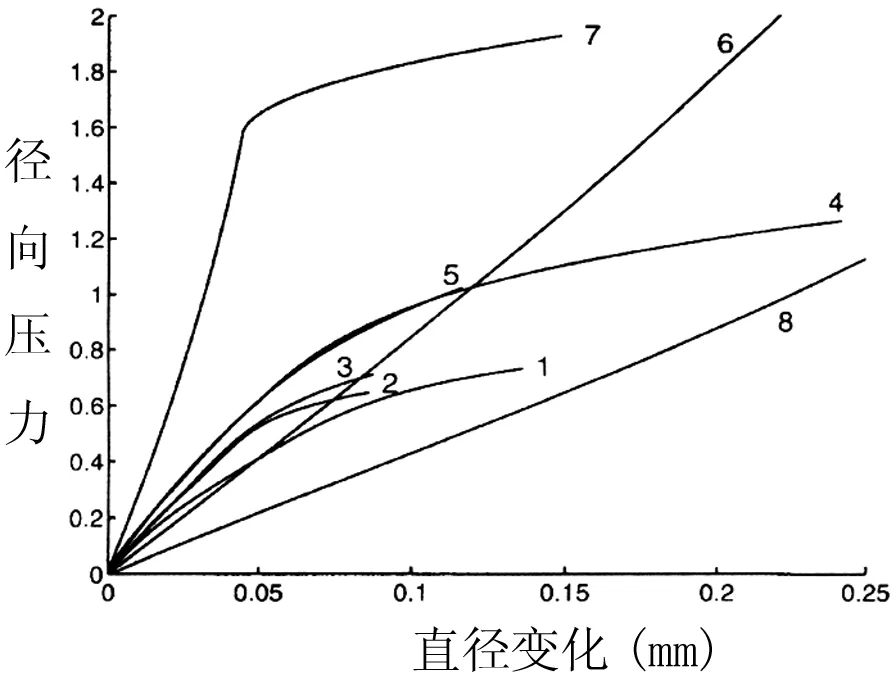
1 Bestent支架; 2 Palmaz-Schatz支架; 3 Crown支架; 4 Palmaz-Schatz II支架; 5 NIR支架; 6 Micro-II支架; 7 Cardiocoil支架; 8 Wiktor 支架1 Bestent Stent; 2 Palmaz-Schatz Stent; 3 Crown Stent; 4 Palmaz-Schatz II Stent; 5 NIR Stent;6 Micro-II Stent;7 Cardiocoil Stent;8 Wiktor Stent
首先,需要明确的是支架设计的不同包括多种因素间的差别,而能对其机械性能产生较大影响的主要包括材料、尺寸、外形等。图2总结了8种不同设计支架的径向抗力与直径变化之间的关系曲线[15],可以看出,支架设计对其性能具有较大影响。而有限元技术通过改变模型数据与参量能够非常方便的对上述因素的影响进行分析,因此,有限元技术正在心动脉支架领域正得到越来越广泛的应用。但是目前的有限元分析还相对简单,主要以支架自身的膨胀及回缩等性能为主。如Francesco等[11]利用有限元法对Palmaz-Schatz支架进行的分析表明:金属所占的面积比以及支架壁厚均对支架径向、轴向回缩以及变形均匀性有影响;低的面积比具有较高的径向和轴向回缩,但是变形均匀性较好;减少壁厚可以减少膨胀压,但是轴向回缩和变形不均匀性增加。Frederique等[16]比较了管状支架(Palmaz-Schatz)与缠绕支架(Freedom)之间的差别,结果表明:管状支架的膨胀压与径向回缩要明显高于缠绕型支架;通过减少管状支架壁厚可以较大的提高其柔顺性。但是Joseph 等[17]通过动物实验却发现缠绕型支架(Gianturco-Roubin II)的径向回缩要明显高于另外三种管状支架(Palmaz-Schatz,Multilink,NIR),同样Paul等[18]通过对23种不同支架的模拟测试也得出:缠绕型支架的径向回缩要高于管状支架。造成这种矛盾的主要原因在于:Frederique等的有限元模拟中仅限于支架本身,未加入血管的作用,因为血管要对支架产生相反的径向压应力,如果支架径向支持力差的话必然产生较大的径向回缩。而Regis Rieu等[19]通过实验研究,Frederique等通过有限元模拟均已得出,缠绕型支架的径向支持力要明显低于管状支架。因此,其有限元分析的结果是可以理解的。
David等[20]利用有限元法模拟了不同加载速度下支架的膨胀,结果显示:过大与过小的加载速度均会产生不利的结果。小的加载速度导致支架变形不均匀,产生明显的弯曲;大的加载速度对应大的支架应。故建议采用中等的加载速度,这对于临床使用具有一定的指导意义,但是目前还没有相关的实验验证,并且在其模拟中载荷是直接加到支架内表面的,未考虑球囊的作用。因此,还有必要增加球囊-支架的接触分析,以提高有限元模拟的仿真性。
在球囊-支架/血管接触分析方面,已经出现了有限元的相关报道。如Campbell等[21]模拟了支架膨胀过程中球囊与血管的相互作用,认为高的膨胀压、大的支架网孔、软的球囊均会导致球囊挤出,将导致大的球囊-血管接触面积与接触应力,必然造成较大的血管损伤。通过对两种不同设计支架的比较,Campbell等提出:波纹环状网孔设计将比槽状网孔设计产生更小的内膜损伤与再狭窄, 这与其动物实验的结果是一致的。
另外,Kwek等[12]利用有限元法模拟了球囊与支架的相互作用,通过对两种不同壁厚的波纹环状S-Stent的比较发现,厚壁支架膨胀过程中等效塑性变形与轴向回缩均有所下降。并认为产生这种结果是有益的,一方面,等效塑性变形减小可以减少球囊膨胀压,造成的血管损伤也相应减少;另一方面,轴向回缩减少可以增加定位的准确性。但是Adnan等[22]通过对651例不同壁厚的Multi-Link支架的术后再狭窄分析发现,薄壁支架的平均再狭窄(15%)明显小于厚壁支架(25.8%)。而Joseph等[23]通过对三种不同设计支架的组织切片结果却显示,支架壁厚对内膜增生影响不大。造成这种差别的原因可能在于支架类型与壁厚范围的不同,因为Adnan等认为只有壁厚≤75um时,壁厚的影响才会变得明显。并且Kwek等的有限元分析中仅涉及球囊与支架间的相互作用,通过支架塑性变形来推论血管损伤,缺乏准确性,因此,有限元分析中应增加支架与血管的相互作用,以提高其仿真性。
Berry等[13]利用有限元法模拟了支架与血管的相互作用,并结合体外与体内实验发现,与血管柔顺性相匹配的软支架可以减少血液动力学紊乱,并能减少血管应力。但是需要注意的是,软的支架在血管压应力的作用下可能对应较大的弹性回缩,并且支持斑块的能力也将受到限制。因此,软支架的优点与应用仍需进一步探讨。
此外,Tan等[24]首次利用有限元法分析了斑块与支架间的相互作用,发现在斑块作用下两种支架(Palmaz-Schatz,Freedom)呈现出不同的变形方式,提出了影响支架膨胀的几种因素,并指出过大与过小的膨胀压都是不利的。Dumoulin等[25]利用有限元法分析了材料缺陷对支架性能的影响,并进行了疲劳寿命的预测。James等[26]研究了支架对血流的影响,发现支架植入会造成涡流与流动停滞,从而促进血小板聚集,认为支架设计对此具有较大影响。这都为有限元技术在心动脉支架领域的进一步应用,开辟了更加广阔的空间。
总之,有限元技术在心动脉支架领域已经获得了一定的应用,支架植入不仅会影响血管内应力,造成血管损伤,而且会影响血流情况,促进再狭窄。因此,支架的优化设计应当从固体力学、流体力学两个方面同时进行,单纯考虑某一方面是不全面的。但是,目前支架的有限元分析还未能同时兼顾这两方面的内容,且尚未形成完全统一的结论,其仿真性还有待于进一步提高。
3 支架优化设计方向
支架的优化设计应当结合临床及动物实验的结果进行,对于可能造成再狭窄的各种可能因素进行分析。利用有限元技术可以方便的改变支架设计,并进行对比分析,这可以极大的减少设计成本与开发周期,具有其它方法所无法替代的优点,这对于理想支架的开发是很有价值的。David等[27]提出了理想支架应具有的特点,而有限元技术能对其多种性能进行预测及模拟,具体应用如表2所示。
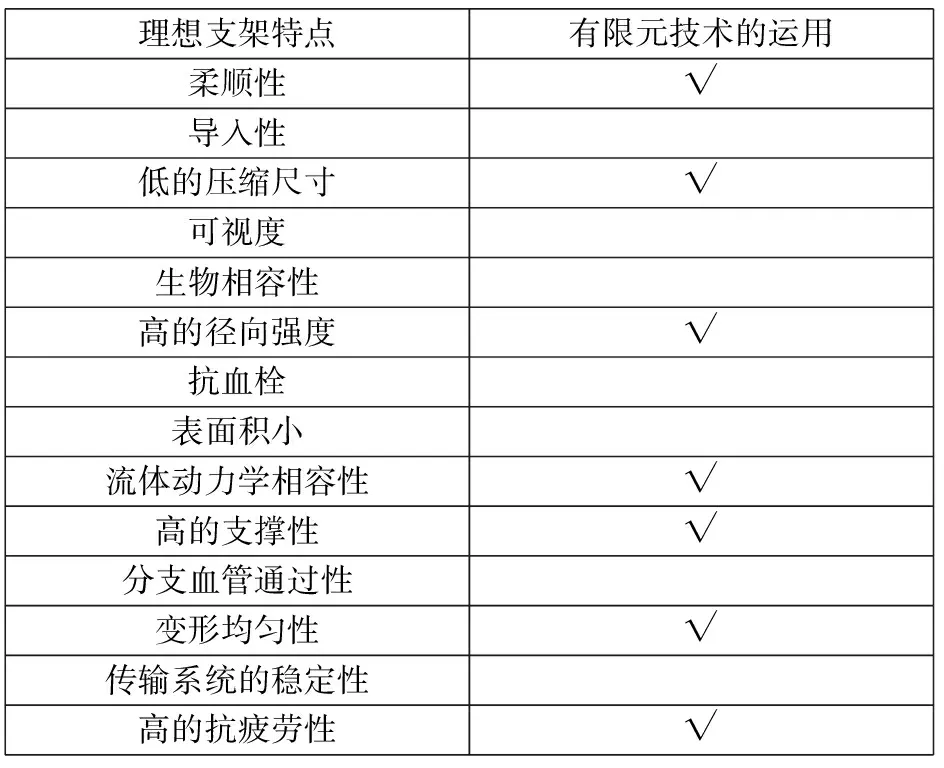
表2 有限元技术在理想支架设计中的应用Tab.2 Use of FEM in the design of ideal stent
但是,目前的有限元分析还处于相对简单的阶段,大部分报道仅限于支架本身的机械性能,而未考虑球囊、血管、斑块等的作用。要实现真正意义上的有限元仿真模拟,应当尽可能的将上述因素考虑在内。综合有限元技术在心动脉支架领域的应用情况,作者提出了支架优化设计的方向:(1)控制变形均匀性,以减少支架不均匀变形对血管的损伤;(2)保证充分变形的基础上,尽量减少球囊膨胀压,以减少由于球囊膨胀与支架刺入对血管的损伤;(3)减少径向与轴向的弹性回缩,一方面可以获得可能大的管腔直径,以保证血流量;另一方面可以减少短缩对支架定位带来的不利影响;(4)足够的柔顺性,保证支架顺利通过血管到达病变部位,并减少对血流的影响;(5)足够的径向支持力,使得支架能够抵抗血管与斑块对支架的压应力,防止支架回缩与崩溃;(6)减少涡流与网孔间的流动停滞,以减少血小板聚集。
可以预见,有限元技术在心动脉支架领域具有广阔的应用前景,不久的将来,有限元技术将成为评价支架效果的有效工具,在其指导下还会出现新的支架体系。
[1] 沈珠军.冠状动脉成形术及支架术后再狭窄[J].基础医学与临床,2001,21(2):104-107.
[2] Eric J Topol,Patrick W Serruys. Frontiers in interventional cardiology[J]. Circulation, 1998, 98:1802-1820.
[3] Compbell Rogers C,Edelman ER. Endovascular stent design dictates experimental restenosis and thrombosis[J]. Circulation,1995,91:2995-3001.
[4] Carter AJ,Scott D,Bailey L, et al. A comparison of stent designs in small diameter porcine coronary arteries[J]. J Am Coll Cardiol, 1997,29:170-172.
[5] Goy JJ,Eeckhout E,Stauffer JC,et al. Stenting of the right coronary artery for de novo stenoses : a comparison of the wiktor and the palmaz-schatz stents[J]. Circulation,1995,92:536-537
[6] Barth KL,Virmani R,Froelich J,et al. Paired comparison of vascular wall reactions to palmaz stents,strecker tantalum stents and wallstents in canine iliac and femoral arteries[J]. Circulation, 1996,5:2161-2169 .
[7] Rogers C,Parikh S,Seifert P,et al. Endogenous cell ceding: remnant endothelium after stenting enhances vascular repair[J].Circulation,1996,94:2909-2914 .
[8] Campbell roger,David Y Tseng,James C Squire,et al. Ballon-artery interactions during stent placement a finite element analysis approach to pressure,compliance and stent design as contributor to vascular injury[J].CircRes1999,84:378 - 383.
[9] 王国强.实用工程数值模拟技术及其在ANSYS上的实践[M].西安:西北工业大学出版社,1999 .
[10] J Awrejcewicz,M Ciach,K Wlodarczyk. Finite element method of non-linear behaviour of implants and stents[J]. ECCOMAS 2000,1-12.
[11] Francesco Migliavacca,Lorenza Petrini,Maurizio Colombo,et al. Mechanical behavior of coronary stents investigated through the finite element method[J]. Journal of Biomechanics 2002,35:803-811.
[12] Kwek Tai Chuan,Yuan Qi,Teo Ee Chon,et al. Design optimization of coronary stent by fea[J]. Journal of American Society for Artificial Internal Organs 2000,Mar,46(2):201-207.
[13] Joel L Berry,Emil Manoach,Choukri Mekkaoui,et al. Hemodynamics and wall mechanics of a compliance matching stent:in vitro and in vivo analysis[J]. J Vasc Interv Radiol, 2002,13:97-105.
[14] F Auricchio,M Di Loreto,E Sacco. Finite-element Analysis of a stenotic artery revascularization through a stent insertion[J]. Computer Methods in Biomechanics and Biomedical Engineering, 2000,00:1-15.
[15] Stephan C Schrader,Rafael Beyar. Evaluation of the compressive mechanical propertyes of endoluminal metal stents[J].Catheterization and Cardiovascular Diagnosis,1998,44:179-187.
[16] Frederique Etave,Gerard Finet,Maurice Boivin,et al. Mechanical properties of coronary stents determined by using finite element analysis[J]. Journal of Biomechanics,2001,34:1065-1075.
[17] Joseph P Carrozza,Susanne E Hosley,David J Cohen,et al. In Vivo assessment of stent expansion and recoil in normal porcine coronary arteries[J]. Circulation, 1999,100:756-760.
[18] Paul Barragan,Regis Rieu, Vincent Garitey,et al. Elastic Recoil of coronary stents: a comparative analysis[J]. Catheterization and Cardiovascular Interventions,2000,50: 112-119.
[19] Regis Rieu,Paul Barragan,Catherine Masson,et al. Radial force of coronary stents: a comparative analysis[J]. Catheterization and Cardiovascular Interventions, 1999, 46: 1380-391.
[20] SN David Chua,BJ Mac Donald,MSJ Hashmi. Finite element simulation of stent expansion[J]. Journal of processing technology,2002,120:335-340.
[21] Compell Rogers,David Y Tseng,James C Squire,et al. Balloon-Artery interaction during stent placement: a finite element analysis approach to pressure, compliance, and stent design as contributiors to vascular injury[J].Circ Res,1999,84: 378-38.
[22] Adnan Kastrati,Julinda Mehilli,Josef Dirschinger,et al. Intracoronary stenting and angiograohic results:strut thickness effect on the restenosis outcome tria[J]. Circulation,2001,103:2816-2821.
[23] Joseph M Garasic,Elazer R Edelman,James C Squire,et al. Stent and artery geometry determine intimal thickening independent of arterial injury[J]. Circualtion, 2000,101:812-818.
[24] LB Tan, DC Webb,K Kormi,et al. A method for investigating the mechanical properties of intracoronary stents using finite element numerical simulation[J]. International Journal of Cardiology,2001,78:51-67.
[25] C Dumoulin, B Cochelin. Mechanical behavior of modeling of balloon-expanded stents[J]. Journal of Biomechanics,2000,33:1461-1470.
[26] James E, Moore JR, Joel L Berry. Fluid and solid mechanical implications of vascular stenting[J].Annals of Biomedical Engineering, 2002,30:498-502.
[27] David E Kandzari,James E Tcheng,James P Zidar. Coronary artery stents: evaluating new designs for contemporary percutaneous intervention[J]. Catheterization and Cardiovascular Interventions,2002,56: 562-576.
