杨梅苷的稳定性研究
2011-12-04赵丽李宗阳张泽生潘瑞乐
赵丽,李宗阳,张泽生,潘瑞乐,*
(1.天津科技大学,天津 300457;2.中国医学科学院中国协和医科大学药用植物研究所,北京 100193)
杨梅苷的稳定性研究
赵丽1,2,李宗阳2,张泽生1,潘瑞乐2,*
(1.天津科技大学,天津 300457;2.中国医学科学院中国协和医科大学药用植物研究所,北京 100193)
采用HPLC和紫外分光光度法研究杨梅苷溶液在pH、温度、金属离子等不同条件下的稳定性。HPLC法采用Venusil MP-C18色谱分析柱(4.6 mm×250 mm,5μm),流动相为乙腈∶水(18∶82,体积比),流速1.0 mL/min,柱温25℃,检测波长352 nm;紫外分光光度法采用352 nm作为检测波长。结果表明杨梅苷在中性或弱酸性条件下稳定,温度升高及金属离子存在时不稳定。杨梅苷溶液应在中性或弱酸性条件下低温或常温保存,并避免接触金属离子。本研究为杨梅苷的贮藏和开发利用提供了理论参考。
HPLC;紫外分光光度法;杨梅苷;pH;温度;金属离子;稳定性
杨梅苷(3',4',5',5,7-五羟基黄酮-3-O-α-L-鼠李糖苷)为天然多羟基黄酮类化合物,广泛存在于杨梅科植物杨梅Myrica rubra Sieb.et Zucc.的树皮及叶子,豆科植物鬼箭锦鸡儿Caragana jubata Poir.的枝叶,蓼科植物扁蓄Polygonum aviculare L的地上部分中[1-2]。杨梅苷具有很强的抗氧化能力,可作为抗氧化剂添加到食品、医药及化妆品等产品中,并于2007年2月取得美国香味料和萃取物质制造者协会(Flavour Extract Manufacturers′Association,FEMA) 的GRAS(Generally Regarded As Safe)批准号[3]。此外,杨梅苷还具有收缩血管、降血糖、保肝、利胆、抗炎、抗突变、抗肿瘤等多种作用[4]。杨梅苷在自然界非常丰富,在杨梅树皮中含量高达10%[5],且提取纯化工艺简单,具有良好的开发应用前景。由于杨梅苷具有多个羟基,极易被氧化,生成低活性甚至没有活性的氧化产物。为了进一步了解杨梅苷的理化性质,对杨梅苷在pH、温度、金属离子等不同条件下的稳定性进行了研究,为杨梅苷贮藏和开发利用提供理论参考。
1 材料与方法
1.1 仪器与试剂
Waters系列高效液相色谱仪,包括:Waters 600 controller,Waters 600 pump,Waters 2487 dual absorbance detector,Waters Empower工作站、万分之一电子天平(FA-1104)及千分之一电子天平(JA-2103N):上海天平仪器厂生产;UV2550紫外可见分光光度计:日本岛津公司;KQ5200B型超声波清洗器:昆山市超声仪器有限公司;PHS-3B型pH计:上海嘉鹏科技有限公司。
杨梅苷对照品是中国医学科学院药用植物研究所,潘瑞乐课题组从杨梅树皮中分得,经UV,IR,MS,1H-NMR,13C-NMR光谱分析鉴定结构,HPLC纯度检测在95%以上(面积归一化法)。HPLC用溶剂乙腈、甲醇为色谱纯:Fisher公司;纯净水:市售;其它化学试剂均为分析纯:北京化工厂。
1.2 色谱条件
色谱柱为VenusiMP-C18柱(4.6mm×250mm,5μm);流动相为乙腈∶水(18∶82);流速:1.0 mL/min;柱温:25℃;检测波长:352 nm;进样量:20 μL。在此色谱条件下,杨梅苷出峰时间为20.6 min,结果见图1。
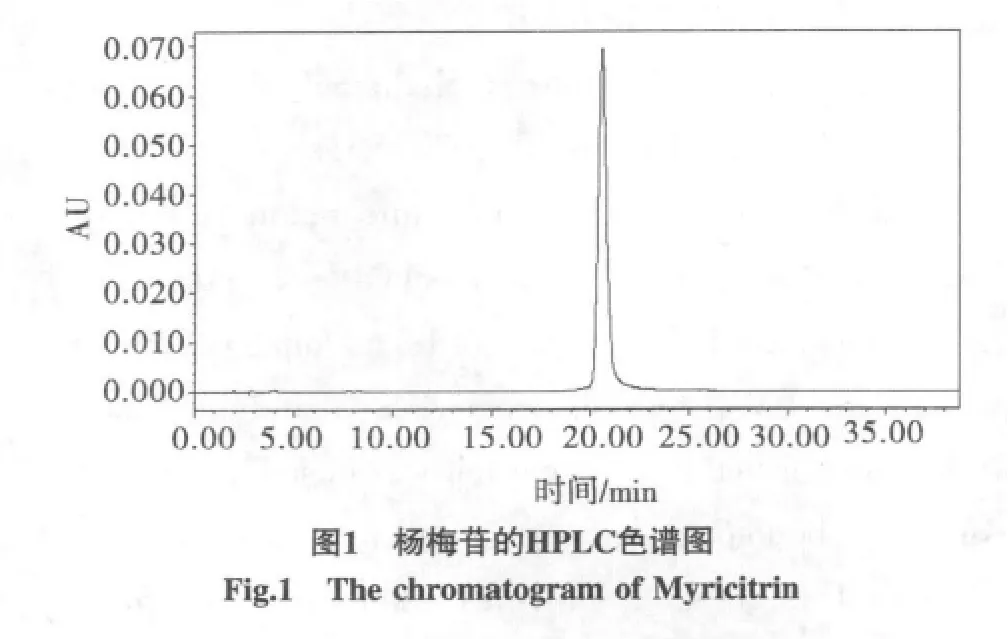
1.3 线性关系考察
精密称取杨梅苷对照品51.3 mg置于50 mL容量瓶中,加入甲醇定容至刻度,配成1.026 mg/mL的对照品贮备溶液。精密量取对照品贮备溶液1.2、1.6、2.0、2.4、2.8、3.2、3.6 mL置于25 mL量瓶中,加流动相定容至刻度,配制成49.25、65.66、82.08、98.50、114.91、131.33、147.74μg/mL系列溶液,在1.2色谱条件下,依次进样20 μL,以杨梅苷峰面积Y对杨梅苷质量X(μg)进行线性回归处理并计算回归方程,Y=1×106X-177040,r=0.9997,线性范围为0.985μg~2.955μg。
1.4 精密度试验
精密吸取同一对照品溶液20 μL,连续进样5次,记录杨梅苷的峰面积,其峰面积的RSD分别为1.8%,表明仪器精密度良好。
1.5 稳定性试验
精密吸取同一对照品溶液20 μL分别于0、2、4、6、8、10 h进样测定,记录杨梅苷的峰面积,其峰面积的RSD分别为1.7%,表明杨梅苷溶液在室温条件下10 h内稳定不变。
2 结果与分析
2.1 pH对杨梅苷溶液稳定性的影响
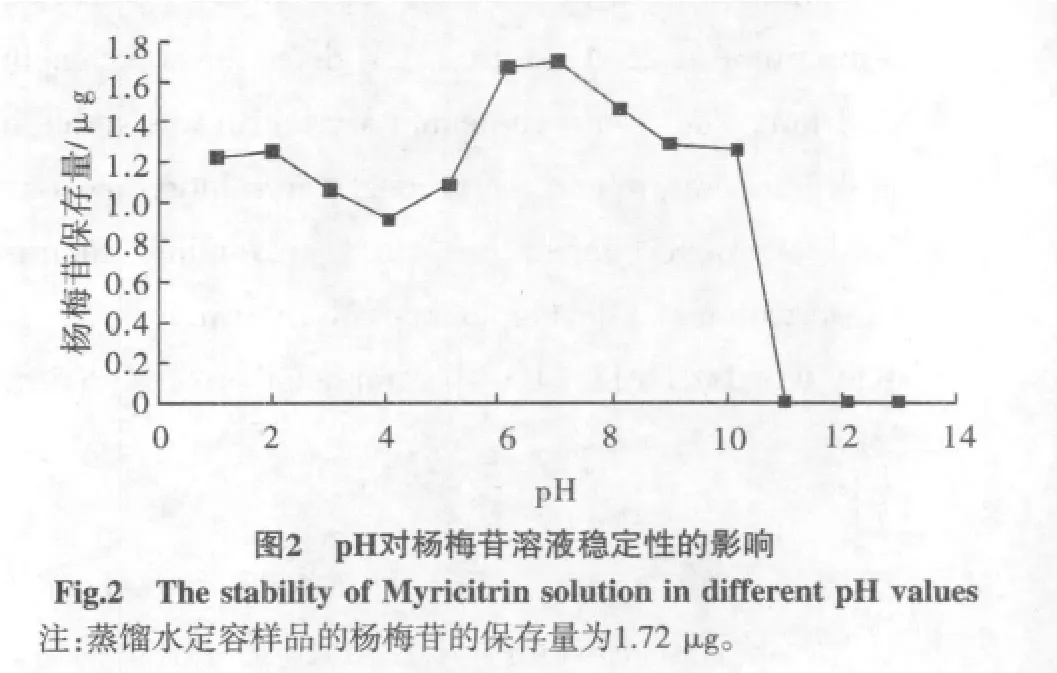
用0.1 mol/L NaOH 及HCl溶液配制成pH为1.0、2.0、3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0、11.0、12.0、13.0 的 溶液(pH采用pH计测定),精密量取14份2.5mL的1.01mg/mL的杨梅苷溶液分别置于25 mL量瓶中,其中1份用蒸馏水定容至刻度,其余13份用上述不同pH溶液定容至刻度,摇匀配制成0.101 mg/mL的不同pH的系列溶液。在4℃的冰箱中放置24 h后,恢复至室温,HPLC测定不同pH条件下杨梅苷的保存量,结果表明在pH为6~7之间时,即弱酸条件下杨梅苷溶液比较稳定,其保存量与蒸馏水定容样品相同;在pH为1~5或8~10时,即强酸或碱性条件下,杨梅苷保存量显著下降;在pH达11时,杨梅苷结构完全被破坏,保存量降至0,结果详见表1及图2。

表 1 不同pH下杨梅苷的保存量Table 1 The contents of Myricitrin in different pH values
2.2 温度对杨梅苷溶液稳定性的影响
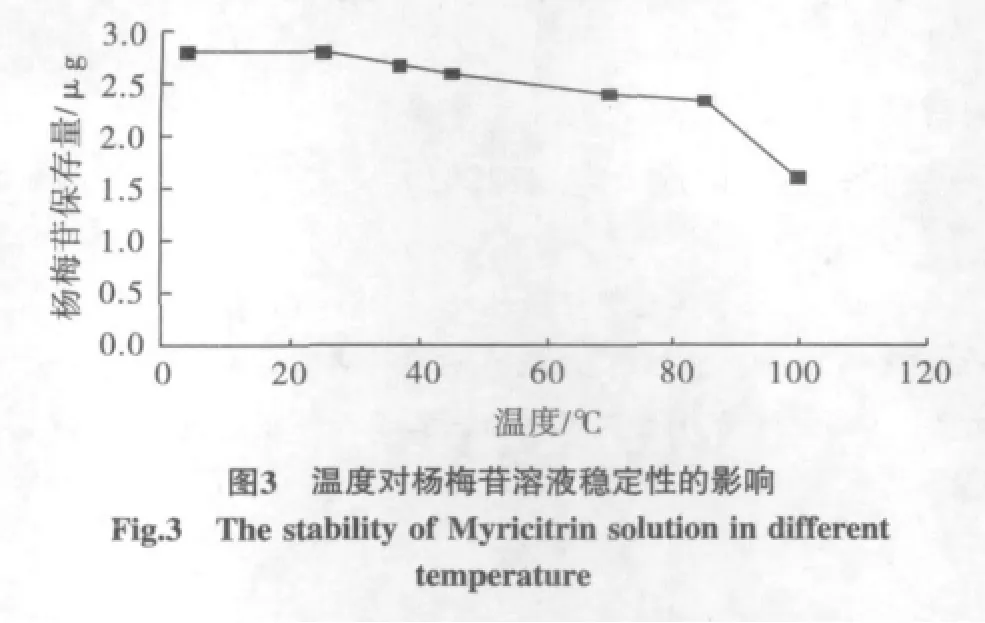
精密称取杨梅苷对照品156.5 mg置于100 mL容量瓶中甲醇定容,精密量取10 mL置于7个100 mL的容量瓶中,用蒸馏水定容至刻度,配制成0.1565 mg/mL的溶液,分别置于4、25、37、45、68、85、100 ℃中保温处理4 h,HPLC法测定杨梅苷保存量,结果表明常温或4℃冰箱中冷藏,杨梅苷溶液比较稳定,随着温度的增高,杨梅苷保存量逐渐降低,在100℃已降至原来的50%,详见表2及图3。
2.3 金属离子对杨梅苷溶液稳定性的影响
精密称取NaCl、KCl、无水MgSO4、无水ZnCl2、无水CuSO4、Pb(CH3COO)2·3H2O、FeCl3·6H2O、AgNO3、无 水CaCl2、Al(NO3)3·9H2O,分别用蒸馏水配制成含金属离子浓度为0.1 mol/L的溶液。精密称取杨梅苷对照品304.0 mg,甲醇定容到100 mL得杨梅苷母液。精密量取杨梅苷母液5 mL共11份置于100 mL容量瓶中,其中一份用蒸馏水定容至刻度,其余10份用上述不同金属溶液定容至刻度,即得11份浓度为0.152 mg/mL的不同金属离子条件下的杨梅苷溶液,于4℃的冰箱中静置48 h后,取出,恢复至室温。结果发现杨梅苷在NaCl、KCl、MgSO4溶液中相对稳定,溶液澄清透明;杨梅苷与铝盐、铁盐、钙盐等试剂反应,生成可溶的黄色络合物,与AgNO3溶液产生黑色沉淀,与CuSO4、ZnCl2、Pb(CH3COO)2·3H2O溶液产生黄色沉淀,与铁盐生成棕褐色溶液。

表 2 不同温度下杨梅苷的保存量Table 2 The contents of Myricitrin in different temperature
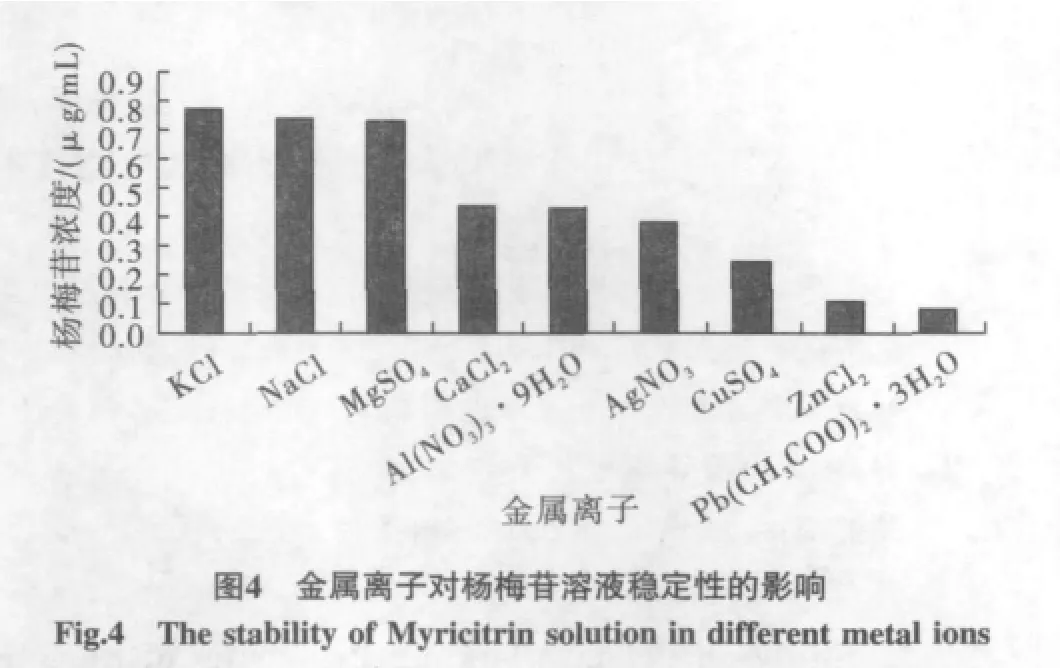
将样品分别稀释5倍(FeCl3·6H2O定容的样品稀释125倍),以蒸馏水为空白,352 nm为检测波长,于紫外分光光度计下测定各样品的吸收度。根据紫外光谱定量分析原理,即样品在某波长处的吸收强度与所测样品的浓度成正比。以蒸馏水定容的样品作为对照,计算以金属离子定容样品的杨梅苷含量。结果显示杨梅苷在本文考察的10种金属离子溶液中均有不同程度的降低,在NaCl、KCl、MgSO4溶液变化较小,在CuSO4、ZnCl2、Pb(CH3COO)2·3H2O溶液中降低比较明显,但在FeCl3·6H2O溶液中紫外光谱吸收值显著增高,可能杨梅苷与FeCl3反应生成的棕褐色络合物在352 nm处有强吸收,详见表3及图4。
2.4 分析
杨梅苷结构中含有5个酚羟基,呈弱酸性,在中性或弱酸性环境中比较稳定,在强碱性环境中结构完全破坏;温度对杨梅苷溶液的影响较大,随着温度的升高,其稳定性降低,在100℃时含量降低了50%。因此,杨梅苷溶液应在低温或常温下保存。由于在杨梅苷在B环上3',4',5'相邻位置均有OH基,3',4'位和4',5'位OH基上具有很强金属螯合能力;在C环4位上羰基也可与3、5位上OH基共同对金属离子发生螯合作用,生成有色络合物,影响杨梅苷溶液的稳定性。本文考察了10种金属离子对杨梅苷溶液的影响,结果表明Na+、K+、Mg2+对杨梅苷影响较小,Al3+、Ag+、Zn2+、Ca2+、Cu2+、Pb2+、Fe3+等影响较大。

表 3 不同金属离子溶液中杨梅苷的浓度Table 3 The concentration of Myricitrin in different metal ions
3 结论
通过本实验研究,杨梅苷溶液应保存于中性或弱酸性、低温或常温条件下,并避免重金属离子的影响。
[1]陈晓虎,陈道峰.萹蓄的化学成分研究[J].中国中药杂志,2004,29(9):918-919
[2]廖华卫,刘恩桂,王定勇.杨梅树皮的化学成分研究[J].中南药学,2006,4(3):196-199
[3]凌关庭.杨梅提取物及其抗氧化作用[J].粮食与油脂,2009(4):38-41
[4]王晓云,姜子涛.天然抗氧剂二氢杨梅素研究进展[J].食品研究与开发,2007,28(2):185-188
[5]张立.杨梅苷对四氧嘧啶模型小鼠降血糖作用的初步研究[J].中国现代药物应用,2009,3(15):29-30
Studies on Stability of Myricitrin
ZHAO Li1,2,LI Zong-yang2,ZHANG Ze-sheng1,PAN Rui-le2,*
(1.Tianjin University of Science and Technology,Tianjin 300457,China;2.Institute of Medicinal Plant,Chinese Academy of Medical Sciences and Peking Union Medical College,Beijing 100193,China)
The stability of Myricitrin solution was studied under different pH values,temperature and metal ions by HPLC and UV spectrophotometry.The contents of Myricitrin was achieved on Venusil MP-C18column(4.6 mm×250 mm,5μm)with acetonitrile-water(18∶82)as mobile phase at the flow rate of 1.0 mL/min,column temperture at 25℃ and the UV detection wavelength was 352 nm.UV spectrophotometry was determined at 352 nm.The results indicated Myricitrin was stable in weak acidic or neutral solution but was unstable under high temperature and metal ions.The solution of Myricitrin should be kept under neutral and weak acidity,at cold or room temperature,and preventing from metal ions.This research provides scientific basis for preservation and development of Myricitrin.
HPLC;UV spectrophotometry;Myricitrin;pH values;temperature;metal ions;stability
中药标准物质研制和开发的技术平台建设(2009ZX 09308-001-1-5)
赵丽(1985—),女(汉),硕士研究生,研究方向:营养与食品卫生学。
*通信作者:潘瑞乐,研究员。
2011-03-22
