氯解磷定注射液细菌内毒素检查法的建立
2011-08-07王贵英贵州省药品检验所贵阳市550004
王贵英(贵州省药品检验所,贵阳市 550004)
氯解磷定注射液属于解毒药类,临床上主要用于有机磷酸酯类中毒的解救,主要用法有肌内注射和静脉注射。该药收载于卫生部药品标准1996年版(二部)第五册[1],原质量标准中无安全性检查项。为了更好地控制其质量,笔者查阅了相关资料,虽有文献[2]报道复方氯解磷定注射液细菌内毒素的检查方法,但关于氯解磷定注射液的细菌内毒素检查方法尚未见文献报道。笔者参照《中国药典》2010年版[3](二部)附录“细菌内毒素检查法”及相关文献[2],对氯解磷定注射液应用鲎试剂进行细菌内毒素检查的方法可行性作了研究。
1 仪器与试药
电热恒温水浴箱(国营创新医疗器械厂);洁净工作台(苏州安泰空气技术有限公司)。
氯解磷定注射液(上海旭东海普制药有限公司,批号:090902、091001、091101、100301,规格:0.5 g ∶2m L);鲎试剂(以下简称TAL,湛江博康海洋生物有限公司,批号:0807170,规格:每支0.1m L,灵敏度:0.25 EU·m L-1;湛江安度斯生物有限公司,批号:1004162,规格:每支0.1m L,灵敏度:0.25 EU·m L-1);细菌内毒素工作标准品(批号:2007-4,效价:每支150 EU)、细菌内毒素检查用水(以下简称BET水,批号:2008-04,规格:每支10m L)均由中国药品生物制品检定所提供。
2 方法与结果
2.1 细菌内毒素限值(L)的确定
根据氯解磷定注射液说明书得知该药用法用量为:肌内注射,每次0.75~1.0 g;静脉注射,每次0.5~0.75 g。严重中毒:1~1.5 g(2~3支)。根据公式:L=K·M-1,其中M为1 500 mg·60 kg-1·h-1=25mg·kg-1·h-1;K=5 EU·kg-1·h-1,则限值L=0.2 EU·mg-1,最终确定限值为0.2 EU·mg-1。
2.2 TAL灵敏度复核
按照《中国药典》2010年版(二部)“细菌内毒素检查法”规定[3],进行TAL的标示灵敏度复核,结果2批TAL经细菌内毒素工作标准品检查灵敏度(λc)与标示灵敏度(λ)一致,结果均符合规定,详见表1(表中“+”表示反应呈阳性,“-”表示反应呈阴性;下表同)。

表1 TAL灵敏度复核结果Tab 1 Recheck of TAL sensitivity
2.3 干扰试验预试验
2.3.1 样品有效稀释浓度(MVC)的计算[2]。计算公式为MVC=λ·L-1,由于L为0.2 EU·mg-1,λ为TAL标示灵敏度,目前市售TAL的λ通常为0.5~0.03 EU·m L-1,则氯解磷定注射液的对应有效稀释浓度为c0.5=2.5mg·m L-1、c0.25=1.25mg·m L-1、c0.125=0.625mg·m L-1、c0.06=0.3mg·m L-1、c0.03=0.15mg·m L-1。
2.3.2 试验操作。将样品(批号:090902)用BET水稀释为含氯解磷定浓度20、10、5、2.5、1.25、0.625mg·m L-1的溶液,将此系列浓度溶液记为NPC。另制备同样系列浓度的供试液,并使每一浓度的供试液中均含有2λ(0.5 EU·m L-1)浓度的细菌内毒素,记此系列溶液为PPC。取灵敏度为0.25 EU·m L-1的TAL,分别与上述NPC和PPC进行反应,每一浓度重复2管,并设阳性对照记为PC和阴性对照记为NC,混匀后封口,置于37℃恒温水浴60m in,反应结果见表2。
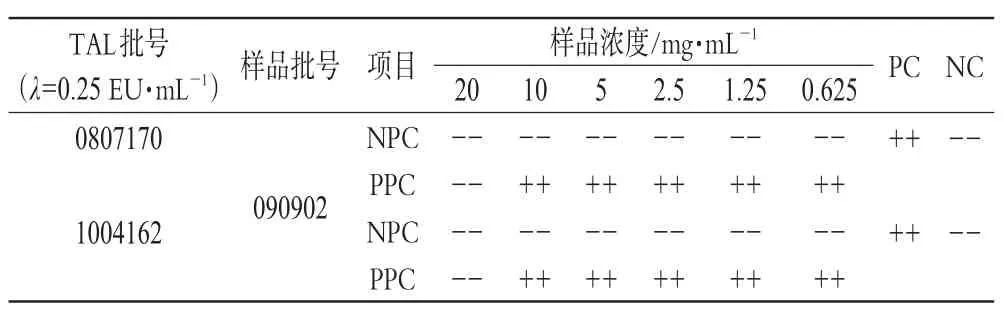
表2 样品干扰试验预试验结果Tab 2 Resultsof prelim inary interference testof samp les
表2结果表明:用灵敏度为0.25 EU·m L-1的TAL对样品进行细菌内毒素试验,结果样品浓度在10mg·m L-1及以下浓度时无抑制干扰作用。
2.4 正式干扰试验
为了最终确认是否存在抑制因素的影响,进行正式干扰试验。取3批样品用BET水稀释至10mg·m L-1,用该浓度溶液和BET水分别将细菌内毒素工作标准品稀释成含内毒素0.5(2 λ)、0.25(λ)、0.125(0.5 λ)、0.06(0.25 λ)EU·m L-1的溶液,分别与2个厂家灵敏度为0.25 EU·m L-1的TAL反应,每一浓度重复4管,并设阴性对照,按《中国药典》2010年版(二部)“细菌内毒素检查供试品干扰试验”项[3]进行试验,结果见表3。
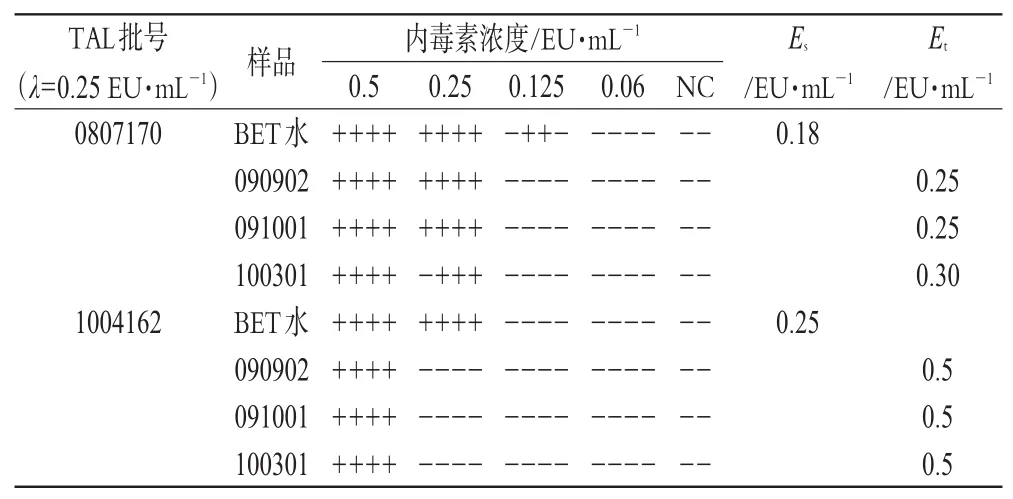
表3 样品干扰试验结果Tab 3 Resultsof interference testof sam ples
表3结果表明:3批样品浓度为10mg·m L-1时用2个厂家灵敏度均为0.25 EU·m L-1的TAL进行试验,结果BET水制成的内毒素溶液的反应终点浓度的几何平均值(Es)在0.5λ~2λ(包括0.5λ和2λ)及供试品溶液制成的内毒素溶液的反应终点浓度的几何平均值(Et)在0.5 Es~2 Es(包括0.5 Es和2 Es)内,符合《中国药典》规定,确认供试品在该浓度下无干扰作用。
2.5 样品细菌内毒素检查
按《中国药典》2010年版(二部)“细菌内毒素检查法”[3],将4批样品稀释至浓度为10mg·m L-1,设立NPC、PPC、PC和NC,用2个厂家灵敏度为0.25 EU·m L-1的TAL进行细菌内毒素检查,结果见表4。
3 讨论
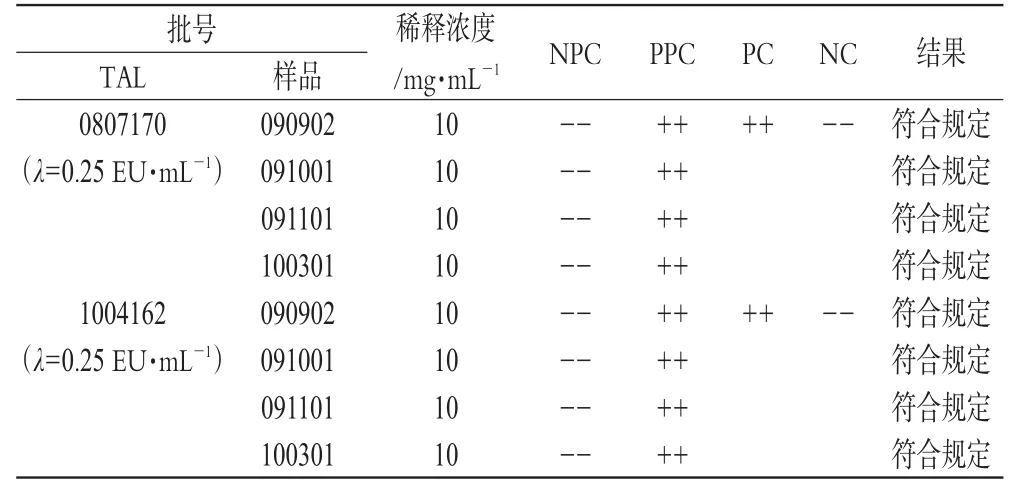
表4 4批样品细菌内毒素检查结果Tab 4 Results of bacteria endotoxin test for four batches of samp les
由预干扰试验结果可知,氯解磷定注射液稀释至10mg·m L-1及以下浓度后与灵敏度为0.25 EU·m L-1的TAL反应无抑制性干扰。正式干扰试验用3批样品稀释至浓度为10mg·m L-1,用2个厂家灵敏度为0.25 EU·m L-1的TAL进行试验,结果Es/Et均在0.5~2内,确认无干扰影响。对4批样品依法检验,结果均符合规定。
与文献[2]方法比较,二者限值(L)相同,但文献方法是将理论限值降低了0.05 EU·mg-1而成0.2 EU·mg-1,因为复方制剂要求更加严格。因此参照文献[2],本文在进行干扰试验预试验时,最低浓度只稀释到0.625mg·m L-1,节约了成本。2种方法不同之处在于进行方法验证试验时,对样品进行细菌内毒素检查所用的稀释浓度不同:文献方法是按最小有效稀释浓度(1.25mg·m L-1)进行试验,本文则按预试验时确定的不干扰浓度(NIC,10mg·m L-1)进行试验[4]。因为预试验的目的就是为了确定NIC,为后续的验证试验选择适当的样品稀释浓度。样品在较高的稀释浓度下进行内毒素检查能合格,更能说明方法是可行的,既减少了稀释步骤和污染环节,也节约了成本和时间。有关文献[5]要求验证试验选择的稀释度至少要比NIC大1~2倍,但不可超过最大有效稀释倍数。
本试验结果证实,氯解磷定注射液细菌内毒素限值确定为0.2 EU·mg-1,可应用TAL进行细菌内毒素法检查。因此,为提高药品质量标准,更有效地控制药品质量,建议氯解磷定注射液增加细菌内毒素检查项。并拟定质量标准如下:取本品,依法检查,每1mg氯解磷定中含内毒素的量应小于0.2EU。
[1]中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准(二部)[S].1996年版.第5册.1996:101.
[2]高 锦,付 聪,嵇 扬,等.复方氯解磷定注射液细菌内毒素的检查方法[J].药学实践杂志,2008,26(2):133.
[3]国家药典委员会.中华人民共和国药典(二部)[S].2010年版.北京:中国医药科技出版社,2010:附录99-100.
[4]彭 燕,施 震,罗 毅.盐酸左氧氟沙星注射液中细菌内毒素法的研究[J].中国药房,2005,16(1):60.
[5]王彦厚.细菌内毒素检查方法建立中应注意的几个问题[N].新药注册临床信息快讯,2007:43.
