成人肝移植患者围手术期营养管理证据总结
2024-03-20戚熠谭艳李旭英李金花胡美华刘佳惠
戚熠 谭艳 李旭英 李金花 胡美华 刘佳惠
肝移植是目前终末期肝病最有效的治疗方式,由于肝脏是身体营养和物质代谢中心,其功能损害会引起身体不同程度的能量代谢障碍,因此,终末期肝病患者在肝移植等待期间往往会出现营养不良、肌肉减少症及活动无耐力等问题[1]。在肝移植患者中,营养不良的发生比例从肝脏代偿期的20%到失代偿期的60%~99%不等[2]。围手术期的创伤应激、免疫抑制剂应用、麻醉等原因,导致患者营养摄入不足与分解代谢增加,进一步加重负氮平衡和营养不良,导致肝移植患者术后门脉高压相关并发症的发生率更高,感染风险增加,等待周期延长和总死亡率增加,住院时间、重症监护室住院时间、插管时间更长[3-5]。有研究表明,早期发现肝移植患者营养不良状况并给予相应的营养支持,可减少并发症和病死率[6]。欧洲肝脏研究协会[7]在2018 年发布了指南,对肝移植患者的营养管理提出了指引,中华医学会器官移植学分会围手术期管理学组[8]在2021 年发布了专家共识,但都缺乏系统的营养管理策略,内容不够聚焦,不利于医护人员快速、全面地获得相关信息,科学性有待考究。本研究旨在通过循证的方法收集关于肝移植患者围手术期营养管理证据,提出相应的策略,减少并发症的发生,并改善肝移植患者的预后。
1 资料与方法
1.1 问题的确立
通过复旦大学循证护理中心PIPOST 工具[9],确定循证实践问题。针对的目标人群(Population)为成人肝移植围手术期患者,干预措施(Intervention)为营养管理策略,应用该证据的专业人员(Professional)为医护人员,关注的结局(Outcome)包括营养不良的发生率和非计划住院率等,证据的应用场所(Setting)包括医院、社区、家庭等,该证据的类型(Type of evidence)有计算机决策系统、证据总结、指南等。
1.2 检索策略
按照循证检索资源的“6S”模型逐层检索,检索了BMJ Best Practice、Up To Date、国际指南协作网、医脉通、英国国家卫生与临床优化研究所网站、苏格兰校际指南网、澳大利亚乔安娜布里格斯研究所(JBI)循证卫生保健数据库、欧洲临床营养与代谢学会(ESPEN)网站、中华医学会肠外肠内营养学会网站、美国肠外肠内营养学会网站、Web of Science、The Cochrane Library、PubMed、中国知网、万方数据库、维普数据库、中华医学期刊全文数据库等各大数据库与网站。中文检索词包括“肝移植”“营养/饮食/肠内营养/全肠外营养/膳食治疗”“围手术期/术前/术后/手术”等,英文检索词包括“liver transplantation”“nutrition/diet/enteralnutrition/parenteral nutrition/nutrition therapy”“perioperative period/preoperative period/postoperative period/surgery”等,检索时限截止至2023 年4 月1 日。以PubMed为 例,具体策略为:((“Liver Transplantation”[Mesh])OR(Liver Transplant*)OR(Liver Grafting)OR(Hepatic Transplant*)OR(LT))AND((Perioperative Period [MeSH Terms])OR(Preoperative Period)OR(Perioperative Period)OR(Postoperative Period)OR(Surger y))AND((Nutrition [MeSH Terms])OR(Nutrit*)OR(Diet*)OR(Enteral Nutrition)OR(Parenteral Nutrition)OR(Nutrition Therapy))。
1.3 文献纳入与排除标准
2 名研究者独立筛选文献,首先根据文章的标题和摘要剔除不符合纳入标准的文献,然后阅读全文进一步筛选,当2 人意见不一致时,与第3 名研究者讨论确定是否纳入文献。文章纳入标准:研究对象为成人肝移植围手术期患者;文章内容涉及营养管理;文章类型包括临床决策、指南、系统评价等中文或英文可阅读。文章排除标准:信息不完整或无法获取全文;简要版本或指南解读类文章。
1.4 文献质量评价
1.4.1 文献质量评价标准
评价临床实践指南质量采用AGREE II 系统[10],包括6 个领域、23 个条目和2 个总体质量评价条目。推荐等级分为A 级(6 个领域得分均≥60%)、B 级(得分≥30%的领域数≥3 个,但有<60%的领域)和C级(得分<30%的领域数≥3 个)[11]。系统评价和专家共识均采用澳大利亚JBI 循证卫生保健中心的评价工具(2016 版)。系统评价包括11 个条目,专家共识包括6 个条目[12]。
1.4.2 文献质量评价过程
2 名经过系统循证培训的评价人员独立进行文献质量评价,并进行核对。对于评价者意见不同的地方,通过讨论达成一致。如果意见无法达成一致,则与第3 名研究者讨论并做出决定。
1.5 证据提取、整合与分级
2 名研究者提取纳入文献的信息,英文内容翻译成中文后,经2 名营养管理护理专家审校,确定最佳翻译稿,形成中文版汇总初稿,随后由1 名循证护理专家、2 名营养管理专家、2 名临床护理管理者通将汇总的证据划分各个主题,而后由2 名研究者对证据进行整合和归类。最终,采用JBI 证据预分级及证据推荐系统形成推荐意见[13]。
2 结果
2.1 纳入文献一般特征
初步检索获得相关文献2 682篇,去除重复文献后剩余1 987 篇,阅读标题和摘要后获得109 篇文献,阅读全文及质量评价后最终纳入文献11 篇,包括指南7 篇[7,14-19]、专家共识3 篇[8,20-21]、系统评价1 篇[22]。纳入文献的一般特征,见表1。
2.2 文献质量评价结果
2.2.1 指南质量评价结果
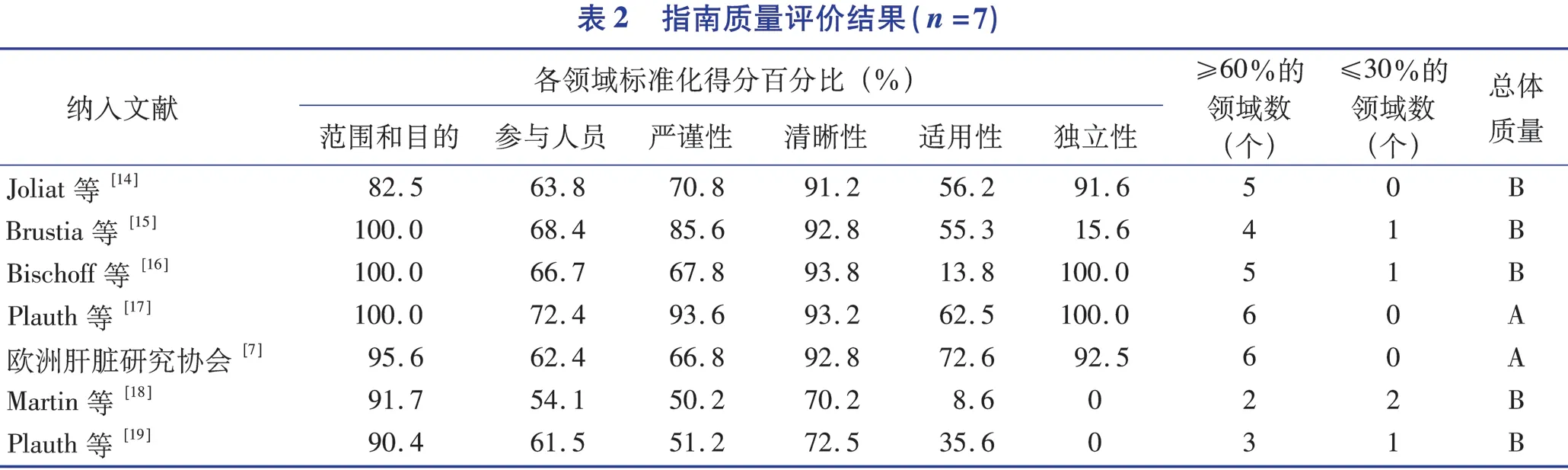
本研究共纳入指南7 篇,经评价,2 篇指南总体质量为A 级,5 篇为B 级,具体质量评价结果见表2。
2.2.2 系统评价质量评价结果
Langer 等[22]的研究质量评价结果显示,所有条目均符合要求,研究设计完整,质量高,纳入本研究。
2.2.3 专家共识质量评价结果
共纳入3 篇专家共识[8,20-21],所有条目的评价结果均符合要求,整体质量高,纳入本研究。
2.3 证据描述及汇总
最终从营养风险筛查与评估、骨骼肌减少症的筛查、体质量管理、术前营养管理、术后营养管理、院外随访6 个方面总结出20 证据,采用2014 版的JBI 证据预分级及推荐级别系统,将证据等级分为5 级。详见表3。
3 讨论
3.1 应科学使用营养风险筛查工具,早期识别营养风险
营养状态评估是营养干预的前提和重要步骤。早期筛查肝移植患者的营养风险,并进行适当的营养治疗,对患者有益,可延缓营养不良的发生和改善预后[23]。NRS-2002是常用的营养风险评估工具[24],但肝病患者存在腹水和水肿,限制了体质量和BMI 的应用,因此,有一定局限性[25]。RFH-NPT 则是一种简单、快捷、有效的营养风险筛查工具,已在英国多家医院进行验证,并被推荐在肝硬化患者中更广泛地使用[26]。这是一种专门针对肝硬化患者的营养风险筛查工具,但目前推广应用有限。肖慧娟等[27]将RFHNPT 与NRS-2002 在肝硬化住院患者营养风险筛查中比较得出RFHNPT 筛查营养风险阳性率显著高于NRS-2002,说明RFH-NPT 比 NRS-2002 对肝硬化患者的营养风险筛查更为敏感。另外SGA 法因明显的腹水、四肢水肿和利尿剂的使用而变得不够精准,人体测量学指标包括体质量指数、上臂围、三头肌皮褶厚度和上臂肌围以及实验室的指标(血红蛋白、血清白蛋白、淋巴细胞总数等)等客观营养评定指标由于肝移植患者肝功能差,合成内脏蛋白的能力降低,并且存在组织水肿和胸腔积液、腹水情况,导致应用受到限制[28]。因此由于各种营养评价方法存在不同程度的局限性,建议临床根据患者的实际情况应用合适的营养评估工具,动态评估,避免漏诊。
3.2 应重点筛查肝移植患者骨骼肌减少症,甄别高危人群
骨骼肌减少症是全身骨骼肌量和肌力减退的综合征,对终末期肝病和肝移植预后不良预测起重要作用,发生骨骼肌减少症患者的肝性脑病发生率、等待移植期间高病死率、肝移植后病死率增高,生活质量差,住院和重症监护病房治疗时间延长,肝移植后感染发生率高以及总体医疗费用增加[28]。通常采用握力、放射学方法进行筛查。当患者握力男性<25 kg,女性<18 kg,CT 图像第三腰椎平面骨骼肌指数,成年男性低于50 cm2/m2,成年女性低于39 cm2/m2时,即可判断患者有骨骼肌减少症的风险,此方法客观、可定量,但在临床实践中应考虑到性别、年龄和种族等因素的影响[29-30]。对骨骼肌减少症进行诊断,有利于提前制定营养干预方案,尽量减少肝移植相关并发症,优化患者的整体恢复过程。
3.3 应合理控制肝移植患者的体质量,防治术后并发症
长期以来,肝移植一直是治疗终末期肝病,肝硬化衰竭和原发性肝恶性肿瘤的金标准,肝移植不仅能延长患者的生命周期,也能提高患者的生活质量和心理健康水平,但由于器官的局限性和肝移植的复杂性,因此,必须仔细选择患者[31]。BMI>40 kg/m2在许多移植中心被认为是肝移植的相对禁忌证,因为肥胖患病率的增加给肝移植带来了许多挑战[32]。与非肥胖患者相比,肥胖的肝移植患者围手术期并发症的风险增加,长期生存率降低[33]。若BMI<18.5 kg/m2,可直接 判定为营养不良[8]。因此,临床中应注重对患者BMI 的判定,在患者没有液体潴留的情况下,BMI 足以识别肥胖(BMI ≥30 kg/m2)[34],在液体潴留的情况下,体质量需要通过评估患者的干重来纠正。有研究表明,当肝移植患者未处于失代偿肝硬化期时,应在营养师的干预下进行饮食调整或者通过运动、手术来进行减重[35]。但也有研究表明,中等水平的体育锻炼会增加肝硬化患者的门脉压力,潜在地增加静脉曲张患者出血的风险[36]。并且肝移植受者减重手术的时机选择仍有争议,肝移植术前行减重手术旨在优化患者在肝移植前的肥胖相关的医疗条件,然而,尝试在肝移植前进行减重手术因其并发症会进一步推迟移植,将减重手术与肝移植相结合的好处是可立即进行肝移植,避免了上述肝移植前的手术延误,减少住院时间,降低成本,减轻压力和疼痛,但易增加伤口并发症的风险[37]。
3.4 应合理选择患者术前的营养方案,保障能量摄入
肝移植患者术前因肝病末期、病史长、饮食摄入受限、吸收不良、合成代谢障碍、分解增加导致摄入的蛋白质和能量不能满足身体的需求,蛋白质-能量营养不良的发生率为18%~65%[38]。充足的蛋白供给可以改善营养不良和肌肉减少症,改善移植效果[39]。有证据证明,与标准饮食建议相比,在肝移植等待期间,在患者的日常饮食中添加富含特殊配方的饮料补充蛋白质、脂肪和碳水化合物能改善患者的营养状况[40]。但一项系统评价认为,以上结论仍没有强有力的证据表明这种干预可有效且长期影响肝移植患者术后的营养状态[22]。但有研究者提出,移植前应进行营养补充,因为可能会利于缩短住院时间,且没有伤害[20]。由于最新证据级别更高的指南推荐术前不使用特殊营养配方,故将证据13 列为推荐意见,因此,在应用该证据的过程中,应考虑患者的具体身体状况和经济条件,审慎地应用。术前禁食水时应遵循加速康复外科的原则,无胃肠道动力障碍患者术前6 h 禁固体饮食,术前2 h 禁流质,避免长期饥饿诱导肠道应激[41],在应用证据14 时,应评估患者的胃肠道功能。
3.5 应加强患者术后的营养支持,定期进行营养监测与随访
肝移植后,患者会发胖并发展成代谢综合征,代谢综合征是肝移植术后的常见并发症,是以肥胖症、糖尿病、高血压病、高脂血症等其中3 项及以上危险因素在个体内共同作用的结果,其并发症相关死亡占肝移植患者总病死率的21%,是肝移植术后远期死亡的主要原因之一[42],另外,术后患者的氮会大量流失,并在较长一段时间内保持负氮平衡,需要增加蛋白质或氨基酸供应,蛋白质或氨基酸供应达到1.0~1.5 g/kg[43],良好的营养可促进伤口愈合、恢复体质量、对抗感染。另外,也有证据证明,肝移植后患者的活动水平、生活质量和运动能力一般都未达到正常水平,但经过运动都改善了患者的生活质量,因此,除饮食指导,也应加强患者的运动指导[44]。移植后,与仅输注液体和电解质相比,术后肠外或肠内营养可减少呼吸机使用时间、ICU 住院时间,并降低细菌感染和胆管并发症的风险[45],在肠外营养和早期肠内营养的直接比较中,两种策略被证明在维持营养状态方面同样有效,但肠内营养降低了并发症发生率和费用[46]。一项Meta 研究结果显示,益生菌的使用能减少术后的感染,推荐临床使用[47]。术后肝移植患者大多需要终身服用免疫抑制剂,并定期监测肝功能和免疫抑制剂血药浓度等项目,医师通过定期随访了解受者康复情况,并根据相关指标变化做出综合判断,从而制订下一步治疗方案[48],除常规的生化和影像学检查外,应对患者进行饮食指导,有效控制肝移植术后的代谢综合征的发生。
4 小结
本研究总结了成人肝移植围手术期营养管理的证据总结,可为临床实践提供参考。然而,纳入的文献大多来自国外,且患者存在个体差异性,建议在实践的过程中,谨慎地使用证据。
