理肺散提取物乙酸乙酯层的化学成分及其对RGC-5细胞损伤的保护作用研究*
2024-02-25王钰君尹国平胡昌华曾令高熊有明
王钰君,尹国平,胡昌华,曾令高,熊有明△
(1.西南大学药学院·黄连开发与利用教育部工程研究中心,重庆 400716;2.重庆市食品药品检验检测研究院·国家药品监督管理局麻醉精神药品质量监测重点实验室,重庆 401121)
理肺散为茜草科耳草属植物攀援耳草Hedyotis scandensRoxb.的全株,又名凉喉茶、接骨丹等,为我国白族、傣族、纳西族、傈僳族等民间常用药食两用植物。理肺散性凉,味苦,归肺、肾经,具有清热解毒、理肺止咳、润肺化痰、接骨续筋等功效,主治肺结核、肺炎、支气管炎、咽喉肿痛、骨折等[1]。研究表明,耳草属植物的主要化学成分为黄酮类、环烯醚萜类、生物碱类等,其主要药理学活性为抗肿瘤、抗菌、镇痛、消炎、抗氧化、神经保护等[2]。理肺散用途广泛且资源丰富,其发挥作用的物质基础具有巨大的研究价值。但目前关于理肺散化学成分的研究仅有3篇文献报道,从其乙醇提取物中分离鉴定了28 个化合物,包括黄酮类6 个、三萜类6 个、甾体类1 个、酚酸类15 个[3-5]。本课题组前期对该植物全株的水提取物进行了系统的化学成分和抗结核活性研究,在此基础上,本研究中进一步对理肺散提取物乙酸乙酯层的化学成分进行研究,并以丙泊酚诱导的RGC-5细胞损伤为活性评价模型,探讨各化合物对RGC-5细胞损伤的保护作用。现报道如下。
1 仪器、试药与细胞
1.1 仪器
400 MHz 核磁共振仪(德国Bruker 公司);LC110 型制备型高效液相色谱仪(赛谱锐思<北京>科技有限公司);LC-20A 分析型和制备型高效液相色谱仪(日本Shimadzu公司);C18制备色谱柱(250 mm×10 mm,日本YMC 公司;250 mm × 20 mm,日本Shimadzu 公司);Varioskan LUX型多功能酶标仪(美国Thermo Fisher公司);MCO-15AC-SC型二氧化碳培养箱(日本Sanyo公司)。
1.2 试药
柱色谱硅胶(200~300 目,青岛海洋化工厂);甲醇(色谱纯,阿达玛斯试剂有限公司);乙酸乙酯、石油醚(分析纯,重庆川东化工<集团>有限公司);二甲基亚砜(DMSO,美国Sigma公司,批号为D2650);Dulbecco改良的Eagle 培养基(DMEM)/F12 培养基(批号为C11330500BT),胎牛血清(批号为10099-141),均购自美国Gibco 公司;胰蛋白酶(批号为C0201),青霉素-链霉素溶液(100X)(批号为C0222),CCK-8 试剂盒(批号为C0039),均购自上海碧云天生物技术有限公司;丙泊酚(美国Aspen 公司,批号为SA084);理肺散采自云南大理,经西南大学胡昌华教授鉴定为正品。
1.3 细胞
小鼠视网膜神经节RGC-5细胞(中国科学院细胞库,批号为BNCC359850)。
2 方法与结果
2.1 提取与分离
取理肺散干燥全草20 kg,粉碎,用盐酸水溶液(pH=5)加热回流提取3 次,每次2 h,浓缩得水提浸膏3 kg。药渣用95%乙醇加热回流提取2次,每次2 h,浓缩得醇提浸膏1 kg。将浸膏以1∶2(m∶V)的比例加水混悬,用氢氧化钠溶液调pH 至9~10,依次用乙酸乙酯和正丁醇萃取,分别得水提浸膏乙酸乙酯层140.0 g 和醇提浸膏乙酸乙酯层171.3 g。
水提浸膏乙酸乙酯层通过中性氧化铝色谱柱分离,利用石油醚-乙酸乙酯梯度洗脱,得7 个组分(Fr.A1~Fr.A7)。Fr.A1(10.6 g)经MCI柱色谱分离,得31个亚组分(Fr.A1.1~Fr.A1.31);Fr.A1.13经制备液相色谱(93%甲醇)分离,得化合物12(32.5 mg)。Fr.A3(12.1 g)经MCI柱色谱分离,得80个亚组分(Fr.A3.1~Fr.A3.80);Fr.A3.24 经制备液相色谱(27%甲醇)分离,得化合物14(10.2 mg);Fr.A3.27 经制备液相色谱(33%甲醇)分离,得化合物15(12.2 mg);Fr.A3.64 经制备液相色谱(66%甲醇)分离,得化合物11(5.1 mg);Fr.A3.76经制备液相色谱(67%甲醇)分离,得化合物1(6.7 mg)。Fr.A4(6.4 g)经MCI 柱色谱分离,得30 个亚组分(Fr.A4.1~Fr.A4.30);Fr.A4.13经制备液相色谱(41%甲醇)分离,得化合物3(7.4 mg);Fr.A4.16 经制备液相色谱(46%甲醇)分离,得化合物4(7.0 mg)和化合物5(16.0 mg);Fr.A4.21 经制备液相色谱(56%甲醇)分离,得化合物6(4.8 mg);Fr.A4.23经制备液相色谱(51%甲醇)分离,得化合物8(10.3 mg)。
醇提浸膏乙酸乙酯层通过硅胶色谱柱分离,利用石油醚-乙酸乙酯梯度洗脱,得10个组分(Fr.B1~Fr.B7)。Fr.B3(7.2 g)经MCI 柱色谱分 离,得34 个亚组分(Fr.B3.1~Fr.B3.34);Fr.B3.10经制备液相色谱(63%甲醇)分离,得化合物13(6.9 mg)。Fr.B4(13.4 mg)经MCI 柱色谱分离,得36 个亚组分(Fr.B4.1~Fr.B4.36);Fr.B4.24 经制备液相色谱(85%甲醇)分离,得化合物9(8.4 mg)和化合物10(18.4 mg)。Fr.B5(14.39 mg)经MCI 柱色谱分离,得60 个亚组分(Fr.B5.1~Fr.B5.60);Fr.B5.16 经制备液相色谱(48%甲醇)分离,得化合物7(6.7 mg);Fr.B5.37 经制备液相色谱(74%甲醇)分离,得化合物2(9.7 mg)。
2.2 结构鉴定
2.2.1 化合物1
黄色油状物。1H-NMR(CDCl3,400 MHz)δ:6.84(1H,d,J=7.9 Hz,H-5),6.78(1H,d,J=1.9 Hz,H-2),6.73(1H,dd,J=8.0,1.9 Hz,H-6),5.34(1H,m,H-14),5.29(1H,m,H-13),4.33(2H,d,J=5.6 Hz,H-7),3.85(3H,s,3-OCH3),2.18(3H,dd,J=9.2,6.0 Hz,H-9,15),1.96(2H,m,H-12),1.63(2H,m,H-10),1.36(2H,m,H-11),0.93(6H,d,J=6.8 Hz,H-16,17)。13C-NMR(CDCl3,100 MHz)δ:130.7(C-1),110.9(C-2),146.9(C-3),145.4(C-4),114.6(C-5),121.0(C-6),43.8(C-7),173.0(C-8),36.9(C-9),25.6(C-10),29.5(C-11),32.4(C-12),126.7(C-13),138.3(C-14),31.2(C-15),22.9(C-16),22.9(C-17),56.2(3-OCH3)。以上数据与文献[6]报道基本一致,故鉴定为capsaicin。
2.2.2 化合物2
黄色油状物。1H-NMR(DMSO-d6,400 MHz)δ:8.16(1H,t,J=5.9 Hz,4-OH),6.79(1H,d,J=1.9 Hz,H-2),6.68(1H,d,J=8.0 Hz,H-5),6.62(1H,dd,J=8.0,1.9 Hz,H-6),4.13(2H,d,J=5.8 Hz,H-7),3.72(3H,s,3-OCH3),2.09(2H,t,J=7.3 Hz,H-9),1.49(3H,m,H-10,16),1.23(8H,m,H-11,12,13,14),1.12(2H,q,J=6.7Hz,H-15),0.84(6H,d,J=6.6 Hz,H-17,18)。13C-NMR(DMSO-d6,100 MHz)δ:130.5(C-1),111.6(C-2),147.8(C-3),145.3(C-4),115.1(C-5),119.6(C-6),41.8(C-7),171.9(C-8),35.4(C-9),25.3(C-10),28.7(C-11),28.7(C-12),29.0(C-13),26.7(C-14),38.4(C-15),27.3(C-16),22.5(C-17),22.5(C-18),55.5(3-OCH3)。以上数据与文献[6]报道基本一致,故鉴定为 homodihydrocapsaicin Ⅰ。
2.2.3 化合物3
黄色油状物。1H-NMR(DMSO-d6,400 MHz)δ:8.59(2H,s,4-OH,4'-OH),6.63(4H,d,J=7.9 Hz,H-2,5,2',5'),6.50(2H,dd,J=7.9,1.9 Hz,H-6,6'),4.50(2H,t,J=5.0 Hz,9-OH,9'-OH),3.68(6H,s,3-OCH3,3'-OCH3),3.38(4H,dd,J=8.2,4.5 Hz,H-9,9'),1.82(2H,m,H-8,8')。13C-NMR(DMSO-d6,100 MHz)δ:132.2(C-1,1'),113.0(C-2,2'),147.2(C-3,3'),144.3(C-4,4'),115.0(C-5,5'),121.1(C-6,6'),34.0(C-7,7'),42.5(C-8,8'),60.2(C-9,9'),55.4(3-OCH3,3'-OCH3)。以上数据与文献[7]报道基本一致,故鉴定为secoisolari-ciresinol。
2.2.4 化合物4
无色油状物。1H-NMR(DMSO-d6,400 MHz)δ:8.76(2H,d,4-OH,4'-OH),6.82(1H,d,J=1.7 Hz,H-2'),6.74(1H,d,J=1.9 Hz,H-2),6.69(1H,s,H-6'),6.67(2H,m,H-5,5'),6.57(1H,dd,J=8.0,1.9 Hz,H-6),4.64(1H,d,J=6.3 Hz,H-7'),3.86(1H,dd,J=8.2,6.5 Hz,H-9),3.74(3H,s,3-OCH3),3.73(3H,s,3'-OCH3),3.65(1H,dd,J=10.8,7.3 Hz,H-9'),3.54(1H,dd,J=8.2,6.5 Hz,H-9),3.45(1H,dd,J=10.8,7.3 Hz,H-9'),2.82(1H,dd,J=13.5,4.8 Hz,H-7),2.57(1H,m,H-8),2.41(1H,dd,J=13.4,10.9 Hz,H-7),2.18(1H,p,J=6.9 Hz,H-8')。13C-NMR(DMSO-d6,100 MHz)δ:131.7(C-1),112.7(C-2),147.3(C-3),144.5(C-4),115.0(C-5),120.5(C-6),32.1(C-7),41.9(C-8),71.8(C-9),134.6(C-1'),110.0(C-2'),147.4(C-3'),145.5(C-4'),115.3(C-5'),118.1(C-6'),81.7(C-7'),52.3(C-8'),58.6(C-9'),55.6(3-OCH3),55.5(3'-OCH3)。以上数据与文献[8]报道基本一致,故鉴定为lariciresinol。
2.2.5 化合物5
无色油状物。1H-NMR(DMSO-d6,400 MHz)δ:6.95(1H,s,H-6),6.92(2H,d,J=6.0 Hz,H-2,2'),6.76(2H,s,H-5,6'),6.47(1H,d,J=15.9 Hz,H-7),6.21(1H,dt,J=15.9,5.3 Hz,H-8),5.46(1H,d,J=6.6 Hz,H-7'),4.09(1H,d,J=3.8 Hz,H-9),3.80(3H,s,3-OCH3),3.75(3H,s,3'-OCH3),3.66(2H,m,H-9'),3.45(1H,q,J=6.4 Hz,H-8')。13C-NMR(DMSO-d6,100 MHz)δ:132.3(C-1),110.4(C-2),147.5(C-3),146.4(C-4),115.3(C-5),118.5(C-6),87.2(C-7),53.0(C-8),62.9(C-9),129.5(C-1'),110.4(C-2'),143.6(C-3'),147.1(C-4'),130.5(C-5'),114.9(C-6'),128.9(C-7'),128.0(C-8'),61.6(C-9'),55.7(3-OCH3),55.6(3'-OCH3)。以上数据与文献[9]报道基本一致,故鉴定为dehydrodiconiferyl alcohol。
2.2.6 化合物6
白色固体。1H-NMR(DMSO-d6,400 MHz)δ:9.23(1H,s,4'-OH),7.96(1H,d,J=9.5 Hz,H-4),7.03(1H,d,J=1.9 Hz,H-5),6.92(1H,s,H-6'),6.88(1H,dd,J=8.1,1.9 Hz,H-5'),6.82(1H,d,J=8.1 Hz,H-2'),6.34(1H,d,J=9.5 Hz,H-3),4.99(1H,d,J=7.9 Hz,H-7'),4.32(1H,m,H-8'),3.78(6H,d,J=2.4 Hz,6-OCH3,3'-OCH3),3.67(1H,m,H-9')。13C-NMR(DMSO-d6,100 MHz)δ:160.0(C-2),113.2(C-3),144.8(C-4),100.8(C-5),145.3(C-6),137.1(C-7),131.7(C-8),138.0(C-9),111.2(C-10),126.7(C-1'),112.1(C-2'),147.6(C-3'),147.3(C-4'),115.4(C-5'),120.8(C-6'),76.2(C-7'),77.8(C-8'),59.8(C-9'),55.9(6-OCH3),55.8(3'-OCH3)。以上数据与文献[10]报道基本一致,故鉴定为cleomiscosin A。
2.2.7 化合物7
黄色油状物。1H-NMR(CDCl3,400 MHz)δ:9.81(1H,s,H-7'),7.39(2H,d,H-2',6'),6.88(3H,s,H-2,4,6),5.67(1H,d,J=7.1 Hz,H-7),3.97(2H,m,H-9),3.93(3H,s,3'-OCH3),3.85(3H,s,3-OCH3),3.69(1H,m,H-8)。13C-NMR(CDCl3,100 MHz)δ:132.2(C-1),119.7(C-2),147.0(C-3),114.7(C-4),146.3(C-5),109.0(C-6),89.7(C-7),52.9(C-8),64.1(C-9),131.6(C-1'),112.5(C-2'),145.3(C-3'),154.3(C-4'),129.0(C-5'),121.1(C-6'),190.8(C-7'),56.2(3-OCH3),56.3(3'-OCH3)。以上数据与文献[11]报道基本一致,故鉴定为curcasinlignan B。
2.2.8 化合物8
黄色油状物。1H-NMR(CDCl3,400 MHz)δ:6.56(4H,br,s,H-2,2',6,6'),5.51(2H,br,s,H-4,4'),4.71(2H,br,s,H-7,7'),4.26(2H,m,H-9,9'),3.88(14H,br,s,H-9,9',11,11',12,12'),3.07(2H,br,s,H-8,8')。13C-NMR(CDCl3,100 MHz)δ:132.3(C-1,1'),103.0(C-2,2',6,6'),147.4(C-3,3',5,5'),134.5(C-4,4'),86.3(C-7,7'),54.4(C-8,8'),72.0(C-9,9'),56.4(C-11,11',12,12')。以上数据与文献[12]报道基本一致,故鉴定为syringaresinol。
2.2.9 化合物9
白色粉末。1H-NMR(DMSO-d6,400 MHz)δ:5.15(1H,t,J=3.6 Hz,H-12),4.28(1H,s,H-3),1.08(3H,s,H-27),0.88(3H,s,H-30),0.86(3H,s,H-29),0.84(3H,s,H-25),0.71(3H,s,H-24),0.66(3H,s,H-23)。13C-NMR(DMSO-d6,100 MHz)δ:38.0(C-1),26.9(C-2),76.8(C-3),38.3(C-4),54.8(C-5),18.0(C-6),32.4(C-7),38.9(C-8),47.1(C-9),36.6(C-10),22.9(C-11),121.5(C-12),143.8(C-13),41.3(C-14),27.2(C-15),23.3(C-16),45.7(C-17),40.8(C-18),45.4(C-19),30.4(C-20),33.3(C-21),32.1(C-22),28.2(C-23),16.0(C-24),15.1(C-25),16.8(C-26),25.6(C-27),178.5(C-28),32.8(C-29),22.6(C-30)。以上数据与文献[13]报道基本一致,故鉴定为oleanolic acid。
2.2.10 化合物10
白色粉末。1H-NMR(DMSO-d6,400 MHz)δ:5.13(1H,s,H-12),3.00(1H,dd,J=10.3,5.6 Hz,H-3),2.11(1H,d,J=11.3 Hz,H-18),1.04(3H,s,H-23),0.92(3H,s,H-29),0.90(3H,s,H-27),0.87(3H,s,H-26),0.81(3H,s,H-30),0.75(3H,s,H-24),0.68(3H,s,H-25)。13C-NMR(DMSO-d6,100 MHz)δ:38.2(C-1),26.9(C-2),76.8(C-3),38.5(C-4),54.8(C-5),18.0(C-6),32.7(C-7),41.6(C-8),46.8(C-9),36.3(C-10),22.8(C-11),124.5(C-12),138.2(C-13),41.6(C-14),27.5(C-15),23.8(C-16),47.0(C-17),52.4(C-18),38.4(C-19),38.3(C-20),30.2(C-21),36.5(C-22),28.2(C-23),15.2(C-24),16.0(C-25),16.9(C-26),23.2(C-27),178.2(C-28),16.9(C-29),21.0(C-30)。以上数据与文献[14]报道基本一致,故鉴定为ursolic acid。
2.2.11 化合物11
白色固体粉末。1H-NMR(CDCl3,400 MHz)δ:8.21(2H,d,J=7.7 Hz,H-2',6'),7.63(1H,t,J=7.7 Hz,H-4'),7.50(2H,t,J=7.7 Hz,H-3',5'),7.10(1H,d,J=8.1 Hz,H-5),6.96(1H,d,J=2.0 Hz,H-2),6.90(1H,dd,J=8.1,2.0 Hz,H-6),3.82(3H,s,3-OCH3),3.72(3H,s,8-OCH3),3.64(2H,s,H-7)。13C-NMR(CDCl3,100 MHz)δ:132.8(C-1),113.7(C-2),151.3(C-3),139.2(C-4),122.9(C-5),121.6(C-6),41.1(C-7),171.7(C-8),129.5(C-1'),130.3(C-2',6'),128.5(C-3',5'),133.4(C-4'),164.7(C-7'),56.0(3-OCH3),52.1(8-OCH3)。以上数据与文献[15]报道基本一致,故鉴定为methyl 4-benzoyloxy-3-methoxybenzeneacetate。
2.2.12 化合物12
无色油状物。1H-NMR(CDCl3,400 MHz)δ:9.38(1H,s,H-20),6.64(1H,d,J=5.7 Hz,H-2),5.90(1H,d,H-3),5.10~4.98(2H,m,H-9,15),2.33(1H,d,J=17.8,1.5 Hz,H-5),2.16(4H,d,J=3.3 Hz,H-7,8),1.99(1H,d,J=17.8,1.5 Hz,H-5),1.92~1.73(3H,m,H-13,14),1.66(3H,s,Me-11),1.62(3H,s,Me-17),1.59(3H,s,Me-12),1.52(3H,s,Me-18),1.39~1.30(1H,m,H-13),1.16(3H,s,Me-19)。13C-NMR(CDCl3,100 MHz)δ:141.5(C-1),145.8(C-2),118.0(C-3),150.8(C-4),42.0(C-5),36.2(C-6),37.8(C-7),25.6(C-8),123.2(C-9),132.3(C-10),17.7(C-11),25.2(C-12),38.4(C-13),25.7(C-14),124.8(C-15),131.1(C-16),25.2(C-17),17.9(C-18),23.9(C-19),193.3(C-20)。以上数据与文献[16]报道基本一致,故鉴定为(R)-6-methyl-4,6-bis(4-methylpent-3-enyl)cyclohexa-1,3-dienecarbaldehyde。
2.2.13 化合物13
黄色固体。1H-NMR(DMSO-d6,400 MHz)δ:8.24(2H,dd,J=5.9,3.3 Hz,H-5,8),8.12(1H,d,J=8.4 Hz,H-4),7.75(2H,m,H-6,7),7.33(1H,d,J=8.5 Hz,H-3),4.02(3H,s,1-OCH3)。13C-NMR(CDCl3,100 MHz)δ:146.9(C-1),155.8(C-2),120.5(C-3),126.0(C-4),127.3(C-5),134.1(C-6,7),127.0(C-8),182.7(C-9),182.3(C-10),133.2(C-11),134.7(C-12),125.9(C-13),127.8(C-14),62.5(1-OCH3)。以上数据与文献[17]报道基本一致,故鉴定为2-hydroxy-1-methoxy-anthraquinone。
2.2.14 化合物14
白色固体。1H-NMR(DMSO-d6,400 MHz)δ:7.89(1H,d,J=9.4 Hz,H-4),7.03(1H,s,H-5),7.01(1H,s,H-8),6.23(1H,d,J=9.4 Hz,H-3),3.86(3H,s,Me-11)。13C-NMR(CDCl3,100 MHz)δ:160.7(C-2),112.5(C-3),144.3(C-4),111.9(C-5),143.9(C-6),151.9(C-7),100.0(C-8),148.3(C-9),111.5(C-10),56.1(C-11)。以上数据与文献[18]报道基本一致,故鉴定为isoscopoletin。
2.2.15 化合物15
白色固体。1H-NMR(DMSO-d6,400 MHz)δ:12.18(1H,s,NH-1),9.94(1H,s,CHO-10),8.28(1H,s,H-2),8.10(1H,d,J=7.8 Hz,H-4),7.51(1H,d,J=7.8 Hz,H-7),7.23(2H,m,H-5,6)。13C-NMR(CDCl3,100 MHz)δ:138.4(C-2),118.1(C-3),123.4(C-4),122.1(C-5),120.8(C-6),112.6(C-7),137.1(C-8),124.1(C-9),184.9(C-10)。以上数据与文献[19]报道基本一致,故鉴定为1H-indole-3-carboxaldehyde。
2.3 生物活性评价
细胞毒性筛选:将RGC-5细胞培养于含有10%胎牛血清的DMEM/F12培养基中,以每孔1×103个的密度接种于96孔板(每孔100µL),培养24 h后,将细胞分为空白对照组、溶剂对照组和化合物组,弃上清液,化合物组每孔加入100 µL 不同浓度(3.75,7.5,15,30 µmol/L)的待测化合物,培养结束后,每孔加入10 µL CCK-8溶液,将培养板置培养箱内孵育1~4 h。用酶标仪测定450 nm 波长处的吸光度(OD)值,计算细胞存活率。细胞存活率(%)=(OD化合物组-OD空白对照组)/(OD溶剂对照组-OD空白对照组)×100%。重复试验3 次。结果溶剂对照组的细胞存活率为100.00%;药物浓度为15µmol/L 时,化合物1,5,7-11,15 均表现出较好的细胞活力,其细胞存活率均大于86%;其他化合物在浓度为30µmol/L时也表现出较好的细胞活力,其细胞存活率均大于87%。故选择细胞存活率不低于85%的药物浓度对丙泊酚诱导的RGC-5 细胞损伤模型进行活性评价,化合物15在30 µmol/L 浓度时细胞存活率存在一定差异,故选择15µmol/L作为化合物15的给药浓度。详见表1。
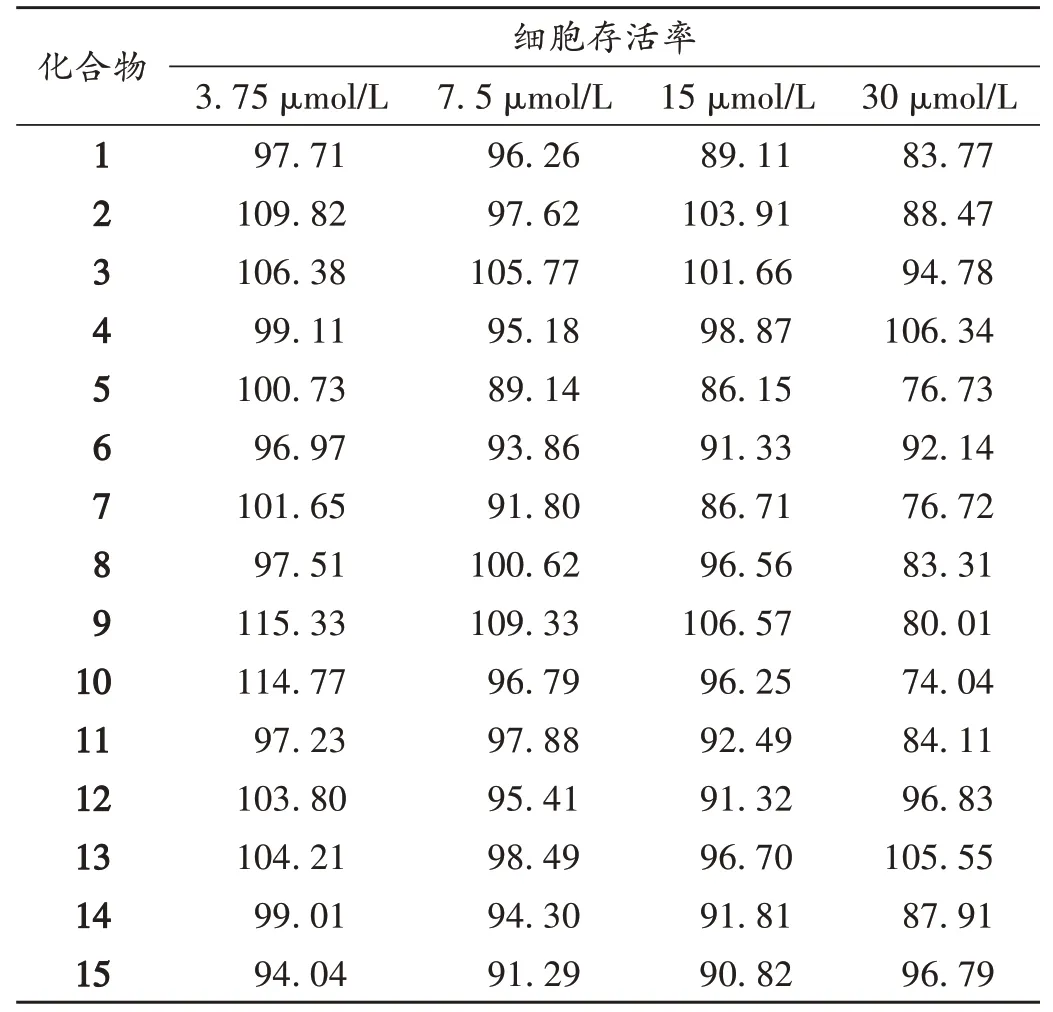
表1 不同浓度化合物对RGC-5细胞的毒性(%)Tab.1 Toxic effects of compounds with different concentrations on RGC-5 cells(%)
RGC-5 细胞损伤模型的保护作用活性评价:将RGC-5 细胞培养于含有10%胎牛血清的DMEM/F12培养基中,以每孔1×103个的密度接种于96孔板(每孔100µL),培养24 h后,将细胞分为空白对照组、溶剂对照组、模型组(400µmol/L丙泊酚)和化合物组(400µmol/L丙泊酚+15,30 µmol/L 待测化合物),弃上清液,按分组加入相应药物培养48 h,培养结束后,向每孔加入10µL CCK-8 溶液,将培养板置培养箱内孵育1~4 h。用酶标仪测定450 nm 波长处的OD值,计算细胞存活率。细胞存活率(%)=(OD化合物组-OD空白对照组)/(OD溶剂对照组-OD空白对照组)×100%。重复试验3次。结果与溶剂对照组比较,模型组细胞出现明显病理改变,细胞存活率显著下降(100.00%比76.27%);化合物1,4,6-8 对丙泊酚诱导的RGC-5 细胞损伤均表现出一定的保护活性,其中化合物4,7 最强,分别使RGC-5 细胞的活力增加15.89%,13.09%。详见表2。
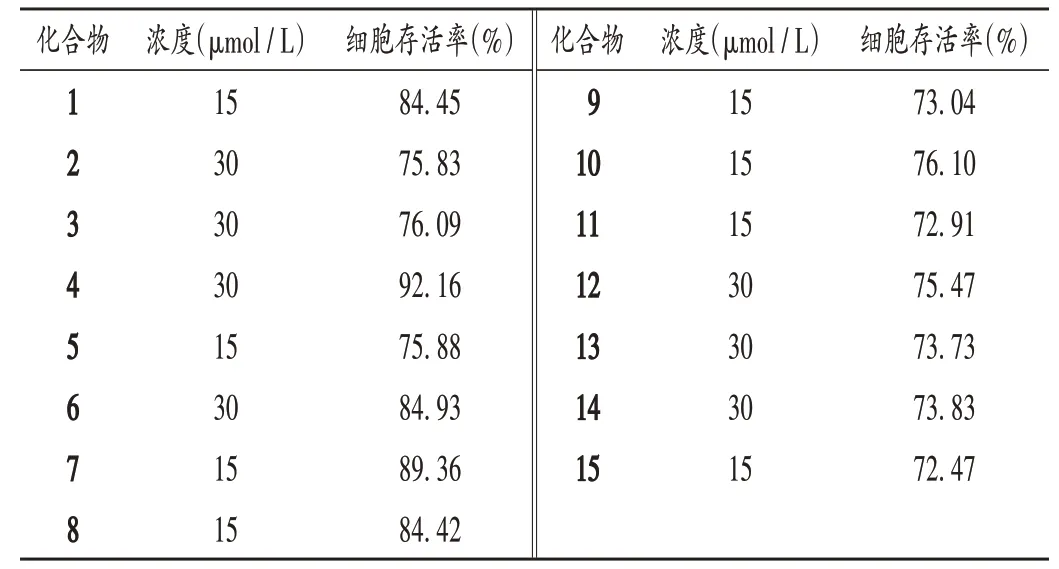
表2 不同化合物对丙泊酚诱导的RGC-5细胞损伤的保护活性Tab.2 Protective effects of different compounds on propofol-induced RGC-5 cell injury
3 讨论
理肺散作为民间常用药食两用植物,应用广泛,资源丰富,是重要的民族药。但目前对理肺散的研究较少,该资源未能被有效开发与利用。本研究中理肺散提取物的乙酸乙酯层经正相硅胶柱和MCI 柱等现代柱色谱技术进行分离,采用制备型高效液相色谱仪进行纯化,应用核磁共振法对化合物进行结构鉴定。最终共分离鉴定出15个化合物,分别为capsaicin(化合物1)、homodihydrocapsaicin Ⅰ(化合物2)、secoisolariciresinol(化合物3)、lariciresinol(化合物4)、dehydrodiconiferyl alcohol(化合物5)、cleomiscosin A(化合物6)、curcasinlignan B(化合物7)、syringaresinol(化合物8)、oleanolic acid(化合物9)、ursolic acid(化合物10)、methyl 4-benzoyloxy-3-methoxybenzeneacetate(化合物11)、(R)-6-methyl-4,6-bis(4-methylpent-3-enyl)cyclohexa-1,3-dienecarbaldehyde(化合物12)、2-hydroxy-1-methoxy-anthraquinone(化合物13)、isoscopoletin(化合物14)、1H-indole-3-carboxaldehyde(化合物15)。其中,化合物1-7 为首次从耳草属中分离发现,化合物9-10,13 为首次从理肺散中分离发现。以丙泊酚诱导的RGC-5细胞损伤为活性评价模型,采用CCK-8 法评估各化合物对RGC-5 细胞的保护作用,活性评价结果显示,化合物1,4,6-8对丙泊酚诱导的RGC-5细胞损伤均表现出一定的保护活性,其中化合物4、化合物7活性最强,为理肺散的进一步开发和利用奠定了基础。
