Tb掺杂Bi2WO6降解盐酸四环素性能
2024-01-23徐梦颖王洁溪余超翼
胡 鑫, 王 晟, 徐梦颖, 王洁溪, 薛 峰, 汪 雨, 余超翼
(南京工业大学 化工学院,江苏 南京 211800)
Bi2WO6
易溶于水且难以降解的盐酸四环素已成为影响生态平衡和人体健康的一个重要问题。各种传统方法,如,生物降解[1]、吸附法[2]、高级氧化技术[3]和光催化技术[4]等已被证明可有效去除环境中的盐酸四环素,但其具有去除效率低、处理周期长和容易造成二次污染等问题。光催化技术因其高去除率和可利用太阳能绿色环保等优点成为一种很有前途的盐酸四环素处理技术。TiO2等传统光催化剂因可见光利用率较低、光生电子-空穴对的分离效率低等问题限制了它们的应用[5],因此开发一种具有更高光催化活性的光催化剂十分必要。
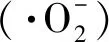
笔者通过水热法制备Tb离子掺杂的Bi2WO6(Tb-BWO),以提高Bi2WO6在可见光下的光催化性能。将Tb-BWO作为光催化剂降解盐酸四环素,探讨Tb-BWO的光催化降解性能、机制。
1 实验
1.1 Tb-BWO的制备
将Bi(NO3)3·5H2O和Tb(NO3)3·6H2O加入体积分数为10%的硝酸水溶液中得到溶液A,然后将Na2WO4溶解在去离子水中得到溶液B,将溶液B滴加入溶液A中形成前驱体溶液。将前驱体溶液转移到100 mL聚四氟乙烯内衬的高压反应釜中,以180 ℃水热处理20 h,待冷却至室温后水洗、干燥得到摩尔分数为x的Tb-Bi2WO6,标记为xTb-BWO。为了对比,前驱体溶液制备过程中不加Tb(NO3)3·6H2O制得Bi2WO6,标记为BWO。
1.2 光催化剂的性能表征
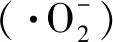
1.3 光催化活性评价
催化剂的光催化活性通过间歇式光催化反应器中250 W的氙灯冷光源(MCL-300X型,南京建盈展驰光电科技有限公司)模拟太阳光光催化降解盐酸四环素(TCH)进行评价。将50 mg光催化剂分散于100 mL TCH溶液(20 mg/L)中,避光搅拌30 min使其达到吸附-脱附平衡。光照后,每30 min取样,通过上海美普达公司的 UV6100 型紫外-可见分光光度计测量试样在356 nm波长的吸光度以分析盐酸四环素质量浓度变化。降解率η计算为
(1)
式中:ρ0和ρ分别为光照前后盐酸四环素水溶液的质量浓度,mg/L。
2 结果与讨论
2.1 Tb-BWO的表征
2.1.1 结构分析
图1(a)为BWO和Tb-BWO光催化剂的XRD图。从图1(a)中可以看出,BWO试样的特征峰对应于正交晶相的Bi2WO6,与标准卡片JCPDs 39—0256一致。不同掺杂量的Tb-BWO试样的XRD图中没有出现新的特征峰,这意味着低浓度Tb离子的掺杂不会产生新的晶相。图1(b)为不同掺杂量的Tb-BWO光催化剂的晶面(131)d XRD图。由图1(b)可知,在2θ为28.32°处归属于晶面(131)的衍射峰,与BWO相比,Tb-BWO在该处的衍射峰往2θ更高的方向移动,这表明Tb离子成功引入Bi2WO6的晶格中。BWO和Tb-BWO的晶格参数a、b、c和晶胞体积V的计算结果列于表1。从表1中可以看出,掺杂了Tb离子后,BWO的晶胞常数与体积减小,这可能是由于Tb3+的离子半径(0.092 3 nm)小于Bi3+的离子半径(0.103 nm),Tb3+掺杂进Bi2WO6时,取代了Bi3+,导致了晶胞常数与体积减小。

表1 结构参数计算汇总

图1 BWO和Tb-BWO的XRD图和晶面(131)的XRD图Fig.1 XRD patterns and (131) crystal plane peak for BWO and Tb-BWO
为了更加深入地分析Tb-BWO表面元素组成和化学状态,对1.2Tb-BWO进行了光电子能谱分析。图2(a)中BWO的O 1s的峰可拟合成结合能,分别为530.1、530.8和532.5 eV的3个独立峰,分别对应于(Bi2O2)2+层状结构中的Bi—O键、羟基和缺陷氧[11]。1.2Tb-BWO的O 1s中归属于缺陷氧的特征峰的结合能从532.5 eV偏移到532.1 eV,这可能归因于Bi—O—Tb键的形成。由图2(a)还可以看出,1.2Tb-BWO的O 1s中归属于缺陷氧的特征峰的面积高于BWO的O 1s中归属于缺陷氧的特征峰的面积,说明Tb离子掺杂增加了BWO晶格中的缺陷氧含量。图2(b)为Tb元素的高分辨率XPS图谱。从图2(b)中可以看出,1 236.9和1 270.8 eV的结合能的峰分别对应于Tb4+氧化态的Tb3d5/2和Tb3d3/2,1 221.8、1 256.7和1 284.4 eV的结合能的峰分别归属于Tb3+氧化态[12]。结合XRD和XPS分析的结果和讨论,可以表明试样1.2Tb-BWO已经成功制备。

图2 BWO和1.2Tb-BWO的XPS图谱Fig.2 XPS spectra of BWO and 1.2Tb-BWO
2.1.2 形貌分析
图3(a)—3(b)分别为BWO和1.2Tb-BWO的SEM图。从图3(a)—3(b)中可以看出,BWO和1.2Tb-BWO均呈现出纳米薄片和纳米板叠堆在一起的形貌,这表明Tb离子掺杂进入Bi2WO6晶格不会影响Bi2WO6的形态。
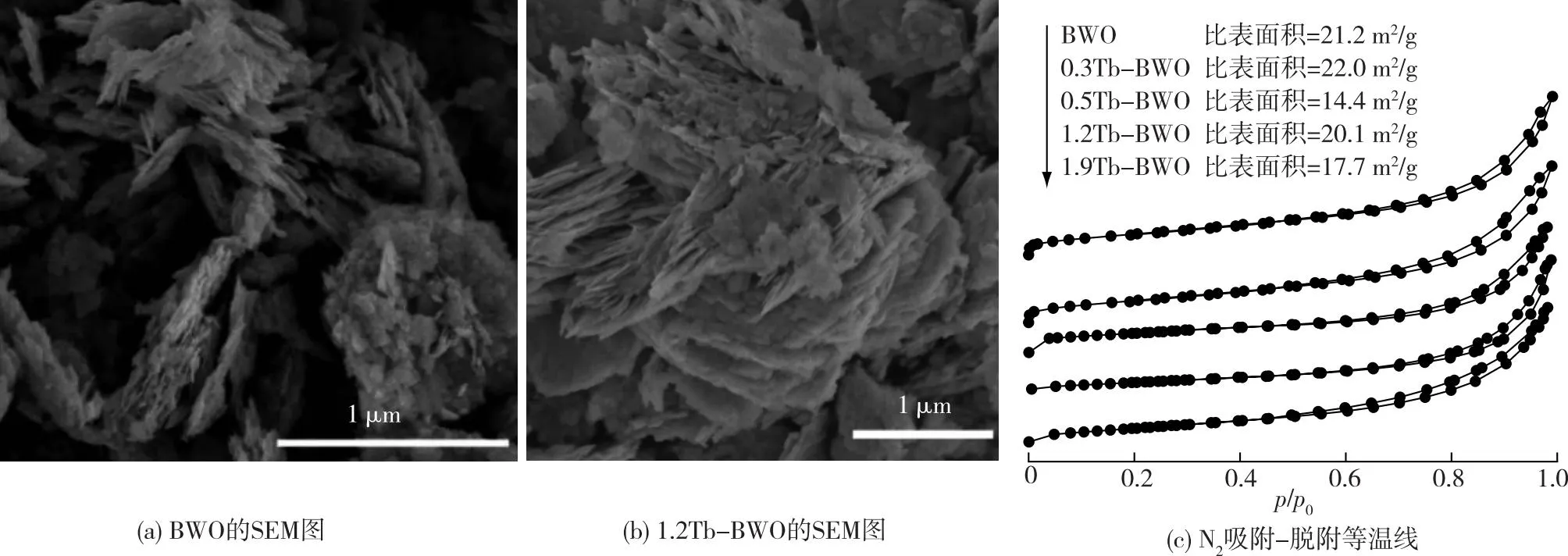
图3 BWO和1.2Tb-BWO的SEM图、BWO和Tb-BWO的N2吸附-脱附等温线Fig.3 SEM images of BWO and 1.2Tb-BWO, N2 adsorption-desorption isotherms of BWO and Tb-BWO
试样BWO和Tb-BWO的N2吸附-脱附等温线和比表面积如图3(c)所示。根据IUPAC分类,5个试样均呈现出Ⅳ型等温线,在0.6~1.0的相对压力范围内具有H3型磁滞回线,这反映了5个试样在纳米片之间存在狭缝的层状堆叠结构[13],与扫描电镜的结果一致。根据BET模型对吸附等温线计算得到5个试样的比表面积,结果见图3(c)。从图3(c)中可以发现,5个试样的比表面积值在14.4~22.0 m2/g,相差不大,表明Tb离子掺杂对Bi2WO6的比表面积没有明显影响。
2.1.3 光学性能和电化学性能分析
图4(a)为BWO和Tb-BWO的紫外-可见漫反射光谱。由图4(a)可知,所有试样均在250~450 nm表现出强吸收,表明这些试样具有较好的可见光吸收能力,且掺杂Tb离子后,4个Tb-BWO试样的可见光吸收区域无明显变化。用Kubelka-Munk方程可计算得到光催化剂的禁带宽度,对于间接跃迁的半导体Bi2WO6[14-15],以(αhv)1/2(α为吸收系数;h为普朗克常数;v为入射光频率)对hv作图(图4(b)),图4(b)中直线部分与X轴的交点的值即为禁带宽度Eg,BWO和Tb-BWO的禁带宽度列于表2中。从表2中可以看出,Tb离子掺杂Bi2WO6后,禁带宽度略有下降,这表明Tb离子掺杂导致Bi2WO6能带间产生了杂质能级。
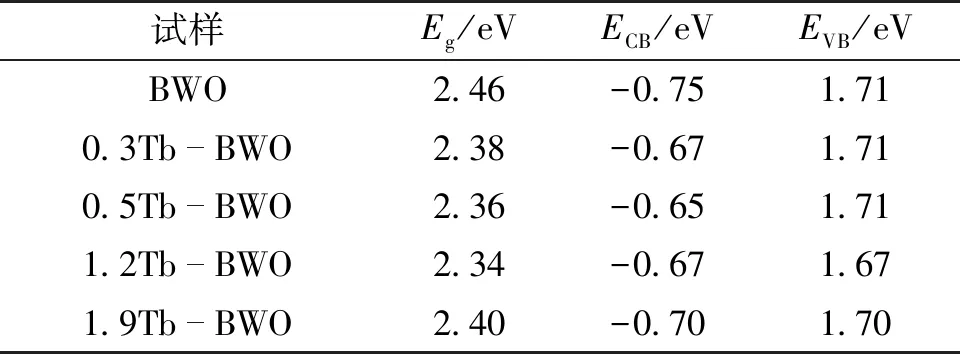
表2 禁带宽度、导带电位和价带电位数据汇总
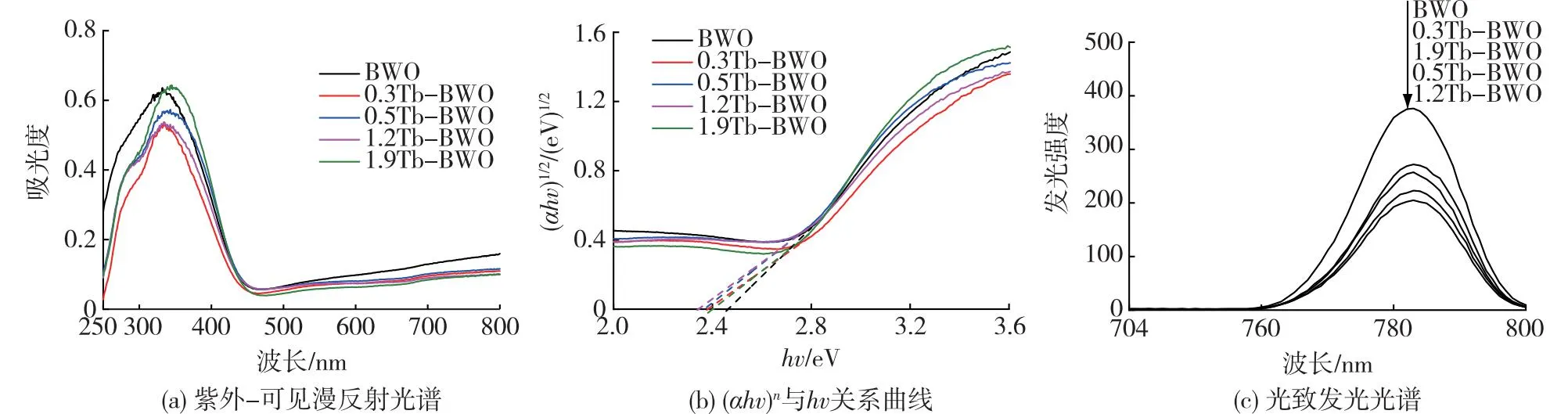
图4 BWO和Tb-BWO的紫外-可见漫反射光谱、(αhv)n与hv关系曲线和光致发光光谱Fig.4 UV-Vis DRS spectra, (αhv)n vs. hv plots and the PL spectra of BWO and Tb-BWO
光致发光光谱可以反映光催化剂的载流子复合率,通常来说,更高的载流子分离效率会造成更低的光致发光[16]。图4(c)为BWO和Tb-BWO试样在260 nm波长激发光下的光致发光光谱。从图4(c)中可以看出,与BWO相比,4个掺杂了Tb离子的Tb-BWO试样均表现出更好的载流子分离效率,并且随着Tb离子掺杂量的提升,载流子的分率效率呈现先增强后减弱的趋势,其中1.2Tb-BWO具有最高的载流子分离效率。
图5(a)为BWO和Tb-BWO试样的Mott-Schottky曲线。由图5(a)可知,BWO和Tb-BWO属于n型半导体[17-18]。通过Mott-Schottky曲线得到BWO和Tb-BWO试样的平带电位,从而得到导带电位[19],再根据ECB=EVB-Eg得出5个试样的价带电位(EVB),其中,禁带宽度为Eg;导带电位为ECB。计算结果汇总于表2中。同时从表2中可以看出,Tb离子掺杂引入的杂质能级主要位于导带附近,对价带附近的能级没有产生太大影响。

图5 BWO和Tb-BWO的Mott-Schottky曲线和瞬态光电流响应曲线Fig.5 Mott-Schottky plots and transient photocurrent response of BWO and Tb-BWO
BWO和Tb-BWO试样的瞬态光电流响应曲线如图5(b)所示。从图5(b)中可以看出,Tb-BWO相比于BWO均呈现出更高的瞬态光电流强度,即具有更高的光生电子-空穴对的分离效率[20],这预示着Tb离子的引入产生的缺陷对抑制载流子复合有着积极的作用。所有试样的光电流由大到小的顺序为1.2Tb-BWO、0.5Tb-BWO、1.9Tb-BWO、0.3Tb-BWO、BWO,该顺序表明随着掺杂Tb离子量的提升,Tb-BWO的光生电子-空穴对的分离效率呈现先增大后减小的趋势,且都高于BWO的光生电子-空穴对分离效率,其中1.2Tb-BWO的光生电子-空穴对分离效率最大。
2.2 Tb-BWO的光催化降解性能
2.2.1 Tb离子掺杂量的影响
图6(a)为BWO和Tb-BWO降解盐酸四环素水溶液的降解曲线。从图6(a)中可以看出,所有试样均有光催化活性,降解240 min后,Tb-BWO为光催化剂时,盐酸四环素的降解率比BWO为光催化剂时盐酸四环素的降解率显著提高,并且随着Tb离子掺杂量的提升,Tb-BWO的降解性能呈现先增大后减小的趋势,由大到小的顺序为1.2Tb-BWO、0.5Tb-BWO、1.9Tb-BWO、0.3Tb-BWO、BWO。BWO虽然有较窄的禁带宽度,但如图4(c)和图5(b)所示,其光生电子-空穴对容易复合,载流子利用效率低,因此其降解盐酸四环素的性能较低。当Tb离子的掺杂摩尔分数为1.2%时,光催化活性最高,在240 min后,降解率达到60.1%。

图6 BWO和Tb-BWO光催化剂降解盐酸四环素的降解曲线、不同牺牲剂对光催化降解盐酸四环素性能的影响、光催化体系中的ESR信号和可能的降解机制Fig.6 Photocatalytic degradation curves of TCH with BWO and Tb-BWO, impact of various scavengers on TCH degradation, ESR signals in the photocatalytic system, and a schematic of the potential mechanism

2.2.2 降解机制
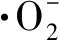

hυ→e-+h+
(2)

(3)

(4)
Tb4++e-→Tb3+
(5)
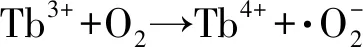
(6)
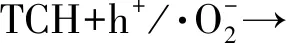
(7)
2.2.3 降解路径
为了研究1.2Tb-BWO对盐酸四环素的降解途径,采用LC-MS对1.2Tb-BWO降解盐酸四环素的中间产物进行检测。图7(a)为降解开始前盐酸四环素在m/z=445处有一个强烈的峰,与去质子化的盐酸四环素很好地吻合[22]。从图7(b)中可以看到,降解60 min后,m/z=477处出现了新的质量峰,这种分子量的增加可能是盐酸四环素发生取代反应引入了羟基的结果[23]。此外,在m/z=413、318、274、230、175、164、149、101、85和73处观察到了另外的10个低质荷比的峰,m/z为413的中间体的产生可能是盐酸四环素先失去一个甲基再经过脱水反应生成的[24],质荷比(m/z)为318的中间体的产生可能是盐酸四环素依次通过脱甲基、脱酰胺、二羟基化、脱羧、羟基化和氢化反应生成的[23],m/z为274的中间体的产生可能是318中间体继续发生脱乙酰化和氧化反应生成[24],m/z为230的中间体的产生可能是m/z为477的物质依次通过去甲基化、脱酰胺化、被氧化环裂解、脱羟基和脱羧生成的[23]。这些m/z分别为477、413、318、274和230的中间体进一步被降解生成m/z为175、164、149和101的较小分子,最后被分解为CO2和H2O等[25-26]。
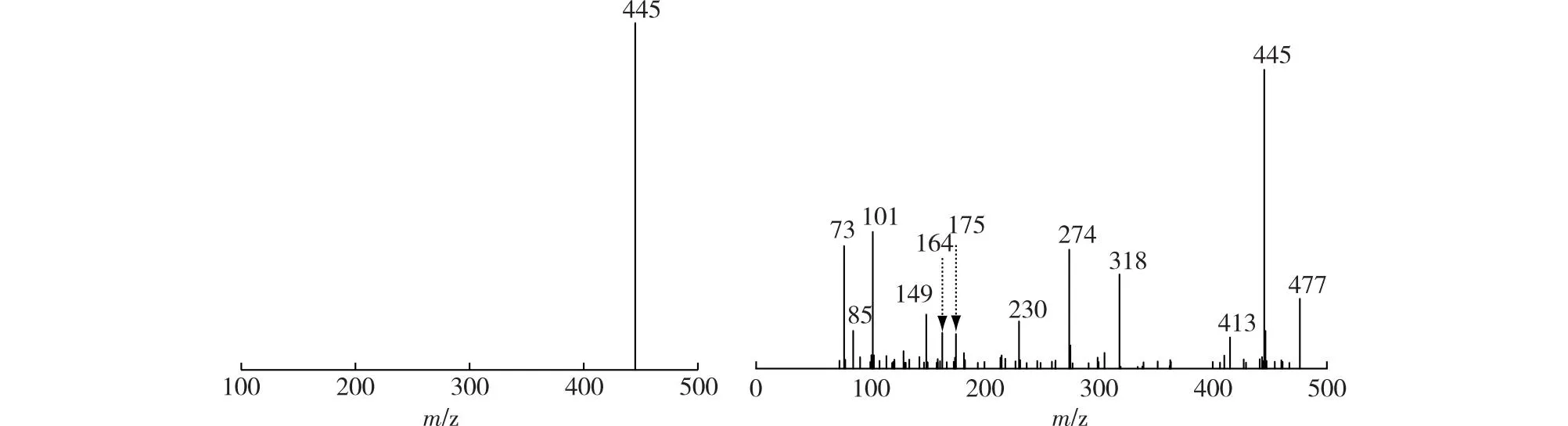
图7 LC-MS的检测结果Fig.7 LC-MS analysis results
以上分析表明盐酸四环素通过光催化被1.2Tb-BWO降解为一系列低分子量的中间体,最终这些中间体被分解为CO2和H2O等,1.2Tb-BWO降解盐酸四环素的可能途径如图8所示。

图8 盐酸四环素的可能降解途径Fig.8 Potential pathway for TCH photodegradation
2.2.4 光催化剂的稳定性
光催化剂的稳定性对于其应用有着重要的意义。为了研究1.2Tb-BWO的稳定性,进行了光催化活性的循环测试,结果如图9(a)所示。第二个循环后盐酸四环素光照240 min后的降解率从第一次的60.1%减少到26.0%。为了探索降解率降低的原因,收集试样离心沉降后于60 ℃烘干。对比反应前与反应后1.2Tb-BWO的红外波谱检测结果(图9(b))可知,反应后1.2Tb-BWO在1 100~1 300 cm-1之间出现了新的特征峰,说明试样表面吸附了有机物。试样反应前、后表面颜色的变化(图9(c))也证实了这点。

图9 1.2Tb-BWO的循环降解性能曲线、反应前后和乙醇洗涤后1.2Tb-BWO的FT-IR曲线、反应前后1.2Tb-BWO的照片Fig.9 Cyclic degradation curve for 1.2Tb-BWO, FTIR spectra before and after photocatalytic reaction and post-ethanol wash, and photographs of 1.2Tb-BWO before and after reaction
将反应后的1.2Tb-BWO分别用丙酮和乙醇超声洗涤,以通过洗掉吸附在光催化剂表面的盐酸四环素的方式提高1.2Tb-BWO的循环降解性能。结果表明,用丙酮洗涤的试样在光照240 min后对盐酸四环素的降解率为26.7%,没有明显提升。但用乙醇洗涤后的试样在光照240 min后对盐酸四环素的降解率提高到56.1%。将乙醇洗涤后的1.2Tb-BWO试样进行红外波谱检测如图9(b)所示。由图9(b)可知,乙醇洗涤后的1.2Tb-BWO试样的红外波谱与反应前相似。由于盐酸四环素不溶于丙酮,但溶于乙醇,说明造成循环降解性能降低的原因就是盐酸四环素吸附在光催化剂表面降低了光催化剂对光的吸收率,乙醇洗涤可恢复1.2Tb-BWO试样的光催化活性。3次循环后(每次都用乙醇洗涤),盐酸四环素的降解效率为54.2%,表明1.2Tb-BWO在光催化反应过程中具有良好的稳定性。
3 结论

3) Tb-BWO在光催化反应过程中具有良好的稳定性,但是每个循环后都要用乙醇将吸附在催化剂表面的盐酸四环素清洗干净。
