气相中碱基与核苷自由基的产生与结构研究
2024-01-20徐诗音焦鲁杨杜梦颖李树奇孔祥蕾
寇 敏,徐诗音,焦鲁杨,杜梦颖,李树奇,孔祥蕾,2,3
(1.南开大学化学学院,元素有机化学国家重点实验室,天津 300071;2.南开大学有机新物质创造前沿科学中心,天津 300071;3.南开大学化学学院,天津市生物传感与分子识别重点实验室,天津 300071)
自由基在涉及蛋白质和DNA等生物分子的反应中发挥着关键作用。核苷自由基在生物体内可能引发一系列重要的反应,如氧化、还原、自由基链式等,这些反应可以导致DNA和RNA的进一步损伤,从而对细胞的正常功能和遗传信息造成影响。近年来,有研究[1-3]表明,核苷自由基是RNA/DNA损伤的关键中间体。以氮为中心的核苷自由基通常是暴露于γ射线或氧化剂的DNA产生的反应中间体,但对其关键结构以及相关反应的细节仍不清楚。为研究反应中形成的瞬态物种,科学家们开发了多种产生核苷自由基的方法,然而,由于不同方法产生的自由基可能具有不同的位点,因此对产生的自由基及其异构体结构的精准确定非常重要,但也非常困难。
一般情况下,DNA电离通过氧化或还原途径进行,分别形成阳离子自由基和阴离子自由基中间体。以腺嘌呤为例,目前公认的碱基自由基形成机制有2种[4]:一种是通过氧化电离产生瞬态阳离子自由基,这些阳离子自由基通过电子或质子转移后进一步反应;另一种是通过还原电离捕获电子,形成短寿命的阴离子自由基,通过阴离子消除或溶剂质子化转化为自由基。在液相研究中,羟基自由基直接进攻核苷是一种常用的方法[5-7],可以选择性地产生羟基自由基,使其与核苷发生反应产生核苷自由基。此外,一些研究人员利用其他自由基氧化剂,如硫酸根自由基[8-9]、氯自由基[10]等,在适当的实验条件下诱导核苷的氧化反应产生核苷自由基,并利用瞬态吸收光谱对其结构进行研究。这些方法均具有较高的选择性和灵敏度,但需要准确控制实验条件和选择合适的试剂。
在凝聚相中产生的这些不稳定自由基很容易与所处的环境分子(如溶剂分子)发生一系列反应,使它们的结构分析更复杂。利用气相中的离子分子不受溶剂和抗衡离子效应干扰的优势[11-12],科学家们在气相中对相关自由基进行研究,通过比较实验结果与理论计算结果,能够从分子水平上更加清晰地获得它们的结构和动力学信息。近年来,随着质谱技术的发展,尤其是串联质谱法以及电喷雾电离(ESI)[13]的广泛应用,使气相自由基的相关研究取得了很大进步。
本文将聚焦基于质谱技术的碱基自由基与核苷自由基的气相研究,详细介绍它们的产生方式、研究方法以及结构研究进展。
1 气相中碱基核苷自由基的产生方法
传统的电子轰击电离(EI)虽然可以用来产生核苷自由基离子,但受产率的影响,难以进行后续的结构研究。为揭示核苷自由基的结构和性质,研究人员开发了一些新的自由基产生方法,如利用碱基与金属离子和相关配体形成的配合物通过碰撞诱导解离(CID)产生自由基离子[14-15],使用不同的前体分子并结合各种离子活化技术在气相中制备多种类型的自由基离子等,示于图1。

图1 气相中碱基、核苷和核苷酸阳离子自由基的形成方法Fig.1 Formation methods of cationic free radicals of base, nucleoside, and nucleotide in gas phase
1.1 EI源直接产生
最早,研究人员采用高能电子撞击电离(EI)技术产生核苷碱基的自由基阳离子,示于图1a。由于含氮的核苷碱基是富电子体,在初期形成核酸自由基时,电子空穴主要集中在碱基上,产生以碱基为中心的自由基。在气相中,核苷碱基的电离能量从低到高依次为鸟嘌呤(G)、腺嘌呤(A)、胞嘧啶(C)、尿嘌呤(U)[16-18]。有关核苷构建模块的报道大多数是基于高能电子碰撞电离方法研究碱基自由基阳离子的碎裂途径[19-20],然而,由于方法本身的局限性,缺乏对自由基深入的研究。
1.2 三元过渡金属配合物
O’Hair等[21]研究表明,一些核苷自由基阳离子可以通过ESI形成的三元金属配合物离子[M(L3)(N)]2+(M:Cu(Ⅱ),Pt(Ⅱ);L:dien,tpy,Nu:A,dA,G,dG,C,dC)的碰撞诱导解离引发分子内电子转移而产生,示于图1b[21]。随后,研究人员先后研究了脱氧胞苷-脱氧鸟苷配对、胞嘧啶、胸腺嘧啶、腺嘌呤[22-25]。以三联吡啶(terpy)作为配体,将ESI产生的[M(Ⅱ)(L3)N]2+(m/z211)作为前体离子,通过CID方法可以在其串联质谱图上观察到胸腺嘧啶自由基阳离子(m/z126),示于图2。
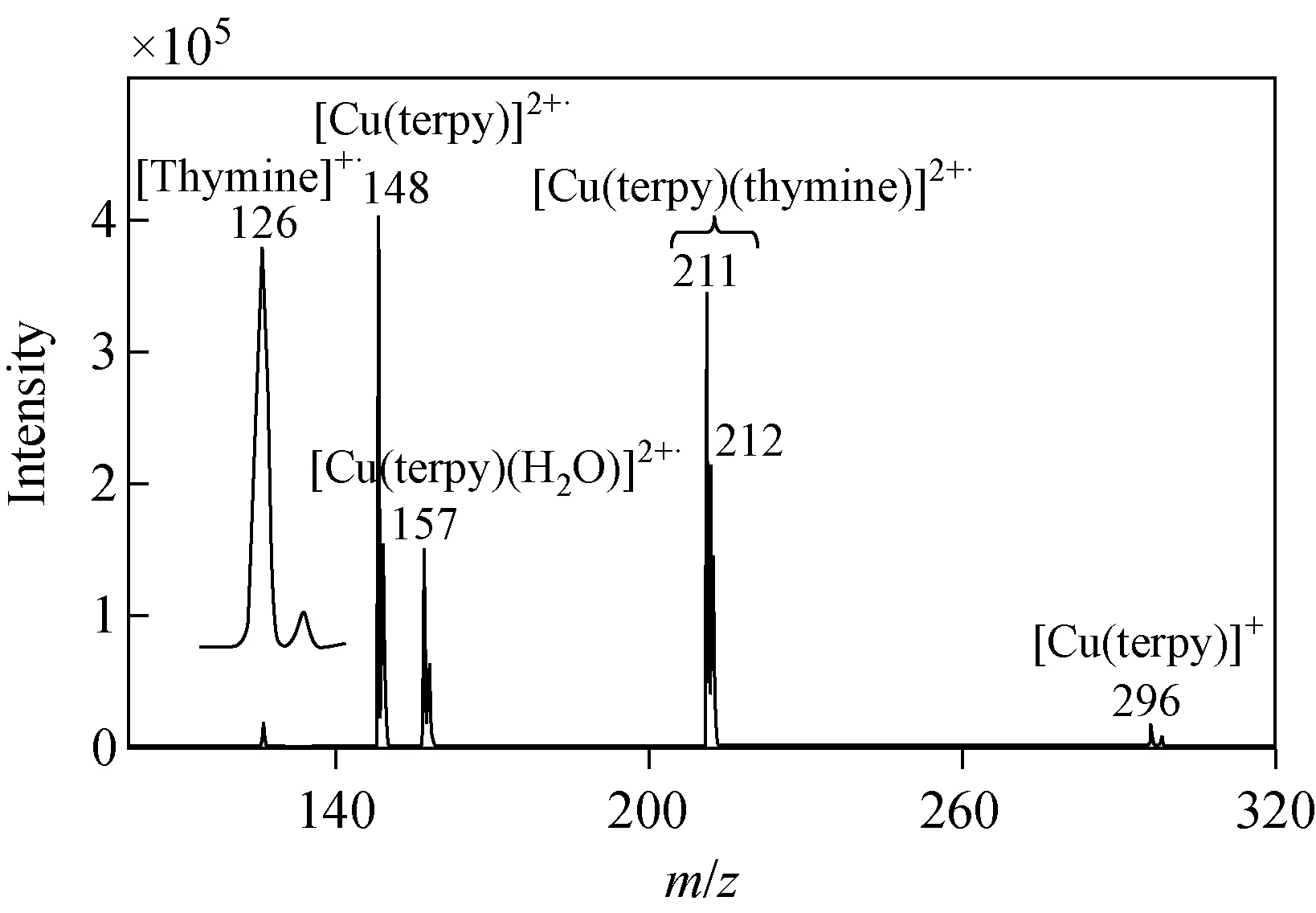
图2 [Cu(terpy)(thymine)]2+·离子的CID质谱图[24]Fig.2 Collision-induced dissociation mass spectrum of [Cu(terpy)(thymine)]2+·[24]
1.3 引入自由基引发剂


注:a.MS2m/z 570;b.MS3m/z 416;c.MS4m/z 291图3 多级串联质谱显示A+·的形成过程[26]Fig.3 Formation process of A+· by multistage tandem mass spectrometry[26]
1.4 电荷基团标记法



图4 m/z 414.5处(12++DBCE)的ETD-MS2质谱图(a),插图为m/z 469处1+·的CID-MS3质谱图;m/z 394.5处(22++DBCE)的ETD-MS2质谱图(b),插图为m/z 429处2+·的CID-MS3质谱图[28]Fig.4 ETD-MS2 spectrum of (12++DBCE) at m/z 414.5 (a), the inset shows the CID-MS3 spectrum of 1+· at m/z 469; ETD-MS2 spectrum of (22++DBCE) at m/z 394.5 (b), the inset shows the CID-MS3 spectrum of 2+· at m/z 429[28]
1.5 紫外光解离法
光解离法通过使用光能将分子激发到激发态进而生成自由基[33-34]。该方法具有灵活性和可扩展性,通过调整激光的波长、强度和脉冲宽度等参数,可以有效控制核苷自由基的产生。孔祥蕾课题组[35]通过在傅里叶变换离子回旋共振(FT-ICR)分析池中对锂离子化或钠离子化的2-碘代核苷阳离子进行UV照射,使其发生C—I键均裂,进而产生核苷及配对核苷自由基阳离子,示于图1f。将锂离子化或钠离子化的2-碘代核苷阳离子选择出来,然后引入紫外激光,在紫外光解离-串联质谱(UVPD-MS2)图中可以观察到相应的腺苷自由基阳离子[36],示于图5。该方法可以通过在不同位置灵活地引入C—I 键来制备不同自由基异构体。
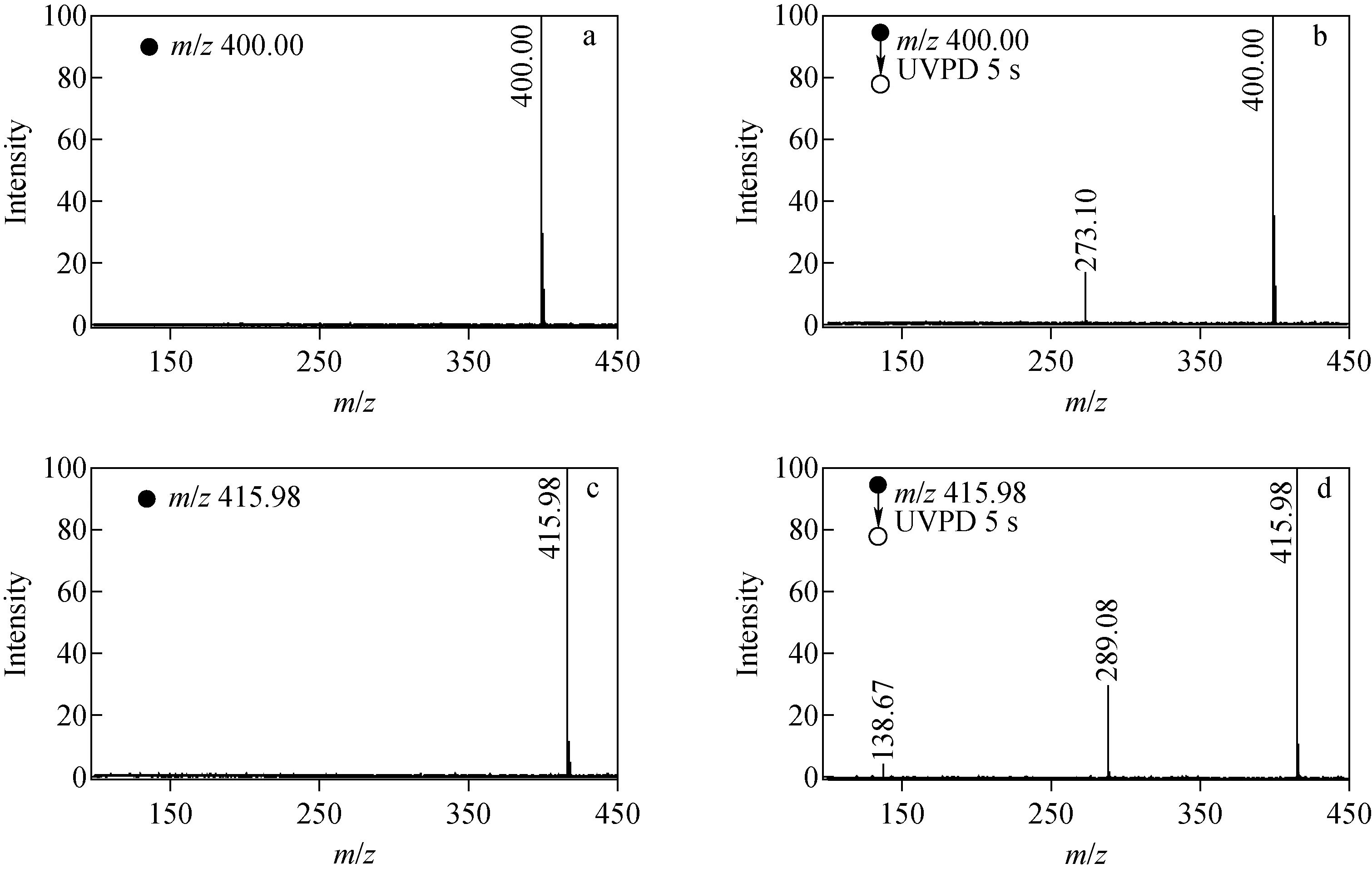
注:a.c.分别为质量选择后的母离子m/z 400.00、415.98;b.d.分别为m/z 400.00、415.98对应的紫外光解离质谱图(280 nm,照射5 s)图5 [IAde+Li]+(a,b)和[IAde+Na]+(c,d)的质谱图[36]Fig.5 Mass spectra of [IAde+Li]+ (a,b)和[IAde+Na]+ (c,d)[36]
1.6 中和-再电离质谱法
2 气相中碱基核苷自由基结构的研究方法
对于在气相中产生与DNA相关的自由基离子,可以在质谱仪中进行质量选择,并利用串联质谱和光解离光谱等方法进一步研究其结构、反应性和动力学。对目标自由基离子进行选择后,可以采用不同的离子活化方法进行活化,并进一步利用串联质谱研究裂解通道和产物。目前,离子活化手段主要有CID、红外多光子光解离光谱(IRMPD)以及紫外-可见光解离(UV-VisPD),采用可调谐激光可进一步获得自由基离子的IRMPD光谱或UVPD光谱。另外,还有一些结合质谱或串联质谱研究离子结构和动力学的方法,如与相关物种的反应质谱[4,37-38]、光电子能谱(PES)[39-45]以及离子碰撞横截面(CCS)测量[46-51]等,示于图6。其中,PES在自由基研究中的应用较广泛,但主要集中于小分子自由基,如丙烯自由基和苯胺自由基等[40-41,44];基于离子迁移的CCS测量已逐渐增多,但只有少数研究涉及若干阳离子自由基[46-51],这是因为自由基的不稳定性导致其在迁移过程中可能伴随CCS改变。

图6 基于不同串联质谱方法的碱基与核苷自由基的结构研究Fig.6 Structural study of free radicals of bases and nucleosides based on different tandem mass spectrometry methods
由于目前大部分商品化质谱仪不提供IRMPD和UVPD光谱的功能,为实现这一目标,需要对其进行改造。这要求所选择的质谱仪应具备较强的多级串联质谱能力或多种活化手段,以便能够产生相应的自由基离子。其中,基于离子阱的用于串联MSn-UVPD光谱学研究的实验装置主要有2种[52]:1种是基于Thermo LTQ质谱仪改造的,以实现将紫外光束引入线性离子阱中,改造的主要方法是在用于产生阴离子的辅助化学电离源的插入块中钻出直径为1 mm的孔,并使用1块在入射光束路径位置上有1个密封石英窗的铝板取代化学电离源的背面真空法兰,示于图7a;另1种是基于Bruker amaZon质谱仪改造的,将紫外光束引入3D离子阱中,在环形电极上钻出2个直径1 mm的孔(分别在顶部中心和底部中心),将改装后的环形电极正上方的真空法兰更换为紫外线窗口法兰,同时将2个反射镜固定在改装后的环形电极下方,示于图7b。

注:a.改造后的Thermo LTQ质谱仪;b.改造后的Bruker amaZon质谱仪;c.实验装置示意图;d,e.实验装置实物图,PG表示脉冲发生器,SC表示快门控制器图7 通过引入可调谐激光,可获取MSn-UVPD光谱的仪器装置(a,b)[52];通过向FT-ICR质谱仪引入可调谐激光,可获取MSn-UVPD和IRMPD光谱的仪器装置(c~e)[35] Fig.7 Instrument setups for obtaining MSn-UVPD spectra by introducing tunable lasers (a, b)[52]; instrument setup for obtaining MSn-UVPD and IRMPD spectra by introducing tunable lasers in a FT-ICR mass spectrometer (c-e)[35]
为了能够在同一台质谱仪上同时获得目标离子的红外及紫外光解离质谱与光谱,孔祥蕾课题组[35]将2束可调谐激光引入到1台磁场强度为7.0 T的FT-ICR质谱仪分析池中,示于图7c、7d。其中,1台是紫外-可见OPO激光器,可用于产生碱基自由基阳离子或核苷自由基阳离子,也可用于研究紫外光解离质谱与光谱;另1台是可调谐红外激光器,输出波长范围为2 700~3 800 cm-1,可以对自由基离子的红外光解离光谱进行研究。该装置虽然不具备ETD功能,但可以实现IRMPD、UVPD、CID等3种离子活化方法的任意结合,并共同作用于同一离子[11-12,35-36]。
3 气相中碱基核苷自由基结构的研究进展
近年来,科学家们基于以上自由基的产生方法和结构研究手段[22-32,36-38],并结合理论计算[53-54],对核苷自由基离子的结构和反应性进行了较全面的研究。核酸中的核苷是由嘌呤或嘧啶碱基与核糖或脱氧核糖缩合而成,一般来说,核糖分子中的碳原子(C1)与嘧啶分子中的氮原子(N1)或嘌呤分子中的氮原子(N9)之间形成糖苷键,称为核糖核苷。为方便文章阅读,对碱基及糖环上的原子进行编号,示于图8。

图8 碱基及糖环上的原子编号Fig.8 Reference numbers for the atoms on base and sugar rings
3.1 腺嘌呤以及腺苷自由基
Turecek等[25]利用三元过渡金属配合物通过碰撞诱导解离形成腺嘌呤(A)和9-甲基腺嘌呤的阳离子自由基,提出了腺嘌呤可能存在的异构体,并通过紫外-可见光谱和基于理论计算的振动光谱证明了离子化的嘌呤核碱基在气相中倾向于形成经典互变异构体结构;为了研究氢原子与腺苷结合位点,该课题组利用固定电荷基团标记法在气相中产生带有固定电荷基团的腺苷自由基,通过串联质谱、氘标记和UV/Vis作用光谱对其进行结构表征,发现带电荷标记的自由基在波长200~600 nm处有紫外吸收;同时还考虑了H原子结合在N1、C2、N3、N7、和C8这5种情况,通过开展氘标记实验,得出H原子仅结合在N1、N3和N7位点上;进一步与分子动力学、从头计算和激发态计算相结合,明确此处产生的腺苷自由基为N7氢原子加合物。Gerbaux等[4]利用NRMS方法产生腺嘌呤自由基,并将电喷雾电离、气相离子化学和碰撞电子转移相结合,发现N1氢原子加合物最稳定,被认为是DNA放射性损伤的初始中间体之一。
为了揭示碱金属离子与腺苷自由基的相互作用,孔祥蕾课题组[36]利用紫外光解离法产生锂离子化和钠离子化的腺苷自由基,示于图9,通过将红外多光子解离与理论计算相结合,确定了2种自由基最稳定的异构体,它们具有金属离子三配位模式的共同特征。对于这2种自由基物种而言,最低能量的异构体都经历了氢转移,但考虑到C—I均裂后直接形成的自由基具有一些相似的光谱特性,不能排除存在经直接均裂后生成的自由基异构体。

图9 [Ade+Li-H]+·(a)和[Ade+Na-H]+·(b)的红外实验光谱图[36]Fig.9 Experimental IRMPD spectra of [Ade+Li-H]+· (a) and [Ade+Na-H]+· (b)[36]
3.2 胸腺嘧啶以及胸苷自由基

3.3 鸟嘌呤以及鸟苷自由基
对于与腺嘌呤结构相似的鸟嘌呤(G)来说,Marek等[29]利用电荷标记法在气相中产生(G+H)·型鸟苷自由基,作者首先考虑了N1、N7、N3、O6这4种质子化位点,然后通过CID、UVPD和紫外-可见光谱与理论计算相结合,表征离子为N7-H鸟苷自由基互变异构体,发现可见光和近紫外区域的吸收带是H原子结合在N7位上特异性(G+H)·型鸟苷自由基的特征。
3.4 胞嘧啶以及胞苷自由基

对于1+·来说,通过监测m/z468(损失H)、358(损失胞嘧啶)、343(丢失甲基胞嘧啶)、272这4个主要的光碎片离子通道,从紫外光谱图中观察到最强的吸收在250 nm处,而在500 nm以上未观察到光解离,示于图10a。对于2+·来说,主要吸收带在250、300 nm处,有m/z428(损失H)、259、203等3个主要碎片离子通道,示于图10b。总体而言,胞苷自由基在动力学和热力学上比先前报道[27,29]的类似腺苷和鸟苷自由基更稳定。
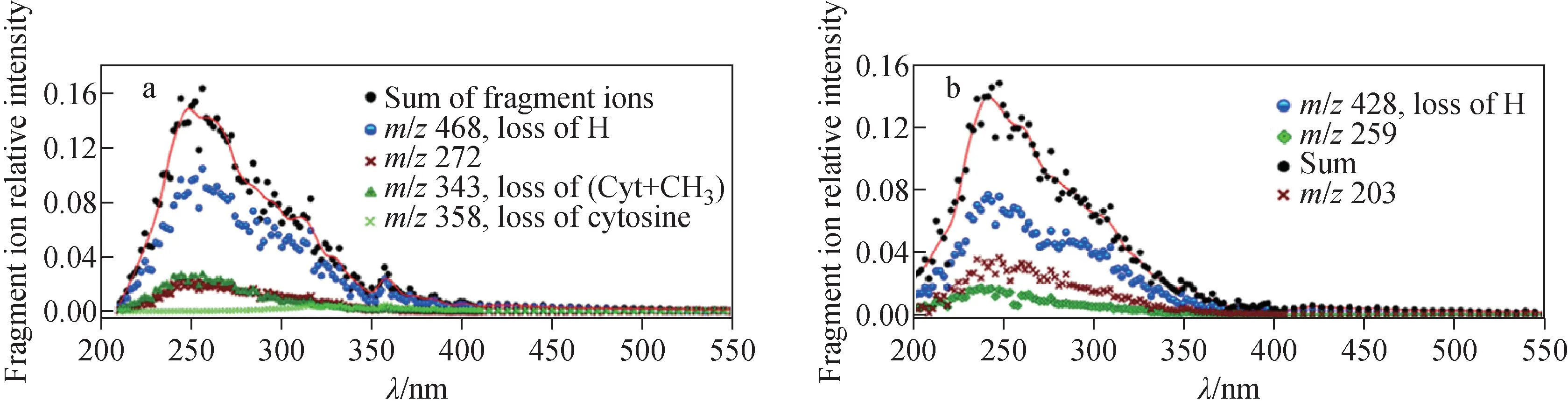
图10 1+·(a)、2+·(b)自由基离子的紫外光解离光谱图[28]Fig.10 Experimental UVPD spectra of 1+· (a) and 2+· (b) radical ions[28]

3.5 尿嘌呤以及尿苷自由基
3.6 鸟嘌呤-胞嘧啶配对
4 总结与展望
通过不同方法产生和研究核苷自由基,为深入了解其形成机制、反应性质以及生物学功能具有重要意义。质谱仪系统中的高真空为高反应性瞬态分子和自由基等提供了惰性环境,有利于它们的生成和结构研究。本文总结了近20年来基于质谱技术的碱基自由基与核苷自由基的气相研究,详细介绍了产生方式、研究方法以及结构研究进展,具体信息列于表1。从产生方法来看,除早期使用的EI法外,目前已有多种方法被应用,如基于碱基或核苷与CuⅡ和配体形成的三元过渡金属配合物或通过引入自由基引发剂的CID方法,基于电荷标记后的ETD方法,以及基于引入碳碘键后的UVPD法等。在结构研究中,既可以通过基于串联质谱的离子活化法获得解离碎片信息,又可以获得重要自由基离子的紫外-可见或红外光解离光谱,并与理论计算结果对比。基于以上方法,许多不同碱基与核苷自由基离子的结构得以明确,但其高活性自由基中间体的结构表征,以及不同自由基位点的自由基异构体的选择性产生仍具有挑战性。目前,相关自由基离子的研究主要集中于阳离子,而对于阴离子的产生和研究仍然非常困难,可以进一步利用反应质谱、光电子能谱以及CCS测量等方法实现对这些物种结构的精准分析。

表1 气相中碱基与核苷自由基的产生以及结构研究方法Table 1 Production and structural research methods of free radicals of bases and nucleosides in gas phase
