药食同源大品种茯苓中多糖与三萜研究进展*
2023-12-28浦雪梅何旭东何金彪刘志博陈晓娇
浦雪梅,李 雪,何旭东,何金彪,刘志博,徐 丹,陈晓娇,张 范,俞 捷
(云南中医药大学中药学院暨云南省南药资源可持续利用重点实验室 昆明 650500)
茯苓为多孔菌科真菌茯苓Poria cocos(Schw.) Wolf的干燥菌核,其味甘淡、性平,具有利水渗湿、益脾和胃及宁心安神等功效[1],常用于水肿尿少、痰饮眩悸和脾虚食少等[2]。茯苓作为中药和膳食补充剂已有两千多年的历史,有“十方九茯苓”之说,其中出自经典名方的有《金匮要略》的苓桂术甘汤、《医原》的霍朴夏苓汤以及《医宗金鉴》的除湿胃苓汤等。此外,被药典收录的复方有桂枝茯苓丸、桂枝茯苓片、桂枝茯苓胶囊。
茯苓多糖和茯苓三萜的化学研究,主要集中在其提取、分离、纯化等方面。茯苓含多糖、三萜和甾体等化学成分,其中茯苓总多糖含量最高,占其菌核干质量的70%-90%[3-4];茯苓三萜类成分含多种四环三萜类化合,主要包括去氢茯苓酸、去氢土莫酸、茯苓酸、土莫酸及依布里酸[5]。
茯苓多糖和茯苓三萜药理活性丰富,主要集中在抗肿瘤、调节免疫及降血糖等领域。此外,茯苓多糖还有改善学习记忆力、抑制大鼠心肌肥厚、预防结石形成等药理活性。茯苓三萜还有镇静、减轻脏器移植排斥反应和改善多囊卵巢综合征的药理活性。茯苓多糖和茯苓三萜运用广泛,研究发现,茯苓多糖可能开发成潜在的免疫佐剂(见图1)。
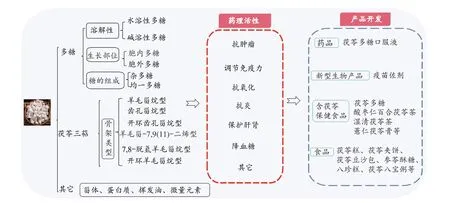
图1 茯苓化学及药理概况研究
1 茯苓多糖和茯苓三萜类成分的提取
1.1 茯苓多糖的提取
茯苓多糖的提取方法常有水提醇沉、酶解和热水浸提等,一般采用纤维素、大孔树脂、葡聚糖凝胶填充的层析柱纯化(表1)。

表1 茯苓多糖的提取、纯化、组成
1.2 茯苓三萜类成分提取
茯苓总三萜类物质主要应用甲醇和乙醇回流超声提取,运用C18填料进色谱分离,目前分离出来的化合物主要为羊毛甾烷[24](表2)。
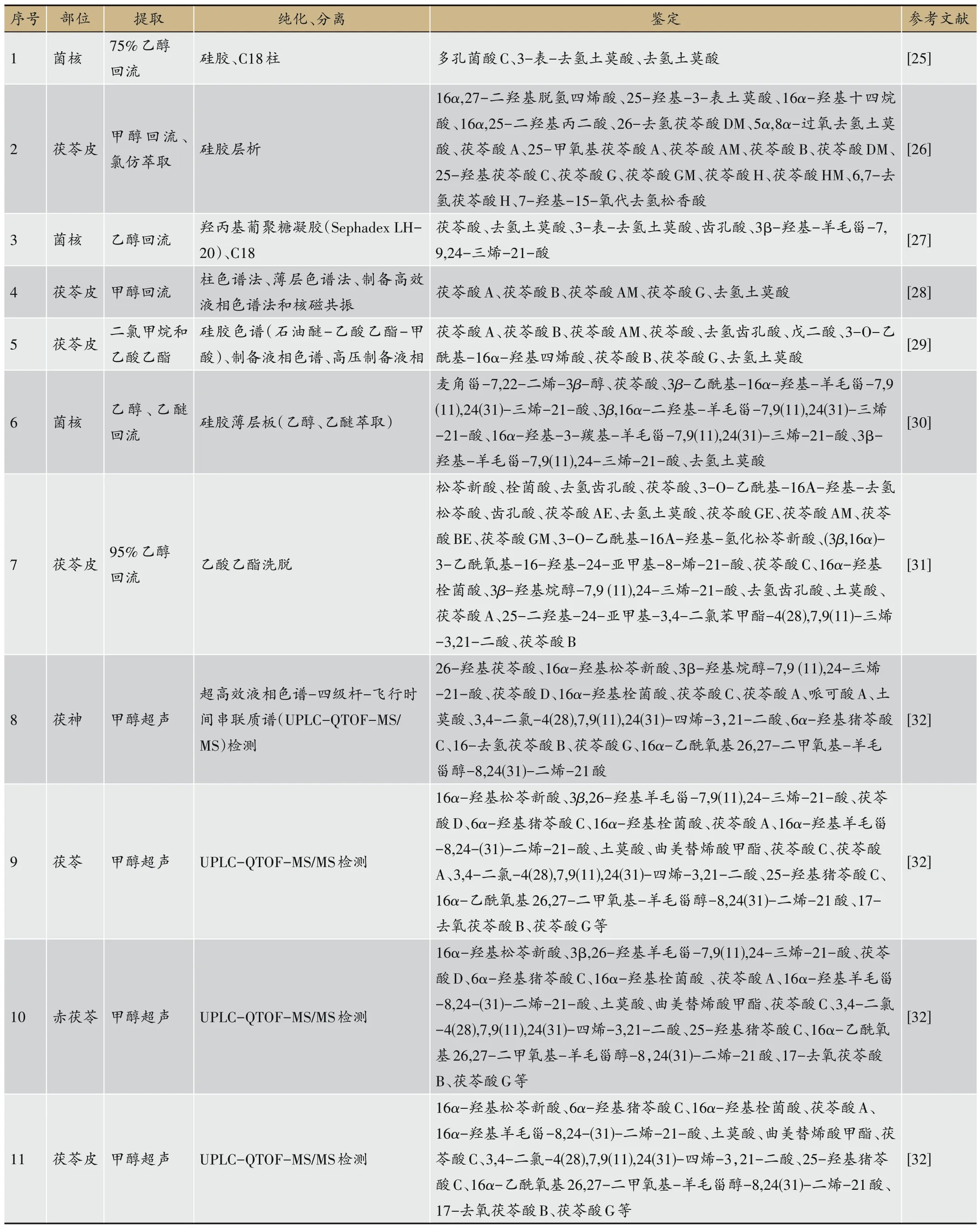
表2 茯苓三萜类成分的提取、纯化、鉴定
2 茯苓多糖和茯苓三萜的分类及含量
2.1 茯苓多糖的分类及含量
2.1.1 茯苓多糖的分类
茯苓多糖根据其单糖组成分为杂多糖和均一多糖,代表性的茯苓杂多糖常以葡萄糖、阿拉伯糖、岩藻糖等组成,而茯苓均一多糖则可能由(1→6)或(1→2)支链的β-(1→3)-D-葡聚糖组成[23]。
此外,茯苓多糖可根据其溶解性分为水溶性多糖和碱溶性多糖。研究表明,茯苓多糖主要药理活性成分是水溶性多糖,但其含量较低,常为0.7%-2.6%[33];而碱溶性茯苓多糖含量较高占70%-90%[34-35],但其药理活性较低。
2.1.2 茯苓多糖的含量
茯苓水溶性多糖分布于茯苓的不同药用部位,其含量比较为菌丝>茯神>菌核>茯苓皮,其含量范围在0.16%-8.89%,其中菌丝中占0.31%-8.89%,茯神中占0.05%-0.95%,菌核中占0.16%-0.91%,茯苓皮中占0.16%-0.66%[36-40]。
茯苓发酵菌丝水溶性茯苓多糖显著高于天然茯苓提示提高液体发酵菌丝产量可能会缓解茯苓水溶性多糖的紧缺,其培养条件的考察也至关重要,下一步可对比天然茯苓菌核和液体培养菌丝中提取的水溶性茯苓多糖成分及比例,这可能为茯苓水溶性多糖的获得增加一个新途径[36]。此外,不同产地、提取方法对水溶性茯苓多糖的含量影响显著,未来探索稳定统一的最佳水溶性多糖提取工艺也将必不可缺[5,26,41]。
2.2 茯苓三萜的分类及含量测定
2.2.1 茯苓三萜的分类
目前从茯苓中分离鉴定的三萜类成分有91种,根据骨架结构可分为6 种类型:羊毛甾烷型、齿孔甾烷型、开环齿孔甾烷型、羊毛甾-7,(11)-二烯型、7,8-脱氢羊毛甾烷型和开环羊毛甾烷型。其中羊毛甾烷型三萜酸类化合物是茯苓的主要药用成分,如:松苓新酸、多孔酸C等,多具有抗肿瘤、增强免疫的药理作用。
2.2.2 茯苓三萜的含量
研究显示茯苓不同药用部位茯苓总三萜含量有显著差异。总三萜含量最高的茯苓皮,提取率均高达3%,茯苓块中三萜含量多为1.5%,茯神中总三萜的含量最低仅0.34%-0.51%[39,42-45]。茯苓皮主要功效为利水消肿,这可能是茯苓皮与茯苓块活性差异的化学基础,也提示茯苓三萜工业提取富集以茯苓皮为原料为佳。
三萜单体含量方面,茯苓皮中羊毛甾烷型四环三萜类化合物含量较高,约为其菌核的十倍,三萜化合物的种类也比茯苓丰富[31]。同时,联合主成分分析和t检验寻找出茯神、茯苓、赤茯苓、茯苓皮差异化合物为茯苓新酸d、松苓酸;茯神与茯苓、赤茯苓、茯苓皮的差异化合物为26-羟基茯苓新酸G、16α-乙酰氧基-羊毛甾-8,24-二烯-21酸、羊毛-7,9(11),24-三烯-21-酸;茯苓与茯神、赤茯苓、茯苓皮间无差异化合物;赤茯苓与茯神、茯苓、茯苓皮的差异化合物为茯苓新酸B、羊毛甾-7,9(11),24-三烯-21-酸;茯苓皮与茯神、茯苓、赤茯苓差异化合物为松苓酸、茯苓新酸B,按形态学由里及表的顺序茯神、茯苓、赤茯苓、茯苓皮中3,4-开环-羊毛甾三萜类化合物含量相对增高,而闭环羊毛甾三萜类化合物含量相对降低[32]。茯苓皮中的三萜类物质种类更多,含量更丰富,更加适合药用成分提取的原料。
另一方面,茯苓培养条件也会影响其三萜含量。对茯苓液体培养的探索研究显示,当菌丝液体培养条件为装液量50 mL,接种体积分数6%,pH = 5.5,温度26℃,转速130 r·min-1,液态培养11 天时,总三萜的含量从0.31%左右提高至8.89%[46]。
3 提高茯苓多糖和茯苓三萜类成分的积累
由于水溶性茯苓多糖含量低,因此,天然药物化学工作者对碱溶性茯苓多糖进行化学结构修饰以增加其水溶性和增强其药理活性,目前常见的化学结构修饰方法有二次碱化法、氯磺酸-吡啶法、硫酸酯化等[47]。
此外,对于茯苓三萜类成分含量低,研究者也采取了优化有性产孢条件、单孢菌株的分离筛选等传统方法,结合转录组学、代谢组学等现代方法综合研究揭示茯苓三萜类化合物生物合成的关键基因及其调控因子,分析其与三萜相关代谢物的关联性,进而对茯苓三萜类化合物生物合成进行基因调控等方法来提高茯苓中三萜类化合物的生物合成和积累。茯苓三萜最典型的生物合成是甲羟戊酸(MVA)途径,MVA途径中法尼基焦磷酸合成酶催化异戊烯基焦磷酸和二甲基丙烯焦磷酸合成法尼基焦磷酸,接着在鲨烯合酶的催化下合成鲨烯,有研究通过增强/提高尼基焦磷酸合成酶鲨烯合酶活性来提高茯苓中三萜含量[5,48],见图2。
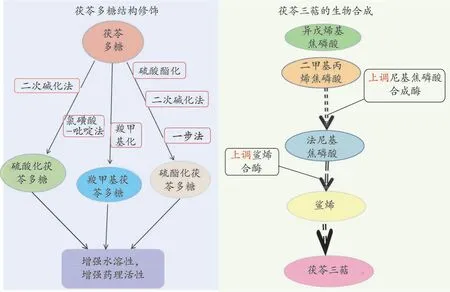
图2 茯苓多糖的结构修饰和茯苓三萜的生物合成
4 茯苓多糖和茯苓三萜类成分的药理活性
4.1 茯苓多糖和茯苓三萜的抗肿瘤作用
恶性肿瘤成为我国居民的主要死亡原因,其发病率逐年上升,但对于恶性肿瘤的研究始终面临难以攻克的壁垒[49]。近年来,大量研究表明中药多糖可以增强机体免疫力,同时也可以提高肿瘤对放化疗的敏感性。研究发现茯苓多糖对乳腺癌、肝癌细胞、胃腺癌等有抑制作用,可改善化疗后的副作用。经过化学修饰后的茯苓多糖对癌细胞增殖抑制作用更明显[50-56]。同时茯苓中的三萜成分对乳腺癌、前列腺癌、肺癌等具有抗肿瘤作用[57-59]。
在作用途径方面茯苓多糖和茯苓三萜对肿瘤的作用均促进癌细胞和癌细胞的炎症因子分泌导致癌细胞凋亡,同时,促进激活B 细胞淋巴瘤/白血病-2 基因(Bcl-2)和兔抗人单克隆抗体(Bax)磷酸化,启动执行凋亡因子含半胱氨酸的天冬氨酸蛋白水解酶7(Caspase-7)、半胱氨酸天冬氨酸蛋白酶-3(Caspase-3)。其中茯苓多糖通过调控核基质结合区结合蛋白(1SATB-1)表达,对肿瘤相关目标基因调控,促使肿瘤细胞分化、凋亡,如表皮生长因子受体(EGFR)基因。EGFR 基因的表达水平与癌细胞的增殖,侵袭和转移密切相关,尤其在肺癌中高表达,可激活巨噬细胞、T细胞诱导肿瘤坏死因子-α(TNF-α)和白细胞介素-2(IL-2)的产生,使癌细胞凋亡。此外茯苓三萜类成分可增加人第10 号染色体缺失的磷酸酶(PTEN)蛋白表达,抑制肿瘤细胞的产生。
4.2 茯苓多糖和茯苓三萜类成分的免疫调节功能
茯苓多糖可通过调节体液免疫和细胞免疫来增强免疫,治疗免疫缺陷性疾病如:复发性流产小鼠妊娠不良、系统性红斑狼疮患者。对于肠道粘膜损伤疾病,茯苓多糖可通过调节结肠内T 淋巴细胞亚群的平衡,降低异常免疫反应的程度促进烫伤大鼠肠黏膜屏障的修复还可作为潜在的食品免疫调节剂[60-63]。在茯苓的另一个主要有效成分群中,茯苓三萜可治疗结肠癌,可增殖免疫淋巴细胞提高免疫[58]。
茯苓多糖和茯苓三萜调节免疫力功能的机制研究显示,茯苓多糖可降低孤儿核受体亚型信使核糖核酸(RORγt mRNA)表达,降低辅助性T 细胞17(Th17)的分化,增加叉头样转录因子(Foxp3)调节T 细胞,调节Th1 细胞和Th2 细胞,使其处于平衡状态,增强免疫力,避免机体被破坏,减弱疾病的发生和发展,增强Toll样受体,当病毒侵犯机体时,加快识别并激活机体产生免疫细胞应答,提高血清中免疫球蛋白A(IgA)、IgM、的含量以杀菌、激活补体、调节免疫,避免遭到病原的入侵。茯苓三萜类可促进淋巴细胞分泌CD3+、CD4+、CD8+的增殖,抑制脾细胞炎症因子的分泌提高免疫。
4.3 茯苓多糖和茯苓三萜类成分的抗氧化
茯苓多糖和茯苓三萜均有较强的抗氧化能力。茯苓多糖对羟基自由基(·OH)的清除率为39.55%-64.07%,对氧离子自由基(O2-·)的清除率为60.21%-71.65%[64]。茯苓胞内多糖对·OH、1,1-二苯基-2-三硝基苯肼自由基(DPPH·)和O2-·的清除率分别为32.07%、90.12%和39.74%[65]。修饰后的硫酯化茯苓多糖对·OH、DPPH·和的清除力在浓度1.0 g·L-1时达到最大,分别为78.11%、89.33%、44.97%[66-68]。另外,茯苓三萜类化合物对DPPH·和·OH 的清除能力均高于维生素C(VC),还原力与VC 相当,其中茯苓酸能减轻氧化应激带来的损伤[69-72]。
茯苓多糖和茯苓三萜抗氧化的机制研究显示,茯苓多糖能升高机体中氧化与抗氧化中至关重要的超氧化物歧化酶,催化超氧阴离子自由基歧化生成氧和过氧化氢;升高谷胱甘肽过氧化物酶将机体产生的过氧化物分解,使有毒的过氧化物还原成无毒的羟基化合物,从而保护细胞膜的结构及功能不受过氧化物的干扰及损害,提高机体的抗氧化能力,减轻氧化应激反应,茯苓多糖抗氧化主要恢复其抗氧化相关的酶活力,如:过氧化氢酶、乳酸脱氢酶、脱氧阴离子。从而提高组织和细胞的抗氧化能力。茯苓三萜类主要控制炎症因子、调控炎症通路,间接减轻氧化应激反应。茯苓三萜主要调控抗氧化酶、血红素氧合酶1,催化血红素分解代谢成亚铁、一氧化碳和胆绿素,抵抗过氧化物,有效阻止其促氧化作用,激活NF-κB相关通路。
4.4 茯苓多糖和茯苓三萜的抗炎作用
茯苓多糖和茯苓三萜均能达到较好的抗炎效果。茯苓多糖能抑制炎症因子、肥大细胞和肉芽组织的形成[73]。研究发现,茯苓多糖能治疗溃疡性结肠炎、炎症引起的溶骨性病变,黏膜炎[70,74]。对于茯苓三萜类成分:茯苓酸可减轻口腔疾病并发症,肿瘤坏死因子α诱导细胞炎症[70]、鼠病毒性心肌炎[72]。
茯苓多糖和茯苓三萜的抗炎机制研究显示,茯苓多糖能降低炎症的浸润程度,减少分布皮肤内脏粘膜下的微血管周围肥大细胞,减少炎症因子的分泌,下调白介素调控的通路,抑制炎症因子,共同产生抗炎作用,可抑制IL-33细胞因子,抑制其受体生长刺激表达基因2 蛋白(ST2)介导的炎症因子产生。茯苓三萜上调Bcl-2 基因,显著抑制细胞凋亡,抑制细胞炎症的发生;下调细胞外调节蛋白激酶(ERK)蛋白时,调节在不同细胞内的减数分裂、有丝分裂、有丝分裂后期的功能防治细胞凋亡过程减来缓炎症因子,同时茯苓三萜类物质减轻炎症因子一氧化氮(NO)的分泌和调节免疫、肿瘤坏死因子。
4.5 茯苓多糖和茯苓三萜对肾脏保护
茯苓多糖和茯苓三萜均可改善大鼠肾功能[75-76]。茯苓多糖和茯苓三萜对肾脏的保护机制研究显示,茯苓多糖抑制丝裂原活化蛋白激酶p38 抗体(p38 MAPK)磷酸化和激活过氧化物酶体增殖物激活受体(PPAR-γ),抑制炎症因子的产生进而保护肾脏。此外,使肾相关疾病患者堆积的肌酐和血尿素氮从肾小球过滤随尿液排出次数增加,降低血清肌酐和血尿氮来减缓对肾脏的生理损坏。茯苓三萜类保护肾脏一方面可降低尿蛋白、减缓尿蛋白过高对肾脏产生炎症的损伤,另一方面抑制肾上皮细胞的死亡,保护肾脏。
4.6 茯苓多糖和茯苓三萜降血糖
茯苓多糖和茯苓三萜均能降血糖[77-80]。茯苓多糖能通过提高糖耐量,改善糖耐异常、改善糖代谢紊乱,从而减缓糖尿病患者体重的负增长。茯苓三萜能使脂质骨骼细胞中负责运输葡萄糖的葡萄糖转运蛋白(GLUT4)蛋白表达增加,磷酸化胰岛素受体底物(IRSs)激活下游效应物,增强胰岛敏感从而降低血糖。茯苓多糖和三萜均可降血糖,可探索它们之间降血糖是否为相互协同,见图3。
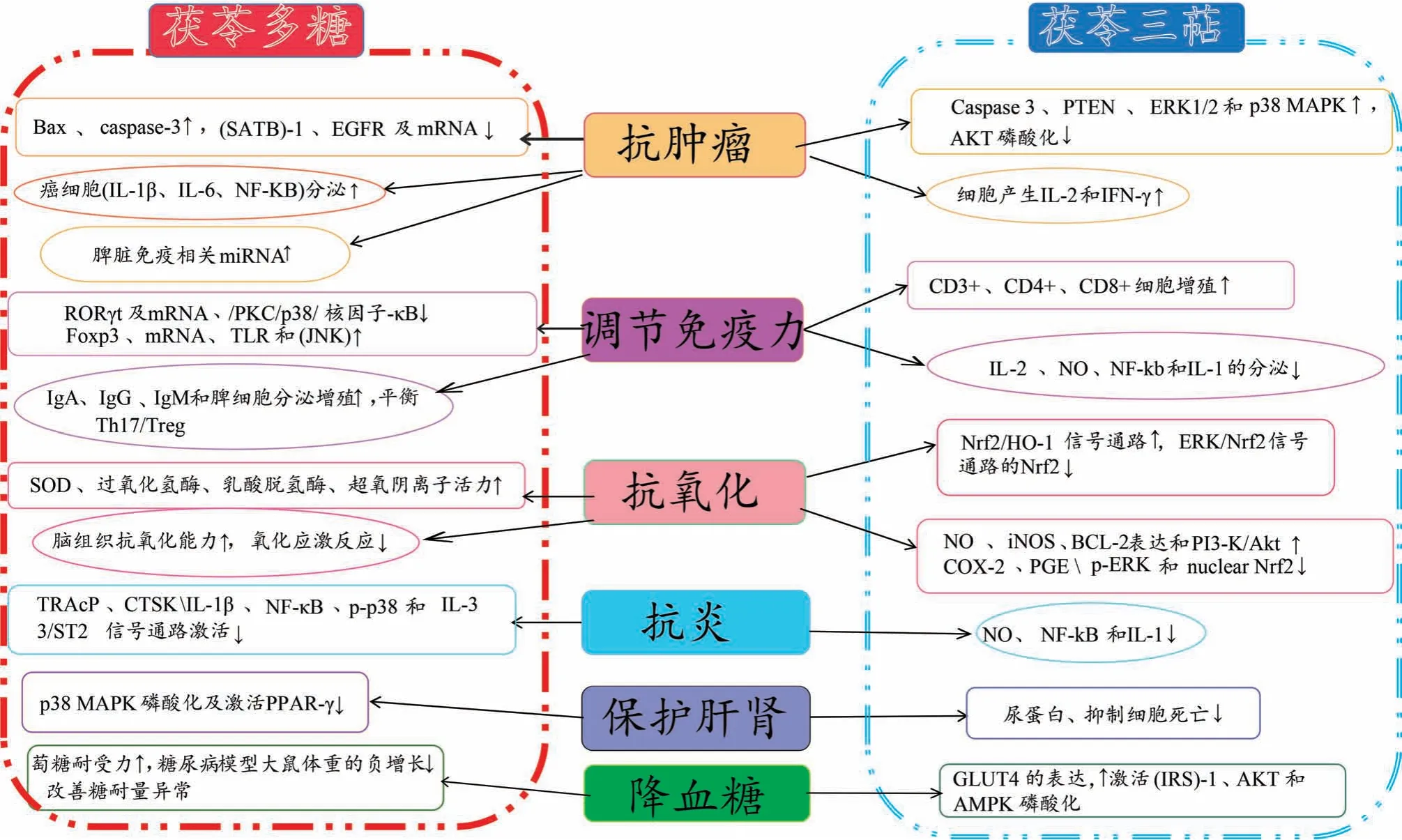
图3 茯苓多糖和茯苓三萜共同药理作用研究
4.7 其他
茯苓多糖、三萜除上述主要药理活性之外,还具有以下药理作用(表3)。
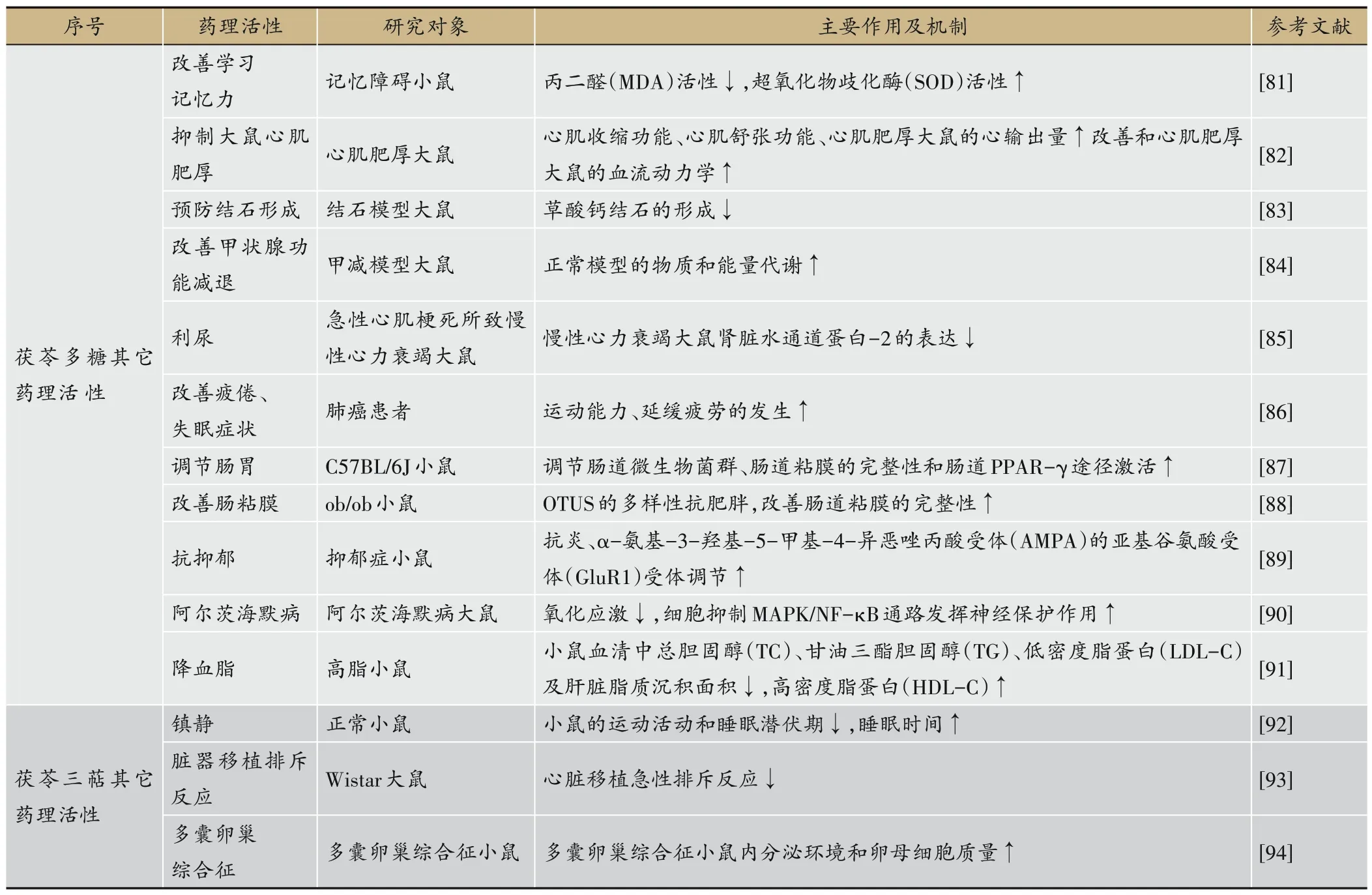
表3 茯苓多糖和茯苓三萜类成分的其它药理活性
5 茯苓多糖类成分的吸收和茯苓三萜类成分的药代动力学
5.1 茯苓多糖类成分的吸收
多糖类药物主要以口服给药为主,且多糖均能通过口服的方式发挥广泛的药理活性,但多糖分子量大,不能完全被肠道吸收,可能口服吸收性差。对多糖口服吸收难易程度如何、是以原型形式还是降解形式被吸收还未清晰[95]。
曹楠等[96]为了研究茯苓多糖的吸收,模拟人体胃肠道环境及在体循环肠灌流,发现在大鼠体内,茯苓多糖主要在胃液中降解、体肠中吸收。茯苓多糖在人工胃液中0.5 h 内被降解,在肠液中几乎不降解,茯苓多糖在体肠的吸收随时间的增加而增大。多糖作为肠道菌群的重要能量来源和食物,肠道中难以吸收的多糖被肠道菌群吸收,促进益生菌的增殖[97]。
此外,文献也有报道,胞吞和肠道派尔集合淋巴结这两种吸收方式也可能是多糖的吸收途径[98]。然而,目前尚未见茯苓多糖通过胞吞和派尔集合淋巴结吸收的报道,后续可开展相关研究将有助于茯苓多糖药理活性的阐释。
5.2 茯苓三萜的药代动力学
Zhang等[99]探索口服茯苓乙醇提取物后,大鼠血浆和组织中4 种三萜类成分,去氢土莫酸、去氢茯苓酸、茯苓酸和去氢齿孔酸的分布。与血浆相比,在分布较高的组织中均能检测到4种三萜类化合物。在肠胃组织中的浓度顺序为:去氢土莫酸>茯苓酸>去氢茯苓酸>去氢齿孔酸,在心、肝、脾、肺、肾组织中浓度顺序为去氢土莫酸>去氢齿孔酸>茯苓酸>去氢茯苓酸。其中,茯苓酸的消除半衰期、血浆浓度-时间曲线下面积、血浆清除率和表观分布体积的药代动力学参数分别为4.96±1.33 h、1466.9±361.7 ng·h-1·mL-1、6.82±1.73 L·h-1和48.85±9.47 L[100]。
对于茯苓不同部位中提取的茯苓新酸B、去氢土莫酸、茯苓新酸A、猪苓酸C、去氢茯苓酸、茯苓酸和松苓新酸在大鼠体内的吸收情况,茯苓新酸AM 在大鼠血浆中无吸收,其余6 种三萜类成分在茯苓皮组中吸收量最大。同时,此项研究在代谢途径中找到15种主要的吸收组分,鉴定了102种成分代谢物,主要的代谢类型为甲基化、氧化、水解、氢化和葡萄糖醛酸结合等,为茯苓皮体内过程的阐明奠定了基础[101]。茯苓不同部位中提取的三萜类成分表现出不同的药代动力学,茯苓酸B、茯苓酸A、茯苓酸、去氢齿孔酸、去氢土莫酸、猪苓酸C 和去氢茯苓酸可能是茯苓利尿作用的主要生物活性化合物[102]。
前期研究发现茯苓三萜类成分提取物及其固体粉末的吸收均较差,通过比较茯苓三萜类成分提取物粉末及软胶囊内容物的药代动力学参数发现,软胶囊内容物的土莫酸和去氢土莫酸药峰浓度及药时曲线下面积均大于粉末,说明软胶囊内容物中植物油的加入可能促进了土莫酸和去氡土莫酸的吸收[103]。
茯苓和桂枝胶囊中提取去氢土莫酸,土莫酸和茯苓酸C 的药代动力学显著不同,桂枝茯苓胶囊吸收更好,消除速度更慢。此外,多种成分在体内的表观分布容积,清除率和平均驻留时间显著增加,尿粪排泄率均降低,延迟最大排泄比率时间,说明配伍后延长活性成分在体内的作用时间[104-105]。
因此,基于药代动力学挖掘茯苓三萜类成分可选择更合适的茯苓三萜类成分进行药物研发及治疗,以达到最佳疗效的作用机制及潜在作用靶点,具有广阔的临床研发和社会应用前景。
6 茯苓多糖、茯苓三萜类成分的应用
单一茯苓三萜作为主要成分的保健食品和药品还无相关报道。茯苓多糖药理活性丰富,现已有药品应用到临床。此外,还有药品和保健品处于研发状态。
6.1 茯苓多糖的应用
6.1.1 临床药品
目前,茯苓多糖在临床中作为药品被使用,如:茯苓多糖口服液、参苓口服液(表4)。茯苓多糖作为潜在临床药品有复方茯苓多糖口服液、羧甲基茯苓多糖口服液等。茯苓多糖除在临床中被应用,还作为兽药应用到实际生产中,如茯苓多糖散,可显著提高猪瘟与猪伪狂犬抗体水平。

表4 茯苓多糖的临床应用
6.1.2 潜在疫苗或免疫佐剂
免疫佐剂是非特异性免疫增生剂,同抗原一起注入机体内能增强机体对抗原的免疫应答能力,应用最常见的疫苗佐剂为铝,不断有研究表明茯苓多糖可作为潜在佐剂,效果优于铝佐剂(表5)。
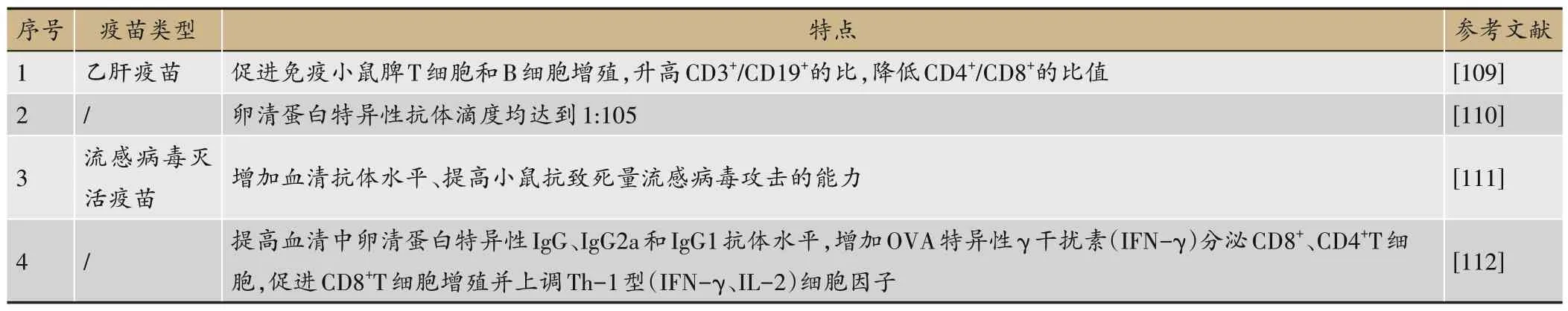
表5 茯苓多糖作为疫苗或免疫佐剂的研究
6.1.3 潜在的茯苓保健食品
茯苓可药食两用,安全性高。研究发现,其主要有效成分茯苓多糖也具备进一步开发成保健品的可能,拥有广阔的市场(表6)。

表6 潜在的保健食品:茯苓多糖
6.2 茯苓三萜的应用
茯苓三萜类成分目前还没有应用到临床中,但是茯苓三萜类成分药理活性丰富,其主要活性成分茯苓酸等活性成分未来有望应用到临床。
7 结论与展望
中国茯苓药用历史悠久,在众多方剂中配伍使用,具有广阔的开发应用前景,本文对药食同源大品种茯苓中多糖和三萜的提取分离、含量测定积累、药理活性、吸收药代动力学和应用进行总结。深入挖掘药食同源大品种茯苓多糖和三萜的生理活性、研发新药推广临床并积极开发相关产品,将对推动茯苓产业有极大的意义。
同时,茯苓多糖、茯苓三萜的现代研究也面临着挑战:首先,茯苓水溶性多糖含量极低且茯苓三萜的水溶性较差,提示传统水煎法能获取的有效成分含量有限,然而这并不影响茯苓发挥良好的临床药效,提示其水溶性多糖及三萜类成分活性非常优越,非常具有潜在研究价值。同时,这也提示了通过化学结构修饰来提高茯苓多糖溶出率相关研究的重要意义;当然,经过化学结构修饰的茯苓多糖,也需要更全面的安全性评价及深入的活性研究,才能最终更好的发挥茯苓的药效。其次,茯苓不同部位的茯苓多糖、茯苓三萜药理活性是否有所差别,经过系统的研究,可更加充分茯苓在临床中的利用;茯苓药理活性成分茯苓多糖、三萜的药理活性与其传统功效相关联的作用机制,也待探索,建立科学、合理的药效评价方法,对于保证茯苓促进健康产业的发展具有重要意义,更能坚定扩大和传承茯苓中医药传统文化。最后,茯苓作为药食同源品种,是保健食品和食品的通用原材料,茯苓多糖可能就是其主要的功效成分及营养成分,针对茯苓多糖的深入研究将有助于更多药品、保健食品及相关健康产品的开发。
