玉蚕颗粒改善足细胞损伤治疗糖尿病肾病的机制研究
2023-11-14张亚亨盛广宇杨雪军
张亚亨,盛广宇,宋 婷,杨雪军
上海中医药大学附属曙光医院肾病科(上海 201203)
糖尿病肾病(diabetic nephropathy,DN)是指由糖尿病所致的慢性肾脏病,病变可累及全肾(包括肾小球、肾小管、肾间质等),现已成为终末期肾病的主要原因。糖代谢异常、肾脏血流动力学改变、氧化应激以及炎症反应是高血糖诱发肾脏损伤的主要病理过程,而这一系列过程进一步引起足细胞损伤是产生蛋白尿,最终导致DN 进展的关键因素之一[1]。在DN 早期,高血糖可通过多种途径损伤足细胞,主要表现在影响足细胞代谢和破坏足细胞骨架结构,受损的足细胞失去维持肾脏过滤屏障的功能,最终导致肾小球疾病[2]。因此,保护足细胞细胞骨架的正常结构和功能至关重要。然而,足细胞损伤往往被认为是不可逆损伤,基于此,临床并无药物可直接延缓,甚至修复足细胞损伤,从而治疗慢性肾脏病,更多是以控制血糖、血压、血脂为出发点,通过纠正基础代谢,以期对疾病进展起到控制作用。但事实上,这些治疗方案的疗效不尽如人意。即使代谢指标恢复正常,随着病程的延长,大部分患者仍会逐渐发展为终末期肾病。
中西医协同是治疗慢性难治性肾脏病的重要思路,在控制各项指标处于正常范围的基础上,中药复方因其成分众多、作用途径多样,在控制蛋白尿、延缓慢性肾脏病进展方面,有其独到的优势。糖尿病肾病属中医学“水肿”“虚劳”“肾消”等范畴,病位在肾,可涉及五脏六腑,病性本虚标实,本虚为脾肾亏虚、气血阴阳俱虚,标实为气滞、血瘀、痰浊、浊毒、湿热等,瘀血贯穿始终,治以益气活血、利湿降浊。玉蚕颗粒(由黄芪、玉米须、蚕茧壳、川芎组成)是上海中医药大学附属曙光医院肾内科杨雪军教授经验方,方中黄芪补气行气,川芎行气活血,蚕茧壳利湿降浊,玉米须消肿利水,临床上治疗DN 运用广泛且疗效确切。本研究通过建立DN模型,观察玉蚕颗粒对DN 小鼠的治疗作用并研究其机制,以期为玉蚕颗粒的临床应用提供实验依据。
1 材料与方法
1.1 材料
1.1.1 动物 SPF级C57雄性小鼠80只,体质量20 g左右,由上海斯莱克动物技术有限公司提供。实验动物生产许可证号:SYXK(沪)2022-0012。实验动物饲养于上海中医药大学实验动物中心。实验动物使用许可证号:SYXK(沪)2020-0009。室内温度25 ℃左右,湿度45%左右,并维持 12 h光照/12 h黑暗的昼夜节律,适应性喂养1 周。实验经上海中医药大学实验动物伦理委员会批准(伦理批准号:PZSHUTCM210305002)。
1.1.2 药物与试剂 玉蚕颗粒(黄芪9 g、玉米须30 g、蚕茧壳30 g、川芎15 g)由湖南易能生物医药有限公司制备。
氯沙坦钾片,浙江华海药业股份有限公司(批号:H20070264);肾脏足细胞裂孔膜蛋白(Nephrin)抗体,美国Abcam 公司(批号:ab216692);肾母细胞瘤基因1蛋白(WT1)抗体,武汉爱博泰克生物科技有限公司(批号:A16319);甘油醛-3-磷酸脱氢酶(GAPDH),美国Proteintech 公司(批号:60004-I-Ig);辣根过氧化物酶(HRP)标记山羊抗小鼠免疫球蛋白G(IgG)、HRP 标记山羊抗兔 IgG、α 微管蛋白(α-Tubulin),上海碧云天生物技术有限公司(批号分别为A0216、A0208、AG0136);聚偏氟乙烯(PVDF)膜,美国Millipore 公司(批号:IPVH00005)。
高糖高脂饲料(59%普通饲料、18%猪油、20%蔗糖、3%蛋黄粉),上海帆泊生物技术有限公司(批号:20210530)。
1.1.3 主要仪器 离心机,美国Beckman 公司(型号:Avanti J-E);生物组织冷冻包埋机、烘片机,浙江省金华市科迪仪器设备有限公司(型号分别为KD-BM、KD-H);酶标仪,美国BioTek 公司(型号:Synergy 2);组织匀浆器,上海净信科技有限公司(型号:JY-24);显微镜,日本Olympus 株式会社(型号:CX33);凝胶成像系统,上海天能科技有限公司(型号:Tanon-5200)。
1.2 分组与造模 实验动物适应性饲养1 周后,选择健康、状态良好且血糖水平正常的小鼠列入观察。将上述小鼠按随机分组法分为正常组(10 只)和造模组(70只)。正常组予普通饲料,造模组予高糖高脂饲料。饲养4 周后,所有小鼠禁食12 h,造模组小鼠予单次腹腔注射链脲佐菌素(STZ)100 mg/kg(STZ 临用前溶解于0.1 mol/L、pH4.5 的柠檬酸缓冲液),正常组小鼠腹腔注射等体积上述缓冲液[3]。注射STZ 72 h 后,尾静脉采血,将随机血糖高于16.7 mmol/L的小鼠列为观察对象。糖尿病小鼠继续喂养1周,然后以随机血糖≥16.7 mmol/L视为DN 小鼠造模成功。将50 只造模成功的小鼠随机均分为5 组,即模型组、氯沙坦钾组及中药低、中、高剂量组,每组10只。
1.3 干预 玉蚕颗粒在给药前预先溶解于蒸馏水,4 ℃条件下保存,有效期3 d,灌胃前温水预热。根据《药理实验方法学》[4]动物计量换算表中“0.02 kg 小鼠与60 kg 成人用药剂量的折算系数为12.33”的标准,换算用药剂量。临床饮片用药剂量为每日每60 kg 体质量84 g,中药饮片收膏率为18%,因此提取物临床等效用药剂量为84 g×18%=15.12 g,小鼠剂量按倍近似计算每日等效剂量为3 g/kg。其中中药低剂量组为1.5 g/kg,中药中剂量组为3 g/kg,中药高剂量组为6 g/kg。氯沙坦钾组采用氯沙坦钾片,使用时研成细粉。换算出小鼠每日使用氯沙坦钾的剂量为10 mg/kg。按10 mg/kg剂量用羧甲基纤维素钠(CMC)配制成浓度为0.4 g/mL的混悬液,4 ℃条件下保存,保质期3 d。灌胃前提前从冰箱中取出药液,放置至常温后使用。正常组及模型组以质量分数为0.9%的氯化钠溶液灌胃,氯沙坦钾组及中药低、中、高剂量组每天8:00 灌胃给药1 次,共干预4 周。最后1 次干预后,小鼠禁食不禁水,0.8%戊巴比妥钠腹腔注射麻醉小鼠,收集血液,取双侧肾脏,切去肾盂,剩余肾组织用于后续相关检测。
1.4 检测指标与方法
1.4.1 一般状态 观察小鼠体型,精神状态,动作及反应灵敏度,并记录体质量。
1.4.2 空腹血糖(FBG)委托上海中医药大学附属曙光医院检验科检测小鼠血清空腹血糖。
1.4.3 肾组织病理形态 小鼠肾组织经4%多聚甲醛固定24 h,梯度乙醇脱水,石蜡包埋,切片(厚度4 μm),脱蜡后进行苏木精-伊红(HE)染色、丽春红酸性品红-苯胺蓝(Masson)染色、过碘酸-雪夫(PAS)染色,中性树脂封片,光镜下观察小鼠肾组织病理形态。
1.4.4 肾小球足细胞超微结构 取2.5%戊二醛固定的肾组织,放入1%锇酸固定液于4 ℃条件下固定2 h。梯度乙醇脱水,包埋在环氧树脂中。在80 ℃下进行24 h聚合,行60 nm 超薄切片,醋酸双氧铀和柠檬酸铅双染色,透射电子显微镜下观察肾小球足细胞超微结构。
1.4.5 蛋白质免疫印迹(Western blot)法检测肾组织
Nephrin、WT1 表达 取20 mg 小鼠肾组织,加入放射免疫沉淀法(RIPA)裂解液200 μL,匀浆机65 Hz 匀浆1 min,4 ℃、12 000 r/min 离心15 min。蛋白提取按照BCA 蛋白质定量试剂盒说明操作制备蛋白样品,置于-80 ℃条件下保存。采用8%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)的凝胶,120 V 电泳,湿转法以100 V、120 min 条件进行转膜,5%脱脂奶粉室温下封闭40 min,0.01%磷酸盐吐温缓冲液(PBST)洗膜3遍后,分别加入Nephrin 抗体(1∶1 000)、WT1 抗体(1∶1 000)、α-Tubulin 抗体(1∶1 000)和GAPDH 抗体(1∶5 000),4 ℃摇床过夜;0.01%PBST 洗膜后加入HRP 标记山羊抗兔和抗鼠1∶1 000,室温孵育1 h,0.01%PBST洗膜后化学发光底物(ECL)发光,暗室曝光。ECL化学发光法显影,凝胶成像系统拍摄。以GAPDH 和α-Tubulin为内参,计算目的蛋白相对表达量。
1.4.6 免疫组织化学染色观察肾组织Nephrin、WT1 阳性表达 肾组织石蜡切片脱蜡至水,抗原修复,3%乙酰胺(BSA)室温封闭 30 min,加入Nephrin抗体(1∶200)、WT1 抗体(1∶200)。4 ℃孵育过夜,加二抗室温孵育50 min,3,3'-二氨基联苯胺四盐酸盐(DAB)显色,中性树脂封片,光镜下观察,以棕黄色颗粒为阳性表达,计算阳性表达的面积比。采用ImageJ 1.8软件分析图片。
1.5 统计学方法 实验数据采用SPSS 22.0 统计软件进行分析。实验数据以表示,多重比较采用方差分析和 LSD-t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 对小鼠一般状态的影响 正常组小鼠精神良好,活动灵敏,被毛光泽,体质量平稳增加。造模组小鼠在喂养高脂高糖饲料的4 周内,体质量平稳增加,而注射STZ 1 周后,出现多饮、多食、多尿、体质量减少的“三多一少”症状,精神萎靡,被毛枯黄无光泽,活动减少。给药后,各给药组小鼠的一般状态得到不同程度的改善。与正常组比较,模型组小鼠体质量降低(P<0.05)。与模型组比较,中药中、高剂量组小鼠治疗后体质量升高(P<0.05)。见表1。
表1 各组小鼠体质量比较(n=10,±s,g)

表1 各组小鼠体质量比较(n=10,±s,g)
注:与正常组比较,*P<0.05;与模型组比较,#P<0.05。
组别正常组模型组中药低剂量组中药中剂量组中药高剂量组氯沙坦钾组治疗后34.62±3.85 24.54±1.29*26.53±1.04 27.37±0.90#28.22±1.32#27.00±0.96治疗前31.32±2.05 31.30±1.99 33.00±1.47 32.54±1.77 32.34±2.10 31.94±2.33
2.2 对小鼠FBG 的影响 与正常组比较,模型组小鼠FBG 明显升高(P<0.05);与模型组比较,中药中、高剂量组小鼠FBG明显降低(P<0.05)。见表2。
表2 各组小鼠空腹血糖(FBG)比较(n=10,±s,mmol·L-1)

表2 各组小鼠空腹血糖(FBG)比较(n=10,±s,mmol·L-1)
注:与正常组比较,*P<0.05;与模型组比较,#P<0.05。
组别正常组模型组中药低剂量组中药中剂量组中药高剂量组氯沙坦钾组FBG 4.67±0.69 24.15±3.03*23.83±3.71 20.82±3.40#21.56±3.37#22.02±4.56
2.3 对小鼠肾组织病理形态的影响 HE、Masson、PAS染色结果显示:与正常组比较,模型组小鼠肾组织结构紊乱,肾小管管腔扩张、管壁变薄,肾间质炎症细胞浸润、纤维化明显,细胞外基质增多;与模型组比较,各给药组小鼠肾小管管腔扩张、炎症细胞浸润、纤维组织增生明显减轻。见图1~图3。

图1 各组小鼠肾组织病理形态(苏木精-伊红染色,×200)

图2 各组小鼠肾组织病理形态(丽春红酸性品红-苯胺蓝染色,×200)
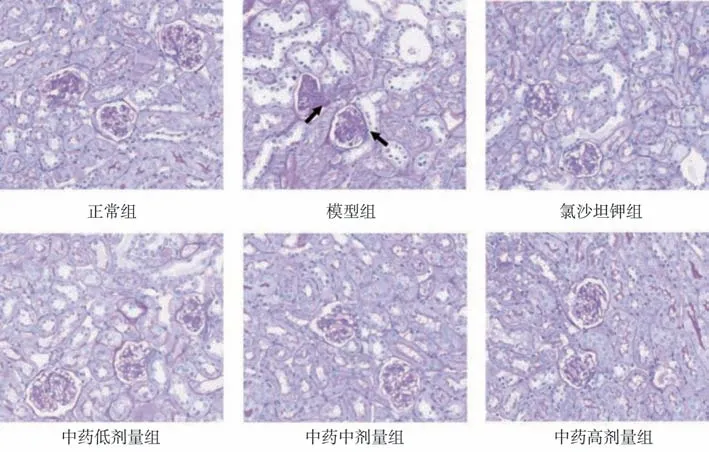
图3 各组小鼠肾组织病理形态(过碘酸-雪夫染色,×200)
2.4 对小鼠肾小球足细胞超微结构变化的影响 与正常组比较,模型组小鼠肾小球足细胞足突相互融合、部分足突消失。与模型组比较,中药各剂量组和氯沙坦钾组足突融合、消失情况明显好转,且中药中、高剂量组对足细胞损伤的改善效果较明显。见图4。
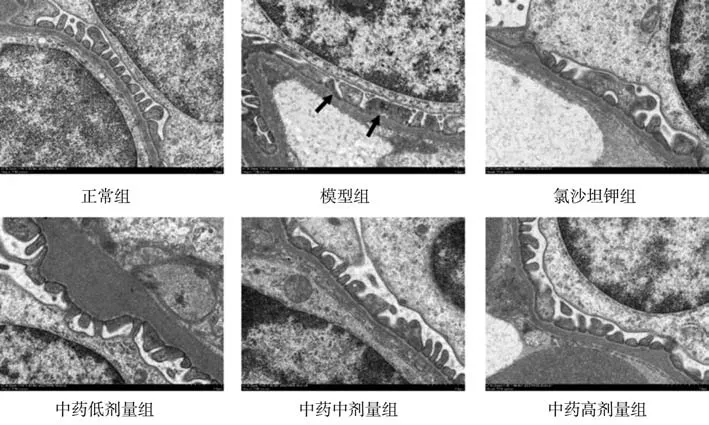
图4 各组小鼠肾组织超微结构(醋酸双氧铀和柠檬酸铅双染色,×3 000)
2.5 对小鼠肾组织Nephrin、WT1表达的影响 与正常组比较,模型组小鼠肾组织Nephrin、WT1 表达显著降低(P<0.05)。与模型组比较,中药高剂量组和氯沙坦钾组小鼠肾组织Nephrin、WT1表达显著升高(P<0.05)。与中药高剂量组比较,中药低、中剂量组小鼠肾组织Nephrin、WT1表达显著降低(P<0.05)。见图5。

图5 各组小鼠肾组织Nephrin、WT1表达
2.6 对小鼠肾组织Nephrin、WT1阳性表达的影响 与正常组比较,模型组小鼠肾组织Nephrin、WT1 阳性表达显著降低(P<0.05)。与模型组比较,中药低、中、高剂量组和氯沙坦钾组小鼠肾组织Nephrin、WT1 阳性表达显著升高(P<0.05)。与中药高剂量组比较,中药低剂量组小鼠肾组织Nephrin、WT1 阳性表达显著降低(P<0.05),中药中剂量组小鼠肾组织Nephrin 阳性表达差异无统计学意义(P>0.05),而WT1 阳性表达显著降低(P<0.05)。见图6、图7,表3。

图6 各组小鼠肾组织 WT1阳性表达(免疫组织化学染色,×200)
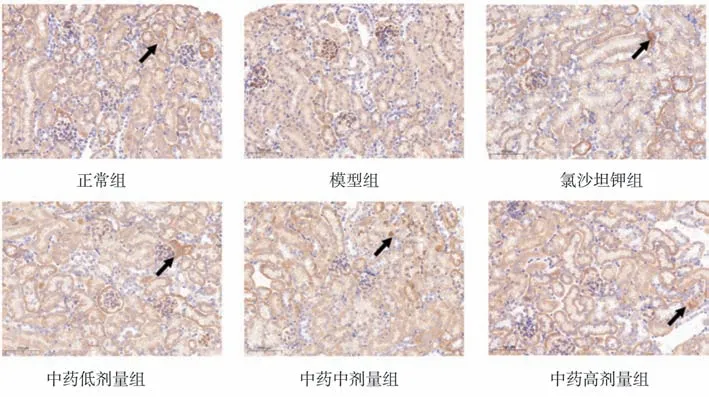
图7 各组小鼠肾组织 Nephrin阳性表达(免疫组织化学染色,×200)
表3 各组小鼠Nephrin、WT1表达比较(n=3,±s)

表3 各组小鼠Nephrin、WT1表达比较(n=3,±s)
注:WT1 为肾母细胞瘤基因1 蛋白,Nephrin 为足细胞裂孔膜蛋白。与正常组比较,*P<0.05;与模型组比较,#P<0.05;与中药高剂量组比较,△P<0.05。
WT1 0.87±0.06 0.29±0.10*0.58±0.10#△0.92±0.05#△1.25±0.02#1.05±0.02#组别正常组模型组中药低剂量组中药中剂量组中药高剂量组氯沙坦钾组Nephrin 1.16±0.00 0.43±0.01*0.84±0.02#△1.12±0.01#1.14±0.01#0.72±0.00#
3 讨论
DN 是糖尿病最常见和最严重的微血管并发症之一,也是糖尿病患者死亡的主要原因[5]。一旦在早期阶段出现蛋白尿,DN 现有治疗措施的疗效极其有限。微量白蛋白尿的存在是糖尿病患者早期肾损害的标志[6]。足细胞与蛋白尿有密切关系,肾小球滤过屏障可阻止血清蛋白渗漏到尿液中,而足细胞是肾小球滤过屏障(GFB)的一个组成部分。足细胞是形成GFB 外层的终末分化细胞,其功能依赖于足突内肌动蛋白细胞骨架的调节,而足突是连接足细胞和肾小球基底膜的结构[7]。足细胞损伤的转归标志是肌动蛋白细胞骨架的失调,最终导致足突回缩和蛋白尿。然而,高血糖可以通过多种机制导致足细胞损伤,包括影响足细胞代谢和细胞骨架结构,进一步导致蛋白渗漏,产生蛋白尿。因此,维持足细胞骨架的正常结构和功能至关重要。
Nephrin 参与维持足细胞的组织结构。细胞外信号可通过Nephrin 的酪氨酸磷酸化传递到每个足突的肌动蛋白核心。通过磷脂酰肌醇-3-激酶/蛋白激酶B(PI3K/Akt)途径,可调节培养出的足细胞形成片状足[8]。除了通过酪氨酸磷酸化进行调节外,Nephrin 的胞质尾部还包含丝氨酸/苏氨酸磷酸化的共有序列,并可被蛋白激酶Cα(PKCα)磷酸化[9]。PKCα 磷酸化Nephrin 导致网格蛋白和动力蛋白介导的Nephrin 内吞作用,这是一种在DN中被激活的途径[10]。
WT1 是足细胞中调节基因表达的最上游的转录因子之一[11],在足细胞中对维持其靶基因的激活状态具有关键作用,对维持GFB 至关重要[12]。WT1 激活下游肾小球足细胞裂隙膜蛋白(podocin)[13],参与形成相邻足细胞之间的细胞-细胞连接结构,是防止蛋白质在过滤过程中离开循环屏障的最重要成分之一。同时,WT1 还能激活突触足蛋白基因,产生维持足细胞骨架完整性的肌动蛋白相关蛋白。伴随着足细胞损伤,WT1的表达减少,在足细胞修复过程中,与转录因子靶基因结合也随之减少,导致足细胞产生不可逆的破坏。这也造成了目前对DN的治疗手段极其有限。
玉蚕颗粒为上海中医药大学附属曙光医院肾内科杨雪军教授治疗DN 的常用方。《本草正义》言:“黄芪,补益中土,温养脾胃,凡中气不振,脾土虚弱,清气下陷者最宜。”现代药理学研究[14]发现,黄芪含皂苷、多糖、多种氨基酸及微量元素,黄芪提取物可扩张肾血管、增加肾血流量、保护肾脏血管内皮细胞功能、减少蛋白尿。有研究[15]发现,黄芪可影响DN小鼠肾组织环氧化酶-2(COX-2)、核因子-κB(NF-κB)的表达,推测黄芪可能通过阻断炎症因子及其受体调节与信号传导通路从而改善DN。
玉米须含多种活性成分,具有降血糖、降血压、降血脂、利尿消肿等作用[16],对代谢类疾病有良好的治疗作用。有研究[17]发现,玉米须提取物可不同程度降低STZ诱导的糖尿病足模型小鼠的血糖,改善血脂及血液流变学指标。蚕茧壳可促进淋巴细胞转化和T 淋巴细胞介导的免疫功能,调节免疫和控制炎症反应[18-19]。有学者[20]观察蚕茧壳水解物灌胃小鼠后的细胞免疫功能相关的22种细胞因子,发现白介素-17(IL-17)、白介素-6(IL-6)、γ 干扰素(IFN-γ)3 种细胞因子分泌最活跃,表明蚕茧壳对免疫功能具有一定的增强作用。
川芎辛散温通,利血脉、促血行、散瘀血,素有“血中气药”之称。有研究[21]发现,川芎中的有效成分川芎嗪能通过抑制醛糖还原酶活性、调控凋亡相关基因B 淋巴细胞瘤-2 基因(Bcl-2)及Bcl-2 相关X 基因(Bax)的表达而抑制细胞凋亡,可明显改善糖尿病小鼠的肾脏结构和功能,减少尿蛋白,延缓DN 的发生和发展。药理研究[22]显示,川芎可抗血小板聚集,扩张小动脉、改善血液循环,进而增加肾脏血流通量,对肾脏高凝状态起到一定的改善效果,此外还具有一定的抗炎效果,可减少肾脏的炎症反应。
目前DN 患者的治疗具体可分为4 个主要方面:降低心血管风险、控制血糖、控制血压和抑制肾素-血管紧张素系统(RAS)。血管紧张素Ⅱ是RAS 的主要活性物质,为强效的血管收缩剂,在高血压的病理过程中起主要作用。血管紧张素Ⅱ在多种组织内与AT1 受体结合,产生包括血管收缩和醛固酮释放在内的多种重要的生物学效应。体内外研究[23]表明:氯沙坦及其具有药理活性的羧酸代谢产物(E-3174)可以阻断血管紧张素Ⅱ所产生的相应生理作用。玉蚕颗粒的作用机制复杂、作用途径多样。前述研究表明,黄芪、川芎具有抗炎、降低心血管风险的作用,同时玉米须、蚕茧壳与免疫调控也息息相关,可针对DN 病理因素,有效改善肾脏结构和功能,从而延缓DN的发展。
本研究结果显示,玉蚕颗粒干预后,DN 小鼠血糖降低,肾组织病理损伤明显减轻,且足细胞损伤状态改善,说明玉蚕颗粒可以减轻DN 小鼠肾组织的损伤。足细胞是肾脏滤过屏障的重要组成部分,WT1 和Nephrin是足细胞特异性标志物。Western blot和免疫组织化学染色结果显示,与正常组比较,模型组WT1 和Nephrin表达降低,而与模型组比较,中药各剂量组WT1 和Nephrin 表达升高。免疫组织化学染色结果与Western blot结果一致,表明玉蚕颗粒可能是通过改善足细胞损伤从而缓解DN小鼠肾组织损伤。
本研究仅从足细胞保护的角度初步探讨了玉蚕颗粒改善DN 小鼠疾病进展的作用机制,玉蚕颗粒能否通过其他途径改善DN 小鼠肾损伤,有待进一步深入研究。另外,中药复方调控机制复杂,作用途径多样,其在临床医学各领域中都大有作为,特别是在糖尿病、肾脏病、蛋白尿等方面的应用,具有较好的应用前景,但还需药理学、病理学研究进一步分析其作用机制,临床效用评估也仍待进一步考究。未来可通过合理应用生物工程技术改善药物提纯水平、分析药物有效成分的分子结构而发现药物新用途,从而进一步探索玉蚕颗粒在细胞生理、病理过程中的作用机制,以期全面发挥其临床价值。
