多参数MRI影像组学模型鉴别高级别胶质瘤与原发性中枢神经系统淋巴瘤的价值
2023-11-07张少茹周云舒张若弟刘世莉陈晓华王卓陈志强
张少茹,周云舒,张若弟,刘世莉,陈晓华,王卓,陈志强
0 前言
原发性中枢神经系统淋巴瘤(primary central nervous system lymphoma, PCNSL)是一种罕见的淋巴结外非霍奇金淋巴瘤,局限在中枢神经系统,其与脑胶质瘤都具有恶性程度高、预后差的特点[1]。非典型PCNSL 常常伴有坏死、囊变等,无坏死或很少坏死的非典型脑胶质瘤也可能模仿典型PCNSL,尽管它们在影像学表现上有一些可区分的特征,但这些特征是主观的,依赖于放射科医生的专业知识和经验[2-4]。目前,疑似PCNSL的标准诊断方法包括立体定向活检和组织病理学分析,然而,这种方法是侵入性的[5],此外PCNSL 的治疗与其他原发性中枢神经系统肿瘤有很大的不同,对于新诊断的PCNSL患者采用甲氨蝶呤的大剂量联合治疗并在诱导治疗时采用包含利妥昔单抗的方案是目前我国专家的治疗共识[6],而脑胶质瘤的主要治疗方案则是大体全切除后进行放、化疗[7-8],因此早期且准确无创的诊断可以避免不必要的手术。影像组学作为新型的研究领域使医学成像从一种简单的诊断工具转变为巨大的临床数据的来源,影像组学在肿瘤诊断、分级、预后和预测基因分型等方面提供了重要帮助[9-13],且这种方法是非侵入性的,可以获得肿瘤中潜在的信息[14-16]。一些功能MRI 技术能为肿瘤的鉴别诊断提供信息,但由于测量方法缺乏标准化,可能存在个体间的差异性,且这些先进序列会延长扫描时间、增加额外的费用,相比之下影像组学特征是定量的数值特征且常规序列的应用范围更广泛[17],不同MRI 序列以及肿瘤分割区域的选择对影像组学模型性能的影响仍然值得探究[18]。本研究旨在探讨多参数MR影像组学模型能否在术前无创性地鉴别PCNSL 和高级别胶质瘤,确定不同MRI序列模型是否具有同等或更优的预测性能以及不同肿瘤ROI的勾画对预测模型性能的影响。
1 材料与方法
1.1 研究对象
回顾性分析2016 年1 月至2022 年7 月期间于宁夏医科大学总医院接受手术或立体定向活检的高级别胶质瘤和PCNSL 患者病例。纳入标准:(1)年龄≥18 岁;(2)接受手术切除或活检后病理证实为PCNSL或高级别胶质瘤;(3)所有PCNSL 均为弥漫性大B 细胞型,所有患者均具有免疫能力;(4)术前进行常规MRI 扫描。排除标准:(1)有其他脑肿瘤或外伤病史;(2)疑似或确诊的周围性淋巴瘤;(3)术前接受糖皮质激素、放疗或化疗的患者;(4)非强化病灶及肿瘤直径<1 cm 的患者。本研究遵守《赫尔辛基宣言》,经宁夏医科大学总医院伦理委员会批准(批准文号:KYLL-2022-0591),免除受试者知情同意。
1.2 仪器及检查方法
使用GE SIGNA EXCITE 3.0 T MR扫描仪和8通道头部相控阵线圈进行图像采集。T1WI 扫描参数:TR/TE 2076 ms/27 ms;T2WI 扫描参数:TR/TE 4600 ms/107 ms;T2 液体衰减反转恢复(fluid-attenuated inversion-recovery, FLAIR)扫 描 参 数:TR/TE 7800 ms/140 ms;对比增强(contrast enhancement,CE)T1WI 扫描参数:TR/TE 2300 ms/13 ms;以上序列FOV 均为240 mm×240 mm, 层厚、层间距均为6.0 mm、1.0 mm。对比剂使用钆喷酸葡胺,剂量为0.1 mmol/kg,注射流速2.0 mL/s。
1.3 图像分割及预处理
肿瘤的分割是由一名具有3 年放射学经验的医学研究者使用3D-Slicer(http://www.Slicer.org, version 5.0.3)软 件 在 轴 位CE-T1WI、T2 FLAIR 图像进行逐层手动勾画,并由另一位经验丰富的神经放射学家进行验证。ROI1 包括肿瘤核心(坏死、囊变和增强区域)排除瘤周水肿,ROI2 包括肿瘤核心及瘤周水肿区,于轴位CE-T1WI 图像进行ROI1 的勾画,T2 FLAIR 图像分别进行两种ROI 的勾画,ROI1 的勾画暂且称为T2 FLAIR1,ROI2 的勾画称为T2 FLAIR2,对于多发病变选取较大病灶进行ROI勾画(图1)。预处理对于提取稳定的特征和获得可重复性的结果至关重要,本研究将所有体素重新采样到1 mm×1 mm×1 mm,随后使用灰度离散化处理(bin宽度为25),将连续图像转换为离散的整数值来减少扫描方案等的影响。
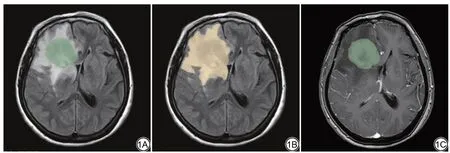
图1 使用3D-Slicer软件手动逐层勾画ROI。1A 为T2 FLAIR 上勾画肿瘤核心的ROI,1B 为T2 FLAIR 上勾画肿瘤核心及瘤周水肿的ROI,1C 为CE-T1WI上勾画肿瘤核心的ROI。Fig.1 Using the 3D-slicer to manually delineate ROI layer by layer.1A is ROI which delineated the core of the tumor on the T2 FLAIR, 1B is ROI which delineated the core of the tumor and peritumoral edema on the T2 FLAIR, 1C is ROI which delineated the core of the tumor on the CE-T1WI.
1.4 数据的平衡
淋巴瘤是一种相对少见但高度恶性的肿瘤,本研究纳入病例中淋巴瘤较少,造成了数据的不平衡,对于大多数基于机器学习的分类模型,这种不平衡可能导致预测精度较低,本研究采用合成少数类过采样技术[19]来解决此类问题。
1.5 放射组学特征提取
使 用Python 软 件(http://www.python.org,version 3.7)中的“PyRadiomics”包进行特征的提取,分别从CE-T1WI及T2 FLAIR序列各提取1037个特征,特征类型及数量如下:14个形态学特征;18个一阶统计特征;75个纹理特征,5种特征类型分别为灰度共现矩阵(gray-level co-occurrence matrix, GLCM)、灰度运行长度矩阵(gray-level run length matrix, GLRLM)、灰度尺寸区域矩阵(gray-level size zone matrix,GLSZM)、灰 度 依 赖 矩 阵(gray level dependence matrix, GLDM)和邻域灰度差分矩阵(neighborhood gray-tone difference matrix, NGTDM),内置滤波器小波、平方、指数都在五个特征类别上启用。
1.6 特征的筛选及组学标签的建立
由于与样本量相比我们提取了大量的特征集,集中高度相关的特征以避免共线性是非常重要的,本研究的特征选择过程如下:(1)使用单变量选择法初始筛选出差异有统计学意义(P<0.05)的特征;(2)采用皮尔逊相关性分析剔除|r|≥0.4 的特征;(3)采用最小绝对收缩和选择算子(least absolute shrinkage and selection operator, LASSO)正则化去除共线特征;(4)采用多元逐步回归保留最小Akaike 信息准则(Akaike Information Criterion,AIC)的特征集,通过对选定特征按其各自的系数加权后进行线性组合来计算每个患者的影像组学评分。在进行特征分析前,所有的特征都经过Z-分数(Z-score)标准化:Z=x-μ/σ,其中μ为平均值,σ为体素值的标准差。
1.7 模型的构建及评价
采用逻辑回归(logistic regression, LR)方法构建分类模型,分别构建基于CE-T1WI、T2 FLAIR1和T2 FLAIR2 及CE-T1WI+T2 FLAIR1 共4 个影像组学模型,通过计算准确率、敏感度、特异度和ROC曲线下面积(area under the curve, AUC)来评估分类器的预测性能。
1.8 统计学分析
所有的统计分析均使用R 软件(http://www.r-project.org, version 4.1.2),采用Mann-WhitneyU检验、卡方检验或Fisher精确检验对高级别胶质瘤与PCNSL、训练集与验证集的临床及影像学特征之间的差异性进行统计学分析,P<0.05 认为差异有统计学意义。
2 结果
2.1 临床与影像资料结果
本研究共纳入99 例高级别胶质瘤和PCNSL 病例,分为训练集(n=69)和验证集(n=30),其中高级别胶质瘤73例,PCNSL 26例,肿瘤是否累及皮质在高级别胶质瘤和PCNSL 之间的差异具有统计学意义(P<0.05),与PCNSL相比,胶质瘤更易累及皮质(表1);在训练组与验证组之间,除了肿瘤的位置在两者之间存在略微的差异外,其他临床及影像学特征之间无显著性差异(P>0.05)。
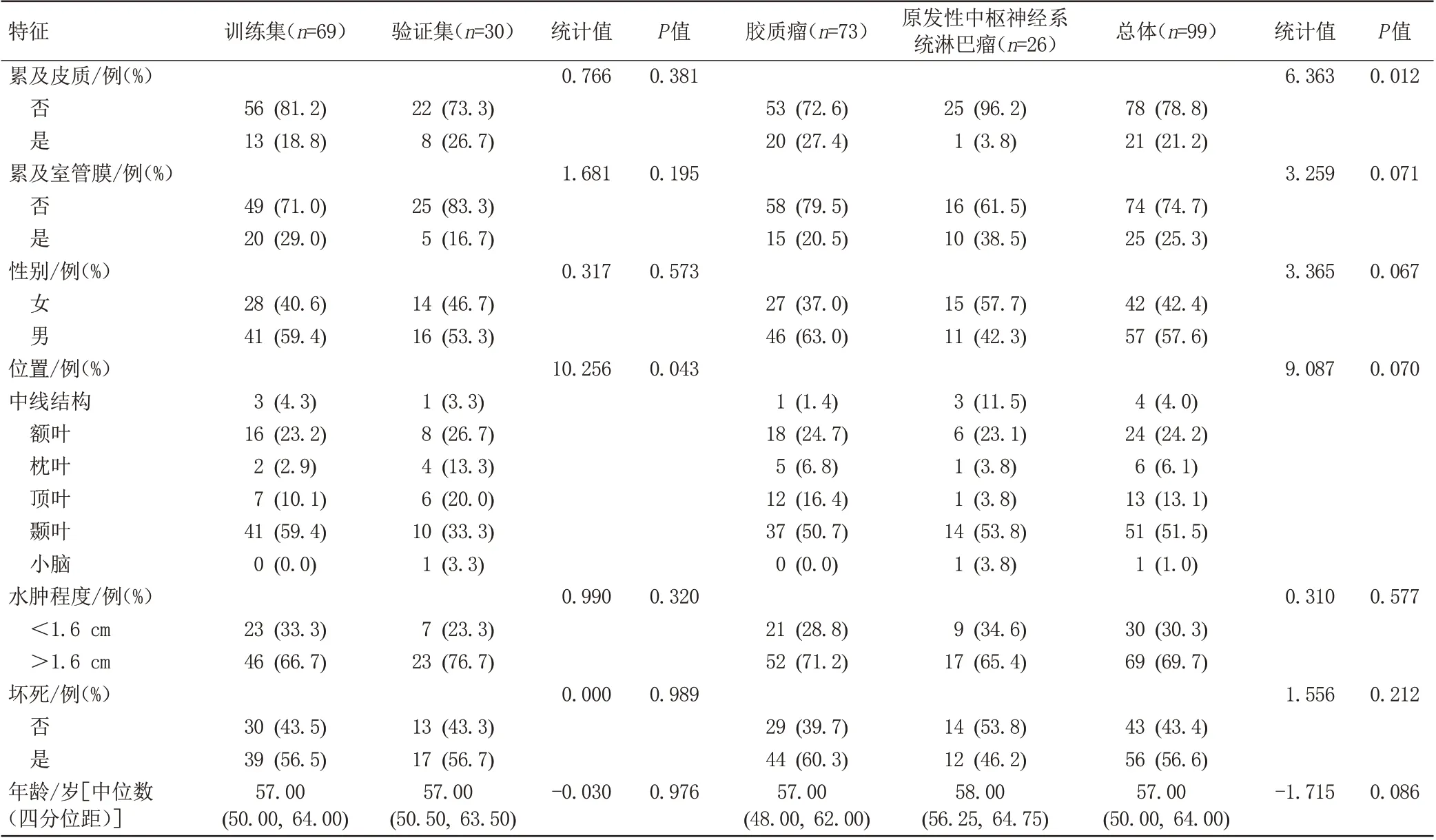
表1 高级别胶质瘤及原发性中枢神经系统淋巴瘤临床及影像学特征之间的比较Tab.1 Comparison of clinical and imaging features between high-grade glioma and primary central nervous system lymphoma
2.2 特征筛选及模型的评价
采用10 折交叉验证的LASSO 算法保留非零系数的影像组学特征,其中CE-T1WI、T2 FLAIR1、T2 FLAIR2 及CE-T1WI+T2 FLAIR1 序列分别保留12、11、6、15个组学特征(表2)。
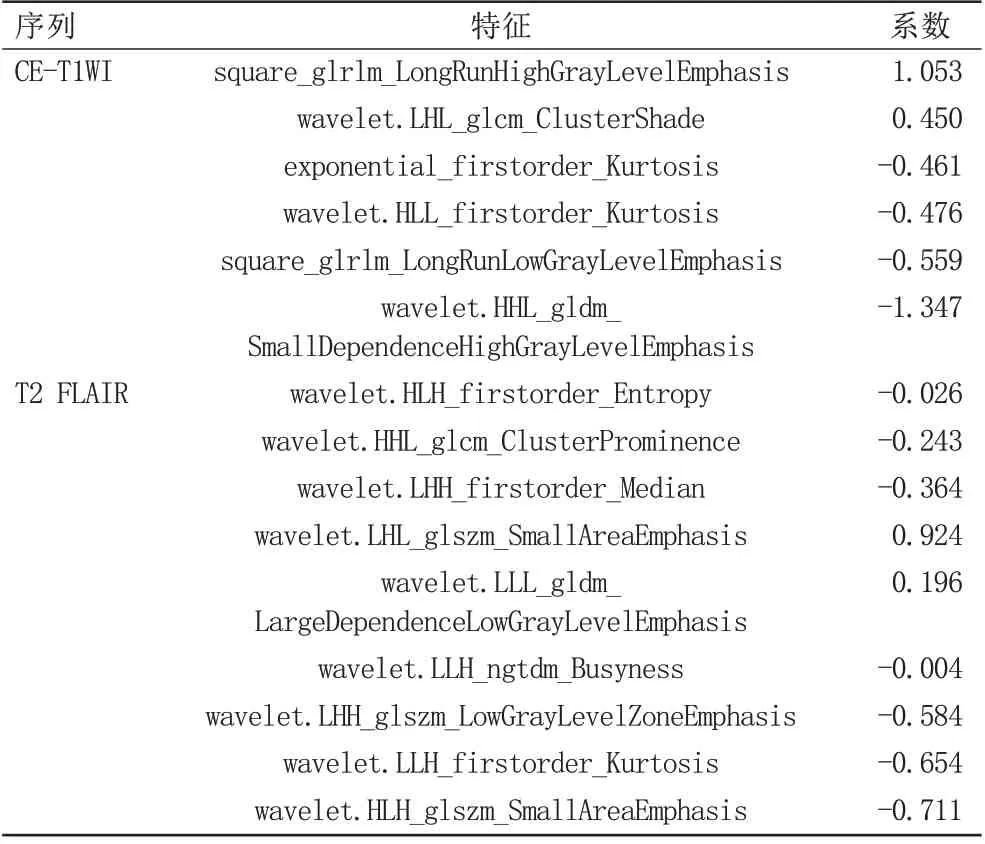
表2 构建联合模型的关键影像组学特征及其特征系数Tab.2 The key radiomics features and their corresponding coefficients from the combined radiomics model
各模型的ROC曲线如图2所示,单序列模型中,基于CE-T1WI 构建预测模型效能优于T2 FLAIR1 和T2 FLAIR2 模型,其在训练集及验证集的AUC 值分别为0.952 vs.0.915 vs.0.852 和0.949 vs.0.898 vs.0.841,准确率分别为92% vs.86% vs.80%和90%vs.77% vs.67%;本研究所构建的4个影像组学模型中,基于CE-T1WI+T2 FLAIR1构建的联合模型预测性能优于各单序列模型,其在训练集及验证集的AUC值分别为0.978和0.983,准确率分别为94%和93%(表3)。
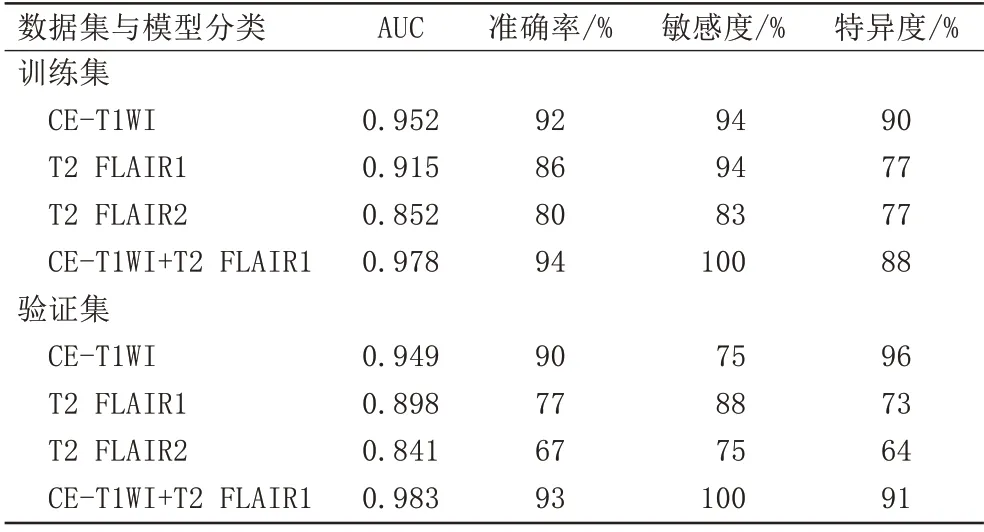
表3 各序列影像组学模型鉴别高级别胶质瘤与原发中枢神经系统淋巴瘤的性能评价表Tab.3 The performance of radiomics models in differentiating primary central nervous system lymphoma from high-grade glioma
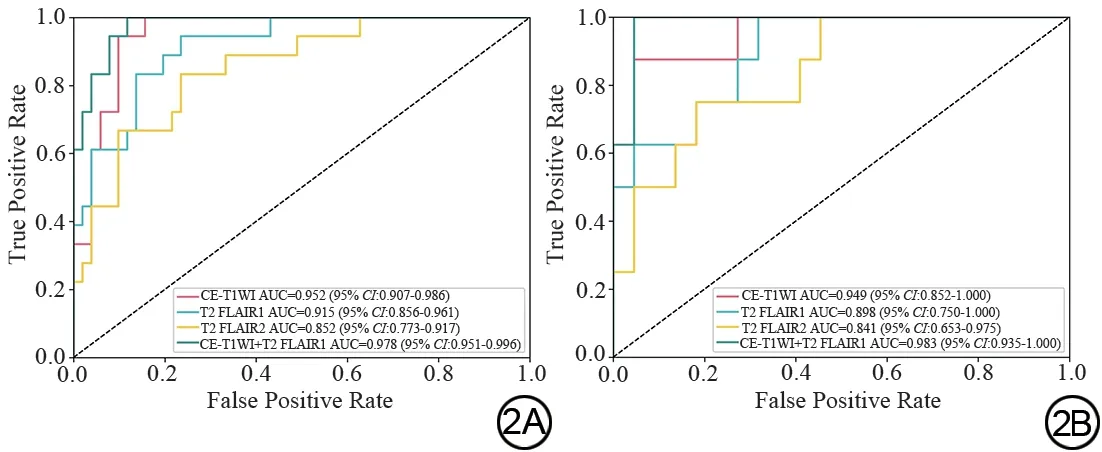
图2 各序列影像组学模型在训练集及验证集的受试者工作特征曲线,2A为训练集,2B为验证集。Fig.2 The receiver operating characteristic curves of the each radiomics model in the training and testing set.2A is training set, and 2B is testing set.
3 讨论
本研究基于CE-T1WI、T2 FLAIR1、T2 FLAIR2 及CE-T1WI+T2 FLAIR1 序列构建LR 模型用于术前无创性区分高级别胶质瘤和PCNSL,结果表明多参数MRI影像组学模型能在术前无创性鉴别高级别胶质瘤及PCNSL,不同序列预测性能不同,各单序列模型中,CE-T1WI模型预测性能优于T2 FLAIR模型;基于肿瘤核心特征所构建模型的预测性能优于基于全肿瘤提取特征;CE-T1WI+T2 FLAIR1 构建的联合模型能更进一步地提高预测模型的性能,能为术前区分高级别胶质瘤及PCNSL提供一种可靠且无创的方法。
3.1 临床及影像组学特征在区分高级别胶质瘤及PCNSL方面的价值
本研究中高级别胶质瘤与PCNSL两队列性别及年龄之间无明显差异(P>0.05),但有研究[6]指出,两者都多见于男性,这可能与我们纳入的病例太少有关,胶质瘤较PCNSL更易累及皮质[20-21],这也与本研究一致。
纹理特征是通过评估图像中像素的灰度强度和位置来量化肿瘤内的异质性[22-23],在最终筛选的非零影像组学特征中CE-T1WI序列的“GLRLM”获得了最高的权重,它是利用不同的波长、振幅和频率来识别图像内的纹理属性,它评估ROI 中像素或体素的百分比,反映不同灰度和运行长度的运行分布,“GLRLM”已被证实可以用来鉴别PCNSL 与胶质瘤[24]。基于单体素或像素分析得到的一阶特征如熵、峰度等也有助于两者的鉴别[25],内置滤波器对原始图像进行过滤和噪声的去除,这些转化的特征可以反映肿瘤微环境中的细胞学特征或分子的特异性表达[26],可以补充纹理信息来鉴别胶质瘤与PCNSL。
3.2 不同肿瘤ROI 的选择在区分高级别胶质瘤与PCNSL方面的价值
本研究分别以肿瘤核心区和肿瘤核心包含瘤周水肿区提取的特征构建了基于T2 FLAIR序列的组学模型,结果发现以肿瘤核心区域特征建立的组学模型性能较优越,PRIYA 等[18]从多个肿瘤的亚区域提取影像组学特征并构建肿瘤的分类模型,其中大多数高性能的特征是来自坏死和增强区域,即肿瘤核心,与本研究结论一致。有研究[27]对CE-T1WI 序列肿瘤坏死和实体增强(排除瘤周水肿)区域的特征进行纹理分析,最终得到交叉验证的平均AUC值为0.924,但其模型性能略低于本研究,原因可能是因为以上研究主要对于一阶特征进行了纹理分析,未涉及二阶及高阶特征。肿瘤的异质性不仅局限于肿瘤的实体还涉及水肿区域[19],KIM 等[28]利用CE-T1WI 序列肿瘤核心区域特征及T2WI 及ADC 序列肿瘤核心加瘤周水肿区域特征成功构建多参数LR 模型,其在训练组及验证组AUC 分别为0.979 和0.956。有研究指出[26]增加肿瘤增强边缘10 mm 内的影像组学特征区分胶质母细胞瘤、淋巴瘤、脑内转移瘤的分类模型得到了比仅使用瘤内和水肿区域特征的模型更高的性能,因此后续的研究中需要继续探讨肿瘤瘤周特征对鉴别PCNSL及其他神经系统肿瘤的价值。
3.3 不同MRI 序列在区分高级别胶质瘤与PCNSL 方面的价值
最近的一项Meta 分析[4]指出不管是机器学习还是深度学习在PCNSL 和胶质母细胞瘤鉴别方面表现良好,AUC 值在89.0%~98.2%之间,准确率最高为97.9%,最低为82.0%,其中基于不同MRI 序列建立的影像组学模型预测性能不同。本研究建立的多个影像组学模型在区分高级别胶质瘤与PCNSL 方面都表现出良好的诊断效能,其中CE-T1WI模型是最佳的单序列模型。XIA 等[29]基于CE-T1WI、FLAIR、DWI、ADC 序列建立了多参数影像组学模型鉴别胶质母细胞瘤及PCNSL,在单序列模型中,基于CE-T1WI序列建立的模型获得最高的AUC 值,AUC 值为0.937,该研究所得最佳的联合序列模型为CE-T1WI+ADC 序列,其AUC 值为0.943,本研究所建立预测性能略高于以上研究,主要原因为以上研究利用肿瘤核心外加瘤周水肿区域的影像组学特征建立预测模型,而本研究建立的最佳单序列模型及联合模型主要基于肿瘤核心特征构建。BATHLA 等[30]分别建立了基于T1WI、T2WI、FLAIR、ADC 及CE-T1WI 的单序列模型及多个序列组合模型,其中基于ADC、FLAIR 及CE-T1WI 构建的联合模型的预测效能最佳。由于我们的研究中具有ADC 序列的病例较少,本文未探讨ADC 序列的价值,在后续的研究中会继续该序列的探讨。有研究[31]构建多参数的卷积神经网络(convolution neural network, CNN)模型,基于FLAIR的CNN模型性能不如CE-T1WI模型,这可能是由于FLAIR 的水肿模式与肿瘤类型的相关性不如增强模式强。多项研究表明CE-T1WI 影像组学模型具有良好的诊断效能,此外多参数MR 影像组学模型通常优于单一序列[27,32-34],CE-T1WI 是脑肿瘤诊断中首选的MRI序列,其包含了肿瘤中局部血管生成和血脑屏障破坏的信息,可以清晰地显示肿瘤实体和坏死[6,35],且多参数的影像组学模型可以提供更多关于肿瘤生物学异质性的信息[28,36]。
3.4 本研究的局限性
本研究还存在以下局限性。(1)本研究的样本量小,且没有设立外部验证组,不可避免地存在模型的过拟合问题,在后续的研究中会继续扩大研究队列并增加外部验证组以提高预测模型的准确性及稳定性;(2)本研究纳入的临床及影像学特征较少,因此未构建临床预测模型;(3)本文仅构建用于区分PCNSL 与高级别胶质瘤的影像组学模型,PCNSL 还需要与其他中枢神经系统疾病进行鉴别,例如单发转移瘤、多发性硬化和肿瘤脱髓鞘等疾病,因此在后续的研究中可以增加多分类任务的研究;(4)本研究只是探讨了肿瘤核心与全肿瘤区域组学特征对预测模型的影响,未进一步探讨肿瘤更小亚区域特征对区分胶质瘤与PCNSL的价值,今后还需要进一步探究肿瘤更小亚区域特征对模型性能的影响;(5)本研究只构建了常规MRI序列的组学模型,后续还需探讨功能MRI序列在区分PCNSL及高级别胶质瘤中的价值。
4 结论
多参数MR 影像组学模型在区分PCNSL 和高级别胶质瘤方面具有良好的诊断效能,基于不同的MRI序列及肿瘤亚区域特征构建影像组学模型,其性能不同;在单序列模型中,基于CT-T1WI 模型预测效能最佳,联合模型预测性能优于单一序列模型;肿瘤核心区域特征与肿瘤的分类任务更相关。
作者利益冲突声明:全体作者均声明无利益冲突。
作者贡献声明:陈志强设计本研究的方案,对稿件重要内容进行了修改,获得了宁夏回族自治区重点研发计划项目、宁夏回族自治区自然科学基金和教育部春晖项目的基金资助;张少茹负责试验操作,试验参数调整,起草和撰写论文,获取、分析或解释本研究的数据;周云舒、张若弟、刘世莉、陈晓华、王卓参与本研究的数据收集、整理和分析,对论文主要内容进行核对;全体作者都同意发表最后的修改稿,同意对本研究的所有方面负责,确保本研究的准确性和诚信。
