生物质废弃物类型和水热pH 对人工腐殖酸性能影响
2023-11-04张睿含智燕彩贾明昊李晓娜王震宇
张睿含,智燕彩,贾明昊,李晓娜,2*,王震宇,2
1. 江南大学环境与土木工程学院/绿色低碳技术与可持续发展研究中心,江苏 无锡 214122;2. 江南大学/生物质能源与减排技术江苏省工程实验室,江苏 无锡 214122
动植物残体在土壤微生物及地球物理化学作用下,经过长达千百年的生物化学过程,最终形成具有芳香结构和丰富官能团的复杂大分子有机物质,称之为天然腐殖酸。天然腐殖酸中包括50.0%-66.0%的碳、20.0%-46.0%的氢和氧,以及丰富的氮、磷、钾大量元素和镁、铁、钙等微量元素(Erhayem et al.,2014)。此外,天然腐殖酸分子具有双亲性,有利于土壤保水保肥(Gomes de melo et al.,2016;Pramanik et al.,2019)。腐殖酸是组成土壤有机质的最主要成分,是土壤肥力的重要表征,关于土壤中腐殖酸的研究已经长达200 余年。
天然腐殖酸主要分布于土壤、泥炭等环境中,其中泥炭地是最富碳的生态系统,储存了三分之一的天然腐殖酸(Dargie et al.,2017)。但是,天然腐殖酸的形成需要严苛的自然环境、耗时长、杂质高,很难作为资源开发。研究表明,泥炭深层中的腐殖酸形成可能需要长达1.50 万年(Visser,1962)。此外,泥炭地仅覆盖了地球陆地表面不足3.00%的面积(Page et al.,2011)。因此,腐殖酸贫瘠是典型的土地资源退化现象之一,腐殖酸被称为保护黑土地的核心和解锁土壤肥力的金钥匙。
人工腐殖酸技术的需求日益迫切。自上而下的人工腐殖酸合成方法即通过绿色化学的方法将生物质废弃物高效地转化为人工腐殖酸。水热合成腐殖酸的过程包括生物质大分子(如,植物单宁和木质素)分解成多酚和醌基团等单体和单体缩合两个阶段(Adani et al.,2004)。该方法既减少了其自然分解的碳排放损失,还能使其固定成为土壤碳或植物碳而形成闭环,促进了碳封存和碳资源化,这是“碳中和”大背景下发展环境友好型低碳技术的必由之路。据统计,我国绿化废弃物年均可高达7.70×107t(李金朝等,2015),传统简单粗放的处理绿化废弃物的方法显然已不能满足当代社会绿色低碳发展的需求。以绿化废弃物为原料制备人工腐殖酸,为循环生态体系的构建提供新思路。
将生物质在酸碱条件下水热反应是模拟自然腐殖化的温和化学方法,所得人工腐殖酸含有丰富的含氧基团和大分子结构,与天然腐殖酸表面形貌高度相似(Yang et al.,2019)。我们的前期研究结果表明,水热合成人工腐殖酸与天然腐殖酸具有相似的表面结构和更加丰富的活性基团,具有显著的植物促生效果(Zhi et al.,2022)。此外,水热合成技术制备的人工腐殖酸可作为超级吸附材料,实现水中重金属和磷素的高效去除与回收(Du et al.,2020;Zhang et al.,2020)。然而,由于水热合成人工腐殖酸的研究还处于起步阶段,人工腐殖酸自身结构和组成非常复杂,原料类型和水热条件如何影响人工腐殖酸的性质还未知,这大大限制了对人工腐殖酸结构与功能关系的分析及对其环境作用机制的理解。因此,本研究以三类常见绿化植物生物质废弃物为原料,分别探究了酸性和碱性水热条件下的生物质水热合成人工腐殖酸的过程、产率和性质,以期为未来发展人工腐殖酸技术提供理论支撑。
1 材料和方法
1.1 原料与试剂
生物质原料收集自江苏省无锡市江南大学,原料类型包括乔木树枝(香樟树,Cinnamomum camphora)、灌木树枝(黄杨树,Buxus sinica)和树叶(香樟树,Cinnamomum camphora)。乔木树枝中纤维素和木质素含量分别为45.6%和34.0%,灌木分别为55.2%和30.7%,而树叶分别为59.8%和24.4%。实验所用试剂包括盐酸、氢氧化钾和硝酸等均为分析纯,购自国药沪试。
1.2 实验设计与水热合成方法
水热合成方法参考Yang et al.(2019)和Zhi et al.(2022),并进行改进(Zhi et al.,2022)。操作如下:将收集到的原料自然风干后进行粉碎便于反应充分。水热反应在300 mL 高压釜中进行,原料添加量为3.00 g,固液比1∶20(Zhi et al.,2022),通过加入盐酸和氢氧化钾调节反应溶液pH 为2、5、9 和12。将反应釜容器密闭并放置于烘箱中,加热至200 ℃保持12.0 h,待温度自然冷却至室温后,取出反应釜。通过0.45 μm 的定性滤膜将未反应原料与液体产物分离,所得液体视为人工腐殖酸(Yang et al.,2019;Zhi et al.,2022)。将乔木为原料制备的人工腐殖酸分别命名为QW-2、QW-5、QW-9 和QW-12,灌木为原料制备的人工腐殖酸分别命名为GW-2、GW-5、GW-9 和GW-12,树叶为原料制备的人工腐殖酸分别命名为ZL-2、ZL-5、ZL-9 和ZL-12。所制备的人工腐殖酸在密闭、避光的4 ℃环境中保存待测。以上各处理均重复3 次。将未反应原料自然风干称重,其与原料添加量的质量差值占原料总添加量的比即为原料降解率。
1.3 人工腐殖酸性质表征
人工腐殖酸的pH 和电导率(EC,Electrical Conductivity)分别通过pH 计(SevenCompactTM,Mettler,瑞士)和电导仪(SevenCompactTM,Mettler,瑞士)测定。人工腐殖酸中总有机碳含量通过总有机碳分析仪(TOC-VCPH,SSM-5000A,Shimadzu,日本)测定,测定过程通入高纯氧气,燃烧管温度850 ℃。人工腐殖酸中营养元素的含量使用电感耦合等离子体质谱仪(ICP-MS)(iCAP-TQ,Thermo Fisher,美国)测定;测定过程中以氩气辅助气,流速1.50 L·min-1,以氩气为冷却气,流速15.0 L·min-1,以氩气为雾化气,流速0.80 L·min-1,测定功率为1.20 kW,MS 的条件和参数设置如下:持续时间为18 min;最大IT 为100 ms;扫描范围70.0-1.05×103m·z-1。人工腐殖酸的荧光组分通过三维荧光光谱仪(F-320,Agilent Technologies,美国)及其配套的工作站软件完成表征(Chen et al.,2003;Gu et al.,2015),仪器分析条件设定为:激发波长(Ex)的范围为200-500 nm,发射波长(Em)的范围为250-600 nm,扫描间隔均为5.00 nm,响应时间设为自动;激发和发射狭缝宽度为5.00 nm,扫描速度为1.20×103nm·min-1。人工腐殖酸经冷冻-真空干燥箱(FD-1A 50,上海比朗,中国)冷冻干燥,用于表面官能团分析。人工腐殖酸的表面官能团使用傅里叶变换红外光谱仪(FTIR,Fourier Transform infrared spectrometer)(IRTracer-100,岛津公司,日本)测定。
1.4 数据分析
本研究中数据处理采用Microsoft Excel 和SPSS 13.0 软件进行,数据显著性分析主要采用t检验,置信区间设置在95%分位,即P<0.05 时认为具有显著性差异。文中图表使用Origin 2022 和Microsoft Excel 绘制。
2 结果与讨论
2.1 不同原料的降解率
水热合成人工腐殖酸过程中,3 种原料在不同水热pH 下的降解率均高于40.0%(图1)。随着水热溶液pH 从2 上升至12,乔木生物质的降解率逐步提高,在pH 为12 的溶液中降解率最高可达59.0%;树叶生物质的降解率则随着pH 的上升而降低,在pH 为2 的溶液中降解率为59.3%,在pH 为12 的溶液中降解率仅为41.0%;而水热溶液pH 对灌木的降解率影响不大。碱性溶液更有利于难分解的木质素中酯键、醚键及碳碳双键的断裂,并削弱纤维素和半纤维素中氢键的结合能,增加酶和自由基等对生物大分子的可及性(Alonso-simon et al.,2010;Piccolo et al.,2019)。因此,木质素含量较高的乔木生物质降解率随溶液pH 的增加而上升。而对于木质纤维素含量相对较低的落叶,其在较温和的水热环境中即可完成水解(Ksiezopolska,2005)。在酸性溶液中,纤维素中苷键如 (1-4)-β-苷键易发生水解断裂,使纤维素和半纤维素聚合度降低,且随着酸度增加,纤维素水解中间产物中水合氢离子数量增加,水解反应更加剧烈(Girisuta et al.,2006)。因此,酸性溶液促进纤维素和半纤维素的水解而对木质素分解效果不显著,本研究中纤维素含量较高的树叶生物质降解率随溶液pH 升高而降低,在pH=2 溶液中降解率最高。

图1 水热合成人工腐殖酸过程中不同原料在不同溶液pH 下的降解率Figure 1 Degradation rate of different raw materials in solution with different pH during the hydrothermal synthesis of artificial humic acids
水热腐殖化过程包括了原料的分解、重组和自缩合过程。通常,生物质中碳水化合物进行反羟醛加成反应,并在水热过程中被分解为含羟基和酮酸的有机酸分子,具有较高的水溶性(李金朝等,2015;Yang et al.,2019)。木质素可在中性和碱性条件下水解为酚类物质,同时使碳质骨架进一步重组和缩合,溶液pH 逐步降低呈自中和过程(Yang et al.,2019)。水热环境中pH 对灌木生物质的降解率并未产生显著影响,这可能主要是由于该类原料中木质素和纤维素含量相当,木质素纤维结构的碳骨架坍塌影响了自由基对键的作用,降低其对剩余木质纤维素的可及度,整个水热过程中保持木质素和纤维素水解的相对平衡(Akin,2008;吉喆,2016)。
2.2 人工腐殖酸的理化性质
天然腐殖酸的形成涉及非生物和生物反应,其中生物反应过程消耗大量的碳。通过水热腐殖化的化学方法合成人工腐殖酸,生物质中碳主要进入腐殖化产物,具有比天然腐殖化过程更优异的碳产量(Yang et al.,2019)。在水热腐殖化过程中,生物质中碳主要以可溶性有机碳的形式存在于人工腐殖酸产物中。溶液中总有机碳是衡量人工腐殖酸中有机物总量的重要指标,也是表示人工腐殖酸产量的关键。如图2a 所示,3 种生物质原料均在碱性(pH=9 和pH=12)条件下具有更高的有机碳产量,约为酸性条件下(pH=2 和pH=5)总有机碳产量的2 倍,这可能是与碱性条件下木质素分解更为完全有关。与木质素的网状无定型高聚物结构相比,纤维素是由D-葡萄糖单体以β-1, 4 糖苷键连接形成的链状高分子聚合物,具有更高的碳组分和亲水性。因此,如图2a 所示,由纤维素相对含量较高的树叶生物质制备的人工腐殖酸(ZL-12)中总有机碳含量最高,为2.60 g·L-1。虽然树叶在碱性条件下降解率降低,但是ZL-12 的人工腐殖酸产量最高,这可能与强碱条件下纤维素分解的中间体缩合程度较高有关。可见,由于水热腐殖化过程包括了分解和缩合两个过程,原料降解率并非人工腐殖酸产量的有效评价指标。

图2 不同原料及pH 条件下制备人工腐殖酸的总有机碳含量,pH 值和电导率Figure 2 Total organic carbon content, pH and electrical conductivity of artificial humic acids prepared under different raw material and pH conditions
水热腐殖化是一个自中和过程,因此,无论初始溶液为强酸性或强碱性,所制备的人工腐殖酸均为弱酸性或中性溶液(图2b)。在水热反应过程中,木质纤维素水解产物以小分子酸和酚类物质为主,且生物质原料根据环境酸碱度分解出相反性质的有机单体,这类物质促进溶液pH 向中性推进(Yang et al.,2020)。天然腐殖化过程与水热腐殖化过程相似,因此,富含天然腐殖酸的黑土地pH 通常接近中性。腐殖酸的核心结构为植物单宁、木质素、葡萄糖苷等分解合成的多酚和醌基等芳香化合物,这些物质的解离使腐殖酸呈酸性(Gomes de melo et al.,2016)。在本研究中,碱性水解条件下,乔木和灌木生物质原料制备的人工腐殖酸酸性强于树叶生物质制备的人工腐殖酸;QW-9 和QW-12 的pH 分别为3.30 和4.00,GW-9 和GW-12 的pH 分别为3.70 和3.60,而ZL-9 和ZL-12 的pH 分别为4.60 和4.70(图2b)。这是由于木质素通常是将酚类结构位点缩合进入腐殖酸中的重要反应前体(Yang et al.,2020)。与树叶相比,乔木和灌木生物质中具有更高木质素相对含量,因此,其所制备的人工腐殖酸酸性更强。
人工腐殖酸在环境修复领域中的应用主要是参与污染物的氧化还原过程(Wei et al.,2022),这与其导电性有关。测定了所制备的12 种人工腐殖酸的电导率可知,相同溶液pH 条件下,ZL 为原料制备的人工腐殖酸电导率强于GW 强于QW(图2c),说明原料中木质素含量越低,所制备的腐殖酸导电性越强。这是由于这类原料所制备的腐殖酸中通常含有醌-酚结构,有利于氧化还原反应中电子传递(Xiao et al.,2020;Monda et al.,2021;Wünsch et al.,2022)。此外,纤维素分解使人工腐殖酸中含有丰富的氮和硫基官能团,这也是其具有电子转移能力的关键(Tang et al.,2014;Li et al.,2021)。此外,溶液pH 也会影响同种原料制备人工腐殖酸的导电性(图2c)。3 种原料制备人工腐殖酸的导电性均表现为随着溶液pH 的升高先降低再上升的趋势,其中pH=9 所制备的人工腐殖酸导电性最差,QW-9、GW-9 和ZL-9 的EC 值分别为1.40、1.10、1.70 mS·cm-1,pH=12 所制备的人工腐殖酸导电性最强,QW-12、GW-12 和ZL-12 的EC值分别为2.20、2.50、3.10 mS·cm-1,因此,与弱酸弱碱条件相比,强酸强碱更有利于人工腐殖酸导电性的增强。这可能是由于强酸强碱促进了木质纤维素中芳香组分的分解氧化,形成更多羧基、羰基等极性官能团(Yang et al.,2020)。不同人工腐殖酸的表面官能团表征将在后文中详细陈述。
2.3 人工腐殖酸的营养价值
人工腐殖酸可以作为合成有机肥料供给植物生长过程中所需营养元素(Maggioni et al.,1987;Khaled et al.,2011)因此,其在提高农作物品质和产量方面效果显著。本研究测定了制备的12 种人工腐殖酸的营养价值。结果表明,水热溶液的pH和原料类型均会影响人工腐殖酸的营养价值。如图3 所示,与弱酸弱碱条件相比,强酸强碱条件下制备的人工腐殖酸具有更高的营养元素总量;强酸环境(pH=2)主要提高了人工腐殖酸中钠、钙和硫等微量元素,而强碱环境(pH=12)主要提高了人工腐殖酸中钠、硫和钾的含量。3 种原料在pH=9 时制备的人工腐殖酸均具有最弱的营养价值(图3)。这可能是由于该温和的条件对木质素的分解作用小,木质素芳香剂结构将营养元素固持在原料中而非溶解在人工腐殖酸中。
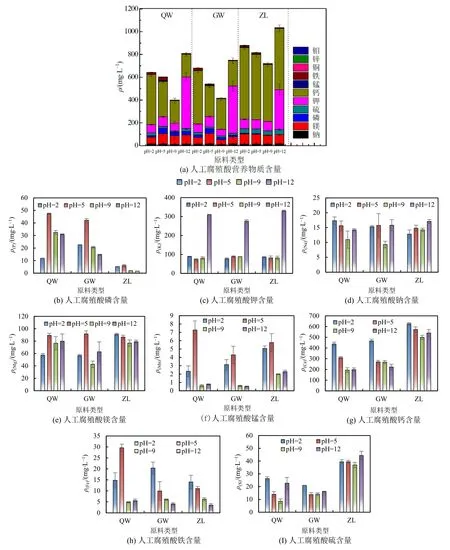
图3 不同原料及pH 条件下制备人工腐殖酸的营养元素含量Figure 3 Nutrient content of artificial humic acid prepared under different raw material and pH conditions
硫施加可通过调节土壤氧化还原电位和pH,增加土壤养分有效性,显著提高作物产量(Wang et al.,2015;钱晓华等,2018)。另有研究表明,在砷污染土壤中施加硫酸钠,显著抑制水稻地上部对砷的吸收累积,降低稻米的砷污染风险(邹丽娜等,2018)。另外,钠是典型碱金属元素,是维持土壤酸碱平衡,促进农业水分循环和土壤保水保肥的关键,也是提高作物产量和品质的重要营养元素。但是,丰富的钠元素也对该类人工腐殖酸的应用提高要求,避免造成土壤盐渍化,抑制植物对养分和水分的吸收(王艺乔,2022)。强碱条件下(pH=12),乔木、灌木和树叶为原料制备的3 种腐殖酸中钾的含量均显著增加,分别为310、275、329 mg·L-1。当pH=9 时,3 种人工腐殖酸中钾含量仅分别为79.0、89.0、82.0 mg·L-1。因此,我们推测强碱条件促进了原料中钾的释放和提取,提高人工腐殖酸中钾含量。弱酸(pH=5)环境的水热合成过程提高人工腐殖酸中镁、锰和磷元素的含量,但不利于硫和钾元素的保留(图3)。研究表明,磷施加显著促进马铃薯幼苗的生长发育,增强马铃薯中淀粉含量,增强马铃薯的环境适应能力(Chun et al.,2014;程瑶,2021)。锰在酶的激活、氧化和存活及蛋白质和碳水化合物的合成与代谢中起着重要作用,因此,锰施加可显著提高马铃薯产量和品质(Mousavi et al.,2007)。硫酸镁促进马铃薯根系生长发育,有利于块茎膨大(王彦宏,2010)。可见,弱酸(pH=5)水热条件制备的人工腐殖酸可能是块茎类作物的重要肥料。
树叶原料制备的人工腐殖酸中含有最高的硫含量(图3)。硫是铁氧还原蛋白和作物叶绿体基粒片层中硫脂的重要组分,为植物补充硫元素有利于提高其光合作用(孙丽娟等,2014),因此,这类人工腐殖酸是叶菜类作物的良好肥料。此外,人工腐殖酸的硫元素主要以硫基官能团的形式存在,其具有强电子转移能力(Sardessai,1999;Sachs et al.,2010;Schmeide et al.,2012),因此,该类人工腐殖酸具有最强的导电性能(图2c)。此外,ZL-12中尤其含丰富的钾元素。众所周知,钾是电和磁的良导体,将富含钾的腐殖酸应用于重金属污染环境中,有利于重金属的吸附去除(梁成华等,2005)。以灌木或乔木为原料在pH=5 的水热环境下制备的人工腐殖酸中富含磷元素(图3),该类人工腐殖酸施加是解决土壤缺磷问题的重要切入口。此外,人工腐殖酸中的磷还可以提高土壤中磷的有效性,增强土壤微生物活性,促进农田生态系统中磷的周转,作为植物生长剂促进作物养分吸收(Gerke,2021)。
2.4 人工腐殖酸的红外光谱图
人工腐殖酸表面官能团是其环境应用的关键(Gomes de melo et al.,2016;Peng et al.,2022)。例如,人工腐殖酸表面的羧基、酚羟基、醇羟基和甲氧基等含氧官能团可以与金属形成稳定的化学键,通过络合固定重金属,降低其迁移性和生物有效性(Olaetxea et al.,2018;Xu et al.,2019;Wei et al.,2022)。不同原料和pH 条件对人工腐殖酸的表面官能团类型无显著影响,但对各个官能团的相对含量有所改变(图4)。12 种人工腐殖酸在3 100-3 400 cm-1波数范围内均有很宽的吸收峰,表明腐殖酸羧酸中酚羟基结构基团缔合形成的氢键(王波等,2009;杜贺贺等,2018),这也决定了人工腐殖酸的水溶性;在2 800-3 000 cm-1波数范围内的吸收峰表明了脂肪性-CH3和-CH2的拉伸振动(Crespilho et al.,2005;Zara et al.,2017),这些官能团可能是来自于原料中脂肪族化合物和碳水化合物的分解;在1 510-1 520 cm-1波数范围内的吸收峰是由于酰胺中-NH 的拉伸振动引起的(Crespilho et al.,2005;Zara et al.,2017);在1 130-1 230 cm-1波数范围内的吸收峰可归因于羧基基团的C=O 拉伸和醚键、羟基等的C-O 峰的吸收振动(Rodriguez et al.,2014);在1 053-1 105 cm-1波数范围内的吸收峰是由于脂肪族C-O 峰的吸收震动(Votolin et al.,2022),这归结于纤维素的分解;在650-900 cm-1波数范围内的吸收峰是由于芳环上C-H 键的面外变形振动(徐栋等,2003);此外,人工腐殖酸在469-695 cm-1波数范围内的吸收峰是无机矿物的震动振动峰(徐栋等,2003),这可能归结于原料中矿质营养元素。
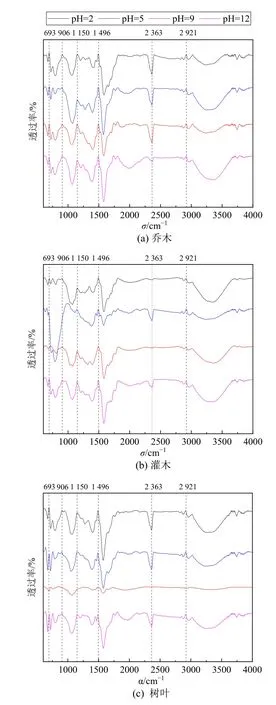
图4 不同原料及pH 条件下制备人工腐殖酸的红外光谱图Figure 4 Infrared spectra of artificial humic acids prepared under different raw materials and pH conditions
当水热溶液pH=9 时,乔木、灌木和树叶为原料制备的人工腐殖酸中官能团数量及吸收峰强依次减弱(图4)。当水热溶液pH=2 时,在1 400 cm-1和1 575 cm-1波数附近的吸收峰由人工腐殖酸中-COO 的反对称伸缩振动和对称伸缩振动引起,该吸收峰强度依次为ZL-2、GW-2 和QW-2(Dick et al.,2004;Rodriguez et al.,2014;Zara et al.,2017),但当水热溶液pH=5、9 或12 时,乔木原料制备的人工腐殖酸在该处吸收峰强度则最高(图4)。当水热溶液pH=5 时,GW-5 和ZL-5 在650-900 cm-1波数范围内的吸收峰强均高于QW-5,表明前两种原料所制备的人工腐殖酸具有更加丰富的芳香结构。当水热溶液pH=12 时,3 种原料制备的人工腐殖酸表面官能团几乎完全一致,这是由于在该条件下,自中和过程更加充分。
人工腐殖酸中的亲水性官能团(如,羧基和酚基)主要参与金属离子的还原和络合。Xu et al.(2020)研究表明,酚羟基可以作为电子供体直接将Cr(VI)还原为Cr(III),或将电子转移到O2以产生更多的活性氧自由基间接参与Cr(VI)的还原,且后者贡献率约为30.0%。Dong et al.(2020)研究表明,腐殖酸中的羧基可以与自然水环境中的Ag+(浓度低于1 μg·L-1)结合,形成Ag+-腐殖酸配体并将Ag+然后还原为金属Ag。人工腐殖酸对重金属的溶解、吸附和络合对控制其环境健康风险和环境修复至关重要(Wu et al.,2020)。乔木富含木质纤维素结构,在水解过程中形成更多的羧基官能团(Yang et al.,2020),该类人工腐殖酸可用于重金属污染水体的修复。此外,人工腐殖酸中的疏水性官能团(如,烷基、醚、酰胺基团)可促进植物生长和改善土壤性质(Spaccini et al.,2009;Jindo et al.,2012)。Jindo et al.(2012)研究发现,人工腐殖酸中的-CH2和酰胺基可以促进植物细胞壁或细胞膜或细胞质产生各种生物化学效性的相互作用,对植物生长具有有益作用(Spaccini et al.,2009)。3种原料制备的人工腐殖酸在2 800-3 000、1 510-1 520、1 130-1 230 和650-900 cm-1的波数范围内均具有明显的吸收峰,表明了疏水性官能团的存在,因此,所制备的人工腐殖酸可用于植物生长,在生态环境中具有较好应用前景。
2.5 人工腐殖酸的三维荧光光谱
人工腐殖酸中的特定结构位点和官能团可在特定入射光强处存在吸收并发出荧光。当水热溶液pH=12 时,3 种原料制备的人工腐殖酸在营养价值、导电性以及表面官能团能等性能方面均最佳。因此,进一步通过三维荧光光谱分析了该类人工腐殖酸的荧光物质组分。图5 为3 种人工腐殖酸的三维激发发射矩阵,结果表明,原料类型显著影响人工腐殖酸的荧光物质组成。
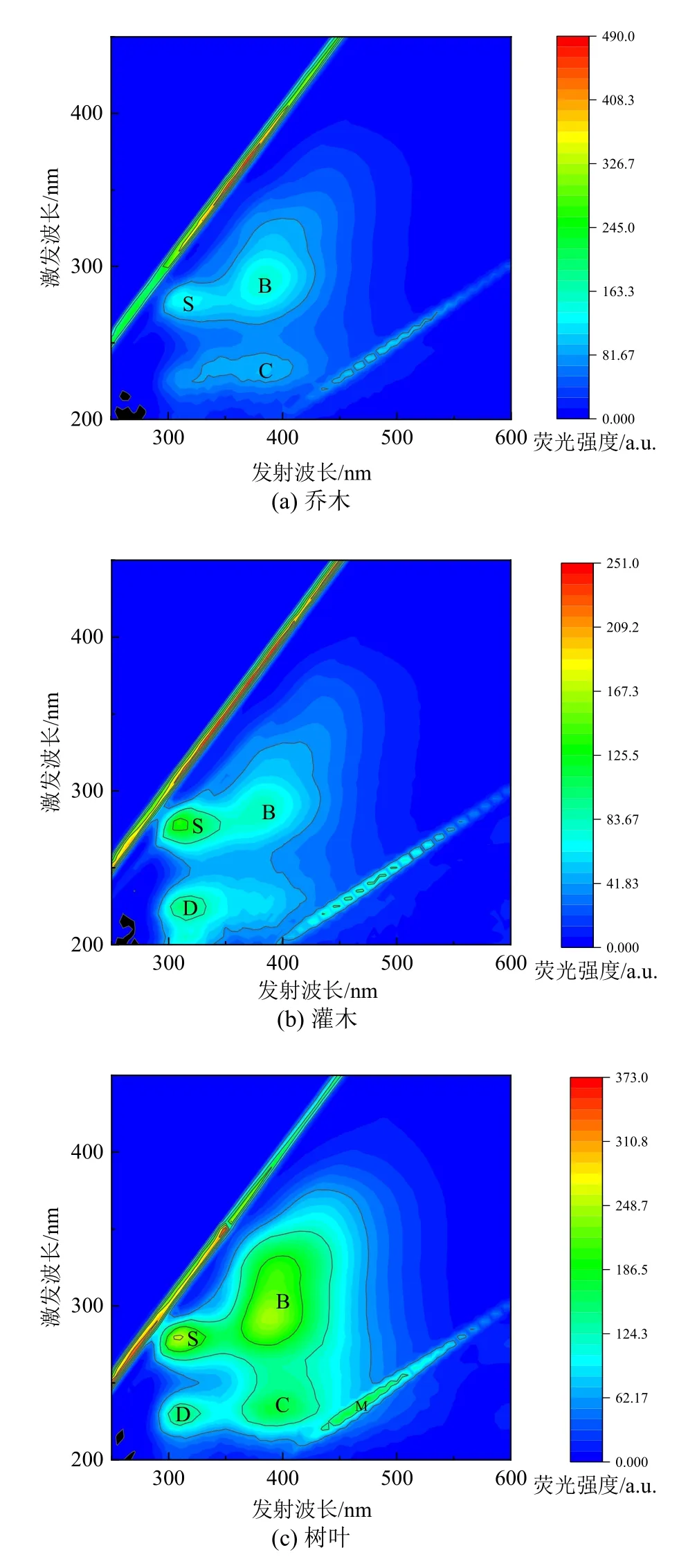
图5 pH=12 条件下3 种原料制备人工腐殖酸的三维荧光光谱图Figure 5 Three-dimensional fluorescence spectra of three raw materials at pH=12
3 种人工腐殖酸均含有荧光峰B(Ex=270-285 nm,Em=360-385 nm)和荧光峰S(Ex=270-285 nm,Em=310-335 nm),表明人工腐殖酸中的类蛋白结构,这与生物质原料中芳环氨基酸结构的分解有关(Wu et al.,2001;Wu et al.,2003a,2003b)。其中,荧光峰B 为类色氨酸特征荧光峰(宋凡浩,2018),QW-12、GW-12 和ZL-12 在该处的荧光强度分别为151、82.0 和241 a.u.。荧光峰S 为高激发波长类酪氨酸的特征荧光峰(傅平青等,2007),QW-12、GW-12 和ZL-12 在该处的荧光强度分别为133、134 和256 a.u.(图5)。ZL-12 在这两种峰均存在最高的荧光强度和最宽阔的峰带,表明该类腐殖酸种含有最丰富的低能量π-π 化学键,即在pH=12 时,树叶原料中芳香结构的π-π 化学键断裂最充分(姜杰等,2012)。
除共有的荧光峰S 和荧光峰B 外,ZL-12 中还含有荧光峰C(Ex=225-240 nm,Em=380-410 nm)、荧光峰D(Ex=215-235 nm,Em=300-330 nm)和荧光峰M(Ex=225-250 nm,Em=445-490 nm),GW-12 中还含有荧光峰D,而QW-12 中还有荧光峰C。荧光峰C 为类富里酸的荧光峰,这与人工腐殖酸中的羰基结构有关(姜杰等,2012)。QW-12 和ZL-12 在荧光峰C 处的荧光强度分别为97.0 a.u.和169 a.u.(图5),ZL-12 在此区域的峰带更加宽阔,这可能由于ZL-12 含有更加丰富的羰基。荧光峰D 为小分子色氨酸和酪氨酸的荧光峰(贾陈忠等,2012)。GW-12 和ZL-12 在荧光峰D处的荧光强度分别为103 a.u.和155 a.u.(图5),ZL-12 在此区域荧光强度较GW-12 更强,这表明ZL-12 含有更多的小分子物质,说明树叶在pH=12条件下的分解较乔木和灌木更加充分。荧光峰M 为紫外类富里酸荧光(祝鹏等,2010)。ZL-12 在该处的吸收强度是178 a.u.,这可能是由于树叶在pH=12 的水解过程中产生了更多的含氧官能团。
3 小结
(1)纤维素相对含量高的树叶制备人工腐殖酸,其原料降解率随溶液pH 升高而降低,所得人工腐殖酸具有较好的导电性、营养价值和荧光特性,而木质素相对含量较高的乔木制备人工腐殖酸,其原料降解率随溶液pH 升高而升高,所得人工腐殖酸具有较丰富的含氧官能团。
(2)强酸强碱条件下制备的人工腐殖酸具有较强导电性和较高的营养元素总量。其中,强酸(pH=2)的水热溶液提高人工腐殖酸中钠、钙和硫等微量元素的含量,强碱(pH=12)的水热溶液提高人工腐殖酸中钠、硫和钾的含量。
(3)强碱(pH=12)的水热溶液更有利于人工腐殖酸的制备,所得人工腐殖酸自中和最佳,有机碳产量最高,导电性的最强,且在营养价值和表面官能团等性能方面均最佳。
