超声造影在胰腺囊/实性病变诊断中的应用现状与进展
2023-11-02袁克荣邓雪松
袁克荣,邓雪松
(深圳市第二人民医院/深圳大学第一附属医院 肝胆胰脾外科,广东 深圳 518035)
随着医学影像技术的不断发展与进步,胰腺囊/实性病变检出率明显提高。CT、MRI等常规影像学检查因造影剂具有肾毒性、价格昂贵以及耗时等因素,导致它们在胰腺病变良恶性鉴别方面存在一定的局限性[1-3]。超声造影(contrastenhanced ultrasound,CEUS)检查是近年来迅速发展起来的一门新型技术,具有操作简单,经济且对患者无损伤等优点,并且能通过对病灶微灌注的情况进行实时、动态的观察,鉴别胰腺囊/实性病变的类型和性质,为临床上胰腺囊/实性病变的诊断提供了新的思路。为此,笔者对近年来CEUS在胰腺囊/实性病变的应用及研究进展作一综述,以期更全面了解CEUS在胰腺囊/实性病变定性分析的诊疗优势及面临的困难。
1 CEUS的原理及特点
CEUS的工作原理主要在超声交变声压的作用下产生非线性震荡,利用特殊的技术提取震荡后产生的谐波信号,同时抑制组织基波信号,从而实现清晰地显示组织及病变灌注信息及组织代谢状态[4]。造影剂是CEUS的基础和关键,其利用含有气泡的液体对超声波有强散射的特性来增强血流的超声多普勒信号和提高超声图像的清晰度和分辨率。第一代造影剂是以空气或氧气为核心,如CO2或混合空气的微泡,因其包膜厚、弹性差,在体内存在时间短,不能通过肺循环,只能用于心脏疾病的诊断,导致其在临床上应用较少。第二代造影剂是以蛋白或脂质包裹于空气微泡的表面,以利声显(Levovist)为代表,其在体内循环中稳定性较好,不易溶于水或血液,适用于低代谢性肿瘤的检测,并且可以进行实时连续超声检查。第三代造影剂主要为氟碳类气体等高分子量的气体,如声诺维(SonoVue)和示卓安(Sonazoid)等,其稳定性与有效性更佳,并且在体内持续时间较长,已成为腹部脏器CEUS检查的首选造影剂[5]。研究[6]表明,CEUS可显示内径细达40 μm的微血管,并可实时动态反映造影剂在肿瘤内的增强和消退的全过程,为诊断提供更为丰富的信息。
CEUS作为一种无创检查技术,已经在肝脏、乳腺等实质性脏器病变诊断方面发挥了重要作用[7-8]。CEUS诊断不同实质脏器性质所观察的参数有所不同。如CEUS诊断肝脏肿瘤时主要观察造影剂的造影时相变化,CEUS诊断原发性肝癌显示快速增强随后快速消退,表现为“快进快出”时相[9];CEUS诊断乳腺肿瘤良恶性时,主要观察病灶的灌注区域和增强模式,乳腺恶性肿瘤有粗大的滋养血管,在CEUS下表现为早期高增强并有较大片的灌注缺损区域[10];CEUS诊断甲状腺良恶性主要观察灌注模式,甲状腺恶性肿瘤主要表现为向心性低强化模式[11]。早在1991年,CEUS已开始应用于胰腺囊/实性病变定性诊断,Koito等[12]使用第一代造影剂CO2微泡对胰腺囊/实性病变进行鉴别诊断,结果显示CEUS诊断病变的敏感度和准确率分别为98%和95%,他们认为通过CEUS可以对胰腺病变内的微血管进行较好的判定,以此来区分病变的良恶性。目前,第三代造影剂SonoVue在临床应用最为广泛,成为CEUS诊断胰腺囊/实性病变主要的造影剂。
2 CEUS在胰腺囊/实性病变诊断中的应用
2.1 CEUS在胰腺囊性病变(pancreatic cystic lesions,PCL)诊断中的应用
PCL是指由胰腺上皮和(或)间质组织形成的含囊腔的病变,根据2010年WHO的胰腺肿瘤组织学分类标准,将胰腺囊性肿瘤(pancreatic cystic neoplasms,PCN)分为上皮源性肿瘤和非上皮源性肿瘤,上皮源性肿瘤包括各种类型的导管内乳头状黏液性肿瘤、黏液性囊性肿瘤、浆液性囊腺瘤等;非上皮源性肿瘤包括良性非上皮性肿瘤(如淋巴管瘤)和恶性非上皮性肿瘤(如肉瘤)等[13]。临床上为使PCL治疗简便,将其分为肿瘤性病变和非肿瘤性病变。胰腺肿瘤性病变包括胰腺浆液性囊性肿瘤(serous cystic neoplasms,SCN)、胰腺黏液性囊性肿瘤(mucinous cystic neoplasms,MCN)、胰腺导管内乳头状黏液性肿瘤(intraductal papillary mucinous neoplasms,IPMN)和胰腺实性假乳头状肿瘤(solid pseudopapillary neoplasms,SPN)。胰腺囊性非肿瘤病变主要为胰腺假性囊肿(pancreatic pseudocyst,PPC)、先天性真性囊肿和潴留性囊肿[14]。目前国际上对PCL还没有统一的影像学分类方法,大多数研究者把PCL按照肾囊肿的Bosniak进行分级[15],分为4种类型:I型,单腔囊肿,内含胰液,壁薄,无间隔或实性成分,常见类型为PPC;Ⅱ型,微囊性病变,囊腔壁薄,由多个小囊腔组成、呈分叶状,最多见的是SCN;Ⅲ型,多数为单囊,囊腔大,常见病变类型为MCN;Ⅳ型,内含实性成分或囊壁不规则增厚,常见类型为囊肿变性型腺癌和SPN[16]。
2.1.1 CEUS在SCN和MCN诊断中的应用 SCN和MCN是PCN的常见类型,分别约占PCN的16%、25%[17]。SCN绝大多数是良性肿瘤,恶变率极低,且患者无任何临床症状,基本采取保守治疗。MCN具有恶性倾向,目前临床上仍以手术切除为主[18-19]。因此,术前对SCN与MCN的准确鉴别尤为重要。金赟杰等[20]回顾性分析了10例经CEUS诊断的PCN,6例SCN和4例MCN的CEUS表现为囊壁及囊间隔区均可见增强;7例造影剂消退同步于胰腺实质,3例消退迟于胰腺实质。李爱丽等[21]用CEUS对90例胰腺囊/实性病变患者进行研究,结果显示,MCN与胰腺实质灌注时相同步,早期灌注增强较高,而晚期灌注增强较低;SCN灌注时相同步且增强幅度等同于胰腺实质,且CEUS诊断PCL准确率为74.4%。Wang等[16]研究了45例病理证实PCL的患者,结果显示SCN和MCN囊壁与囊内之间的间隔区增强,其余部分未有增强,CEUS诊断PCL的准确率为75.56%。卓娜等[22]收集了80例经病理为PCL患者临床资料,CEUS显示MCN囊壁及囊内间隔区呈高度强化,囊内无强化;SCN的增强模式与MCN相似。CEUS诊断PCL的准确率为75.00%,鉴别其良恶性的敏感度为70.00%、特异度为83.33%。刘阳等[23]使用CEUS对SCN与MCN进行鉴别诊断,发现SCN与MCN在CEUS动脉期主要表现为高增强或等增强,静脉期表现为低增强或等增强,CEUS的静脉期增强模式对鉴别SCN和MCN具有意义。上述研究表明,SCN和MCN的CEUS表现为动脉期囊壁及囊间隔区均可见增强,静脉期主要为低增强或等增强。SCN灌注时相和强度等同于胰腺实质;MCN与胰腺实质灌注时相同步,但早期灌注增强较胰腺实质较高。SCN与MCN的鉴别主要依据CEUS静脉期的增强模式,SCN在CEUS静脉期较少表现为低增强,而MCN在静脉期表现为低增强较多。
2.1.2 CEUS在IPMN诊断中的应用 1982年,Ohashi等[24]首次报道了IPMN,其起源于胰腺导管上皮,可以产生大量黏稠液阻塞主胰管或分支胰管,导致主胰管扩张或分支胰管囊状扩张。目前,国内外诊断IPMN主要的方式是CT、超声内镜和MRI,而使用CEUS进行诊断的研究报道较少。2005年,Itoh等[25]研究了21例行CEUS检查的IPMN,病变在CEUS下表现为胰管或侧支胰管囊性扩张,扩张的胰管内可见增强的乳头状结节。2012年,Kurihara等[26]对22例IPMN患者进行了CEUS检查,CEUS显示扩张的胰管内有明显的乳头状增强壁结节,并且壁结节中含有小血管,他们认为这种现象可能与IPMN的性质相关。Chen等[27]研究了20例行CEUS检查的IPMN患者,CEUS显示病灶与主胰管之间相通、扩张以及导管内壁结节增强。李爱丽等[21]对90例胰腺占位病变进行研究,CEUS显示IPMN灌注时相早于胰腺实质,早期灌注增强较高,而晚期灌注增强较低。综上所述,IPMN在CEUS下主要的表现为胰管扩张或分支胰管囊状扩张,囊壁内可见增强的乳头状壁结节,灌注时相早于胰腺实质,早期灌注高增强,晚期灌注低增强。CEUS诊断PCN显示病变有扩张的囊管或分支囊管内有增强的壁结节可作为IPMN的特征性表现。
2.1.3 CEUS在SPN诊断中的应用 1959年,Fratz[28]首次报道了SPN,其是一种罕见的、低度恶性或潜在恶性的PCN,直至1996年才被世界卫生组织正式将其命名为SPN[29]。潘燕等[30]使用CEUS对13例病理结果为SPN患者进行研究,发现CEUS显示病灶实性区增强早期为等增强,其囊性区无增强。祁晓英等[31]收集了52例SPN资料进行研究,CEUS显示病灶周边实质部分环状增强但内部不增强,他们认为这一特征可作为SPN的特征性增强模式。翟渊鹏等[32]研究了12例SPN患者,结果显示SPN在CEUS的增强期为高回声,减退期为低回声。Wang等[33]通过对210例胰腺病变患者进行研究,CEUS显示SPN囊性内部无增强,研究表明CEUS诊断SPN的准确率可达97.63%。由此可见,SPN的CEUS主要表现为病灶周边实质区高增强或环状增强,囊内部实性成分及分隔区呈稍高增强,而内部的囊液区不增强。
2.1.4 CEUS在PPC诊断中的应用 PPC是最常见的胰腺非肿瘤性囊性病变,常伴有急性胰腺炎发作病史和腹部外伤病史。PPC表现为单发或多发囊肿,形态类圆或椭圆形,囊肿壁较厚,其在常规US上呈现出典型的等回声或低回声像,在CEUS的任何时期均不出现增强[34]。据报道[35],CEUS在诊断PPC方面的敏感度和特异度高达100%。因此,欧洲医学和生物学超声协会联盟指南[36]指出,CEUS可准确区分PCN和PPC。以上研究表明,结合CEUS典型显影模式和病变解剖特征,在很大程度上可以鉴别胰腺占位病变的类型和性质,是良性还是恶性,为定性诊断提供重要参考价值。
然而,需要注意的是,PCL的非典型病变在CEUS表现下容易混淆,特别是Ⅳ型囊性病变,当病变囊内坏死出血时,性质难以区分,易被误诊为恶性病变,常需要结合其他的检查手段来确定病变性质。不同类型PCL的CEUS特征见表1。
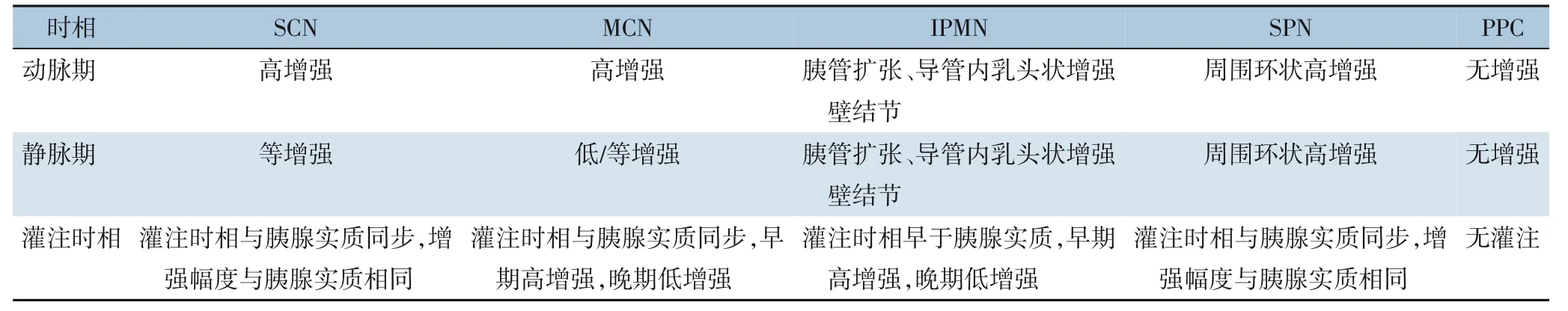
表1 不同类型PCL的CEUS表现特征Table1 CEUS characteristics of different types of PCLs
2.2 CEUS在胰腺实性病变(solid pancreatic lesions,SPL)诊断中的应用
2.2.1 CEUS在胰腺癌(pancreatic cancer,PC)诊断中的应用 SPL包括PC、胰腺神经内分泌肿瘤(pancreatic neuroendocrine tumors,PNET)及肿块型胰腺炎(mass pancreatitis,MP)[37]。PC在CEUS典型的表现为病灶增强较胰腺实质晚,达峰时间长,造影剂由病变周边缓慢向中央灌注,呈现低增强或向心性增强模式[38]。金赟杰等[20]研究表明,PC在CEUS增强期和减退期均为低回声,CEUS诊断胰腺恶性肿瘤的敏感度、特异度和准确率分别为80.0%、88.2%和85.2%。Fan等[39]通过对90例SPL患者进行CEUS检查发现,PC的CEUS表现为增强早期及晚期呈不均匀低增强,增强晚期病灶边界显示更加清楚,CEUS诊断PC的敏感度、特异度和准确率分别为91.7%、87.0%和88.9%。Serra等[40]研究了127例行CEUS检查的SPL患者发现,PC在CEUS下表现为低增强模式,诊断准确率为91.3%,敏感度为96.8%,特异度为85.3%。Gupta等[41]使用CEUS诊断53例SPL患者,结果显示PC表现为低增强或向心增强模式,并发现CEUS诊断PC的敏感度和特异度分别为80.6%、67.7%。Wang等[33]收集了行CEUS检查的SPL患者资料,证实了PC在CEUS表现为低增强或向心增强,符合PC诊断模式,并发现CEUS诊断PC的准确率达87.62%。可见,PC的CEUS表现模式主要为增强早期和晚期均低增强或向心性增强,病灶开始增强较胰腺实质晚,达峰时间较胰腺实质长。并且通过上述研究数据表明,CEUS诊断PC的诊断效能高,在临床上有重要的应用价值。
2.2.2 CEUS在PNET诊断中的应用 PNET是临床上一种罕见的惰性恶性肿瘤,发病率为0.48/10万[42]。PNET属于富血供肿瘤,组织中肿瘤细胞丰富,坏死组织及纤维间质成分少,微血管较周围胰腺实质丰富。因此,多数PNET的CEUS表现为高增强模式。Serra等[40]前瞻性研究了127例SPL患者,结果显示95.8%的PNET有丰富的血管供应,CEUS表现为高增强。CEUS诊断PNET的敏感度、特异度和准确率分别为83.3%、60.0%和72.0%。王延杰等[43]回顾性分析了16例PNET的患者在CEUS下的表现,结果显示12例病灶呈高增强,4例呈低增强,均表现为均匀性增强。他们认为以CEUS呈高增强模式可作为PNET诊断标准之一,并发现其诊断的敏感度、特异度、准确率分别为75.0%、83.3%、80.4%。杨道辉等[44]回顾性分析了18例PNET患者,研究结果显示PNET病灶常表现为各时相高增强或等增强,并发现CEUS诊断PNET的敏感度、特异度、准确率分别为77.8%、100.0%、94.5%。最近,Wang等[33]通过研究发现,PNET在CEUS下表现为高增强模式,诊断准确率高达92.89%。上述研究可以表明,PNET是一种含丰富血管的病灶,在CEUS下主要表现为高增强模式,少数表现为等增强或低增强,以均匀性增强为主。CEUS对PNET的诊断有较高的诊断效能,可作为鉴别PNET的常规方式。
2.2.3 CEUS在MP诊断中的应用 MP是一种较为特殊的慢性胰腺炎,其发生的主要原因为胰腺小叶和胰管间出现炎症,发生炎性细胞浸润现象,附近的纤维组织出现增生等病理现象,继而形成了肿块[45]。由于MP与PC都有占位性表现,二者在临床症状和病理学特征上存在一定的重叠性,导致临床上鉴别诊断困难。Fan等[39]纳入90例行CEUS的胰腺病变患者进行研究,其中28例为MP,结果显示MP在CEUS下表现为等增强模式,并发现CEUS诊断MP的敏感度、特异度和准确率分别为82.1%、67.9%和91.9%。郝冬兰等[46]对56例胰腺病变行CEUS检查,15例经病理证实为MP,发现MP的增强特征与正常胰腺组织无明显差异,均为等增强;与周边正常胰腺实质同步均匀增强、同步廓清。Vitali等[47]使用CEUS区分MP与PC肿块发现,MP增强较周围实质低,与正常胰腺组织相比呈低增强,表明炎症性病变与正常胰腺实质相比,并没有更早或更强的血管强化。Wang等[48]研究了136例SPL,其中MP 25例。CEUS显示早期和晚期等增强或局灶性低增强为MP的增强模式,其诊断的敏感度、特异度和准确率分别为72.0%、95.5%和91.2%。Wang等[33]通过使用CEUS对SPL患者进行研究,发现MP表现为等增强或合并局灶性低增强,并且其诊断MP的准确率为89.1%。因此,CEUS诊断MP的增强模式,绝大部分表现为等增强,较少表现为低增强。MP的灌注时相与周围胰腺实质同步、均匀性增强。使用CEUS鉴别MP、PNET和PC,在临床上发挥重要的应用价值。
综上所述,CEUS可实时、动态观察胰腺病灶的整个增强过程,并显示其血管微灌注的特征,对PC的诊断及鉴别诊断具有重要意义。CEUS对绝大部分的PNET和MP病变有较高的诊断效能,但对于一些不典型的病变,二者造影表现有交叉,不易鉴别,需结合其他影像检查手段进行鉴别诊断。不同类型SPL的CEUS特征见表2。
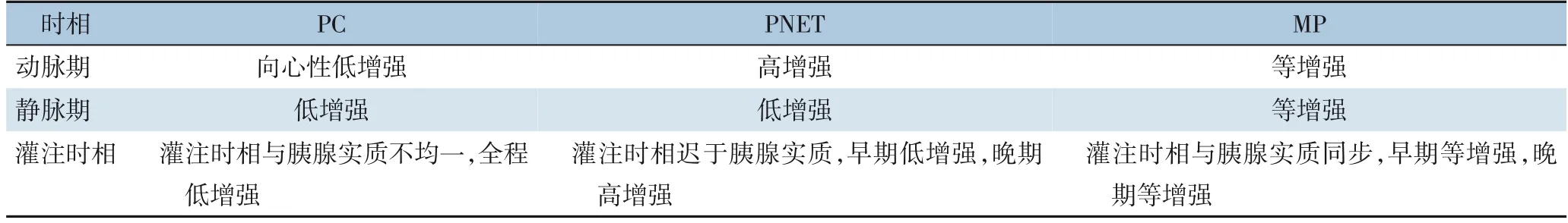
表2 不同类型SPL的CEUS表现特征Table2 CEUS characteristics of different types of PCLs
3 展 望
近些年来随着诊断技术和方法的不断改进和提高,CEUS在胰腺囊/实性占位病变的诊断效能也有了很大的提高,但还存在一定的局限性。由于受胃肠内气体与腹部脂肪限制的影响,超声医生对腹腔深部器官CEUS图像中病灶增强模式以及灌注范围的判断很大程度上依赖于自身临床经验,诊断具有主观性,导致检查结果的准确性受到影响。Ishigami等[49]为了改善胰腺病变CEUS显影效果,通过使用口服聚乙二醇-水旋转涂层(simethicone-water rotation,SWR)超声造影剂进行CEUS检查,发现口服SWR超声造影剂显著改善了胰腺病变的显影效果,在很大程度上消除了因胃肠内气体与腹部脂肪限制对胰腺病变诊断的影响。未来可以开展更多相关研究。
术中超声造影技术主要用于辅助诊断术前未确定的实质脏器肿块和确定肿瘤病理,对手术方式选择和切除范围具有重要应用价值。但是术中超声造影在胰腺肿瘤手术的应用较少,较多地应用于肝脏肿瘤手术。Spinelli等[50]研究了34例传统开腹胰腺肿瘤患者,他们都使用术中超声造影技术,发现术中超声造影相较于传统术中超声作用区别不明显。近年来,微创胰腺肿瘤手术使传统的开放手术变得更安全和更可行,大大降低了术后并发症以及病死率,其有可能彻底成为胰腺疾病的外科治疗方式。目前,尚未有关于微创胰腺肿瘤手术与术中超声造影的研究,笔者认为将二者结合,可能对微创胰腺肿瘤手术的方式以及患者预后具有重要应用价值。
利益冲突:所有作者均声明不存在利益冲突。
作者贡献声明:袁克荣负责本综述的相关文献调研、整理,综述整体结构的构思以及写作;邓雪松对本综述进行审核及修改。
