N-乙酰-D-半乳糖胺修饰头孢克洛-壳聚糖纳米乳的制备及释药性能研究
2023-10-09李华榕郑品劲孔松芝郑心宜郝钰婷梁丽娟廖铭能
李华榕,郑品劲,孔松芝,郑心宜,郝钰婷,梁丽娟,廖铭能
(广东海洋大学,广东 湛江 524000)
头孢克洛为β-内酰胺类抗生素,属于第二代头孢菌素类药物,其抗菌作用机制与其它头孢菌素类药物相似,主要通过与细菌细胞内的青霉素结合蛋白(PBPs)结合,抑制细菌细胞壁的生物合成而起到杀菌作用。作为市面上较为常用的抗生素药物,头孢克洛剂型有很多,如片剂、颗粒剂、胶囊剂、干混旋剂等。由于头孢克洛微溶于水,头孢克洛制剂普遍存在稳定性较差、易产生耐药性等问题[1]。将头孢克洛设计为适宜的载药纳米乳等缓释制剂,可以有效降低药物使用剂量,延长药物在病灶部位的滞留时间,提高药物生物利用度[2-3]。
壳聚糖具有生物降解性、细胞亲和性和生物效应等独特性质,尤其是含有游离氨基的壳聚糖,是天然多糖中唯一的碱性多糖[4]。壳聚糖微球表面富有多糖链,能被特异性细胞或组织识别,可靶向投递药物至病灶部位贮存、释放;壳聚糖微球表面可连接功能基团,通过吸附或包裹方式负载不同药物。壳聚糖作为药物载体,可以稳定药物成分,延缓或控制药物的溶解速度,促进药物吸收,帮助药物到达靶器官,且具有抗酸、抗溃疡功效,可防止药物对胃的刺激。壳聚糖载药纳米乳的药物释放与壳聚糖分子量有关,一般药物的释放速率随壳聚糖分子量的增大而减慢,且壳聚糖浓度越高,药物从壳聚糖中扩散进入生物介质的速率越慢[5]。
在此,作者采用低能乳化法制备N-乙酰-D-半乳糖胺修饰头孢克洛-壳聚糖纳米乳[6],测定纳米乳的粒径和Zeta电位[7-8],通过比较纳米乳和头孢克洛混悬液的累积释药率、考察释放介质和乳化剂用量对纳米乳累积释药率的影响初步研究其释药性能。
1 实验
1.1 试剂与仪器
头孢克洛(纯度≥99%)、N-乙酰-D-半乳糖胺(纯度≥98%)、壳聚糖(脱乙酰度 90%)、聚氧乙烯氢化蓖麻油(S25692)、磷酸二氢钾(分析纯),上海源叶生物科技有限公司;醋酸(分析纯)、吐温-80(化学纯)、十二水合磷酸氢二钠(分析纯),广东光华科技股份有限公司;实验用水为蒸馏水。
FR124CN型电子天平,奥豪斯仪器(常州)有限公司;DL-5-B型低速大容量离心机,上海安亭科学仪器厂;TU-1901型双光束紫外可见分光光度计,上海生析超声仪器有限公司; 集热式恒温加热磁力搅拌器,上海羌强仪器设备有限公司;DK-98-Ⅱ型电子万用炉(电压220 V,AC功率1 000 W),天津泰斯特仪器有限公司;普通透析袋(分子量8 000~14 000),上海源叶生物科技有限公司。
1.2 N-乙酰-D-半乳糖胺修饰头孢克洛-壳聚糖纳米乳的制备方法
1.2.1 溶液的制备
壳聚糖醋酸溶液:精密量取1 mL醋酸于50 mL容量瓶中,用蒸馏水定容至刻度,得到2%醋酸溶液;精密称取0.5 g 壳聚糖于烧杯中,加入2%醋酸溶液,磁力搅拌30~60 min,直至壳聚糖完全溶解,得到壳聚糖醋酸溶液,静置,待搅拌时产生的气泡除净后即可使用。
PBS缓冲溶液:精密称取磷酸二氢钾0.011 5 g、十二水合磷酸氢二钠0.248 6 g于50 mL容量瓶中,用蒸馏水定容至刻度,摇匀并超声溶解5 min,得到PBS缓冲溶液,其pH值在7.3~7.5范围内。
N-乙酰-D-半乳糖胺的PBS溶液:将适量N-乙酰-D-半乳糖胺加入到含PBS缓冲溶液的烧杯中,搅拌均匀,得到N-乙酰-D-半乳糖胺的PBS溶液。
1.2.2N-乙酰-D-半乳糖胺修饰头孢克洛-壳聚糖纳米乳的制备[9-12]
精密称取2.4 g聚氧乙烯氢化蓖麻油于小研钵中,加入0.1 g头孢克洛,在加热条件下不停搅拌,使头孢克洛全部溶解于蓖麻油中;随后将其加入到含4.5 g乳化剂吐温-80的烧杯中,磁力搅拌30 min,得到油相;依次将6.5 mLN-乙酰-D-半乳糖胺的PBS溶液、5.5 mL壳聚糖醋酸溶液加入到另一空烧杯中,搅拌均匀,得到水相;将油相缓慢加入到水相中, 磁力搅拌30 min后,超声15 min,得到N-乙酰-D-半乳糖胺修饰头孢克洛-壳聚糖纳米乳(以下简称纳米乳)。
1.3 头孢克洛标准曲线的绘制
精密称取头孢克洛10 mg于50 mL容量瓶中,加入适量蒸馏水超声溶解并定容至刻度,摇匀,得到浓度为0.2 mg·mL-1的头孢克洛标准溶液。分别精密量取0.05 mL、0.25 mL、0.5 mL、1 mL、1.5 mL、2 mL、2.5 mL头孢克洛标准溶液于10 mL容量瓶中,用蒸馏水定容至刻度,摇匀,静置10 min,采用紫外分光光度法测定263 nm处吸光度。以浓度(c,μg·mL-1)为横坐标、吸光度(A)为纵坐标绘制标准曲线,拟合得线性回归方程为A=0.02154c+0.0112,R2=0.9999。头孢克洛浓度在1.0~50.0 μg·mL-1范围内与吸光度线性关系良好。
1.4 头孢克洛混悬液的制备
精确称取与纳米乳所含药物等量的头孢克洛,加入5 mL蒸馏水,混匀,得到头孢克洛混悬液。
1.5 包封率和载药量的测定
精密量取4 mL纳米乳于透析袋中,用透析袋夹夹紧两端,置于装有200 mL蒸馏水的烧杯中;在30 ℃下磁力搅拌(100 r·min-1)3 h后,取一定量透析介质,采用紫外分光光度法测定263 nm处吸光度(A)。分别按式(2)、式(3)计算包封率和载药量:
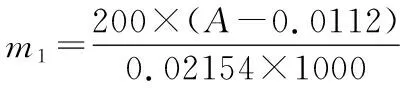
(1)
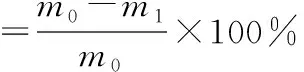
(2)
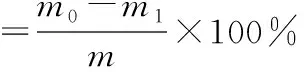
(3)
式中:m0为头孢克洛的加入质量,mg;m1为透析介质中头孢克洛的质量,mg;m为4 mL纳米乳的质量,mg。
1.6 体外累积释药率的测定[13-14]
采用透析法测定纳米乳的体外累积释药率。精密量取5 mL纳米乳于透析袋中,用透析袋夹夹紧两端,置于装有350 mL释放介质的溶出杯中, 将溶出杯置于恒温磁力搅拌器上,在30 ℃、100 r·min-1条件下进行释药;分别在0.5 h、1 h、2 h、4 h、6 h、8 h、10 h、12 h、24 h吸取5 mL释放介质,同时补充5 mL等温新鲜释放介质。 将取出的释放介质经0.45 μm微孔滤膜过滤后,采用紫外分光光度法测定 263 nm处吸光度,并按式(4)计算纳米乳的累积释药率(Q):
(4)
式中:cn为第n次取出释放介质中头孢克洛浓度,mg·mL-1;ci为第i次取出释放介质中头孢克洛浓度,i=n-1,mg·mL-1;V0为释放介质总体积,即350 mL;Vi为取出的释放介质体积,即5 mL;m为纳米乳所含头孢克洛总质量,mg。
2 结果与讨论
2.1 纳米乳的表征
2.1.1 粒径分析(图1)
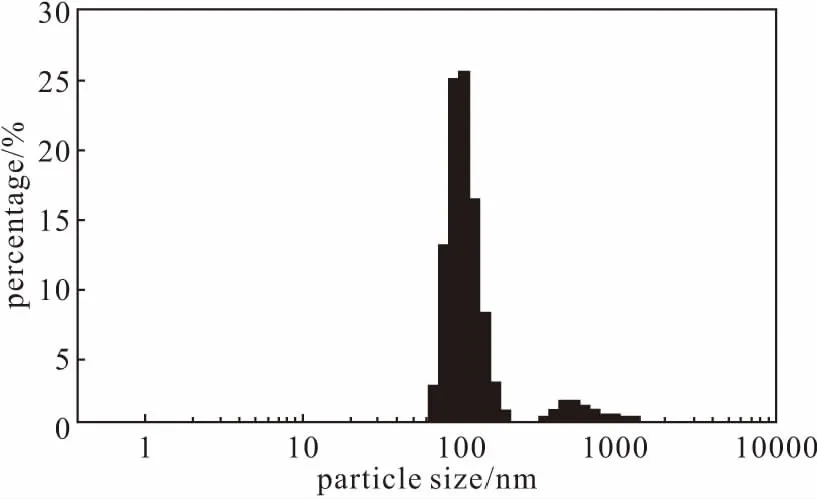
图1 纳米乳的粒径分布Fig.1 Particle size distribution of nanoemulsion
由图1可知,纳米乳的粒径在60~250 nm范围内。
2.1.2 Zeta 电位分析(图2)
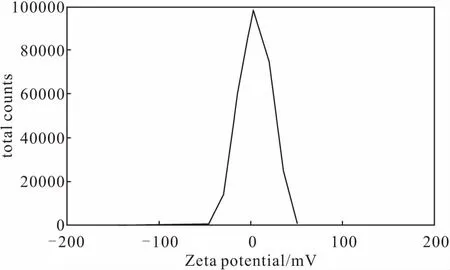
图2 纳米乳的Zeta电位分布Fig.2 Zeta potential distribution of nanoemulsion
由图2可知,纳米乳的Zeta电位为(3.63±0.32) mV。
2.2 纳米乳的包封率和载药量(表1)

表1 纳米乳的包封率和载药量Tab.1 Encapsulation rate and drug loading rate of nanoemulsion
根据表1数据,3#、7#、8#样品的包封率和载药量较高且更接近,后续选用3#、7#、8#样品进行体外释药性能研究。
2.3 纳米乳的体外释药性能
2.3.1 纳米乳与头孢克洛混悬液的累积释药率比较
以蒸馏水为释放介质,按1.6方法测定24 h内纳米乳和头孢克洛混悬液的累积释药率,结果见图3。
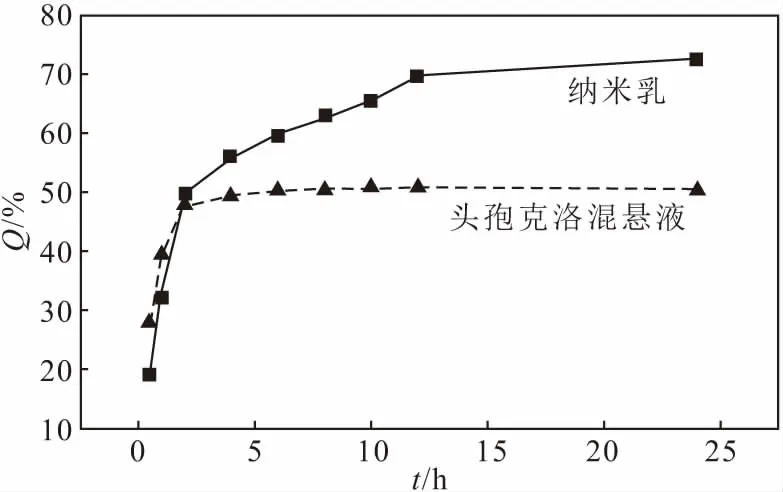
图3 纳米乳和头孢克洛混悬液的累积释药率-时间曲线Fig.3 Cumulative drug release rate-time curves of nanoemulsion and Cefaclor suspension
由图3可知, 随着时间延长,纳米乳和头孢克洛混悬液的累积释药率均先迅速升高。对于头孢克洛混悬液,前2 h释药较快,且其累积释药率比纳米乳的高,可能是由于,部分头孢克洛溶于水后浓度较大, 析出较快;2 h后,其累积释药率升幅趋缓后趋于稳定,24 h累积释药率仅50.53%,这是因为,头孢克洛微溶于水,透析袋中可能还存在未溶解的头孢克洛,且透析袋内外的浓度达到一致时,头孢克洛不再透膜析出,故而对其累积释药率有较大影响。对于纳米乳,2 h时,其累积释药率达到49.61%; 2 h后,其累积释药率仍逐渐升高,24 h累积释药率达到72.43%,可见纳米乳的累积释药率上升趋势相对明显,释药性能更优,可能是由于,纳米乳可提高药物溶解度,从而提高药物的生物利用度。
2.3.2 释放介质对纳米乳累积释药率的影响
分别以蒸馏水和pH值7.3的PBS缓冲溶液为释放介质,按1.6方法测定24 h内纳米乳的累积释药率,结果见图4。

图4 不同释放介质中纳米乳的累积释药率-时间曲线Fig.4 Cumulative drug release rate-time curves of nanoemulsion in different release media
由图4可知,以PBS缓冲溶液为释放介质时,纳米乳的24 h累积释药率仅31.87%;以蒸馏水为释放介质时,纳米乳的累积释药率较高,24 h累积释药率为72.43%,释药性能更优。可能是由于,头孢克洛为弱酸性药物,而PBS缓冲溶液的pH值为7.3, 偏碱性,弱酸性药物在碱性环境下易解离,透析膜内非离子型多,不易转运,对药物穿过透析膜有一定影响,因此纳米乳在PBS缓冲溶液中的累积释药率较低。
2.3.3 乳化剂用量对纳米乳累积释药率的影响
乳化剂用量分别为3 g、5 g、8 g,其它条件不变,按1.2.2方法制备纳米乳,按1.6方法测定24 h内纳米乳的累积释药率,结果见图5。
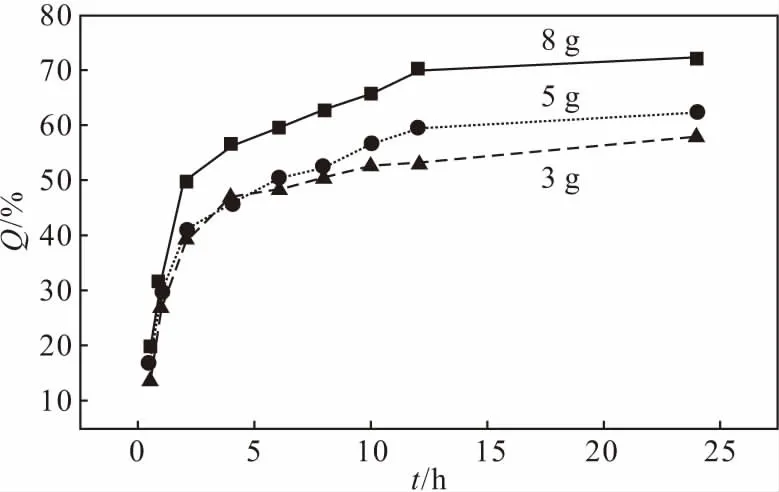
图5 不同乳化剂用量下纳米乳的累积释药率-时间曲线Fig.5 Cumulative drug release rate-time curves of nanoemulsions with different emulsifier dosages
由图5可知,随着乳化剂用量的增加,纳米乳的累积释药率逐渐升高;当乳化剂用量为8 g时, 24 h累积释药率最高达到72.43%。
2.4 释药模型拟合
对纳米乳在0.5~24 h的累积释药率-时间曲线进行拟合,得到释药模型方程:零级方程:Q=1.84882t+40.18943,R2=0.5829;一级方程:ln(1-Q)=0.63021t+66.03777,R2=0.9534;Higuchi方程:Q=11.99124t1/2+24.84411,R2=0.7942。零级方程的R2为0.582 9,说明纳米乳的释药行为与零级释药模型拟合度较差,纳米乳并不是恒速释放药物;一级方程的R2为0.953 4,说明纳米乳的释药行为符合一级释药模型;Higuchi方程的R2为0.794 2,说明纳米乳的释药行为与Higuchi释药模型拟合度也不高,不符合Higuchi释药模型。
3 结论
制备的纳米乳的粒径在60~250 nm范围内,Zeta电位为(3.63±0.32) mV;相较于头孢克洛混悬液,纳米乳的释药性能更优,但纳米乳不适合在偏碱性环境(pH≥7.3)中释药;在3~8 g范围内,随着乳化剂用量的增加,纳米乳的累积释药率逐渐升高,当乳化剂用量为8 g时,24 h累积释药率最高达到72.43%;纳米乳的释药行为符合一级释药模型。纳米乳是一种释放性能较好的药物剂型,在药物传递过程中可达到缓释效果,但该研究未优化制备纳米乳的药物配方,其包封率和载药量偏低,因此纳米乳的制备工艺有待进一步深入研究。
