全无机钙钛矿量子点的疏水改性及LED应用
——推荐一个本科生综合化学实验
2023-10-07周文理张兵宋文丽张吉林邱忠贤韩跃李承志余丽萍
周文理,张兵,宋文丽,张吉林,邱忠贤,韩跃,李承志,余丽萍
湖南师范大学化学化工学院,长沙 410081
国家中长期教育改革和发展规划纲要(2010-2020年)中提出全面提高高等教育质量、提高人才培养质量,着力培养本领过硬的高素质专门人才和拔尖创新人才[1]。探索多种创新复合型人才培养体系模式,并切实推行素质教育创新思维教育理念方式方法、突出重视培养当代学生强烈的现代科学精神、创新性思维训练和科学创新应用能力。
综合化学实验是一门旨在提高学生综合运用化学基础知识的能力和培养学生科研创新意识的实验课程。在实验过程中,除了培养学生熟练掌握基础化学实验技能外,还需要学生综合运用所学化学知识,发现问题、提出问题、分析问题和解决问题;科研反哺教学类型的综合化学实验能够缩短学生所学专业基础知识与科研、生产实践中解决实际问题能力之间的差距,培养学生的创新能力和科研精神[2]。综合化学实验顺应了时代发展的新趋势和教育改革的新潮流,体现了创新人才培养的基本要求,是培养学生创新精神与创新能力的重要途径[3]。
近年来,全无机钙钛矿量子点(PQDs)因优异的光电特性,如直接带隙及可调的禁带宽度、强吸收系数、低激子结合能(35 meV)、高量子效率(90%)、半峰宽窄(12-40 nm)、覆盖全可视发光范围等优点而备受关注[4-8]。但由于PQDs自身的离子特性导致其水、光、热稳定性差,限制了PQDs在实际中的应用。研究表明CsPbX3量子点表面包覆SiO2、Al2O3、聚甲基丙烯酸甲酯(PMMA)和聚苯乙烯(PS)[9,10]等无机或有机化合物可以有效地保护PQDs,提高量子点的稳定性。无机氧化物可以通过有效阻止氧气或水分的渗透,保护PQDs免受环境破坏,但无机氧化物的形成一般是由正硅酸乙酯、双(仲丁醇)正硅酸三乙基正硅酸酯铝盐等前驱体水解反应形成的,前驱体的水解速率和需水量是重要的前提条件,而纯PQDs在水中极不稳定、易发生荧光猝灭,故采用该方法对实验过程控制要求较高。有机聚合物在包覆PQDs时往往具有易加工、密度轻、灵活性高等优点,但会产生挥发性有机废物,不利于环保,而且加工中可能存在PQDs分布不均。
基于我们对量子点稳定性的研究工作[11,12],我们以盐酸、氨水为催化剂,使正硅酸乙酯水解获得SiO2气凝胶,再经三甲基氯硅烷改性SiO2气凝胶呈疏水性,疏水SiO2气凝胶吸附PQDs制备的复合材料具有良好的存放稳定性、热稳定性、紫外光照射稳定性,并应用该复合材料组装成单色或白光LED器件。该综合性实验的设计充分体现了材料合成、表征和应用的特点。通过该综合实验,学生不仅可以掌握PQDs合成的基本实验技能、常规的分离纯化、改性方法以及典型无机化合物的表征手段,还能提升学生综合运用化学原理解决实际问题的能力。整个综合实验始终强调学生中心,从背景调研、实验设计、实验实施、数据处理与分析、论文撰写等各个方面对学生展开全方位训练,激发学生的科研热情。
1 实验目的
(1) 了解全无机钙钛矿量子点的性能及应用前景。
(2) 巩固称量、移液、陈化、洗涤、干燥等无机合成基本操作。
(3) 掌握超疏水SiO2气凝胶的改性原理。
(4) 掌握热注入法制备PQDs。
(5) 掌握无机化合物结构表征的常用方法,如红外光谱、粉末X射线衍射谱、荧光发射光谱和紫外-可见吸收光谱的原理及相应的谱图分析。
(6) 熟练使用Origin软件处理各种实验数据。
2 实验原理
以盐酸、氨水作为催化剂,使得正硅酸乙酯水解得到SiO2的气凝胶,然后用三甲基氯硅烷和莫来石纤维增强气凝胶的疏水性和韧性,随后以该超疏水气凝胶吸附PQDs获得复合材料,并制作LED器件。
正硅酸乙酯在酸催化剂的作用下与少量水发生水解,其中C-O键断裂与水中的质子和羟基结合最终得到硅氧烷单体和乙醇。两个硅氧烷单体脱去一分子水,得到Si-O-Si链结构。此外,硅氧烷还可与未反应的正硅酸乙酯发生脱醇反应得到Si-O-Si链结构。脱水和脱醇反应同时发生,最终可使正硅酸乙酯完全水解。气凝胶中的Si-O-Si链结构与羟基相连,羟基属于亲水基团,所以此时得到的气凝胶为亲水材料。利用三甲基氯硅烷与亲水的SiO2气凝胶反应,气凝胶表面的羟基被三甲基氯硅烷的-Si(CH3)3所取代,使得气凝胶表面存在大量甲基,而甲基属于疏水基团,所以经过三甲基氯硅烷处理后的气凝胶为疏水材料。气凝胶制备及改性原理如图1所示。

图1 气凝胶制备及改性机理示意图
3 仪器和试剂
仪器:平底电热套,数显型磁力搅拌器,智能温控器,热电偶,集热式磁力搅拌器,高速离心机,pH计,紫外暗箱分析仪,恒温干燥箱,台式粉末压片机,分析天平,制冰机,冰箱。
试剂:正硅酸乙酯(A.R.),无水乙醇(A.R.),三甲基氯硅烷(TMCS,G.C.),盐酸(A.R.),氨水(A.R.),油胺(A.R.),1-十八烯(ODE,G.C.),正己烷(A.R.),碳酸铯(99.90%),氯化铅(A.R.),溴化铅(A.R.),碘化铅(98%),莫来石纤维粉(雷晶耐火材料公司),365和460 nm LED芯片(深圳市金唐科技实业有限公司),(Sr,Ca)AlSiN3:Eu2+荧光粉,AB胶,去离子水。
4 实验步骤
4.1 SiO2疏水气凝胶的制备
正硅酸乙酯、无水乙醇和去离子水的物质的量比为1 : 7 : 3的混合溶液在40 °C的水浴中搅拌均匀后,缓慢滴加0.5 mol·L-1盐酸溶液,调节溶液pH至2-3,水解2 h后,缓慢滴加0.5 mol·L-1氨水再将溶液pH调至7-8,然后加入2 g莫来石纤维粉[13],继续搅拌使溶液呈凝胶状,接着在40 °C的水浴中陈化10 h (凝胶结构继续固化)。然后以正硅酸乙酯、无水乙醇体积比1 : 4的母液浸泡气凝胶8 h,无水乙醇清洗3-4次后,再用正己烷浸泡8 h。然后以TMCS和正己烷体积比1 : 9的混合溶液浸泡气凝胶10 h,对气凝胶表面基团进行改性。最后用正己烷洗涤产物3-4次,缓慢加热干燥后得到三维网状结构的疏水SiO2气凝胶。
4.2 CsPbX3 QDs的制备
4.2.1 油酸铯的制备
将0.8 g Cs2CO3、30 mL ODE加入到100 mL三颈烧瓶中,升温到120 °C后抽真空1.5 h至无气泡产生。然后关闭真空泵通入N2约1 h,待降温到100 °C,快速注入2.5 mL油酸,接着通入N2,直至固体试剂全部溶解。室温下油酸铯会从ODE中析出,因此使用时须加热至120 °C备用。
4.2.2 CsPbX3 QDs (X = Cl,Br,I)的制备
取0.18 mmol PbX2、5 mL ODE置于100 mL三颈烧瓶中。然后抽真空,升温至120 °C,保温30 min至无气泡产生。关闭真空泵并通入N230 min,注入油胺和油酸各0.5 mL,然后溶液升温至150-180 °C范围(一般来说含Cl的PQDs合成温度较低,含I的PQDs则需要更高的温度。参考温度:蓝色CsPbCl1.5Br1.5,150 °C;绿色CsPbBr3,165 °C;红色CsPbBrI2,180 °C),接着快速注入120 °C预热的油酸铯溶液0.4 mL,高温下继续反应5 s后将三颈烧瓶快速转移至冰水浴中冷却结晶。用10 mL正己烷洗涤,粗溶液在8000 rpm下离心5 min,弃去上层清液,下层沉淀分散于10 mL正己烷中,存储于4 °C的冰箱中备用。
4.3 CsPbX3@SiO2气凝胶复合材料的制备
取0.2 g气凝胶与已经合成好的CsPbX3QDs在磁力搅拌下混匀10 min,然后4000 rpm离心5 min,干燥,收集固体产物即为CsPbX3@SiO2气凝胶复合材料。
4.4 材料表征及LED器件制作
利用旋转滴界面张力仪(上海中晨JC2000C)测定气凝胶和复合材料的接触角,测量范围0-180°。利用傅里叶红外光谱分析仪(美国NEXUS)在400-4000 cm-1范围内测定粉末样品的红外吸收光谱。物相分析使用X射线粉末衍射仪(日本Rigaku Ultima IV)对粉末样品进行测试,扫描范围10°-90°。利用紫外-可见分光光度计(日本岛津UV-2450)测定吸收光谱,测试范围200-800 nm,扫描速度1200 nm·min-1。粉末样品的发射光谱使用荧光光谱仪(日立F4500)测试,氙灯175 W,操作电压200 V。
分别将蓝、绿和红色CsPbX3@SiO2复合材料与硅树脂混匀后涂覆在365 nm蓝光LEDs芯片上,制作单色LEDs器件;将绿色CsPbBr3@SiO2复合材料与红色(Sr,Ca)AlSiN3:Eu3+荧光粉以一定的比例混匀后,再与硅胶树脂混合均匀后涂覆在460 nm蓝光LEDs芯片上,制作白光LEDs器件。使用ZWL分析系统测试器件的电致发光谱。
5 结果与讨论
5.1 表面改性分析
图2为气凝胶和量子点气凝胶复合材料的接触角(Contact Angles,CA)照片。从图中可以看出,未进行疏水改性的SiO2气凝胶的平均接触角约为30.3°,属于亲水材料。TMCS改性后的SiO2气凝胶的平均接触角约为140.57°,属于疏水材料。而吸附了PQDs的复合材料的接触角略微减小,这意味着合成的CsPbX3QDs@SiO2气凝胶复合材料表面具有疏水性。

图2 SiO2气凝胶(a),TMCS改性SiO2气凝胶(b)和CsPbBr3@SiO2气凝胶(c)复合材料的接触角照片
气凝胶及量子点气凝胶复合材料的红外光谱如图3所示。a曲线3468和1635 cm-1处分别对应着-OH的不对称伸缩振动和弯曲振动,说明该羟基为“氢键缔合的强羟基”或可能存在残留的吸附性水,说明此时SiO2气凝胶为亲水性材料;1061 cm-1处强而窄的峰对应Si-O-Si反对称伸缩振动,证实气凝胶结构中可能存在硅酸盐骨架,该振动峰是SiO2气凝胶中重要的特征峰[14];c曲线是TMCS改性SiO2气凝胶的红外光谱,与未改性的SiO2气凝胶相比,在2962和2908 cm-1处出现了归属于-CH3的反对称伸缩和对称伸缩振动,1470和1375 cm-1处为-CH3的弯曲振动峰,证明改性后的SiO2气凝胶结构中存在甲基,预示TMCS改性成功。改性后的SiO2气凝胶中对应-OH的不对称伸缩振动明显减弱,证实-CH3取代部分-OH使得其数量减少。此外,在843和756 cm-1处出现了Si-C的伸缩振动,由气凝胶改性机理可知,该化学键在改性后才出现,从另一个角度说明利用TMCS改性SiO2气凝胶,使SiO2表面接枝上疏水的-CH3,与接触角数据变化吻合,改性后的SiO2气凝胶为疏水材料。e曲线为量子点复合材料的红外光谱,在2926和2852cm-1处分别是伯胺基团产生的对称振动和非对称伸缩振动,1463 cm-1处是油胺中N-H和C-H基团的弯曲振动的耦合峰,进一步说明SiO2气凝胶与量子点形成了复合材料。
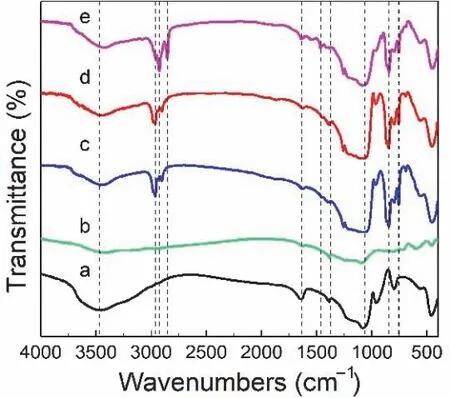
图3 典型样品的红外光谱
5.2 物相分析
莫来石是由Al2O3-SiO2组成的矿物材料,Al2O3的质量分数一般在72%-78%。图4黑色实线为莫来石XRD谱图,SiO2气凝胶为无定形材料,加入莫来石改性后在16.7°、26.5°、35.5°均出现属于莫来石的特征峰,说明莫来石改性SiO2气凝胶成功。SiO2气凝胶材料吸附量子点后,可以观察到位于21.5°和30.64°归属于量子点的衍射峰,一方面说明量子点的结晶度较高,另一方面也说明气凝胶材料的比表面积大,吸附了足够多的量子点。随着量子点组成由Cl → Br → I变化,21.5°处对应于(110)晶面的衍射峰逐渐向低角度移动,预示着更大的晶面间距,与卤素离子半径变化一致。

图4 (a) 莫来石、SiO2气凝胶和CsPbBr3@SiO2复合材料的XRD图谱;(b) CsPbX3@SiO2复合材料在20°-23° XRD的放大图谱
5.3 光谱分析
图5(a)为CsPbX3@SiO2复合材料的荧光发射谱和紫外吸收光谱。蓝、绿、红色复合材料的发射峰分别位于463、522和656 nm,蓝色复合材料的半峰宽25 nm,绿色复合材料增大到27 nm,红色复合材料的半峰宽最大,为39 nm。由蓝到红复合材料的发射峰逐渐红移,紫外吸收截面逐渐变宽。红色复合材料的吸收截面远远大于蓝色和绿色复合材料,说明红色复合材料拥有更宽的激发范围,激子结合能变小,禁带宽度变窄[15]。最大吸收与最大发射峰之差为Stokes位移,由于电子在激发态向基态跃迁时,会产生部分能量损失,因而发射光的能量小于激发光的能量。

图5 (a) 蓝绿红复合物的紫外可见吸收光谱图(虚线)和荧光发射光谱图(实线),内插图为蓝绿红复合材料在日光(左)和紫外灯下(右)的照片;(b) 蓝绿红复合材料的色坐标图
图5(a)中的内插图为蓝、绿、红色复合材料在日光和紫外灯照射下的照片。蓝、绿、红色复合材料的色坐标分别为(0.1373, 0.0573),(0.1231, 0.7559),(0.6988, 0.301)。根据公式(1)和(2)计算,色域值为0.1978,为标准色域的125%,如图5(b)所示。
5.4 LEDs器件的光学性质
将绿色复合材料与红色(Sr,Ca)AlSiN3:Eu2+氮化物荧光粉涂覆在460 nm蓝光芯片组装成的白光LEDs器件,其电致发光谱如图6(a)所示。该白光LEDs器件的CIE色坐标位于(0.334, 0.327),色温5405 K。图6(a)内插图为白光LEDs器件的点亮照片。白光、蓝、绿、红单色LEDs的CIE色坐标如图6(b)所示。根据公式(1)和(2)计算可知,利用蓝、绿、红色量子点复合材料制作的单色LEDs的显示范围覆盖了133% NTSC,可以满足显示需求。

图6 (a) 白光LEDs电致发光光谱图,内插图为白光LEDs器件点亮的照片;(b) 蓝、绿、红单色LEDs和白光LEDs器件色坐标图,内插图为蓝绿红单色LEDs点亮照片
6 实验开设建议
6.1 实验安排
本实验为24学时的综合化学实验,适合20人左右的小班开设。具体实验安排如下:
(1) 实验准备(课外):提前2-3周给出有关实验知识内容,要求学生利用图书馆网络资源查阅相关文献、书籍,撰写有关PQDs研究进展及合成方法的预习报告,并要求学生系统复习红外光谱仪、紫外-可见光谱仪和X射线衍射仪的工作原理、接触角测试原理、分子荧光的产生等内容。教师需提前检查学生的预习报告,不达标者不能开展后续实验。
(2) 第1次实验:8学时,实验内容为4.1小节,SiO2气凝胶的制备及疏水改性,2人/组。教师听取学生分组展示的PQDs研究进展汇报并进行点评。
(3) 第2次实验:8学时,实验内容为4.2、4.3和4.4小节中的LEDs器件制作。学生分为三个大组,分别制备CsPbCl1.5Br1.5、CsPbBr3和CsPbBrI2量子点。最后每2人/组的同学均需完成CsPbX3@SiO2气凝胶复合材料的制备。分组制作单色LEDs和白光LEDs器件。
(4) 第3次实验:8学时,实验内容为4.4小节中的材料表征。分组测定SiO2气凝胶与CsPbX3@SiO2气凝胶复合材料的红外光谱、紫外-可见吸收光谱、荧光发射光谱、接触角、XRD谱及电致发光光谱。
(5) 实验结果处理及实验小论文撰写(课外):要求每位学生在认真完成上述实验后,利用Origin软件处理实验数据,深入分析实验结果,总结实验操作中存在的问题并提出改进措施,按照学校毕业论文的写作格式按时完成研究小论文。
(6) 学生实验成果反馈:指导教师针对学生实验过程及与小论文中出现混淆的相关问题进行讲解点评与教学指导,进一步引导学生深刻理解PQDs研究成果。有条件的情况下可以鼓励学生开展CsPbX3@SiO2气凝胶复合材料在空气氛中的长期稳定性、紫外灯照射稳定性及热稳定性的研究,进一步拓展实验内容。
6.2 教学方法
在进行该实验课程的教学设计中,采用了以问题导向教学法形式进行案例教学。
问题1:什么是钙钛矿的量子点?
问题2:钙钛矿量子点在生产、生活中有哪些应用?
问题3:钙钛矿量子点可以应用在哪些领域?限制该量子点应用的瓶颈是什么?
问题4:材料疏水改性的实质是什么?气凝胶改性原理是什么?除了三甲基氯硅烷外,你认为还有哪些试剂可作为疏水改性剂?
问题5:了解红外光谱分析仪、紫外-可见光谱仪、荧光光谱仪和X射线衍射仪的仪器构成和工作原理。分子荧光是如何产生的?紫外-可见光谱仪和和红外光谱仪有区别吗?我校制作的虚拟仿真实验项目“光能转换材料及多层复合荧光薄膜在植物生长中的应用”[16]中含有相关仪器的工作原理及测试流程,学生可以在课外进行自主学习。该软件提供了引导模式和考核模式,可实时记录学生的操作,并给出评分,为学生的自主学习提供了质量保障。
在整个课堂教学中,教师负责问题的提出,引导学生思考、回答问题,参与问题讨论,学生始终作为主体,完成整个实验课程教学任务。除此之外,线上、线下的混合式教学模式同样可以引入实验教学,教师借助网络教学平台,如超星“学习通”、“雨课堂”等,提供预习PPT及检索用关键词;及时推送优质资源,扩大学生视野[17];虚拟仿真平台可以对学生线上大型仪器的操作进行实时评分,加强实验的过程考核;学生在网络平台上传小组撰写的研究进展、实验过程中的操作视频、产品图片等内容供教师进行实验过程评价,教师除了在实验过程中指导外,还可以在学生上传的内容中发现一些共性问题,及时进行教学反馈。
本实验已在本校的大学生创新训练项目中进行了多次尝试,学生在实验完成后表示“通过本实验我体会到了科研的魅力”“PQDs真是一个神奇的材料,组分的调控就可以实现发光颜色的变化”“我也可以自己做有应用价值的显示材料”“希望有机会从事新材料的科学研究工作”等。因此,本实验的开展不仅可以加深学生对化学原理的理解,提升实验技能,还可以激发学生的科学研究兴趣,培养学生的创新能力。
7 结语
本文介绍的全无机钙钛矿量子点的疏水改性及LED应用实验源于教师的科学研究项目,所设计的实验内容涵盖了材料制备、表征及应用3个重要环节。在整个实验教学过程中,学生的文献查阅和整理能力、Origin软件使用能力以及实验操作技能得到有效提升,有助于培养学生跟踪科技前沿的能力,激发学生对科学研究的兴趣,提升学生的创新能力。实验中制备的CsPbX3@SiO2气凝胶复合材料可以利用365 nm的紫光手电筒照射呈现出蓝、绿、红等不同颜色,可操作性强,适合化学、应用化学等本科专业的综合性实验教学。
