大豆分离蛋白颗粒稳定的鲢鱼油Pickering乳液的制备及其性能表征
2023-09-19刘香玲李真王金厢李学鹏徐永霞米红波仪淑敏励建荣高瑞昌张宇昊
刘香玲,李真,王金厢,李学鹏*,徐永霞,米红波,仪淑敏,励建荣,高瑞昌,张宇昊
(1. 渤海大学 食品科学与工程学院,国家鱼糜及鱼糜制品加工技术研发分中心,辽宁 锦州 121013;2. 江苏大学 食品与生物工程学院,江苏镇江 212013;3. 西南大学 食品科学学院,重庆 400715)
Pickering 乳液是以固体颗粒为稳定剂的乳状液,由互不相溶的两相组成,一相以液滴的方式分散在另一相中。相比使用表面活性稳定的常规乳液,Pickering乳液具有绿色、无污染、安全性高和稳定性强等优点,Pickering 乳液在食品领域的应用独具优势且逐渐成为研究热点,如应用于冰淇淋、蛋白饮料、蛋黄酱、沙拉酱等[1]。Pickering 乳液不仅能使产品质地均匀、稳定,而且其固体颗粒的包埋形式在营养物质、功能性成分的传递方面发挥着重要作用[2]。
稳定Pickering 乳液的食品级颗粒主要有蛋白质、多糖等成分[3]。其中,蛋白质是由多种氨基酸组成的天然有机物质,表面具有极性和非极性基团,是稳定食品级Pickering 乳液安全、清洁的首选。蛋白基Pickering 乳液的颗粒通常以球形、纤维状、微凝胶和纳米凝胶的形式存在。其中固体颗粒作为Pickering 乳液稳定剂的前提是具有适当的润湿性并且颗粒尺寸应明显小于目标尺寸至少一个数量级。固体颗粒界面膜理论和三维网络结构理论是Pickering 乳液潜在的稳定机制[4]。为了提高乳液稳定性,蛋白颗粒通常经过热处理改性或反溶剂沉淀法制备[3,5],热处理是蛋白颗粒改性的一种简单、高效的方法。研究表明,大豆分离蛋白(soy protein isolate,SPI)在乳化前进行热处理,可以减小蛋白颗粒的粒径并增加界面蛋白吸附量,提高SPI乳液在贮藏过程中的物理稳定性,且较高的加热温度与乳液的稳定性呈正相关[6]。此外,可以通过降低液滴粒径、提高连续相黏度的方式提高乳液的稳定性,进而防止乳液分层[3]。
如今,已研究出多种蛋白质可作为稳定Pickering乳液的固体颗粒,例如大豆分离蛋白[6]、藜麦蛋白[7]、花生分离蛋白[8]、醇溶蛋白[9]。大豆分离蛋白占大豆蛋白含量90%以上,含有人体必需氨基酸,营养丰富,不含胆固醇,具有良好的营养价值,可替代动物蛋白[10]。SPI具有良好的乳化特性和稳定界面层的能力,因而广泛应用于食品、药品、化妆品工业生产中[11]。例如,在传统乳液中,SPI 可以有效包裹鱼油[12]、肉桂精油[13]、灵芝孢子油[14]等,保护在空气中容易被氧化变质而不易储存的优质脂肪;在Pickering 乳液中,SPI 颗粒可以迅速转移到油水(空气-水、油-水)界面上形成类凝胶网络从而稳定Pickering 乳液。
冷冻鱼糜生产过程中往往会经过漂洗程序,洗去鱼肉中的酶、脂肪等物质。作为鱼糜加工副产物的鲢鱼脂肪中含有大量不饱和脂肪酸,其中二十碳五烯酸(eicosapentaenoic acid,EHA)、二十二碳六烯酸(docosahexaenoic acid,DPA)含量处于较高水平,具有降血压、血脂,增强免疫力,保护神经系统的功能[15]。如何利用鲢鱼脂肪制备功能性食品配料、提高其利用价值,是水产品加工行业关注的重要问题。鉴于此,本文以鲢鱼脂肪制备的鲢鱼油为原料,以SPI 为稳定剂,制备SPI 颗粒稳定的鲢鱼鱼油Pickering 乳液,通过探究SPI浓度、油相体积分数、离子强度对Pickering 乳液理化特性及稳定性的影响,为鱼油Pickering 乳液的制备及其在食品中的应用提供参考。
1 材料与方法
1.1 材料与试剂
大豆分离蛋白(食品级):浙江诺一生物科技有限公司;鲢鱼脂肪:辽宁安井食品有限公司。
1.2 仪器与设备
APV-1000 高压均质机:丹麦APV 公司;Discovery DHR-1 流变仪:美国TA 公司;80i 光学显微镜:日本Nikon 公司;Turbiscan Lab Expert 稳定性分析仪:法国Formulaction 公司。
1.3 试验方法
1.3.1 鲢鱼油的制备将固态鲢鱼脂肪于70℃水浴融化,在25℃、7 000r/min离心两次取上清液,每次15 min,-20 ℃储存。
1.3.2 Pickering 乳液的制备
参考Wang 等[6]的方法,略作修改。称取SPI 于烧杯中配制3%蛋白母液,磁力搅拌2 h,过夜水化。95 ℃加热15 min,冷却至室温,放入4 ℃冰箱保存备用。将母液与鲢鱼油混合,以8 000 r/min 剪切2 min,30 MPa均质两次,分别研究不同SPI 颗粒浓度(1.0%、1.5%、2.0%、2.5%、3.0%)、油相体积分数(0.1、0.2、0.3、0.4、0.5)、离子强度(0、0.1、0.2、0.3、0.4 mol/L NaCl)对乳液理化性质和稳定性的影响。
1.3.3 乳化活性及乳化稳定性的测定
参考Jang 等[16]的方法。将均质完毕的乳液倒入小烧杯中,立即使用移液枪吸取20 μL 乳化液,置于5 mL 0.1% 十二烷基磺酸钠(sodium dodecyl sulfate,SDS)溶液中稀释250 倍,测定500 nm 处的吸光值A0,乳化活性(emulsifying activity,EAI)及乳化稳定性(emulsifying stability,ESI)计算公式如下。

式中:X 为乳化活性,m2/g;Y 为乳化稳定性,%;C为乳化之前蛋白的浓度,g/100 mL;φ 为乳化液中油相体积分数;N 为稀释倍数;A0为乳状液在0 min、500 nm处吸光值;At为乳化液在2 h、500 nm 处吸光值。
1.3.4 粒度分布的测定
参照李笑笑[17]的方法,利用激光粒度分布仪测定,添加样品,在遮光率达到10%~15%时停止加样,参数设置为颗粒吸收率0.001,颗粒折射率1.481,介质折射率1.333。
1.3.5 光学显微形貌分析
将乳液稀释5 倍,取少量稀释后的样品滴在载玻片上,放置在10 倍物镜下观察并拍摄,在电脑上记录拍摄的图片。
1.3.6 流变特性的测定
参考Zeng 等[18]的方法,采用流变仪测定,使用40mm平行板石英夹具,取1 mL 乳液于测试台上。
表观黏度:模式Flow Sweep,取适量样品于平板上,记录剪切速率从0.01~100 s-1的过程中乳液的黏度变化。
黏弹性质:在恒定应变下(0.5%),频率为0.1~10 Hz,获得弹性模量(G′)和黏性模量(G″),表征Pickering 乳液的动态黏弹性。
1.3.7 冻融稳定性的测定
参考Qin 等[7]的方法,将制得的乳液于-20 ℃放置24 h,循环冷冻-解冻,共3 次。记录外观变化,通过观察乳析层的变化评价乳液的稳定性,测定冻融过程中乳析指数(creaming index,CI)。

式中:X 为乳析指数,%;HC为乳清层高度,cm;HB为起始乳状液高度,cm。
1.3.8 多重光散射分析
将20 mL 乳液放入多重光专用瓶中,每隔25 s 检测一次,持续1 h,得到稳定性动力学指数(turbiscan stability index,TSI)。TSI 指数反映样品不稳定的程度,TSI 越大,越不稳定[19]。

式中:X 为稳定性动力学指数;xi为背射光强的平均值;xBS为xi的平均值;n 为扫描次数。
1.4 数据统计与分析
试验均重复3 次,采用SPSS 19.0 进行方差分析,结果表示为平均值±标准差,并用Origin 8.0 作图。
2 结果与分析
2.1 乳液的粒度分布
SPI 颗粒浓度、油相体积分数、离子强度对乳液粒度分布的影响见图1。
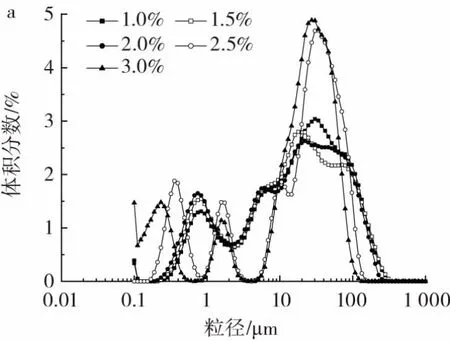
图1 SPI 颗粒浓度、油相体积分数、离子强度对乳液粒度分布的影响Fig.1 Effects of SPI concentration,volume fractions of oil phase and NaCl concentration on particle size distribution of emulsion
粒径是评价乳液稳定性的重要指标,粒径越小,分布越集中,乳液越稳定。由图1a 可知,所有乳液均呈多峰分布,随着SPI 颗粒浓度增加,主峰总体向左移动,说明粒径逐渐减小。Ning 等[8]研究发现,在花生分离蛋白乳液中,当蛋白颗粒浓度较低时,能够覆盖油滴表面的有效颗粒较少,颗粒数量不足以充分稳定油滴,形成较大尺寸的油滴。所以,当SPI 颗粒浓度为2.5%~3.0%时,体系蛋白颗粒含量增加,产生更多油水界面(界面面积增加),从而使乳化油滴数量增多、粒径变小。
如图1b 所示,乳液粒径呈多峰分布,油相体积分数增加,主峰位置总体向右移动,粒径加大。Wang 等[6]研究发现,油相体积分数在0.1~0.6,由SPI 稳定的茶油Pickering 乳液的平均粒径也呈现增加的趋势。说明在浓度一定的情况下,SPI 包埋能力有限,随着油相增加,体系产生了更多的油水界面,然而油滴单位界面面积可获得颗粒数一定,所稳定的界面面积有限,从而加重了油滴颗粒之间的聚集,油滴变大。
由图1c 可知,加入NaCl 后,乳液由多峰分布变为双峰分布且粒径减小,说明NaCl 能使液滴大小更加均一。研究发现,NaCl 分解出Cl-可以增加液滴间的空间位阻和静电斥力,使乳液的平均液滴尺寸降低,增强蛋白质分子间的相互作用,有助于液滴絮凝形成不易变形的界面层[20-21]。
2.2 乳化活性及乳化稳定性
SPI 颗粒浓度、油相体积分数、离子强度对乳化活性及乳化稳定性的影响见图2。

图2 SPI 颗粒浓度、油相体积分数、离子强度对乳化活性及乳化稳定性的影响Fig.2 Effects of SPI concentration,volume fractions of oil phase and NaCl concentration on EAI and ESI of emulsion
乳化活性主要反映蛋白到界面的吸附速率、降低界面张力的速率,在乳化时降低界面张力的速率越高,乳化活性越高,反之乳化活性则降低[22]。乳化稳定性表征蛋白质维持乳液稳定而不被破坏的性质,与乳液的存放时间有关[23]。由图2A 可知,乳液的EAI 随SPI颗粒浓度的增加而降低,而ESI 先升高后降低,当SPI颗粒浓度为2.5%时,ESI 达到最大值97.3%。EAI 逐渐降低可能由于蛋白颗粒之间发生缔合,改变了亲水亲油值(hydrophile-lipophile balance,HLB),从而使EAI降低。此外蛋白含量升高,乳液黏度增大,蛋白质吸附在界面的速率降低,降低了EAI;另一方面,蛋白含量增大,发生絮凝等聚集现象,降低了蛋白/纤维的表面活性作用,最终降低了乳液的EAI[24-25]。蛋白颗粒之间存在分子间或分子内作用力,SPI 颗粒浓度增加,分子作用力增强,不利于蛋白颗粒吸附到油滴表面,进而导致乳液的ESI 在SPI 颗粒浓度为3.0%时略有下降。
如图2B 所示,随着油相体积分数的增加,Pickering 乳液的EAI 逐渐增加,ESI 则在油相体积分数为0.2 时达到最高后逐渐降低。表明在SPI 颗粒浓度一定的情况下,油相体积分数增加,蛋白颗粒越易吸附至界面上,降低界面张力的速率越快,乳化活性就越高[22]。当油相体积分数为0.2 时,ESI 最高,说明此时乳液的稳定性较好。
如图2C 所示,随着离子强度的增加,乳液的EAI先降低后升高,ESI 变化不显著。可能由于加入盐离子后,体系产生静电屏蔽效应,导致蛋白颗粒间的相互作用增强,乳液滴絮凝,导致乳液黏度增加,蛋白扩散速率低,EAI 降低;当盐离子浓度过高时,乳液在油水界面的扩散速率变大,EAI 升高[21]。与之相对应,由于蛋白颗粒间较强的相互作用使得乳液的ESI 不易随时间的变化而变化,进而表明离子强度的添加对该Pickering 乳液的乳化稳定性影响不大。
2.3 乳液的表观黏度
SPI 颗粒浓度、油相体积分数、离子强度对乳液表观黏度的影响见图3。

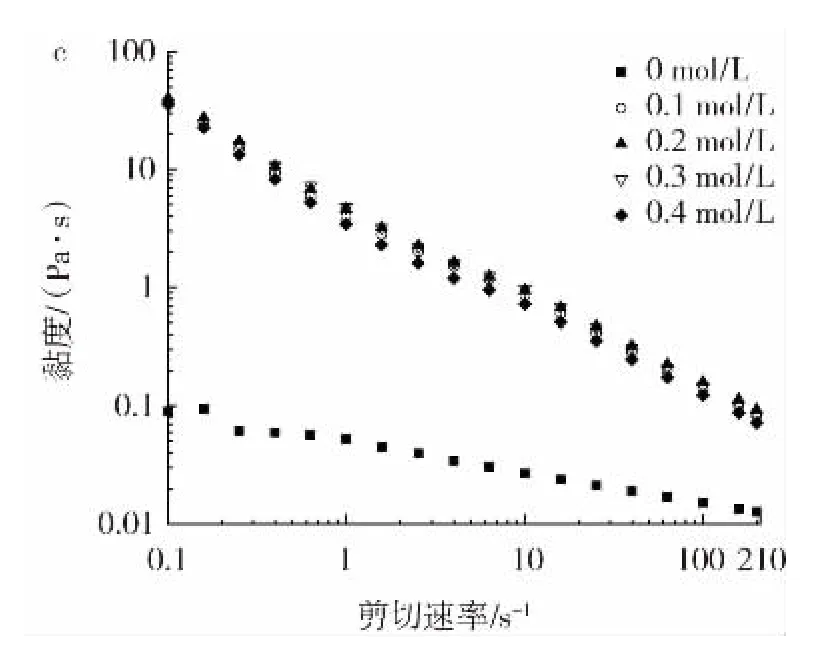
图3 SPI 颗粒浓度、油相体积分数、离子强度对乳液表观黏度的影响Fig.3 Effects of SPI concentration,volume fractions of oil phase and NaCl concentration on apparent viscosity of emulsion
乳液的流变性能是指在外力或无外力作用下的流动学,在许多应用中起着决定其功能性能的重要作用,如黏度、黏弹性、屈服应力或弹性模量,研究乳液的流变性不仅可以了解其流动特性和稳定性,还可以了解它的失稳机制。表观黏度能看出乳液的流动性,有利于表征液滴间的相互作用进而反映乳液的稳定性[26]。由图3a 可知,乳液表现为典型的非牛顿假塑性行为,产生了剪切稀化的现象,这是由于较高的剪切速率可以抑制布朗运动使乳液的流动阻力变小,进而说明乳液滴之间的相互作用较弱,在高剪切力下液滴易被破坏[27]。随着SPI 颗粒浓度的增加,体系中产生越来越多的蛋白颗粒稳定油水界面,使液滴间的距离减小,相互作用增强,所以提高了乳液的表观黏度。乳液的表观黏度将直接影响液滴之间的相互作用,进而影响乳液的冻融稳定性。
从图3b 可以看出,乳液出现剪切稀化现象,说明液滴之间的弱相互作用。Wang 等[6]研究结果表明SPI乳液存在剪切稀化的流体特性,这与本研究结果一致。随着油相体积分数的增加,乳液表观黏度增加,这是由于油脂的升高增强了蛋白质分子之间的相互作用,并使它们之间的联系更紧密,进而形成了絮凝网络结构,油滴之间更大的接触面积阻碍了乳状液在剪切场中的自由流动,从而增加了其黏度。试验中发现当油相体积分数大于0.3 时,此时的乳液黏稠,不易流动,放置几天后近似凝固状态,高黏度的乳液可以通过抑制液滴的自由移动,增强乳液的稳定性[28-29]。
根据Stokes 方程,通过增加连续相的黏度,降低液滴粒径或分散相与连续相之间的密度差,可以使乳液更稳定[30]。如图3c 所示,加入盐离子能显著提高体系黏度,从而获得更加稳定的乳液,这是因为盐离子存在,可以使乳液体系形成静电屏蔽,促使连续相中未吸附的蛋白颗粒从水相向界面的扩散和吸附,界面膜变厚,蛋白质分子之间相互作用增强,从而形成凝胶网络结构[31]。
2.4 乳液的黏弹性质
SPI 颗粒浓度、油相体积分数、离子强度对乳液黏弹性的影响见图4。
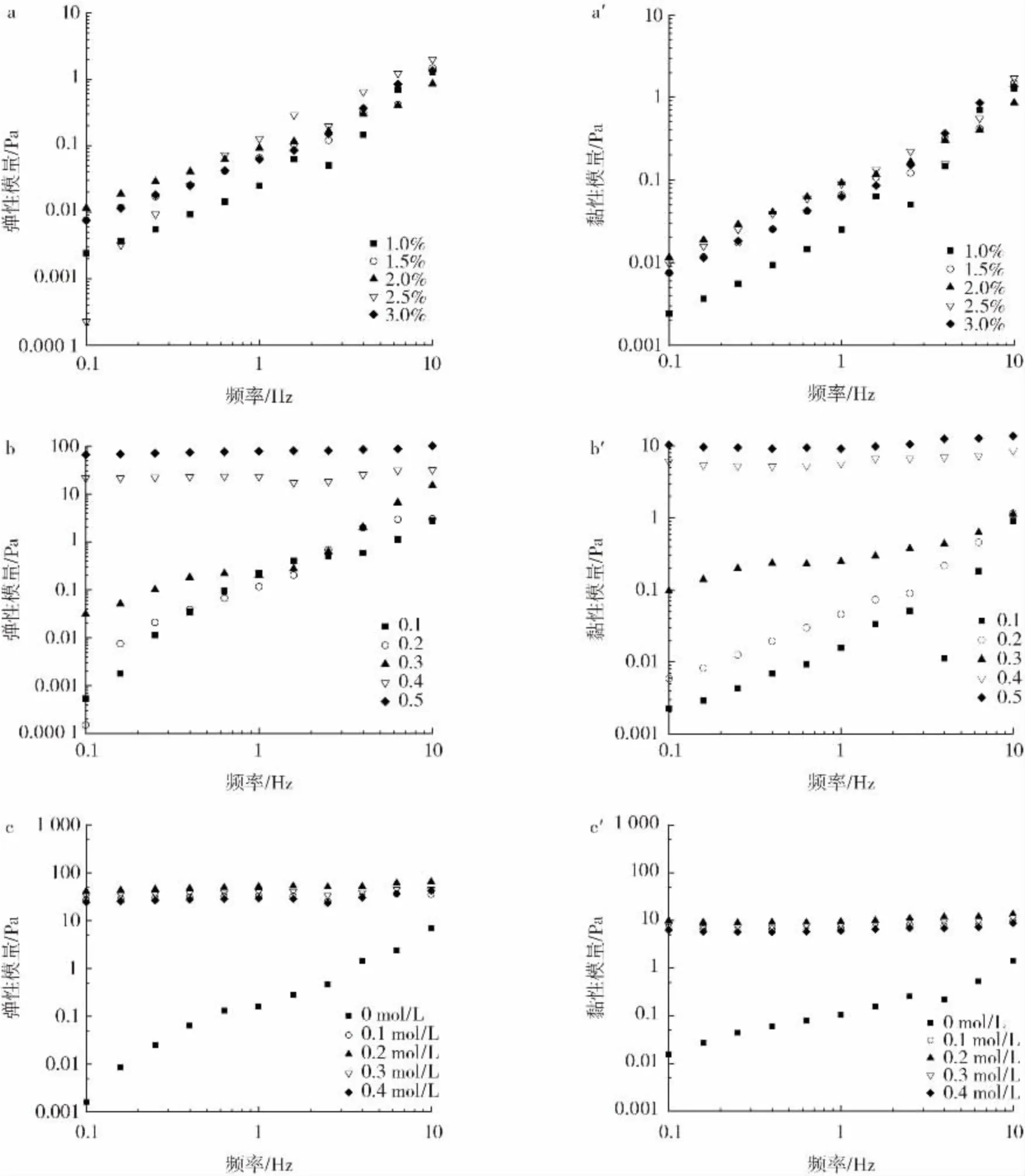
图4 SPI 颗粒浓度、油相体积分数、离子强度对乳液黏弹性的影响Fig.4 Effects of SPI concentration,volume fractions of oil phase and NaCl concentration on viscoelasticity of emulsion
由图4a 可知,乳液的G′略大于G″,在同一频率下,随着SPI 颗粒浓度增大,G′和G″均增大,这是因为SPI 颗粒浓度增加,体系中蛋白含量增加,从而使三维网状结构增强,增强了乳液的稳定性。随着频率的增加,乳液模量增加,说明乳液形成以弹性为主的弱缔合相互作用的网状结构,而模量差距不大说明乳液具有较好的流动性[32-33]。
从图4b 可以看出,不同油相体积分数的乳液的G′>G″,体系形成以弹性为主网状结构。当油相体积分数较低时,乳液具有频率依赖性,说明乳液具有较好的流动性。当油相体积分数在0.4~0.5 时,乳液由于液滴聚集具有较高的黏性,乳液呈类凝胶状,形成了类凝胶网状结构,所以模量不易受频率的变化而改变,此时的乳液稳定性强,这与Ning 等[7]研究结果一致。
由图4c 可知,在0.1~0.4 mol/L NaCl 存在下,不同离子强度的乳液G′均远大于G″,表明乳液形成了以弹性为主的凝胶网状结构,但不同离子强度之间变化很小。乳液的模量基本不具有频率依赖性,说明形成了较强的凝胶网状结构并降低了液滴的流动性,从而提高了乳液的稳定性。这可能是由于加入Na+后,蛋白质聚集程度加重,从而使蛋白分子之间的结合更加紧密,制成乳液后的结构也较为紧密,黏度和模量均有所增加,这与王小庆等[34]报道的结果一致。
2.5 乳液的贮藏稳定性
SPI 颗粒浓度、油相体积分数、离子强度对乳液TSI 的影响见图5。
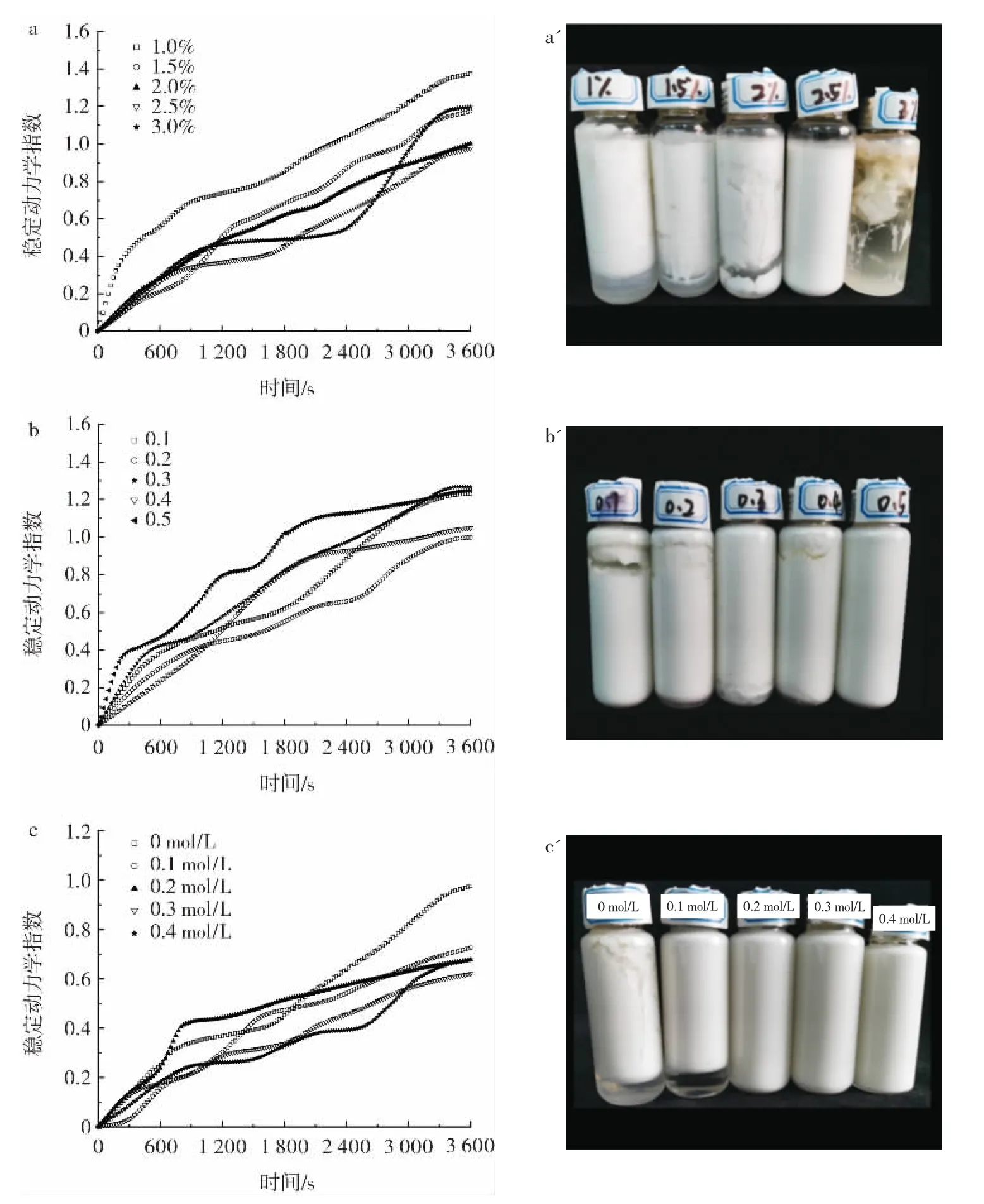
图5 SPI 颗粒浓度、油相体积分数、离子强度对乳液TSI 的影响Fig.5 Effects of SPI concentration,volume fractions of oil phase and NaCl concentration on turbiscan stability index of emulsions
Pickering 乳液的贮藏稳定性可以用稳定性动力学指数(TSI)、视觉外观来共同评价,TSI 是评估乳液稳定性的一个重要参数。稳定性分析仪应用多重光散射的原理,在样品无损的条件下表征物理不稳定现象,TSI 值越小、斜率越小,表明乳液越稳定[35]。从图5a 可以看出,随着SPI 颗粒浓度的升高,乳液的整体稳定性呈现先升高后略微降低的趋势。SPI 颗粒浓度较低时,不足以覆盖油滴,导致乳液稳定性差[8]。当SPI 颗粒浓度达到2.5%时,乳液稳定系数最低,为0.98,刚好达到乳液最适浓度,与贮藏20 d 后外观图相对应,高颗粒浓度有利于小液滴的形成,较高的颗粒可以稳定较高的界面面积,当颗粒浓度大于能吸附在界面上的最大浓度时,未吸附颗粒形成空间位阻,乳液稳定性升高;但当SPI 颗粒浓度达到3.0%时,颗粒浓度过高导致未吸附颗粒聚集,乳液整体稳定性降低。
由图5b 可知,油相体积分数为0.2 时,乳液稳定系数越低,为0.10。说明当油相体积分数为0.2 时,乳液的稳定性最好。贮藏20 d 后的视觉外观图中油相体积分数0.1~0.4 都有轻微的破乳现象,油相体积分数越高乳液常温贮藏时稳定性越好,与图3b 相对应,这主要是由于高油相可以通过增加体系的黏度使乳液的稳定性增强[36]。但在冻融试验中油相较高时,蛋白颗粒不足以覆盖油水界面,会发生析油、破乳等现象,反而不利于乳液的冻藏。
图5c 为不同离子强度对乳液贮藏稳定性的影响。当离子强度为0.3、0.4 mol/L 时,乳液的TSI 最小,乳液相对稳定。盐离子的加入进一步提升了乳液的贮藏稳定性,乳液常温贮藏20 d 后仍未出现分层现象。Zhu等[37]研究指出NaCl 的存在能实现有效的静电屏蔽,改善SPI 颗粒的乳化效率和界面填充性能,进而提高乳液的稳定性,与本文研究结果一致。
2.6 乳液的冻融稳定性
SPI 颗粒浓度、油相体积分数、离子强度对乳液冻融稳定性的影响见图6。
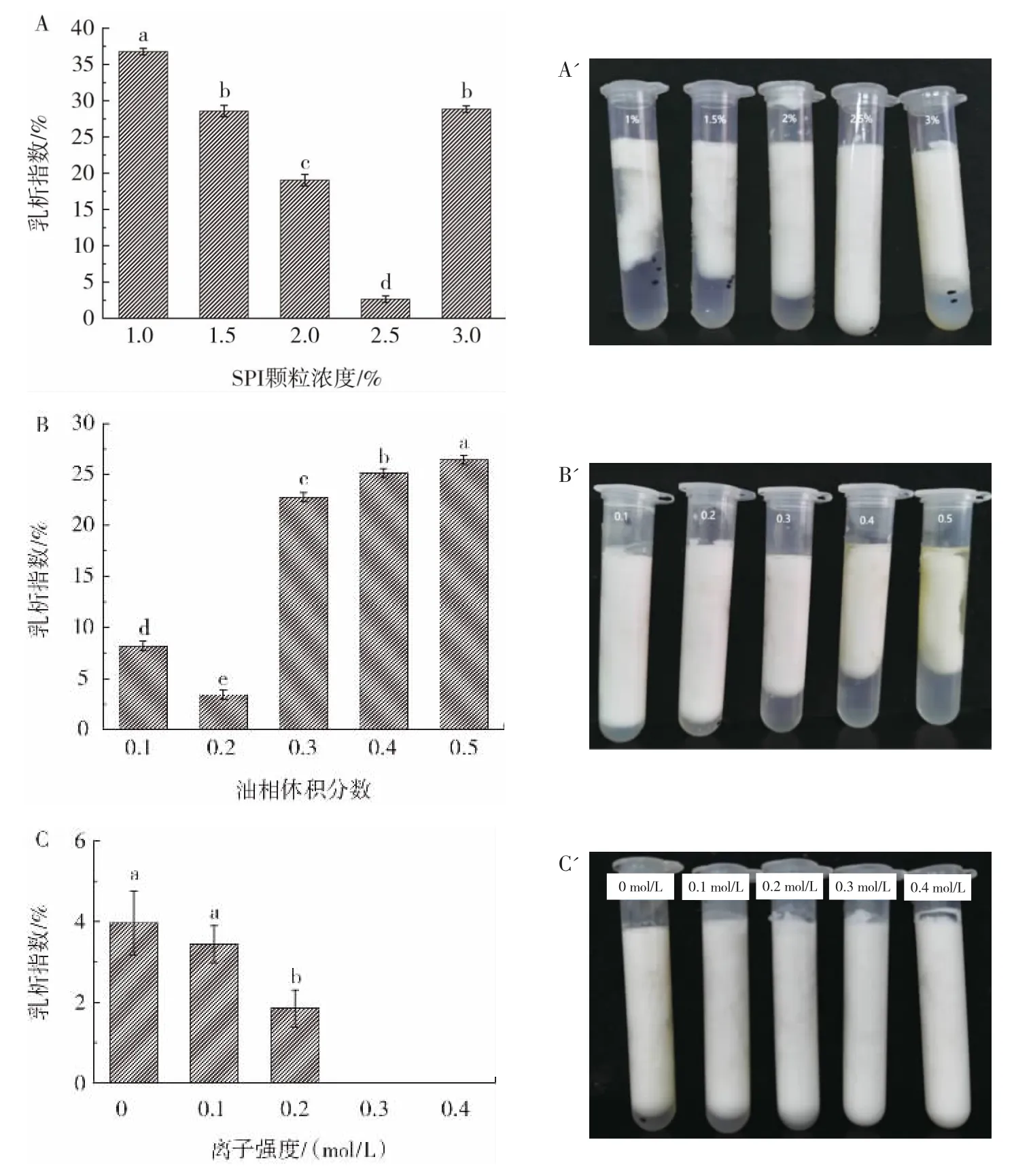
图6 SPI 颗粒浓度、油相体积分数、离子强度对乳液冻融稳定性的影响Fig.6 Effects of SPI concentration,volume fractions of oil phase and NaCl concentration on freeze-thaw stability of emulsion
乳液食品在储藏、运输过程中需要经过冷藏或冷冻,所以较高的冻融稳定性对市场实际应用具有重要意义。乳析指数(CI)是乳液中所析出水及油的高度与乳液总高度的比值,乳析指数越低,乳液越稳定。由图6a 可知,乳液冷冻过程中蛋白竞争性的吸附于冰晶和油滴,油相、水相结晶,融化时从界面解吸从而失稳;而试验中3 次冻融循环都未出现明显的油析出,说明吸附蛋白完全覆盖了油水界面。冻融循环过程中,随着SPI 颗粒浓度的升高,CI 先降低后升高,当SPI 颗粒浓度为2.5%时,CI 达到最小值为2.6%,表明此时乳液的冻融稳定性最高。SPI 颗粒浓度在1.0%~2.5%时,乳液稳定性逐步上升,原因是连续相中未吸附的蛋白颗粒与液滴形成了三维网络结构可以抵抗冷冻带来的损伤,此外固体颗粒吸附在油水界面上形成厚而坚硬的界面层可以抵抗冰膨胀而产生的应力。当SPI 颗粒浓度为3.0%时,CI 升高到28.8%,是因为体系中未吸附蛋白质颗粒增多,一方面未吸附蛋白质颗粒之间在零度以下的聚集行为[38];另一方面界面吸附颗粒与水相中未吸附颗粒之间相互缠结,聚集程度加深,进而使高浓度SPI 乳液的CI 增加[39]。
图6b 可以看出,随着油相体积分数的增加,乳液CI 越来越高,在3 次冻融过程中,油相体积分数为0.1~0.2 时,乳液仅出现破乳现象;而油相体积分数为0.3~0.5时,乳液析油与破乳现象同时出现。研究表明,不同油相比例的SPI 乳液的凝固点在-19.78~-16.26 ℃[38,40],说明在冻融过程中两相都会发生结晶,而粗鱼油在4 ℃就可发生凝固,所以随着体系中鱼油含量升高,乳液凝固点升高,进而说明油相体积分数越高,乳液将在冷冻过程中越容易发生结晶。此外,冷冻过程中,蛋白竞争性的吸附于冰晶和油滴,融化时从界面解吸,使油滴暴露出来,导致失稳。
由图6c 可知,离子强度决定了乳液的失稳程度。对于不加盐的乳液会出现严重的破乳现象,这表明其冻融稳定性非常低。离子强度在0.3~0.4 mol/L 时,乳液较稳定。说明盐离子的存在极大地提高了乳液在冻融循环过程中的抗分层稳定性。乳液加入盐后液滴发生絮凝,在冻融过程中液滴堆积可能会形成类三维网络结构。Qin 等[7]研究表明藜麦蛋白乳液中添加盐离子的乳液液滴具有较小的尺寸,且在冻融过程中“盐析”效应有效抑制了水结晶体的形成,使得乳滴界面处形成了凝胶状三维网络和多层结构。
3 结论
SPI 颗粒浓度、油相体积分数、离子强度对大豆蛋白颗粒稳定的鲢鱼油Pickering 乳液的粒径、微观结构、流变特性、乳化特性、冻融稳定性等性能具有显著影响。在SPI 颗粒浓度为1.0%~3.0%时,随SPI 颗粒浓度的增加,乳液粒径变小,液滴聚集程度降低,乳化活性逐渐降低,乳液冻融过程中的乳析指数先降低后升高;当SPI 颗粒浓度为2.5%时乳化稳定性最高,冻融后乳析指数最低,乳液最稳定。随着鲢鱼油油相体积分数的升高,乳液粒径逐渐增大,液滴聚集程度加深,乳化活性显著增高,冻融时乳析指数不断升高,甚至出现析油现象;当油相体积分数为0.2 时,乳液乳化稳定性ESI 最高,冻融乳析指数最低,乳液最稳定。加入不同盐浓度后,液滴粒径增大、聚集程度加深,乳液表观黏度、弹性模量和黏性模量显著增加;当离子强度在0.4 mol/L 时乳液稳定性好、未出现破乳现象。同时,乳液具有剪切变稀的现象,其弹性模量大于黏性模量,乳液形成三维网状结构。综上,当SPI 颗粒浓度为2.5%、鲢鱼油体积分数为0.2、离子强度为0.4 mol/L时,制得的Pickering 乳液具有较好的稳定性。
