超声造影对肝细胞癌微波消融疗效评估及对局部复发预测价值研究
2023-08-31马春燕符叶柳张植兰罗彦冰
马春燕, 符叶柳, 张植兰, 陈 列, 罗彦冰, 曾 荣
中南大学湘雅医学院附属海口医院 超声医学科,海南 海口 570208
肝细胞癌(hepatocellalar carcinoma,HCC)为临床高发肿瘤,以手术切除作为首选治疗方案,但HCC起病隐匿,多数患者发现时已错过最佳手术时机,部分患者多伴随肝炎、肝硬化等,难以耐受手术,此时多考虑微创介入治疗[1]。微波消融(microwave ablation,MWA)利用微波的热效应使癌细胞蛋白质变性进而凝固性坏死,对人体损伤较小,治疗HCC疗效显著[2]。目前,临床以增强磁共振成像(contrast-enhanced MRI,CEMRI)、增强CT(contrast-enhanced CT,CECT)作为HCC消融效果评价的金标准[3]。有研究报道,MWA治疗HCC复发风险较高,对于术后复发的高危患者,应早期识别并积极监测、及时诊断[4-5]。超声造影(contrast-enhanced ultrasound,CEUS)可通过肝实质与肿瘤的增强差异对消融疗效进行评价,并通过观察组织内血流灌注评估消融灶的灭活情况并检出复发肿瘤[6]。本研究旨在探讨CEUS对HCC患者MWA疗效的评估价值及对局部复发的预测价值。现报道如下。
1 对象与方法
1.1 研究对象 选取中南大学湘雅医学院附属海口医院自2020年1月至2022年1月收治的106例接受MWA治疗的HCC患者为研究对象。纳入标准:经穿刺或手术病理证实为HCC;单发病灶,病灶最大径≤5 cm,无血管侵犯及肝外转移;符合MWA适应证;肝功能Child-Pugh分级A~B级。排除标准:伴严重心、脑、肾功能障碍或血管疾病者;无法耐受MWA者;伴急慢性感染或血液、免疫系统疾病者;入组前6个月内有手术史者;对造影剂过敏者。其中,男性66例,女性40例;年龄42~71岁,平均年龄(57.94±6.12)岁;病灶直径1~5 cm,平均(3.21±0.73)cm。本研究经医院伦理委员会批准。所有患者均签署知情同意书。
1.2 研究方法 (1)CEUS检查:常规扫查肝,记录病灶数目、位置、回声等。注入2.4 ml SonoVue,记录病灶动脉相(10~30 s)、门静脉相(31~120 s)及延迟相(121~360 s)强化特点,获得时间-强度曲线定量参数,包括上升时间(rise time,RT)、达峰时间(time to peak,TTP)、峰值强度(peak intensity,PI)、平均通道时间(mean transit time,MTT)、曲线下面积(area under the curve,AUC)。(2)CECT检查:平扫肝,经肘浅静脉高压注射造影剂2 ml/kg,分别于30 s、55 s、60~65 s行动脉相、门脉相及延迟相扫查,观察内部强化、廓清消退情况。(3)CT引导下MWA治疗:采用KY-2000微波消融仪,患者取平卧位,消毒、铺巾,1%利多卡因局部麻醉,尖刀切皮将15G微波天线直入病灶部位,消融范围超过周边0.5~1.0 cm。
1.3 观察指标 术后1个月评估消融疗效[7]。CEUS:病灶未见增强,呈“黑洞”样,为完全消融(阴性);动脉期不规则增强,门脉期及延迟期低增强,为局部残留(阳性)。CECT:完全消融为动、门脉期无强化;局部残留为动脉期异常强化,于门脉期及延迟期消退。临床诊断:依据CEUS、CECT检查、血清肿瘤标志物、穿刺活检等综合判断,由2位经验丰富的超声医师共同确定。CEUS对局部复发的预测价值:MWA后随访3个月、6个月、1年时行CEUS复查,可疑复发时行CEMRI、CECT检查。当CEUS和CECT结果不同时,以活检结果为准。
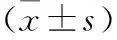
2 结果
2.1 HCC患者MWA消融效果的临床诊断结果 106例HCC患者行MWA后,最终90个病灶完全消融,16个病灶局部残留。完全消融率为84.90%(90/106)。16例病灶局部残留患者中:12例术后1个月复查提示局部残存,血清甲胎蛋白下降不明显,再次消融,密切随访诊断为完全灭活;4例经CEUS与CECT均提示残留,但实验室检查正常,超声引导下组织穿刺活检证实有癌细胞残存,后经家属要求最终行手术切除治疗。
2.2 CEUS与CECT评估消融疗效 CEUS、CECT评估消融疗效的准确性分别为92.45%(98/106)、94.34%(100/106),差异无统计学意义(P>0.05)。见表1。

表1 CEUS与CECT对消融疗效结果比较/例(百分率/%)
2.3 随访1年复发影响因素单因素分析 根据随访1年复发情况,将106例患者分为复发组(n=21)与未复发组(n=85)。两组患者性别、年龄、肿瘤位置、Child分级、肿瘤分化程度、PI、MTT、AUC比较,差异均无统计学意义(P>0.05)。复发组、未复发组患者肿瘤直径比较,差异有统计学意义(P<0.05)。复发组患者RT、TTP均低于未复发组,差异均有统计学意义(P<0.05)。见表2。
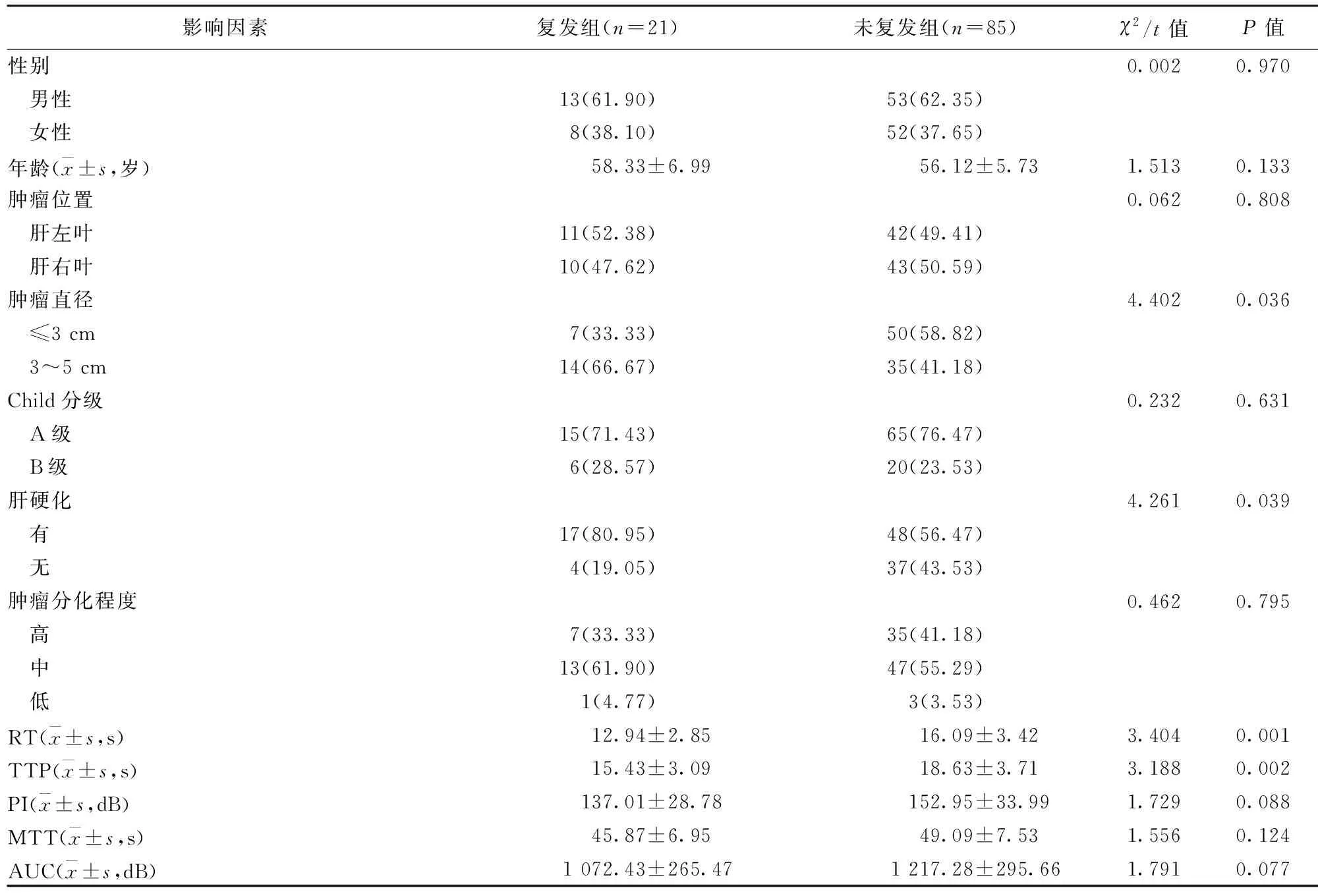
表2 随访1年复发影响因素单因素分析/例(百分率/%)
2.4 多因素Logistic回归分析 多因素Logistic回归分析结果显示,RT、TTP均为HCC患者MWA后局部复发的影响因素(P<0.05)。见表3。
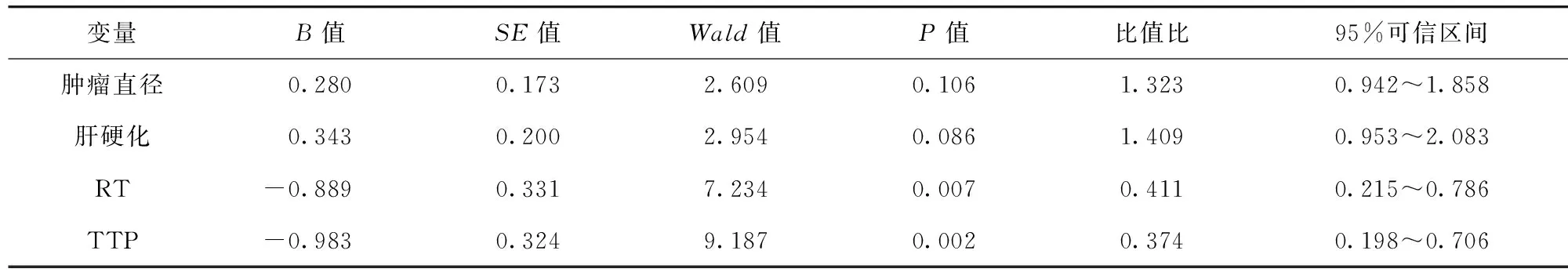
表3 多因素Logistic回归分析
2.5 CEUS定量参数预测肿瘤复发的ROC曲线 RT联合TTP预测HCC患者MWA治疗后复发的ROC曲线下面积为0.903(95%可信区间0.835~0.961)。见图1。
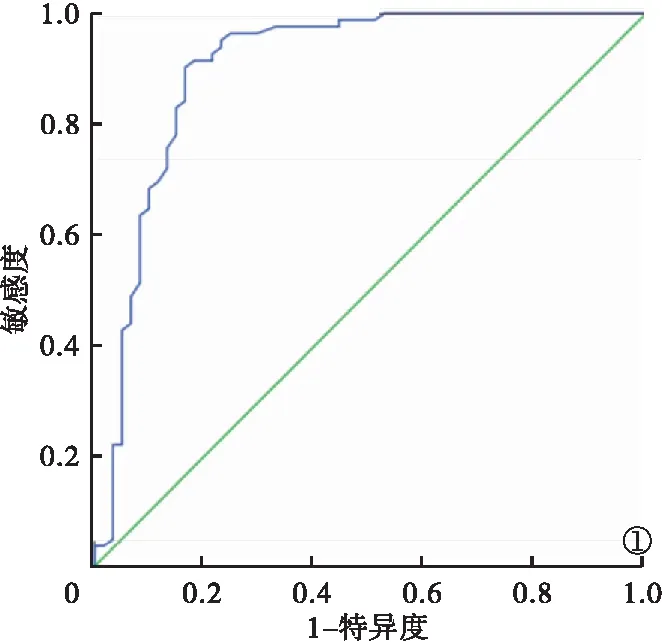
图1 RT联合TTP预测HCC患者MWA治疗后复发的ROC曲线
3 讨论
有研究报道,MWA的热效应会造成原病灶回声混合不均、边界模糊等问题,二维超声对MWA后的完全消融病灶和局部残存病灶有一定难度[8]。CEUS可获得肿瘤内微循环信息,直观显示出病灶灭活范围与程度,提供详细的血供信息,减少呼吸、伪像等影响,有利于增强对病灶内细微血流的检出能力,进而评估病灶消融效果[9]。
本研究结果显示,106例HCC患者行MWA后,90个病灶完全消融,16个病灶局部残留,CEUS、CECT评估消融疗效的准确性分别为92.45%(98/106)、94.34%(100/106)。这提示,CEUS对消融疗效的评估可达到与CECT相当的效果。CEUS具有较高的空间分辨率与对比分辨率,MWA术后病灶残留多表现为病灶旁或内部结节/月芽状,残留较多者可见病灶周边环状不规则增强区,且增强模式与治疗前病灶相似,为“快进快退”[10]。CEUS图像能使残留病灶在CEUS动脉相上的高增强与治疗后造影缺失区域(黑洞)形成强烈对比,能较好地辨认是否存在病灶残留,进而评估MWA疗效[11]。CEUS评估消融疗效会受到病灶炎症、微小动静脉瘘等影响,可能原因为炎症、微小动静脉瘘的存在会使CEUS动脉相呈不规则斑片状强化,门静脉相、延迟相等强化,可通过密切随访、穿刺活检等避免误诊[12-13]。本研究结果显示,RT、TTP均为HCC患者MWA后局部复发的影响因素(P<0.05),当临界值分别为14.65 s与17.28 s时,RT、TTP预测HCC患者MWA治疗后复发的ROC曲线下面积为0.903(95%可信区间0.835~0.961)。敏感度与特异度分别为0.905、0.847。这提示,CEUS不仅可用于病灶的消融疗效评估,还可通过检测定量参数RT、TTP对复发风险进行预测和评估。RT和TTP可反映肿瘤病灶血供情况,主要受到肿瘤血供中肝动脉与门静脉的比例,动脉血供占比越高,病灶上升越快,达峰越早,因此RT与TTP越短[14]。HCC属于富血供肿瘤,且肿瘤血供以肝动脉为主,因此CEUS检查时在动脉相早中期造影剂就会充填完全,并快速达峰,即“快进”[15]。HCC患者多伴随肝炎、肝硬化,通常存在正常肝小叶结构破坏、纤维增生等,使门脉高压及动门脉瘘形成,动脉血供代偿性增多,造成RT和TTP进一步缩短[16]。HCC患者MWA治疗后复发风险越高,复发原因多为首次治疗时病灶残留或癌细胞经门静脉播散[17]。有研究报道,单纯CEUS对检查者有一定依赖,当复发灶微小且靠近周围肝组织或大血管时易被漏诊;而当仪器调节不当时,容易将屏幕的伪影误诊为复发病灶[18-19]。时间-强度曲线通过定量数据排除对检查者的依赖,对肿瘤局部复发的评估更为客观[20]。有研究报道,MWA治疗前CEUS的RT和TTP越短,说明存在的细小滋养血管越多,消融时难免有细小滋养血管被漏掉,复发风险就越大,使得RT与TTP可在一定程度上预测肿瘤复发[21]。“快进快出”与病灶动脉期增强为判定复发的主要征象,但有时复发病灶观察不到动脉期增强,分析原因在于部分复发肿瘤的分化程度高,滋养动脉细,同时接受一定比例的门静脉供血,因此动脉期增强不明显,难以通过肉眼辨认,门脉期和延迟期造影剂廓清速度较缓慢[22]。CEUS可将图像与定量数据相结合,在“快进快出”与动脉期增强等征象基础上,结合RT和TTP定量数据,可提高对病灶残留及复发情况的诊断准确性,避免穿刺活检等创伤性操作,准确预测复发。
综上所述,CEUS检查可用于HCC患者MWA治疗的消融疗效评估,同时CEUS定量数据可对肿瘤的局部复发进行有效预测,可作为后续随访、检查的手段。
