包装饮用水臭氧处理过程中溴酸盐的生成与控制研究
2023-08-07吴小勇
吴小勇
咸阳市食品药品检验检测中心
李雪雪
咸阳市食品药品检验检测中心
李小鹏
咸阳市食品药品检验检测中心
陶桂松
咸阳市食品药品检验检测中心
胡梦瑶
咸阳市食品药品检验检测中心
包装饮用水,是指密封于符合食品安全标准和相关规定的包装容器中,可供直接饮用的水[1]。包装饮用水主要分为饮用天然矿泉水、饮用纯净水、饮用天然泉水、饮用天然水和其他饮用水。近年来,包装饮用水行业发展迅速,但通过食品安全监督抽检发现,包装饮用水溴酸盐超标问题检出率较高,这与包装饮用水经臭氧(O3)杀菌处理有密切关系。
O3作为消毒剂可迅速杀灭各种细菌、病毒和原虫等微生物,且无毒无味,安全、经济、可靠,是目前饮用水生产企业广泛应用的消毒灭菌剂。一般情况下,水中不含溴酸盐,但普遍含有溴化物。采用O3对饮用水进行消毒灭菌时,溴化物会与O3发生反应生成溴酸盐。研究表明,当人们长期饮用溴酸盐含量为5.0μg/L 或0.5μg/L 的饮用水时,其致癌危险度分别为10-4和10-5[2]。溴酸盐被国际癌症研究机构定为2B 级潜在致癌物。
根据GB 5749—2022《生活饮用水卫生标准》规定,生活饮用水中溴酸盐的限量值为0.01mg/L[3]。该标准与世界卫生组织的规定一致。根据国家市场监督管理总局和各地方市场监管部门发布的通告可知,容易出现溴酸盐不合格的产品主要有饮用天然矿泉水和饮用天然水。因饮用天然矿泉水和饮用天然水的生产工艺不同于饮用纯净水,为保证矿物质指标、微生物指标满足相应产品标准要求,生产企业往往采取增加O3投量的方式控制微生物,忽略了消毒灭菌过程中副产物溴酸盐的生成,导致包装饮用水存在一定程度的安全隐患。
1 溴酸盐的生成原理
溴酸盐的生成原理相对复杂,受多种因素的影响。1983年,Haag 等[4]提出O3氧化时BrO3-的生成机制。Br-被O3氧化成OBr-,OBr-被O3进一步氧化生成BrO3-;而且,OBr-也会与 O3发生反应,再次转化成Br-。1994 年,Von 等[5]提出O3氧化过程中生成BrO3-的两个途径:O3直接氧化和HO·(氢氧根自由基)氧化。Br-被O3氧化为次溴酸(HOBr),HOBr 被O3和HO·(氢氧根自由基)进一步氧化生成BrO3-。1998 年,Von等[6]完善了BrO3-的生成机制:①Br-被O3氧化生成中间态的HOBr/OBr-,HOBr/OBr-被O3和HO·进一步氧化生成BrO3-。②Br-与HO·反应生成原子溴(Br·),Br·被O3直接氧化成溴氧自由基(BrO·),BrO·绕过HOBr/OBr-进一步生成 BrO3-。由此可见,BrO3-的生成途径很复杂,O3和HO·可能同时参与Br-的转化(图1)。
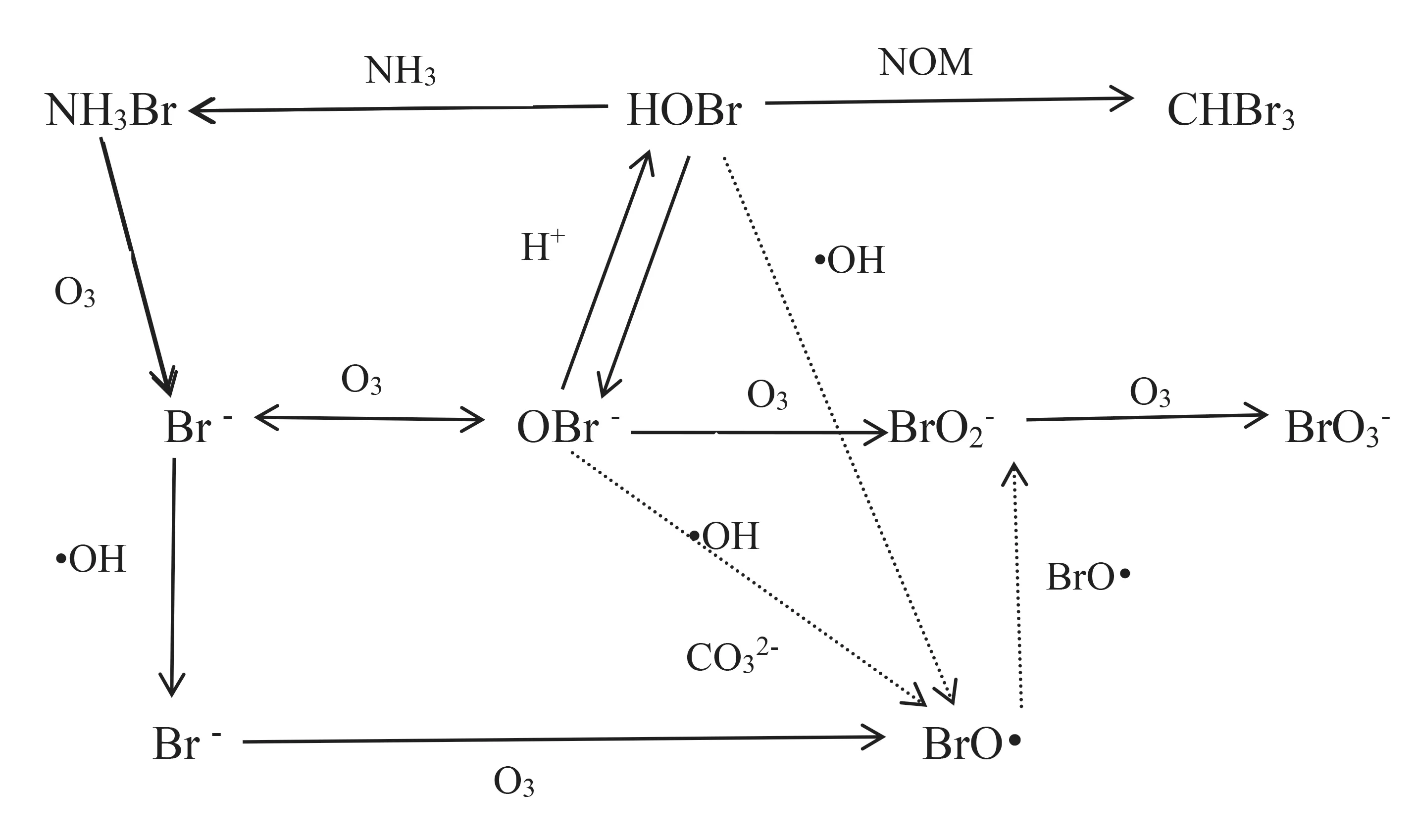
图1 溴酸盐生成原理
2 溴酸盐生成的影响因素
O3氧化过程中,溴酸盐的生成受很多因素的影响,如Br-浓度、O3投量、O3投加方式、温度、反应时间等[7]。本文探讨了Br-浓度、pH、O3投量和投加方式、反应时间对溴酸盐生成的影响。
2.1 Br-浓度
在O3投量和反应时间相同的情况下,溴酸盐的生成量基本与Br-浓度呈线性关系[8]。源水是流动的,水中Br-浓度不断变化,溴酸盐的生成量也随之变化。
笔者通过实地调研进一步考察Br-浓度对溴酸盐的影响。通过调研一家饮用天然矿泉水生产企业,产品为富锶矿泉水。该企业之前出现过溴酸盐含量超标现象,为使溴酸盐和微生物指标均合格,将O3投量降到0.07mg/L,同时在管道上加装了3 组紫外线灭菌装置。连续15 天在同一时间段采集源水和成品水,检测源水中溴化物、锶的含量及成品水中溴酸盐、锶的含量和铜绿假单胞菌的结果。溴化物、铜绿假单胞菌、锶和溴酸盐的测定参考GB 8538—2022《食品安全国家标准 饮用天然矿泉水检验方法》[9]。
结果显示,成品水中铜绿假单胞菌未检出。源水中溴化物、锶的含量测定结果和成品水中溴酸盐、锶的含量测定结果如图2、图3 所示。由图2 可知,溴酸盐的生成量与源水中Br-的浓度呈正相关。由图3 可知,成品水中锶的含量略低于源水中锶的含量,但是变化不大。

图2 源水中溴化物和成品水中溴酸盐的测定结果(μg/L)

图3 源水和成品水中锶的测定结果(mg/L)
经过工艺改良后,成品水中微生物指标(铜绿假单胞菌)、界限指标锶和溴酸盐都符合GB 8537—2018《食品安全国家标准 饮用天然矿泉水》的要求[10]。虽然此次溴酸盐含量得到了有效控制,但是需要注意的是,源水中溴化物浓度对溴酸盐的生成起决定性作用,如何在既要保留矿物质又要杀灭微生物的基础上,有效控制源水中溴化物浓度,是行业内亟需解决的问题。
2.2 pH
当O3投量一定时,降低pH可以使氢氧自由基含量降低,从而抑制溴酸盐的生成。研究表明,pH 对溴酸盐生成的影响最大,降低一个pH 单位,溴酸盐的生成量可以减少50%[11]。由此可见,降低pH 是控制溴酸盐生成的有效办法之一。可以通入二氧化碳来降低pH,但是对于碱度较大的源水,生产成本将大大增加。
2.3 O3 投量和投加方式、反应时间
在氧化过程中,随着O3投量增加和反应时间延长,溴酸盐生成量也不断增加。因此,可以通过降低O3投量来控制溴酸盐的生成。需要注意的是,降低O3投量可能无法将水中微生物完全破坏,影响成品水中微生物指标。研究发现,当O3投量不变时,增加投加点可降低溴酸盐的生成量[12]。原因可能是多个投加点加入缩短了O3的接触时间,降低了水中剩余O3的浓度。
综上,降低O3投量、缩短反应时间以及增加O3投加点,可减少溴酸盐的生成。考虑到生产企业的投资成本,一般设3~4 个投加点即可。
3 溴酸盐的控制方法
去除溴酸盐的方法分为:①消毒灭菌前,去除源水中Br-以抑制溴酸盐的生成;②消除已生成的溴酸盐。
3.1 去除源水中Br-
作为BrO3-的前体物,Br-主要来自矿物溶解、海水入侵地表水或地下含水层[13]。调研结果显示,Br-浓度对BrO3-的生成起决定性作用。
目前,去除源水中Br-的方法主要有膜分离技术、电化学技术和吸附技术。膜分离技术包括反渗透、纳滤、电渗析和反向电渗析等技术,目前被广泛应用的是反渗透技术。反渗透技术的净化效果高,能很好地去除水中的Br-,被广泛应用于纯净水的生产。纳滤技术多被应用于饮用天然矿泉水或饮用天然水的生产,但源水的杂质不同,膜的更换频次不同,成本相对较高。电化学技术常用于处理工业废水。采用吸附技术去除水中Br-时,吸附剂的种类、添加量、吸附效率等需要不断试验,且可能带入新的污染源,吸附材料主要有水滑石、活性炭、银掺杂活性炭、碳气凝胶、离子交换树脂、铝基吸附剂等[13]。
这几种方法都可以有效去除水中Br-,在企业生产运行中,膜分离技术中反渗透技术被广泛应用于纯净水的生产,纳滤技术被大多天然饮用矿泉水/饮用天然水的生产企业使用,但源水的杂质不同,膜的更换频次不同,导致部分企业运营成本较高。而吸附技术更容易被应用,但吸附剂的选择、吸附剂的添加量、吸附效率等也需要不断试验,而且可能带入新的污染源。
3.2 溴酸盐的消除
目前,消除溴酸盐的方法有:零价铁还原、亚铁离子还原、光催化还原、高级还原技术、紫外线分解、活性炭吸附等[13]。
3.2.1 零价铁还原
在零价铁(Fe0)还原过程中,Fe0并不是唯一的还原剂,反应生成的Fe2+、Fe0腐蚀产生的H2等也会参与溴酸盐的还原。此外,pH 在7~8 时,氧化产物Fe2+和Fe3+会生成 Fe(OH)2和Fe(OH)3,有很强的吸附絮凝性[13],也能去除水中的溴酸盐。需要注意的是,投加大量的Fe0并不一定能有效消除溴酸盐,而且可能会使水中的铁超标。
3.2.2 亚铁离子还原
亚铁离子(Fe2+)被认为是最有可能应用于实际的还原剂,可以将BrO3-还原成Br-,此化学反应的进行可能受反应物浓度、时间、pH、温度等因素影响[14]。此外,水中具有氧化性物质如溶解氧、硝酸根也会与Fe2+发生反应,导致BrO3-还原效果降低。因此,需要添加高浓度的Fe2+,但是反应过后浑浊度可能会高,残留在水中的铁也需要进行再处理。
3.2.3 光催化还原
研究表明,二氧化钛(TiO2)表面的光电子能将BrO3-还原成Br-,从而达到去除溴酸盐的目的[13]。为了使光催化效率更高,可以向TiO2表面负载铂(Pt),溶液中添加醇(甲醇/乙醇),三氧化二铝(Al2O3)修饰TiO2,但是TiO2表面负载重金属可能会使重金属溶出,存在潜在的风险。此外,光催化剂的成本较高,目前尚处于实验阶段,并没有得到广泛应用。
3.2.4 高级还原技术
以紫外线/亚硫酸盐(UV/SO32-)体系为代表的高级还原技术可以有效地去除卤代有机物(如1,2-二氯乙烷、氯乙烯、氯乙酸、全氟化合物)和无机含氧酸根[如高氯酸盐(ClO4-)、BrO3-]。UV/SO32-体系对BrO3-的还原作用机制与活性物质的形成有关,如水合电子(eaq-)、原子氢(H·)和亚硫酸根自由基(SO3·-)。研究发现,在有氧条件下,UV/SO32-体系对溴酸盐 (50μg/L)的去除效果并不理想,当投加160mg/L SO32-时,溴酸盐的去除率为40%左右[13]。因此,O2的存在会大大抑制UV/SO32-体系对溴酸盐的去除效果。
3.2.5 紫外线分解
研究表明,短波紫外线不仅可以消毒灭菌,还可以有效去除水中溴酸盐,可将BrO3-还原成Br-,随着辐射能量的增加,溴酸盐的浓度不断降低。用中压汞灯消除水中500μg/L 溴酸盐所需的紫外线辐射强度为10 500mJ/cm2[15]。调研的生产企业成品水中溴酸盐的含量为20μg/L,使用的UV 辐射强度为80mJ/cm2,所以在实际生产过程中,需要多处增加紫外灯,相应增大企业成本。也有研究表明,紫外线辐射消除溴酸盐的反应过程复杂,可能还会增加溴酸盐的含量[16]。由此可见,单一采用紫外线辐照法去除水中溴酸盐并不具有可行性。
3.2.6 活性炭吸附
研究表明,活性炭在一定条件下对溴酸盐有很好的消除作用。活性炭不仅可以通过微小的孔吸附杂质,去除色、味、嗅、溴酸盐改善水质,还能降解复杂的有机大分子,使其转化为小的有机分子,甚至可以将有机大分子氧化成无害物质[16]。目前公认的活性炭消除溴酸盐的原理是,溴酸盐先被吸附,再被还原,溴离子随水流冲走。活性炭是控制溴酸盐的有效措施,但是使用一段时间后,溴酸盐的去除率明显下降,可能是受到水中有机碳、阴离子(Cl-、SO42-、NO3-)等的影响。活性炭表面也可能被吸附在表面的细菌覆盖,更可能滋养出新的微生物,也无法实时监测去除效果,给饮用水的质量安全埋下隐患。
理论上,利用氧化还原反应是可行的,但若投入生产,还原率和还原速度会受很多因素的影响。另外,结合包装饮用水产品的特性,若采用Fe0还原、Fe2+还原,其在消除溴酸盐的同时会引入其他副产物,可能更不利于人体健康。因此,为得到理想的溴酸盐消除效果,企业应根据实际情况对O3浓度和反应时间进行不断试验,也要考虑消除后的安全性,及可能产生的副产物。
4 结论及建议
当使用O3对包装饮用水进行消毒灭菌时,产生的溴酸盐可以通过改善源水和生产工艺进行控制。研究表明,生产中通过降低水中pH、温度等方式减少溴酸盐的生成不具有可行性,但可以通过膜分离技术来减少源水中Br-含量;采用O3和紫外线联合消毒灭菌、降低O3投量或者增加O3投加点的方式降低溴酸盐含量的同时,又能确保微生物指标符合规定。生产企业也可以在工艺上进行完善,源水在经过砂滤、碳滤等粗滤后,加装紫外线灭菌装置,瞬时的强辐射紫外线可有效抑制微生物,而后精滤,O3消毒灭菌时可以降低投量,微生物指标和溴酸盐都合格,饮用水就更加安全。需要注意的是,当生产天然矿泉水时,使用膜分离技术可能会导致矿物质及营养成分含量降低。因此,为满足GB 8538—2022 中界限指标的要求,企业需要根据源水特性、工艺特点、成本等进行不断尝试,以实现溴酸盐、微生物指标、界限指标三者之间的平衡。
