银屑灵颗粒质量标准的研究
2023-07-10张云玲笔雪艳冯乐然赵荣生高飞那微
张云玲 笔雪艳 冯乐然 赵荣生 高飞 那微


【摘 要】 目的:控制银屑灵颗粒质量。方法:采用薄层色谱(TLC)法鉴别制剂中赤芍、山银花、黄柏、防风;采用高效液相色谱法(HPLC)测定制剂中苦参碱的含量。结果:TLC斑点清晰,分辨率好,阴性无干扰。苦参碱的测定在0.137501~4.400046 μg之间有良好的线性关系,线性方程Y=2.0270×106A-2843.7361,r=0.9999,平均回收率为100.07%(RSD=2.2%,n=6)。结论:该质量标准項目设置合理,操作便捷、准确,可用于对银屑灵颗粒的质量控制。
【关键词】银屑灵;质量标准;薄层色谱 ;含量测定
【中图分类号】R284.1 【文献标志码】 A【文章编号】1007-8517(2023)11-0050-05
Abstract:Objective Establish the quality control method of Yinxieling granules.Methods Radix Paeoniae Rubra,Flos Lonicerae,Cortex Phellodendri and Radix sileris were identified by TLC,and the contents of matrine in the preparation were deter mined by HPLC.Results TLC spots were clear,good separation and negative.The content deter mination method of matrine showed a good linear relationship between 0.275003-4.400046 μg.The average recovery of matrine in Yinling granules was 100.07%,(RSD 2.2%,n=6).Conclusion The method is simple,accurate and effective in separation,andcan be usedto evaluate the quality of Yinling granules.
Keywords:Yinxieling; Quality Standard;TLC Identification; Content Deter Mination
银屑病,是临床上常见的一种慢性皮肤病,在中医上又称其为白疕,这种疾病的发病机制复杂并且容易复发[1]。临床上患者深受其扰,生活质量大大下降。对于银屑病的治疗,中医药展现出了其独特的优势,能极大改善银屑病的预后[2-3]。银屑灵颗粒是由苦参、白鲜皮、土茯苓、山银花、黄柏、蝉蜕、防风、连翘、赤芍、地黄、当归、甘草等十二味中药材组成的复方制剂。其中苦参,去湿杀虫,疗风热细疹,治赤痢恶疮;白鲜皮在《雷公炮炙药性解》中可疗杨梅诸疮热毒,和血脉,通九窍;土茯苓,益脾胃,化湿邪,善治杨梅恶疮,毒窜筋骨;三药配合可增强祛风止痒、杀虫疗癣之功。山银花、连翘,主寒热,疗痈肿恶疮,消痈散毒,善行上焦;黄柏燥湿清热,主泻下焦之火;相和使用可清一身之火。蝉蜕,轻浮发散,逐邪热。防风祛邪外出,防护腠理;蝉蜕、防风二药可引药达表,增强药物作用效果。当归、甘草合用调营养血,以防血虚化燥生风。地黄、牡丹皮、甘草、赤芍,为常用清热凉血药配伍药对[4]兼能活血祛瘀。全方上下与表里同治;驱邪与补益药同用以防损耗正气。具有清热解毒、通络活血祛湿之效。用于湿热蕴肤,郁滞不通所致的白疕,症见皮损呈红斑湿润、偶有浅表小脓包,多发于四肢曲侧部位[5]。
银屑灵颗粒现行质量标准号为YBZ10512005-2009Z,为企业标准;为更好的对产品的内在质量进行控制,对银屑灵颗粒质量控制的方法进行了实验研究,取消了原标准中苦参碱和当归的薄层鉴别,保留了赤芍和盐酸小檗碱的薄层鉴别,建立了处方中防风的薄层鉴别方法和山银花特征鉴别;同时采用HPLC法测定苦参碱的含量,将原质量标准HPLC法测定绿原酸删除。经方法学验证、方法基本可行,可纳入质量标准,以期能为其更全面的质量控制提供依据。
1 仪器与材料
1.1 仪器 Sartorius CP225D电子分析天平(德国赛多利斯公司产);Julabo TW20水浴锅(日本产);Waters e2695高效液相色谱仪(日本沃特世公司);超声波清洗仪(上海科导超声仪器有限公司,220v,250w)。高效液相用色谱柱—Angilent SB-C18;Kromasil 100-5-C18;phenomenex Luna C18。
1.2 试剂与试药 色谱级乙腈、甲醇;水为超纯水;其它试验所用试剂均为分析纯;盐酸小檗碱对照品(110713-202015)、赤芍对照药材(121093-201804)、防风对照药材(120947-200907)、5-O-甲基维斯阿米醇苷对照品(111523-200404)、灰毡毛忍冬皂苷乙对照品(111814-201604)、苦参碱对照品(110805-202010、98.7%)均来源于中国食品药品检定研究院。硅胶G预制薄层板为青岛海洋公司生产。银屑灵颗粒15批(哈尔滨大洋制药股份有限公司)。
2 方法与结果
2.1 薄层鉴别
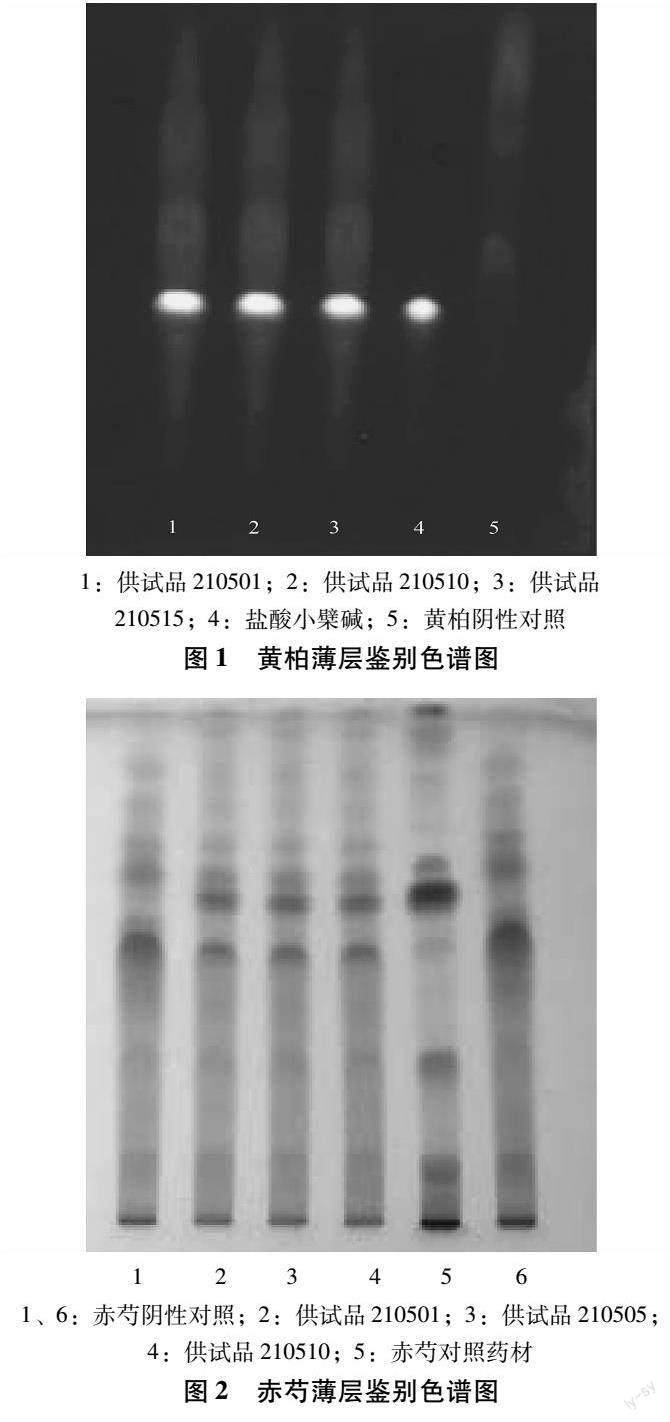
2.1.1 黄柏 取本品20 g,研细,加入50 mL无水乙醇,加热回流40 min,过滤,滤液蒸至约1 mL,作为供试品溶液。按处方配比以同样方法制备的黄柏阴性样品,按供试品同样方法制备作为阴性对照溶液。再取盐酸小檗碱对照品,加乙醇制成每1 mL含30μg的溶液,作为对照品溶液。分别取待测溶液 2 μL、阴性对照溶液 2 μL、对照品溶液 5 μL,点在同一硅胶 G 薄层板上。以正丁醇-冰醋酸-水(7∶1∶2)为展开剂,展开,取出,干燥,在紫外灯(365 nm)下检测。在供试品的色谱图中,与对照品比较在色谱图的对应位置,显示相同颜色的荧光点,而阴性对照溶液在与盐酸小檗碱色谱相应位置上未出现相同荧光斑点,表明阴性对照无干扰,该方法专属性良好。如图1所示。
2.1.2 赤芍 取本品20 g,研细,加入30 mL乙醇溶液,经30 min超声处理,过滤,滤液蒸干,残渣加入15 mL水使其溶解,过滤,滤液用乙醚振摇萃取2次,每次15 mL,弃乙醚溶液,用水饱和正丁醇萃取3次,每次15次 mL,合并正丁醇提取液,蒸干,使残渣溶解于1 mL乙醇溶液中,作为供试品溶液。取另一份按规定比例制备的缺赤芍阴性样品,用同样的方法制备阴性对照溶液。取0.5 g赤芍对照药材,加入10 mL乙醇,振摇萃取5 min,过滤,滤液蒸干,残渣中加入2 mL 乙醇,使其溶解,作为对照药材溶液。吸取上述3种溶液各5 μL,并将它们分别点在以羧甲基纤维素钠为粘合剂的同一硅胶G薄层上。以氯仿-甲醇-乙酸乙酯(8∶4∶1)为展开剂,展开,取出,自然晾干,喷以5%香草醛硫酸溶液,加热至颜色清晰,出现斑点。供试品色谱图中,与对照药材色谱图对应的位置有相同颜色的斑点,而阴性对照溶液在与对照药材色谱相应位置上无相同颜色斑点出现,表明阴性对照液对赤芍的鉴别无干扰,专属性良好。如图2所示。
2.1.3 防风[6-7] 取本品20 g,研细,加入50 mL丙酮溶液,并经过20 min的超声处理,过滤,将滤液浓缩至5 mL,作为供试品溶液。同时按照处方比例将制备好的无防风阴性样品采用同样的方法制成阴性对照溶液。另取防风对照药材1 g,同样方法制备对照药材溶液。再取5-O-甲基维斯阿米醇苷对照品,加入乙醇制成浓度为1 mg·mL-1的溶液。吸取上述4种溶液各5 μL,分别点在同一硅胶 GF254薄层板上。以氯仿-甲醇(4∶1)为展开剂,展开,取出,晾干。喷上10%硫酸乙醇溶液,105 ℃高温加热至斑点显色清晰,置于365 nm紫外光灯下观察。供试品色谱图中,与对照药材色谱图和对照品色谱图对应的位置有同色荧光点,阴性样品在防风对照药材和5-O-甲基维斯阿米醇苷对照品相应位置上无斑点干扰,表明该方法专属性良好。如图3所示。
2.1.4 山银花[8-9] 取山银花 15 g,研细,加入60 mL甲醇溶液,超声15 min,过滤,将滤液蒸干,加入25 mL水使残渣溶解,用水饱和正丁醇提取两次,每次30 mL,将两次正丁醇提取液合并,用氨水洗涤两次,每次30 mL,将正丁醇溶液蒸干,使残渣溶于2 mL甲醇溶液中,作为供试品溶液。同时取按处方配比制备的无山银花的阴性样品,采取同样方法制备阴性对照溶液。此外,取灰毡毛忍冬皂苷乙对照品,加乙醇制成浓度为1 mg·mL-1的溶液,作为对照品溶液。吸取上述3种溶液各 5 μL,分别置于同一硅胶 G 薄层板上,展开剂采用氯仿-甲醇-水(6∶4∶1),展开,取出,晾干,喷上10%硫酸乙醇溶液,105 ℃加热至出现清晰的斑点颜色,在日光下观看。供试品色谱图中,与对照品色谱图对应的位置有同色荧光点。阴性样品在与灰毡毛忍冬皂苷乙相应色谱位置无干扰,表明该方法专属性良好。如图4所示。
2.2 含量测定[10-13]
2.2.1 色谱条件 以氨基键合硅胶为填料;使用乙腈-异丙醇和3%磷酸溶液(异丙醇-3%磷酸溶液 (5∶15)(88∶12) 作為流动相;检测波长为203 nm。按苦参碱峰计算理论板数应不低于3000。
2.2.2 对照品溶液的制备 精密称取适量苦参碱对照品,加入流动相配成浓度为50μg·mL-1的溶液,即得。
2.2.3 供试品溶液的制备 在装量差异项下称取适量本品,研细,经精密称量,取约5g,置于锥形瓶中,精密加入25 mL三氯甲烷-甲醇-浓氨溶液(50∶50∶1)的混合溶液,密塞,称重,超声处理(功率250 W,频率35 Khz)20 min,冷却后再次称重,减失的重量用三氯甲烷-甲醇-浓氨溶液(50∶50∶1)的混合溶液补足,摇匀后滤过。精密量取10 mL续滤液,加入中性氧化铝色谱柱(100-200目,5 g,内径1.0 cm)中,先用40 mL氯仿洗脱,再用30 mL氯仿-甲醇(7∶3)混合液洗脱(流速为30滴/min),将洗脱液进行合并,并回收溶液至干,残渣中加入适量流动相使其溶解,转移至10 mL容量瓶中,加入流动相至刻度,摇匀,即得。
2.2.4 阴性对照溶液的制备 按处方比例,取除苦参以外的其他处方量药材,按处方制备方法制备不含苦参的阴性对照样品,并按“2.2.3”项下相同方法制备阴性对照溶液
2.2.5 系统适用性 分别精密吸取对照品溶液与供试品溶液各10 μL,按“2.2.1”的项下色谱条件进样。结果表明,在供试品的色谱图中,在对照品色谱图中相应位置有相应的色谱峰,阴性样品在苦参碱峰相应位置无干扰,分离度及理论板数均符合要求。色谱图如图5~7所示。
2.2.6 线性关系 取苦参碱对照品适量,精密称定,22.29 mg于50 mL 容量瓶中,加入流动相至相应刻度,用移液管精密量取5 mL于10 mL 容量瓶中,然后从10 mL 容量瓶中精密量取5 mL,放入10 mL 容量瓶中,加流动相定容至刻度,依次制成6个不同浓度的对照品溶液,进样量为10 μL。以峰面积为纵坐标,进样量为横坐标,绘制关系曲线,回归方程为:Y=2.0270×106 A- 2843.7361,相关系数r=0.9999.结果表明苦参碱在0.137501~4.400046 μg范围内浓度与吸收峰面积值呈良好的线性关系。
2.2.7 精密度试验 取“2.2.2”项下对照品溶液10 μL,注入液相色谱仪,连续进样5次测定苦参碱峰面积,RSD值为1.0%,结果显示仪器精密度良好。
2.2.8 稳定性试验 取“2.2.3”项下的供试品溶液,按含量测定方法进样后每隔5 h进样1次,连续进样9次,测定峰面积。结果苦参碱含量相对标准偏差(RSD)为3.3%,苦参碱随时间增加峰面积有增大趋势,40 h内总体稳定性良好。
2.2.9 重复性试验 取批号为210509的样品,照“2.2.3”项下所述方法处理,平行制备6份,所得溶液依“2.2.1”项下色谱条件测定,计算含量。结果苦参碱的平均含量为0.2430 mg·g-1(RSD值为1.5%,n=6),表明重复性结果良好。
2.2.10 回收率试验 精密取“2.2.2”项下制备的对照品溶液(浓度为0.055 mg·mL-1)1.50 mL,分别置6个容器中,使干。精密称取本品适量,各按2.2.3项方法制备6份供试品溶液,按“2.2.1”项色谱条件测定含量,并计算回收率。平均回收率为100.07%,RSD值为2.2%。结果见表1。
2.2.11 耐用性试验 取本品含量测定项下的对照品溶液与供试品溶液,分别以色谱柱①Thermo APS-2 HYPERSIL、②Phenomenex Luna NH2 100A、③MEDJEN Magasil NH2分別进行分析测定,结果显示分离度均大于1.5,含量结果RSD为4.7%,耐用性良好。
2.2.12 样品含量测定 按“2.2.1”项下方法,对生产企业提供的15批样品进行苦参碱含量测定,15批产品含量均值为:0.1996 mg·g-1,3.99 mg/袋。结果见表2。
3 讨论
3.1 薄层鉴别 盐酸小檗碱的原质量标准方法可行,阴性样品无干扰,后续研究中发现,赤芍鉴别的供试品溶液中也可检出盐酸小檗碱,可与赤芍鉴别共用供试品溶液。金银花与山银花功效相近、成分相似,均具有抗菌、抗炎、抗病毒等作用;有研究[14-15]表明山银花中绿原酸含量远高于金银花,而有机酸与金银花和山银花的抗菌、清热解毒作用有关,山银花的水提物具有抗病毒的作用。由于二者成分相近且在价格上相差较大,故现企业根据实际情况确定了现处方投料为“山银花”。
3.2 含量测定 原质量标准中含量测定下指标“绿原酸”成分不稳定,且专属性不强,无法对产品进行质量控制,故将之删去。从品种处方看,苦参为方中君药,苦参碱为目前公认的苦参药材活性成分,有免疫调节、抗病毒及抗肿瘤等作用。故建立以“苦参碱”为对照的含量测定方法对品种进行含量控制。
3.3 色谱条件选择
3.3.1 提取方法的选择 在预实验实验中,通过甲醇超声处理、氯仿超声处理,加水溶解后用三氯甲烷振摇提取、三氯甲烷超声处理后滤液过中性氧化铝柱,4种方法进行比较。甲醇超声获得的供试品溶液,色谱分离未见苦参碱色谱峰;样品经水溶解继用三氯甲烷萃取的供试品,在萃取过程中乳化现象严重,苦参碱色谱峰位置处有杂峰干扰且含量低;经三氯甲烷超声的两个供试品制备方法均可分离得到苦参碱,单位质量内过中性氧化铝柱制备的供试品溶液含量远高于单用三氯甲烷液超声处理的供试品溶液。故选用“2.2.3”项下方法制备供试品溶液。
3.3.2 流动相的选择 试验分别使用了C18柱、氨基柱;以液相系统①乙腈-0.1%磷酸溶液;②甲醇-乙腈-三乙胺-磷酸盐缓冲液(10∶17∶0.1∶73);③甲醇-磷酸盐缓冲液溶液(7∶93);④乙腈-0.02 mol/L磷酸二氢铵(33∶67);⑤乙腈-无水乙醇-3%磷酸溶液(80∶10∶10);⑥乙腈-异丙醇-3%磷酸溶液(80∶5∶15),进行分离样品中的苦参碱。结果表明,分离系统⑥乙腈-异丙醇-3%磷酸溶液(80∶5∶15)可以使样品中的苦参碱获得良好分离,故选择此流动相作为分离系统;试验中DAD检测器200~400 nm波长扫描,苦参碱最大吸收波长203 nm。
[LL]
4 结论
盐酸小檗碱及赤芍的原质量标准方法可行。原标准处方投料为“金银花”,现企业根据实际情况确定了现处方投料为“山银花”;所以用山银花的专属性成分灰毡毛忍冬皂苷乙做为鉴别点。通过本实验建立的银屑灵颗粒的薄层色谱法操作便捷,斑点清晰,专属性强。高效液相色谱法中选用最大吸收波长203 nm,选用最佳分离系统乙腈-异丙醇-3%磷酸溶液(80∶5∶15)。试验结果表明该方法稳定、可靠,可作为银屑灵颗粒的质量控制标准。
参考文献
[1]李志锋,李立红,李小静.针药合用对红皮病型银屑病患者外周血中T淋巴细胞亚群及TH1/TH2影响与免疫学机理分析[J].四川中医,2018,36(6):173-175.
[2]张晓彤,高云逸,宋坪.寻常型银屑病中医辨证特点概况及思考[J].中医杂志,2019,60(20):1732-1736.
[3]谢扬,向阳.中医动态思想防治寻常型银屑病的探讨[J].云南中医中药杂志,2020,41(6):11-13.
[4]谈依菱.基于数据挖掘研究当代名老中医治疗银屑病方药证治规律[D].广州:广州中医药大学,2017.
[5]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2020:1618.
[6]谭红声.十味鹅黄颗粒质量控制研究[D].南宁:广西中医药大学,2019.
[7]张锐,马天翔,顾志荣,等.消风止痒颗粒质量标准研究[J].甘肃中医药大学学报,2021,38(6):33-40.
[8]孙旭刚.金银花及莲花清瘟系列药物中山银花鉴别方法的研究[J].临床医药文献杂志,2018,5(104):181.
[9]笔雪艳,张清波,刘晓凤,等.七种常用中药制剂中金银花与山银花的应用初探[J].药物分析杂志,2010,30(11):2208-2211.
[10]季雪,李宪刚,崔韶婧,等.HPLC法测定喘嗽宁片中苦参碱的含量[J].药物研究,2019,19(85):152-155.
[11]杨健,郭书台,李凡,等.妇炎宁栓质量标准研究[J].现代中医药,2019,39(2):104-107.
[12]李振兴,单雪梅,袁万瑞,等.HPLC测定十味苦硝熏洗散中苦参碱和氧化苦参碱的含量[J].海峡药学,2020,32(11):58-61.
[13]赵丽艳,李明春,马燕,等.清咽颗粒的HPLC指纹图谱研究[J].热带医学杂志,2020,20(10):1288-1291.
[14]肖美凤,刘文龙,周晋,等.金银花和山银花研究现状及质量控制的关键问题[J].中草药,2018,49(20):4905-4911.
[15]张静,许保海,潘旭.金银花和山银花的鉴别要点研究[J].北京中医药,2019,38(1):73-76.
(收稿日期:2022-09-30 编辑:陶希睿)
