钛表面掺钴-钙磷涂层成血管作用的体外研究
2023-03-28瞿晓非戚孟春冯丽芳
瞿晓非,戚孟春,冯丽芳
华北理工大学口腔医学院,河北唐山(063210)
种植体在植入颌骨后,其与骨组织的结合不仅取决于成骨能力,还与其周围组织的成血管功能和血液供应有关[1]。优良的种植材料应同时具有诱导血管和新骨形成的功能,才会形成更好的骨结合(osseointegration),临床成功率也会更高[2]。钴(cobalt,Co)具有成本低、稳定性好等优点,常被用于骨修复材料[2];并且Co 能够促进血管生成基因的表达和管状结构生成[3],加速血管形成[4]。钙磷(Ca/P)涂层中的Ca 和P,作为成熟动物骨骼内的主要无机成分[5],在促成骨方面发挥巨大作用[6],但其成血管能力有限,因此有学者主张将其与其他元素复合来改变涂层材料的理化性能及生物特性[7]。本实验旨在研究Co 和Ca/P 复合涂层是否具有更好的促进血管生成作用,为新型钛种植体涂层制备提供新思路。
1 材料和方法
1.1 主要材料与器材
10 mm×10 mm×1 mm 纯钛钛片(杭州融天航瑞文科技有限公司,中国);乙酸钴(西陇化工,中国);醋酸钙(河南华瑞生物科技公司,中国);β-甘油磷酸钠(都莱试剂,中国);人脐静脉内皮细胞(human umbilical vein endothelial cells,HUVECs)(丰晖生物,中国);内皮细胞培养基(ACTT 公司,美国);胎牛血清(FBS)(BI,以色列);青霉素-链霉素双抗(Gibco,美国);Matrigel 基质胶(BD,美国);微弧氧化电源(SOYI-7003,安徽粤辉智能装备有限公司,中国);定时电动双叶搅拌器(JJ-1,江苏科技大仪器科技有限公司,中国);倒置相差荧光显微镜(1-70-S8F2,Olympus,日本);扫描电镜(GEMINI450,Zeiss,德国);能谱分析仪(JSM-F100,日本电子,日本)。
1.2 实验方法
1.2.1 钛片处理 将10 mm×10 mm×1 mm 的正方形钛片依次用500#、800#、1 000#、1 500#碳化硅砂纸依次抛光,然后依次在乙醇、去离子水中超声清洗15 min,室温干燥。
1.2.2 实验分组根据微弧氧化电解液加入元素成分不同,制备的涂层分为掺钴组(Co 组)、掺钴-钙磷组(Co-Ca/P 组)和纯钛片对照组(Ti 组)。
1.2.3 涂层制备 采用微弧氧化法制备涂层。以预处理的钛片为阳极,阴极选用不锈钢块,两极间距10 cm,两极完全浸没于电解液中;电动搅拌棒置于两极之间,以25 r/min 速度搅拌,使电解质溶液得以分布均匀。涂层制备采用交流电模式:正向电压500 V,反向电压150 V,正向电流3 A,反向电流1.5 A,正占空比为80%,反占空比50%,处理时间为10 min。Co-Ca/P 涂层所用电解液含乙酸钴、醋酸钙和β-甘油磷酸钠,按钴:(钴+钙)=1∶5的比例配制电解液,取β-甘油磷酸钠8.64 g,醋酸钙39.54 g,乙酸钴8.85 g 溶于500 mL 去离子水中;Co涂层电解液的制备为取乙酸钴8.85 g溶于500 mL去离子水中。涂层制备后,试件置于去离子水中超声震荡处理5 min,常温干燥。
1.2.4 涂层理化性质检测 应用场发射扫描电镜(scanning electron microscope,SEM)观察各组试件表面微观形貌;应用能谱分析仪(energy dispersive spectrometer,EDS)对钛试件表面元素进行分析,每组选择3 个试件测量。
1.2.5 细胞培养 人脐静脉内皮细胞(HUVECs)在内皮细胞培养基中37 ℃、5%CO2条件下培养。ECM 培养基成分为DMEM(930 μL/mL)+FBS(50 μL/mL)+内皮细胞生长因子(10 μL/mL)+青霉素/链霉素(10 μL/mL)。每2 d 换1 次培养基,待细胞融合达80%左右时,用胰蛋白酶消化传代;选用第3 代细胞进行试验。
1.2.6 浸提液制备 3 只离心管分别注入3 mL ECM 培养液,分别放入已制备好的Co、Co-Ca/P、Ti组试件,每组5 个大小为10 mm × 10 mm × 1 mm。浸泡3 d,制备相应的标准浸提液,用于体外血管生成实验。
1.2.7 体外微血管形成实验 将-20 ℃保存的基质胶在4 ℃冰箱里溶解过夜,在96 孔板内每孔加50 μL 基质胶,于37 ℃培养箱中放置30 min 至胶凝结。取第3 代生长良好的HUVECs 用浸提液制备成细胞悬液,按6 × 105个/mL 均匀接种于基质胶上,每孔加入0.5 mL 细胞悬液,每组设置3 个孔。培养4、8 h 后倒置相差显微镜下观察微血管形成情况,每孔随机选取6 个视野进行拍照,照片使用Image J(v1.8.0.172)图像处理软件进行分析,比较3 组微血管环数(血管管壁围绕形成圆环的个数)和节点数(2 个或2 个以上血管管壁交叉形成的交点个数)差异。
1.3 统计学分析
采用SPSS26.0 软件对数据进行统计学分析。定量资料使用均数±标准差表示,对3 组微血管环及节点数进行单因素方差分析,检验水准为α=0.05。
2 结 果
2.1 涂层大体观察
Co 组显示为深灰色涂层,Co-Ca/P 组显示为淡粉色涂层,Ti 组则显示出纯钛片的原本金属色泽(图1)。

Figure 1 Obervation of coatings on titanium surfaces in three groups图1 三组钛表面涂层大体观察
2.2 试件微观形貌观察
经微弧氧化处理的Co 组、Co-Ca/P 组涂层表面除孔隙外,出现了许多不规则晶体沉积,晶体直径大多<2 μm;晶体沉积间有少量微孔,数目较少且分散,考虑是微弧氧化处理时晶体沉积覆盖所致。与Co 组比较,Co-Ca/P 组沉积的晶体较多且分布均匀;而未经微弧氧化的Ti 组则只观察到打磨留下的划痕,未见到微孔及晶体沉积(图2)。

Figure 2 Micromorphology of coatings on titanium surfaces under scanning electron microscope observation图2 扫描电镜下观察钛表面涂层表面微观形态
2.3 涂层元素能谱分析
EDS 分析结果显示(图3,表1),Co 组元素检测显示只有Co、Ti 和O 元素,说明Co 被掺入到涂层表面;Co-Ca/P 组除了Co、Ti、O,还有Ca、P 等元素,说明Co 和Ca、P 元素一起被掺入到涂层中。Ti 组显示只有Ti 和O 元素,说明无三种元素掺入。

Figure 3 Element analysis of three groups coatings on titanium surfaces by energy dispersive spectrometer图3 三组钛表面涂层元素能谱分析图
表1 钛表面涂层表面化学元素成分及含量的能谱分析(n=3)Table 1 Element composition and content of coatings on titanium surfaces analysized by energy dispersive spectrometer(n=3)mass%,±s
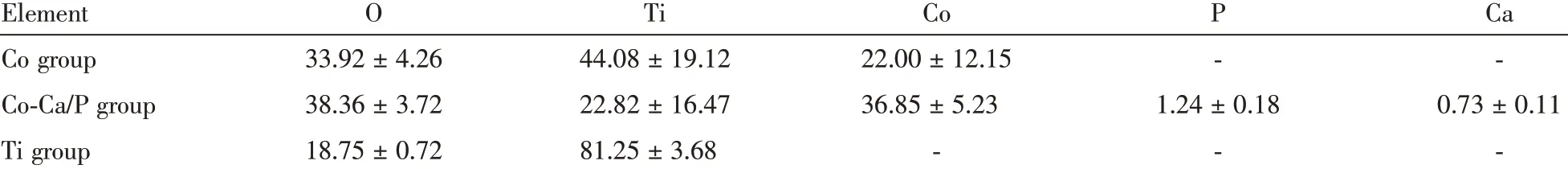
表1 钛表面涂层表面化学元素成分及含量的能谱分析(n=3)Table 1 Element composition and content of coatings on titanium surfaces analysized by energy dispersive spectrometer(n=3)mass%,±s
Co group:cobalt-loaded group;Co-Ca/P group:cobalt and calcium-phosphorus group;Ti group:untreated pure titanium group
Ca Element O Ti Co P-0.73±0.11-Co group Co-Ca/P group Ti group 33.92±4.26 38.36±3.72 18.75±0.72 44.08±19.12 22.82±16.47 81.25±3.68 22.00±12.15 36.85±5.23--1.24±0.18-
2.4 体外微血管生成
利用体外微血管生成实验来检验Co-Ca/P 涂层的促血管生成能力。结果显示,细胞培养4 h 后,三组涂层表面均出现了管腔样结构,其中Co-Ca/P 组微血管环数和节点数最高,其次为Co 组,而Ti 组最低(P<0.05),说明Co 具有促进微血管生成的能力,而Ca、P 元素的加入会进一步增强Co 的促血管生成作用。
细胞培养8 h 后,三组涂层表面生成的微血管较4 h 时更多更粗,且有更多血管环和节点。三组比较,Co-Ca/P 组血管环数及节点数仍然最高,其次为Co 组,而Ti 组最少(P<0.05);进一步证明了Co的促微血管生成作用及Co、Ca、P 三种元素联合应用进一步促进微血管生成的效果(图4)。
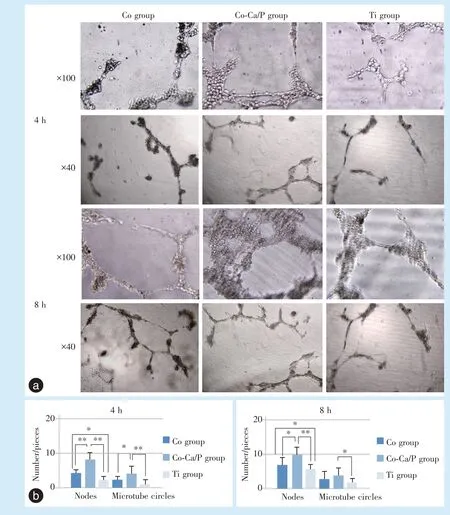
Figure 4 Microangiogenesis of different coatings on titanium surfacesin vitro图4 钛表面不同涂层的体外微血管生成情况
3 讨 论
钛种植体植入体内后,其周围颌骨组织良好的成骨能力是种植体骨结合成功的关键;然而,这些过程离不开局部骨组织良好的血液供应;因而,种植体植入后局部骨组织的重新血管化或新血管再生成为种植体骨结合的必备前提,对提高种植体成功率具有重要意义。
种植体植入后,骨组织局部微环境中血管内皮细胞可以在各种信号刺激下,发生增殖、迁移、微血管重构和形成[8],从而为新生骨组织提供血液和养分;同时,骨微环境中基质细胞、成骨细胞及血管内皮细胞自身还可分泌血管内皮生长因子(vascular endothelial growth factor,VEGF)和各种细胞因子,作为信号蛋白调控微血管生成[9],加快新骨形成,促进种植体骨结合[10]。除上述促血管生长因子及细胞因子外,一些金属元素也被证实具有促微血管生成的作用,如镁、铜、钴、锌等[8,11-14];因而在种植体表面涂层中引入适合的金属元素,达成促进种植体周围微血管生成,加速新骨形成,促进种植体骨结合的目的;该策略已成为研发新型高生物活性涂层种植体的新思路。本研究正是基于该思路,首次通过微弧氧化方法将具有成血管能力的Co 与Ca、P 元素结合,制备掺Co-Ca/P 复合涂层,以证实该复合涂层促进HUVECs 体外微血管生成的能力。扫描电镜及能谱分析,均证实三种元素被成功掺入Co-Ca/P 复合涂层,涂层表面具有含三种元素的晶体。
Co 良好的促进微血管生成能力已被许多既往研究证实[2-3,15]。Zhao 等[2]利用Co 支架体外诱导血管形成,证明掺Co 浸提液可以促进HUVECs 增殖,并形成血管样结构。Co 还可通过模拟缺氧条件来促进血管生成[16]。Co2+作为脯氨酰羟基化抑制剂,可抑制低氧诱导因子-1α(hypoxia inducible factor-1α,HIF-1α)降解并使其稳定;HIF-1α 可上调血管生成基因VEGF 的表达[17],从而有利于血管的生成。在血管生成信号的刺激下,HUVECs 增殖、迁移、分化,多个信号通路调节这一过程,进而加速血管生成[15]。本研究发现,掺Co 涂层较纯Ti 试件组具有更好的微血管生成能力,进一步证实了Co的促血管生成作用。既往研究只单独验证了Co 对成血管的作用;本研究在证实Co 促微血管形成能力的同时,在掺Co 涂层中进一步引入了Ca、P 元素,以期进一步增强涂层的生物学效应。
既往研究发现,Ca/P 涂层释放的Ca 和P 离子同样具有促进血管再生的作用[18]。Ca、P 元素是生物体硬组织中无机成分的重要组成部分,其生物活性与骨诱导性优异,多用于骨组织修复的表面涂层中。但该涂层韧性低、脆性大,限制了其临床应用[19]。戴文捷[20]通过溶胶-凝胶法和仿生矿化法在钛合金基体表面制备锶镁离子掺杂钙磷涂层,发现同时增强了成骨和成血管生物活性,为种植体改性和骨整合改善提供了参考。羟基磷灰石(hydroxyapatite,HA)是人体骨骼内最常见的钙磷化合物,是一种能促进体内成骨、提高组织相容性的良好涂层[21]。作为骨无机质的成分之一,HA 能诱导骨髓间充质干细胞(bone mesenchymal stem cells,BMSCs)向成骨细胞分化,极大地促进种植体骨结合[22]。骨折的修复是一个再生过程,骨生长支架在血管再生和成骨中发挥巨大作用,它可以通过拓扑结构和微观尺度差来实现细胞黏附及血管再生,从而实现骨生成[23]。血管再生促进骨生成,反之良好的骨再生促进骨内血管新生,如此循环往复,更好达到成骨的作用[24-26]。尹先珍[25]通过层层自组装法在携载抑炎因子白细胞介素-4(interleukin-4,IL-4)的二氧化钛纳米管表面制备海藻酸钠/壳聚糖自组装膜,显著促进了内皮细胞的黏附与生长,可诱导生成较多血管,IL-4 控释体系具有良好骨免疫调节性能,通过其表面特性与巨噬细胞共同作用,显示出优异的促进体内外血管生成和修复骨组织缺损的作用[27-29]。王青等[24]发现利用化学沉积法制备的含有Ca/P 涂层的铝合金支架能够在体内外促进血管新生和修复骨缺损。龙智生等[28]发现HA/CS(chitosan)微管结构在成血管与成骨方面具有显著的优良效果。Suo 等[30]利用电泳沉积法制备HA/CS/GO(graphene oxide)复合涂层,证明该涂层可以促进BMSCs 的生长与分化,并且促进了体内种植体骨结合的能力。近年来国内外有关钛种植体Ca/P 涂层促微血管生成的研究较少,它们与Co 元素的联合应用更未见报道。
根据本研究得出的结论:Ca/P 与Co 联合制备的微弧氧化涂层,微血管环及血管节点数均显著高于单独掺Co 涂层组,证实体外三种元素联合应用在涂层中可进一步增强微血管生成能力,从而进一步提高钛金属涂层的生物活性。
综上所述,本研究通过微弧氧化法在钛金属表面成功制备了掺Co-Ca/P 复合涂层;该涂层具有独特的微观形貌和沉积的晶体,在体外比纯钛试件及单独掺Co 涂层具有更好的成血管能力,为新型高生物活性钛种植体涂层的研发提供了新思路。
【Author contributions】Qu XF designed the study, collected and processed the data, wrote the article.Qi MC revised the article and designed the study.Feng LF revised the article.All authors read and approved the final manuscript as submitted.
