Fe3O4/GO/ZnO材料的制备及其对盐酸土霉素吸附研究
2023-02-27龙星宇王志敏张江群韦万丽肖明春李胜霞强玲芳
龙星宇,王志敏,张江群,韦万丽,肖明春,李胜霞,强玲芳
(贵州师范大学 化学与材料科学学院,贵州 贵阳 550025)
0 引言
盐酸土霉素(Oxytetracycline hydrochloride,OTC-HCl)属于较为常见的四环素类抗生素,具有高效、价格便宜、抗菌谱广、毒副作用较小等优点,被大量使用于兽药(用以促进动物生长发育或者降低动物的发病率)。但却存有在生物体内不能被完全吸收唯有通过代谢排出体外[1]的情况。而进入到环境中的残余抗生素,由于难以被清除,同时还极易产生抗性基因的出现与传播,大大增加了对环境和人类的风险[2],因此对盐酸土霉素的吸附去除成了社会关注的焦点。展海银等[3]对环境中四环素类抗生素污染治理方法进行了较为系统的阐述。目前,对盐酸土霉素的去除常采用生物降解[4],化学法[5],芬顿处理[6-8],臭氧处理[9]和吸附法[10-11]等,其中吸附法因操作较为简单、吸附效果好、成本廉价,且不易产生二次污染物成为了最有效的方法之一。近年来,壳聚糖[12]、改性碳[13]、磁性活性炭[14]、水凝胶[15]等材料被广泛应用于吸附废水中四环素类抗生素的研究中[16]。
磁性纳米材料也因具有较大的比表面积、易于分离以及优良的吸附能力受到了极大的关注,其研究范围涉及环境中重金属离子的去除[17-18]及有机物的吸附[19-21]。石墨烯作为近几年来颇受关注的新型纳米材料,不仅比表面积较大、吸附性能优异,还可通过Π-Π相互作用对环境中的有机物等进行吸附以达到去除,故在环境治理中受到了研究者们的青睐[22]。但石墨烯本身却属于超轻型材料,具有高表面能,在水中容易形成分散体系,吸附过后难以从悬浮液中进行分离再利用且极大可能产生二次污染。为此,不少研究者通过采用各种方法对石墨烯进行改造以克服其缺点[23-24]。本实验拟通过结合Fe3O4与石墨烯制备出具有磁性的石墨烯复合材料,该材料除了具有优异的吸附性能外还具有较高的超顺磁性,并且通过进行快捷的磁分离技术被反复使用,可增加材料的使用率。
ZnO在处理环境中的抗生素上同样具有极大的研究价值,可用于四环素类抗生素的吸附[18],具有较高的稳定性、较强的光催化作用以及无毒廉价等优点。罗灵芝等[25]以“一锅法”得到γ-Fe3O4/ZnO材料,对材料进行表征以及优化反应的各种条件后,将其作为光催化剂对水中的四环素进行降解。因ZnO的表面有较为稳定的Fe3O4,增加了原有ZnO的光吸收宽度,对四环素的光催化降解率可达到97.2%,降解性能优异且能很好地去除四环素。于晓彩等[26]同样用制备材料纯度较高的化学沉淀法制备出纳米ZnO,对该纳米材料进行表征,优化材料的煅烧温度、时间以及用量等条件后,将材料应用于养殖场中盐酸土霉素的去除研究,基于各种优化后的条件,盐酸土霉素在废水中的去除率为75.45%且未产生二次污染物,具有较高的研究价值。单艺伟等[27]采用以纳米纤维素为辅,Zn(NO3)2、CNF为原料制备得到C-ZnO材料,主要考察材料制备时水热温度以及CNF的用量对四环素去除率的影响,在该实验条件下得到的光催化剂,光照2 h后,对四环素可达到96.1%的去除率,去除效果优异。
本研究将通过采用制备材料纯度较高的溶剂热法制备Fe3O4材料,并以离子强度法对Fe3O4进行修饰得到Fe3O4/GO复合材料,最终通过化学共沉淀法制备Fe3O4/GO/ZnO磁性纳米材料。利用Fe3O4方便磁分离的特点,加上GO较强的吸附能力与ZnO的强氧化性,形成吸附力强、便于操作的磁性纳米材料,将其作为纳米吸附剂用于盐酸土霉素的吸附研究中。
1 实验材料与方法
1.1 实验仪器与试剂
1.1.1 实验仪器
紫外可见分光光度计(UV-1102)、超声波清洗器(KQ3200DE)、电子天平(FA2004,精确至0.1 mg)、集热式恒温加热磁力搅拌器(DF-101S)、精密pH计(PHS-3C)、涡旋振荡器(SCILOGEX MX-S)、电热鼓风干燥箱、不锈钢反应釜、移液管。
1.1.2 实验药品及试剂
六水合三氯化铁、氧化石墨烯、盐酸土霉素可溶性粉、氢氧化钠、盐酸、乙二醇、硫酸锌、尿素、无水醋酸钠、无水乙醇。
1.2 Fe3O4/GO/ZnO复合材料的制备
1.2.1 Fe3O4的制备
Fe3O4材料采用溶剂热法制备,以FeCl3·6H2O作为原料,参照文献[27],做一些修改,具体操作为:干燥的烧杯内加入80 mL乙二醇,称取10.8 g 的FeCl3·6H2O黄色固体溶于乙二醇中,溶液进行超声分散至固体完全溶解后再称取无水CH3COONa 6.5 g 加入到溶液中继续进行超声一段时间,超声结束后将溶液转移到不锈钢反应釜中,鼓风干燥箱的温度调节为200 ℃,材料在该温度下进行反应8 h。冷却至常温的反应液移入至干燥的烧杯中进行磁分离,弃尽上清液,剩余在烧杯底部的产物用蒸馏水和无水乙醇作为清洗剂分别洗涤3次,洗涤过程中均采用磁铁进行固液分离。置于60 ℃烘箱中干燥,即为Fe3O4磁性材料。
1.2.2 Fe3O4/GO的制备
参照文献[28-30],Fe3O4/GO材料制备的具体操作为:配置1 g/L的氧化石墨烯溶液(称取0.1 g氧化石墨烯GO固体分散在100 mL蒸馏水中,超声分散使GO均匀分布于其中)。取干燥的烧杯2只,分别加入1 mol/L的CH3COONa溶液5 mL,将一定量的 GO溶液加入到其中一只烧杯中,另一只烧杯加入0.2 g的 Fe3O4材料,对两烧杯中溶液进行超声处理使CH3COONa溶液中均匀分布有Fe3O4、GO溶液。再混合两烧杯中的溶液继续超声分散1 h后采用磁铁进行产物的分离,以蒸馏水和无水乙醇作为清洗剂各反复洗涤3次,洗涤过后的产物转入烧杯内,置于鼓风干燥箱内60 ℃下蒸发表面的水分,可得到黑色Fe3O4/GO材料。
1.2.3 Fe3O4/GO/ZnO的制备
参照文献[28,31-32],方法稍作修改。通过机械搅拌加热的方法制备Fe3O4/GO/ZnO材料。具体为:将0.12 g的Fe3O4/GO固体加入到400 mL乙醇溶液中(蒸馏水与乙醇体积之比为1∶1)进行超声分散,称取6 g尿素和0.046 8 g ZnSO4·7H2O加入至分散液中,超声混合后在温度为90 ℃的磁力搅拌器中搅拌2 h。静置冷却至室温后进行磁分离,将所得产物进行数次的洗涤后放置于烘箱内做烘干处理。烘干后的产物即为Fe3O4/GO/ZnO磁性复合材料,将材料研磨成粉状。
1.3 盐酸土霉素溶液标准曲线的绘制
称取1.000 0 g盐酸土霉素可溶性粉于100 mL容量瓶中,用去离子水定容至容量瓶刻度线。再通过逐级稀释精确配置出浓度为6 mg/L、9 mg/L、12 mg/L、15 mg/L、18 mg/L的盐酸土霉素标准溶液,调节紫外分光光度计波长为380 nm,在该波长处测定对应浓度下盐酸土霉素的吸光度值,构建盐酸土霉素的标准曲线方程。由图1可知,盐酸土霉素溶液在浓度范围为6~18 mg/L内呈现出较好的线性关系。经计算可得到相关系数R2=0.999 7,标准曲线方程表示为A=1.292c+0.004。表达式中A表示吸光度,c表示OTC-HCl浓度。
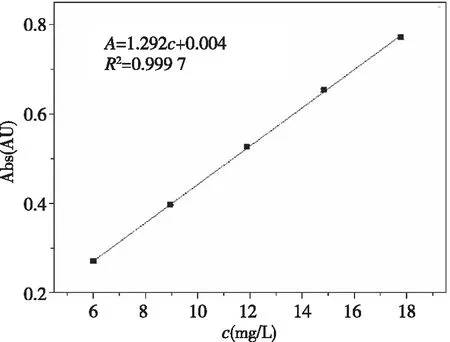
图1 盐酸土霉素的标准曲线Fig.1 Standard curve of oxytetracycline hydrochloride
1.4 Fe3O4/GO/ZnO对盐酸土霉素溶液吸附-脱附研究
1.4.1 吸附量的计算
将一定量(m)的Fe3O4/GO/ZnO纳米材料加入到盛有一定体积(V)并已知浓度(C0)的盐酸土霉素溶液PE管中,室温下涡旋震荡一定时间,静置片刻后,进行磁分离,取PE管中的上清液做吸光度值的测定并计算对应的盐酸土霉素浓度(C1),可对比得出吸附前与吸附后盐酸土霉素浓度间的差异,以此差异计算出该复合材料对盐酸土霉素的吸附量值。公式为:吸附量(mg/g)=(C0-C1)·V/m。其中C0表示溶液的起始浓度,C1表示吸附后溶液浓度,V表示溶液体积,实验中为15 mL,m为吸附剂的质量。
1.4.2 解脱率的计算
在完成影响吸附剂对盐酸土霉素吸附量的因素实验后,取最佳用量的Fe3O4/GO/ZnO加入到浓度为(C0)的盐酸土霉素溶液中,室温下充分震荡一段时间后进行磁分离,弃尽上清液,剩余材料中加入一定量的NaOH解脱剂,超声5 min使盐酸土霉素被充分解脱后测定上清液吸光度,并计算对应的盐酸土霉素浓度(C2),根据解脱前后盐酸土霉素浓度的差异,从而计算材料对盐酸土霉素的解脱率(%)。具体计算公式为:解脱率(%)=[C2/C0]×100%。
2 实验结果与分析
2.1 最佳初始浓度的选择
配置浓度为12 mg/L、15 mg/L、18 mg/L、21 mg/L、24 mg/L、27 mg/L的盐酸土霉素于6支PE管中,各向其中加入0.003 2 g左右的Fe3O4/GO/ZnO复合纳米材料,常温下在涡旋振荡器中震荡一定时间后,外加碳场磁分离,调节分光光度计波长为380 nm,在该波长处测定上清液吸光度值,并计算对应的吸附量后进行作图。结果如图2所示,材料对盐酸土霉素的吸附量随着浓度的增加逐渐发生变化,呈现先增加后趋于平缓的趋势。呈现该趋势的主要原因为,当盐酸土霉素浓度较低时,吸附剂拥有较多的吸附位点,容易结合盐酸土霉素,随着浓度不断增高吸附量也随之增大,当吸附剂的吸附位点达到饱和时,吸附也趋于饱和状态,即使增加盐酸土霉素浓度,吸附量也不会有太大的波动。图2中当盐酸土霉素浓度处于18 mg/L时吸附量达到最高点并趋于相对稳定状态。故在该实验条件下,选择浓度为18 mg/L作为盐酸土霉素的最佳初始浓度。
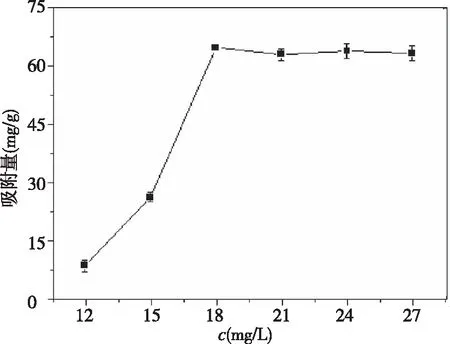
图2 盐酸土霉素初始浓度对吸附的影响Fig.2 Effect of initial concentration of oxytetracycline hydrochloride on adsorption
2.2 Fe3O4/GO/ZnO材料用量对吸附的影响
分别移取18 mg/L盐酸土霉素标准液置于6支PE管中,向其中各加入0.002 2 g、0.003 2 g、0.004 2 g、0.005 3 g、0.006 4 g、0.007 2 g的Fe3O4/GO/ZnO复合材料,室温下震荡后进行磁分离,于比色皿中收集上清液,同样调节吸光度为380 nm,测定上清液的吸光度值。计算出相应用量的磁性材料对盐酸土霉素的吸附量并绘图。由图3可得,当Fe3O4/GO/ZnO复合纳米材料用量为0.003 2 g时,该磁性复合材料对盐酸土霉素有最大吸附量,吸附量为37.97 mg/g,故选择0.003 2 g材料作为实验最佳用量。
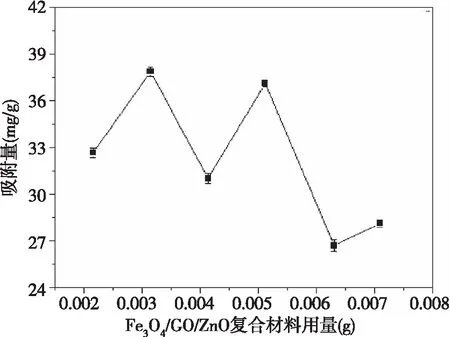
图3 Fe3O4/GO/ZnO材料用量对吸附的影响Fig.3 Effect of Fe3O4/GO/ZnO material amount on adsorption
2.3 盐酸土霉素溶液的起始pH对吸附的影响
用混合磷酸盐、邻苯二甲酸氢钾、硼酸钠调节浓度为18 mg/L的盐酸土霉素初始pH分别为2.04、3.03、5.05、6.04、7.04、8.03、9.04,在不同的初始pH下,均加入用量为0.003 2 g的吸附剂,于常温条件下震荡30 min后考察吸附效果。计算对应pH下材料对盐酸土霉素的吸附量并绘图。结果如图4所示,随着pH的逐渐增大,对盐酸土霉素的吸附量呈现出不同趋势的变化,但当pH=3.03时,材料对盐酸土霉素的吸附量达到最高,为63.87 mg/g。主要原因为Fe3O4/GO/ZnO的零点电位约为7.5,当溶液的pH低于7.5时,Fe3O4/GO/ZnO吸附剂带正电。而土霉素属于两性物质,本身具有氨基、羧基等极性基团,具有两级解离常数[33],pH低于3.2时,主要以正离子状态存在,当pH处于3.2~7.7时,以两性离子存在,pH高于7.7时,以负离子形式存在。故当pH处于3.2~7.5时,吸附剂与吸附质之间虽发生静电引力作用,但因盐酸土霉素在酸性条件下比较稳定,溶液的碱性逐渐增加,使得盐酸土霉素稳定性较弱。pH高于7.5时,材料与盐酸土霉素间发生静电排斥作用且在强碱性条件下,吸附剂被解析,难以达到吸附效果。依据该实验结果,在后续实验中,均采用盐酸土霉素pH为3左右作为最优pH。
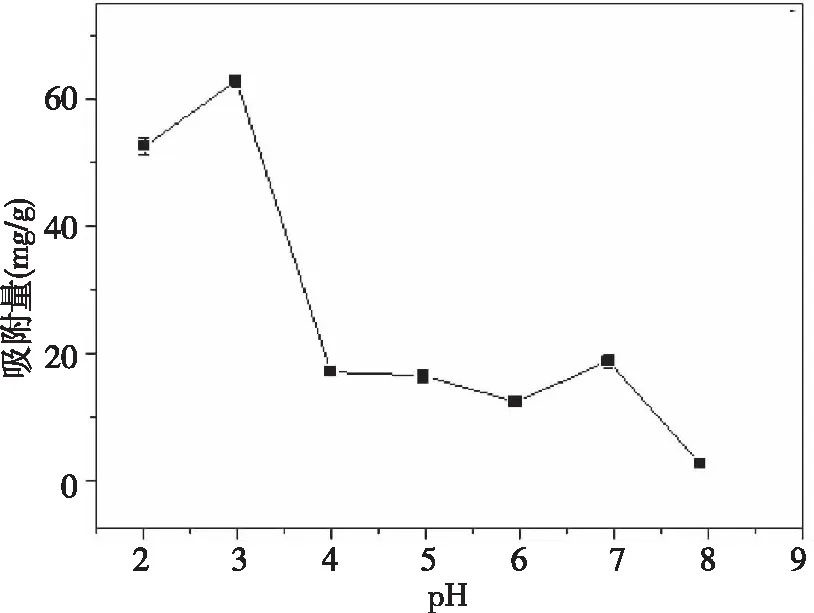
图4 盐酸土霉素起始pH对吸附的影响Fig.4 Effect of initial pH of oxytetracycline hydrochloride on adsorption
2.4 震荡时间的影响
考察震荡时间,Fe3O4/GO/ZnO材料对盐酸土霉素吸附效果的影响。吸附剂材料的用量为0.003 0~0.003 4 g,调节盐酸土霉素pH为3左右。具体为:取7支干燥的PE管,向其中加入浓度为18 mg/L、pH=3左右的盐酸土霉素溶液15 mL,再加入0.003 2 g吸附剂,室温下进行震荡,震荡时间为5 min、10 min、20 min、30 min、60 min、90 min、120 min,震荡后于波长380 nm处测定吸光度值,依据公式计算吸附量并绘图。如图5所示,伴随时间的增加,材料Fe3O4/GO/ZnO对盐酸土霉素的吸附效果也逐渐变强,当震荡时间为60 min时,该磁性复合材料对盐酸土霉素有最大吸附量,吸附量可达62.73 mg/g,本着节约时间,吸附量大的原则,选取涡旋震荡时间为60 min作为最佳震荡时间。
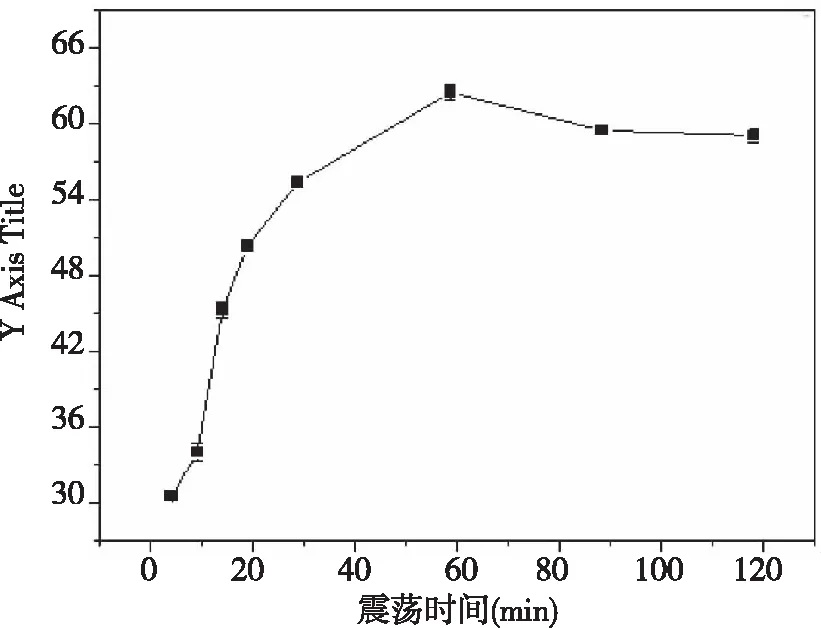
图5 震荡时间对吸附的影响Fig.5 Effect of oscillating time on adsorption
2.5 解脱剂的选择
合适的解脱剂能够有效去除废水中的盐酸土霉素,而吸附剂的循环再利用是可以提高吸附剂效率的[34-35]。本实验采用NaOH作为解脱剂,考察不同浓度NaOH相应的解脱率。取5支干燥的PE管,向其中各加入15 mL 27 mg/L的盐酸土霉素标液,分别取0.003 2 g左右的材料加入其中,常温下震荡5 min后进行磁分离,再次调节仪器波长为380 nm,测定上清液吸光度值。弃尽上清液后的PE管中各加入15 mL 0.01 mol/L、0.1 mol/L、0.5 mol/L、1 mol/L NaOH以及去离子水,再次震荡5 min后测吸光度,依据计算所得的吸附量作图。由图6所示,0.01 mol/L NaOH对吸附剂具有较好的解脱率,解脱率可达80%以上,故选择浓度为0.01 mol/L NaOH作为解脱剂。

图6 NaOH浓度对解脱的影响Fig.6 Effect of NaOH concentration on extrication
2.6 Fe3O4/GO/ZnO材料回收再循环性能研究
实验采用0.01 mol/L NaOH作为解脱剂对材料吸附盐酸土霉素后进行解脱,具体操作为:向 3支干燥的PE管中加入浓度为18 mg/L、pH=3左右的盐酸土霉素溶液15 mL以及0.003 2 g左右的吸附剂,室温下震荡60 min后测上清液吸光度。采用解脱剂浓度为0.01 mol/L NaOH进行数次的洗涤、磁分离后,将其放入鼓风干燥箱中烘干,再次基于最优条件对盐酸土霉素进行吸附实验。实验共进行5次再生利用操作,计算每次循环过后以材料对盐酸土霉素的吸附量,以其为纵坐标并绘图。如图7所示,吸附剂再生循环5次后,前3次Fe3O4/GO/ZnO磁性纳米材料对盐酸土霉素的吸附量在150 mg/g左右,后两次有减少趋势。故该材料的稳定性尚可,可以进行回收循环利用。
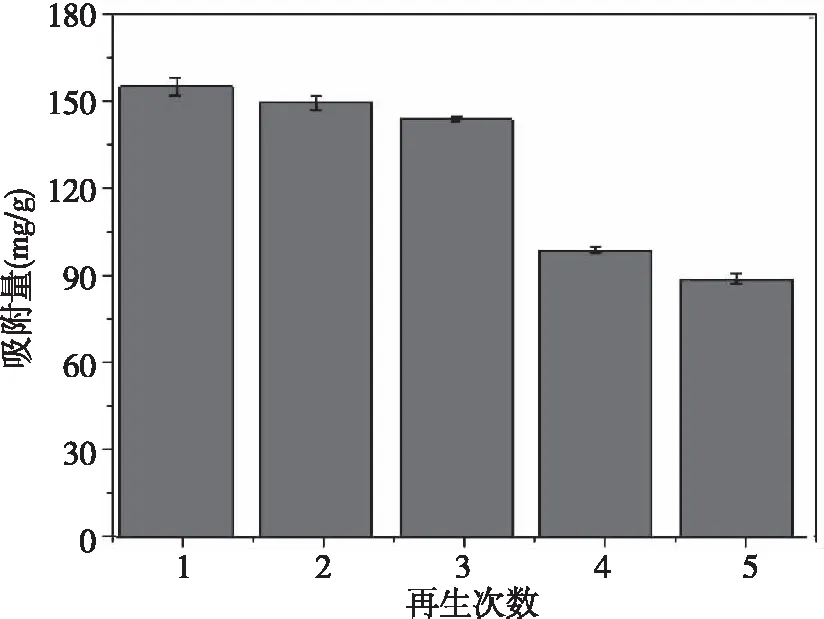
图7 Fe3O4/GO/ZnO材料的回收循环性能研究Fig.7 Study on recycling properties of Fe3O4/GO/ZnO materials
2.7 最大饱和吸附量
材料对盐酸土霉素溶液的最大饱和吸附容量是利用改变Fe3O4/GO/ZnO的用量来进行衡量的。基于本实验的各种优化条件,取材料分为5组(0.002 0 g、0.003 3 g、0.004 3 g、0.005 2 g、0.006 1 g),对浓度(12 mg/L、15 mg/L、18 mg/L、21 mg/L、24 mg/L、27 mg/L、30 mg/L、33 mg/L、36 mg/L)的盐酸土霉素分别进行吸附。吸附过后,磁分离并收集上清液于分光光度计内测定吸光度值,计算对应的吸附量,找出每组中的最大饱和吸附量,以其作为纵坐标进行绘图(图8)。最大饱和吸附量计算公式为qmax=(C0-Ct)·V/m,根据数据处理可得出qmax=191.93 mg/g。
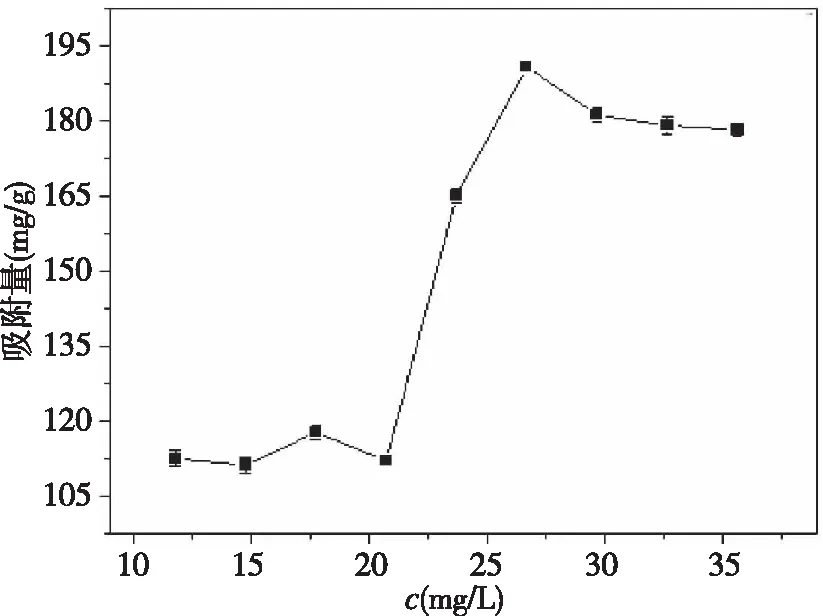
图8 最大饱和吸附量(qmax)Fig.8 Maximum saturated adsorption capacity (qmax)
3 结论
1)本研究以FeCl3·6H2O作为初始原料,先采用溶剂热法可制备得到Fe3O4,通过离子强度法对Fe3O4进行修饰得到Fe3O4/GO磁性复合材料,最后以化学共沉淀法制备得到Fe3O4/GO/ZnO磁性纳米材料。
2)将制备的Fe3O4/GO/ZnO磁性材料用于盐酸土霉素的吸附研究。
3)对实验中影响材料对盐酸土霉素吸附量的诸多因素进行优化,当盐酸土霉素初始浓度为18 mg/L、溶液的起始pH为3、材料用量为0.003 2 g、震荡时间为60 min时,吸附剂对溶液有着较大的吸附量,最大饱和吸附量为191.93 mg/g。
4)最优条件下选择0.01 mol/L NaOH作为解脱剂,对材料进行5次再生吸附循环过程后,可检测Fe3O4/GO/ZnO的循环再生利用性能。由结果可知材料对盐酸土霉素的吸附量前3次仍旧可达150 mg/g,吸附性与稳定性较好。故Fe3O4/GO/ZnO 纳米材料作为吸附剂具有良好的吸附性能,对盐酸土霉素也具有优异的吸附去除功能。
