基于指纹图谱研究金樱子肉饮片、标准汤剂、配方颗粒相关性
2023-02-20张辉许树萍黄凯伟赵伟志郑晓英谭沛
张辉,许树萍,黄凯伟,赵伟志,郑晓英,谭沛
(1.华润三九医药股份有限公司,广东深圳 518110;2.华润三九现代中药制药有限公司,广东惠州 516000)
金樱子为蔷薇科植物金樱子Rosa laevigataMichx.的干燥成熟果实,为花托发育而成的假果,呈倒卵形,切开后,花托壁厚,内有多数坚硬的小瘦果,内壁及瘦果均有淡黄色绒毛[1]。金樱子最早载于南北朝《雷公炮炙论》,在历代本草与古籍文献中,除南北朝为同名异物外,此后多以金樱子为正名,并记载有别名。金樱子味酸涩,性温、平,归脾、肾、肺、膀胱经,具有滋补益气的保健功效[2]。现代研究表明,金樱子含有黄酮、三萜、鞣质、苯丙素、甾体、多糖类等化学成分;具有收涩止泻、免疫调节、抗氧化、抗菌抗炎、抗肿瘤、保肝护肾、降血脂、保护神经等生物活性;可用于治疗糖尿病肾病、慢性肾炎蛋白尿、遗精遗尿、特发性血小板减小性紫癜、慢性顽固性腹泻等疾病[3]。金樱子肉的炮制工艺为:取净金樱子,略浸,润透,纵切两瓣,除去毛、核,干燥,制得金樱子肉饮片。《中国药典》明确规定金樱子的饮片为金樱子肉,而非金樱子,目前国内临床使用以及文献报道上,对金樱子药材的饮片认识存在不足,使用上存在错误的情况[1]。本研究将首次对金樱子肉饮片、标准汤剂、配方颗粒指纹图谱进行研究。
目前,对金樱子药材和配方颗粒指标成分含量的相关质量控制研究报道较多,而对金樱子肉的相关研究报告较少。中药标准汤剂是在中医药理论的指导下,作为衡量中药配方颗粒是否与临床汤剂基本一致的物质基础。金樱子肉配方颗粒是以金樱子肉饮片为原料,经过提取、分离、浓缩、干燥、制粒、包装等生产工艺加工制成供中医临床配方用的颗粒。本研究采用高效液相色谱法建立了金樱子肉配方颗粒的指纹图谱,并考察分析金樱子肉饮片、标准汤剂、配方颗粒之间的相关性和差异性,进而有效提高金樱子肉配方颗粒的质控水平和整体质量,也为金樱子肉配方颗粒替代传统饮片的可行性研究提供参考。
1 仪器与试药
1.1 仪器
Waters(Alliance2695 型)高效液相色谱仪;XS204、XS205、XSE205 万分之一天平(瑞士梅特勒)、ME36S 百万分之一天平(瑞士梅特勒)、超声仪(上海科导超声仪器有限公司)、水浴锅。
1.2 试药
没食子酸(批号:110831-201605,纯度90.8%)、鞣花酸(批号:111959-201602,纯度89.3%)对照品、金樱子对照药材(批号:121047-201204)均购于中国食品药品检定研究院;鞣花酸-4-O-α-L-阿拉伯糖苷(批号:22012502)购于上海诗丹德标准技术服务有限公司;槲皮素-3-O-β-D-吡喃葡糖苷酸(批号:080097-202111)购于上海鸿永生物科技有限公司;乙腈为色谱纯,水为超纯水;其他试剂均为分析纯。
15 批金樱子药材产地分别来自安徽省(A1-A3)、江西省(A4-A6)、湖南省(A7-A9)、贵州省(A10-A12)、广东省(A13-A15),经安徽中医药大学的刘守金教授鉴定为金樱子Rosa laevigataMichx.的干燥成熟果实。15批金樱子肉饮片(样品编号B1-B15)严格按照2020 年版《中国药典》一部金樱子项下饮片炮制规定进行炮制[1]:取净金樱子,略浸,润透,纵切两瓣,除去毛、核,干燥,制得金樱子肉饮片。15 批金樱子肉饮片标准汤剂(样品编号C1-C15)严格按照《医疗机构中药煎药室管理规范》和《中药配方颗粒质量控制与标准制定技术要求》中煎药方法进行制备:取金樱子肉饮片,提取制得标准汤剂,为了标准汤剂的长期储存,根据《中药配方颗粒质量控制与标准制定技术要求》,进行低温减压浓缩,冷冻干燥,得金樱子肉饮片标准汤剂冻干粉。15 批金樱子肉配方颗粒(样品编号为D1-D15)由水提取,浓缩、干燥、制粒等步骤得到。
2 方法与结果
2.1 色谱条件
以十八烷基硅烷键合硅胶为填充剂色谱柱:Waters AtlantisTMT3(250 mm×4.6 mm,5 µm);以乙腈为流动相A,以0.1%磷酸溶液为流动相B,进行梯度洗脱(0 min:3%A-97%B;35 min:25%A-75%B;40 min:40%A-60%B;检测波长为260 nm;柱温30 ℃);流速为1.0 mL/min;进样量10 μL。
2.2 参照物溶液的制备
取金樱子对照药材约2.0 g,置具塞锥形瓶中,加入水50 mL,加热回流45 min,放冷,滤过,滤液蒸干,加入70%甲醇25 mL,密塞,超声处理(功率300 W,频率40 kHz)45 min,放冷,摇匀,滤过,取续滤液,即得对照药材参照物溶液。取没食子酸、鞣花酸-4-Oα-L-阿拉伯糖苷、鞣花酸、槲皮素-3-O-β-D-吡喃葡糖苷酸对照品适量,精密称定,加甲醇溶液分别制成每1 mL含对照品20µg的溶液。
2.3 供试品溶液的制备
2.3.1 金樱子肉饮片供试品溶液 取金樱子肉饮片粉末约2.0 g,置具塞锥形瓶中,加入水50 mL,加热回流45 min,放冷,滤过,滤液蒸干,加入70%甲醇25 mL,密塞,超声处理(功率300 W,频率40 kHz)45 min,放冷,摇匀,滤过,取续滤液,即得。
2.3.2 金樱子肉饮片标准汤剂冻干粉供试品溶液取金樱子肉饮片标准汤剂冻干粉约0.8 g,置具塞锥形瓶中,加入70%甲醇25 mL,密塞,超声处理(功率300 W,频率40 kHz)45 min,放冷,滤过,取续滤液,即得。
2.3.3 金樱子肉配方颗粒供试品溶液 取金樱子肉配方颗粒适量,研细,取约0.8 g,置具塞锥形瓶中,加入70%甲醇25 mL,密塞,超声处理(功率300 W,频率40 kHz)45 min,放冷,滤过,取续滤液,即得。
2.4 方法学考察
2.4.1 专属性试验 分别精密吸取阴性溶液、参照物溶液及供试品溶液,按“2.1”项色谱条件进样测定,结果见图1-6。可见供试品溶液色谱峰与参照物溶液色谱峰保留时间相对应,且阴性溶液对供试品溶液色谱各特征峰无干扰,表明该分析方法专属性良好。

图1 供试品溶液(配方颗粒)和没食子酸(峰1)、鞣花酸(峰7)、槲皮素-3-O-β-D-吡喃葡糖苷酸(峰8)对照品色谱图Figure 1 Chromatograms of test solution (formula granules) and reference substances of gallic acid(peak 1),ellagic acid(peak 7),quercetin-3-O-β-D-glucopyranosylic acid(peak 8)
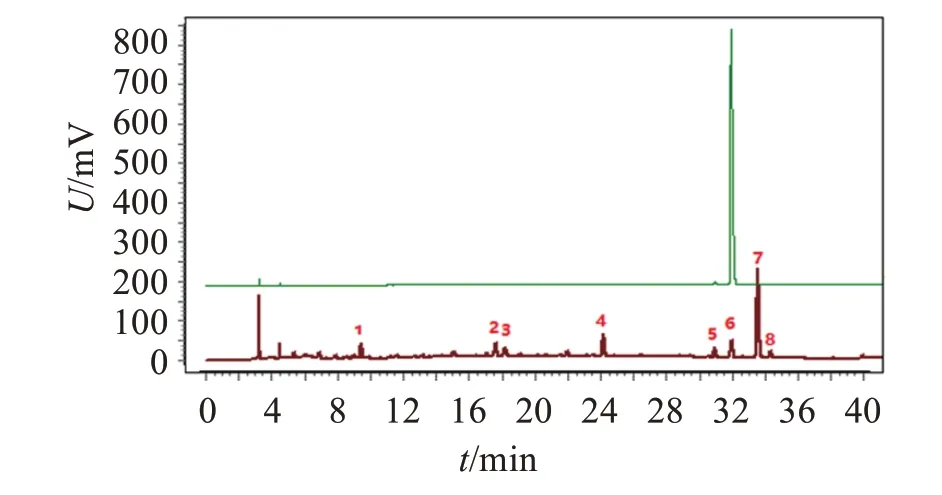
图2 供试品溶液(配方颗粒)和鞣花酸-4-O-α-L-阿拉伯糖苷(峰6)对照品色谱图Figure 2 Chromatograms of test solution (formula granules)and reference substance of ellagic acid-4-O-α-L-arabinoside(peak 6)

图3 供试品溶液HPLC色谱图Figure 3 The HPLC chromatograms of test solution
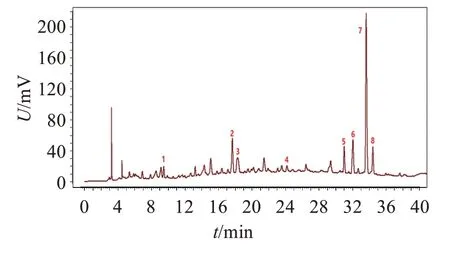
图4 金樱子对照药材HPLC色谱图Figure 4 The HPLC chromatogram of Rosa laevigata reference material
2.4.2 精密度试验 取同一份金樱子肉配方颗粒(D4)供试品溶液,按“2.1”项下色谱条件连续进样6 次,测定各共有峰的相对保留时间和相对峰面积,结果各特征峰与参照物S 峰(7 号峰)的相对保留时间以及相对峰面积的RSD范围分别为0.01%~0.10%和0.13%~1.51%,表明仪器精密度良好。
2.4.3 重复性试验 取同一份金樱子肉配方颗粒(D4),按“2.3.4”项的供试品制备方法重复制备6份,并且按照“2.1”项下色谱条件测定各共有峰的相对保留时间和相对峰面积,结果各特征峰与参照物S 峰(7 号峰)的相对保留时间及相对峰面积的RSD范围分别为0.01%~0.16%和2.03%~2.95%,表明该方法的重复性良好。
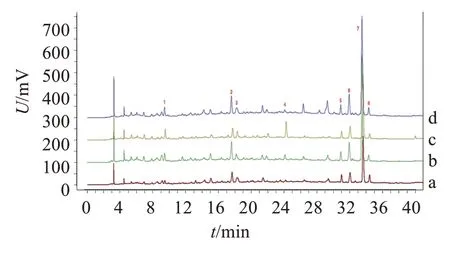
图5 金樱子对照药材与供试品溶液HPLC色谱图Figure 5 The HPLC chromatograms of Rosa laevigata reference material and test solutions

图6 阴性溶液HPLC色谱图Figure 6 The HPLC chromatogram of negative solution
2.4.4 稳定性试验 取同一份金樱子肉配方颗粒(D4)供试品溶液,按按“2.1”项下色谱条件分别在0、2、4、8、12、18、24 h 进样,测定各共有峰的相对保留时间和相对峰面积,结果各色谱峰与参照物S 峰(7号峰)的相对保留时间及相对峰面积的RSD范围分别为0.01%~0.12%和0.38%~3.58%,表明供试品溶液在24 h内稳定。
2.5 指纹图谱及其参数的建立与相似度评价
2.5.1 指纹图谱及其参数的建立 分别取15批金樱子肉饮片、15 批标准汤剂、15 批配方颗粒,按“2.3”项方法分别制备供试品溶液,按“2.1”项色谱条件进样测定,记录色谱图。采用药典委员会编制的指纹图谱相似度评价软件“中药色谱指纹图谱相似度评价系统2012 版”,用15 批金樱子肉饮片、15 批金樱子肉标准汤剂、15 批金樱子肉配方颗粒分别生成对照指纹图谱R1、R2、R3(图7-9);色谱匹配之后,得到8个响应值较合适、分离度较好、纯度较高的共有特征峰(图10-12)。通过查阅文献,对金樱子肉配方颗粒各个特征峰的化学性质进行分析,选用没食子酸、鞣花酸-4-O-α-L-阿拉伯糖苷、鞣花酸、槲皮素-3-O-β-D-吡喃葡糖苷酸对照品对其进行定位指认,确定1号峰为没食子酸,6号峰为鞣花酸-4-O-α-L-阿拉伯糖苷,7 号峰为鞣花酸,8 号峰为槲皮素-3-O-β-D-吡喃葡糖苷酸。
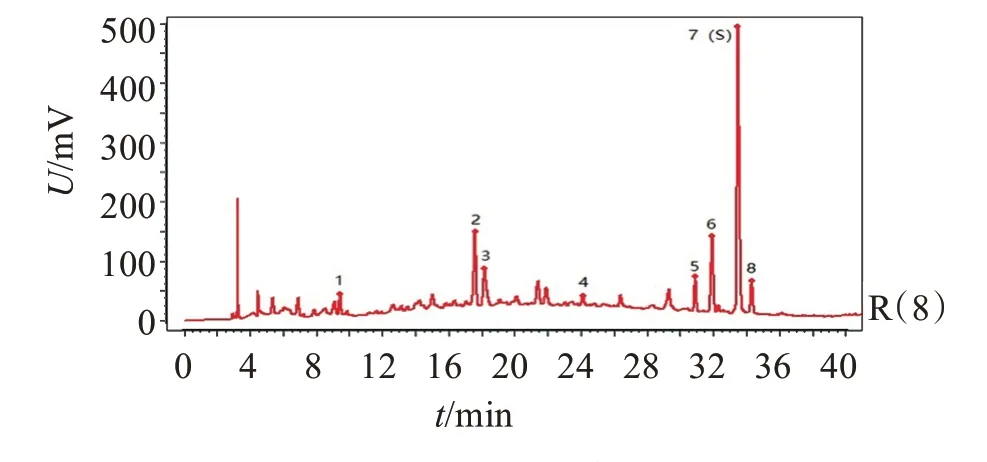
图7 金樱子肉饮片对照指纹图谱Figure 7 The fingerprint of Rosa laevigata fructus
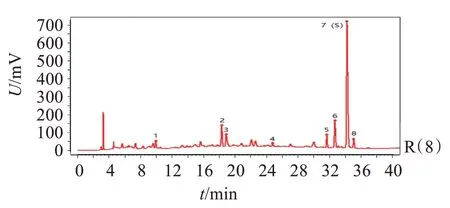
图8 金樱子肉标准汤剂对照指纹图谱Figure 8 The fingerprint of Rosa laevigata fructus standard decoction
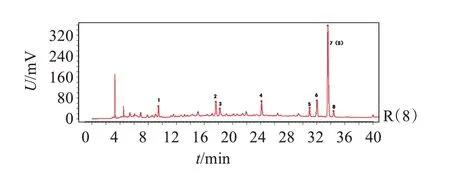
图9 金樱子肉配方颗粒对照指纹图谱Figure 9 The fingerprint of Rosa laevigata fructus formula granules
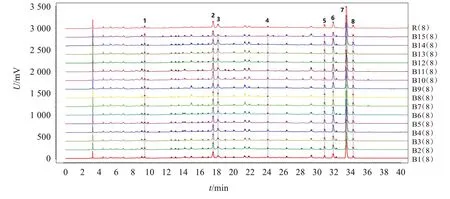
图10 15批金樱子肉饮片指纹图谱Figure 10 Fingerprints of 15 batches of Rosa laevigata fructus
2.5.2 相似度评价研究 用药典委员会编制的指纹图谱相似度评价软件“中药色谱指纹图谱相似度评价系统2012 版”,将15 批金樱子肉饮片、标准汤剂、配方颗粒指纹图谱导入并计算各批次与其对照图谱的相似度,结果见表1。结果表明15 批金樱子肉饮片、标准汤剂、配方颗粒的指纹图谱与其相应对照指纹图谱(R1、R2、R3)的相似度均大于0.95,表明不同批次金樱子肉饮片、标准汤剂、配方颗粒的质量较为稳定。
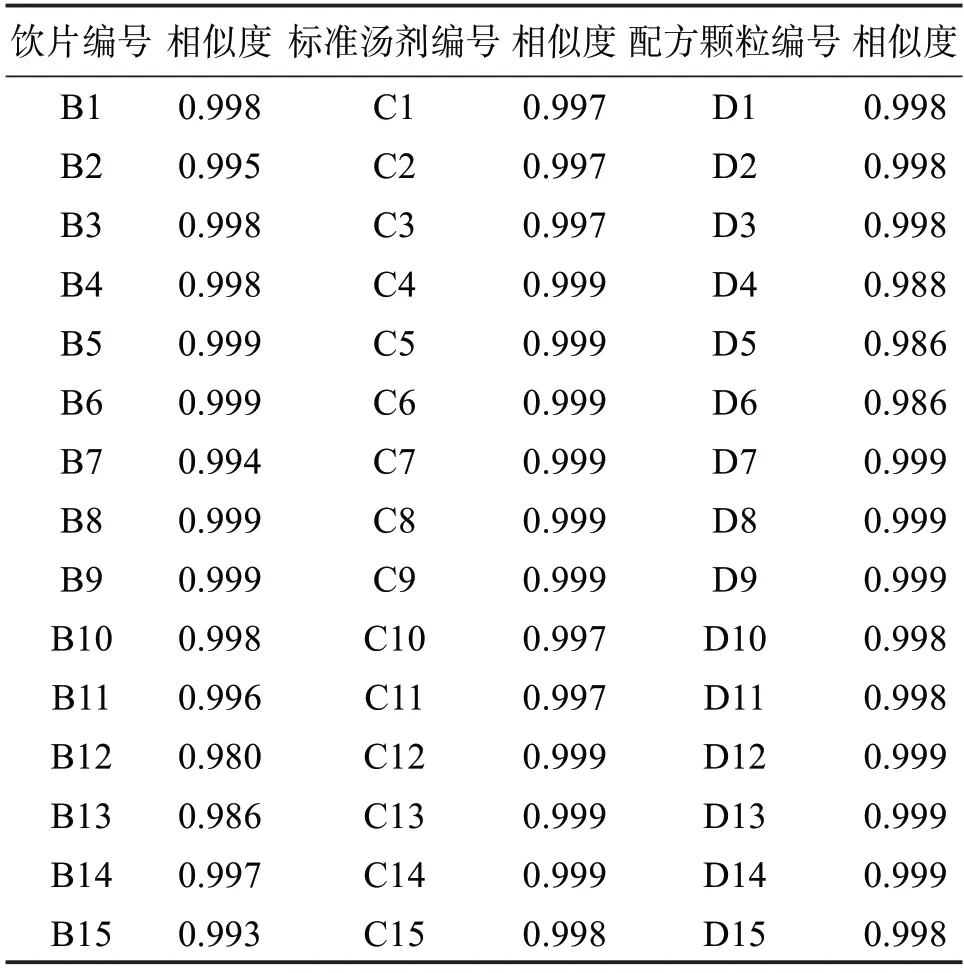
表1 15批金樱子肉饮片、标准汤剂、配方颗粒指纹图谱相似度结果Table 1 Results of similarity analysis of 15 batches of Rosa laevigata fructus pieces,standard decoction and formula granules

图11 15批金樱子肉标准汤剂指纹图谱Figure 11 Fingerprints of 15 batches of Rosa laevigata fructus standard decoction
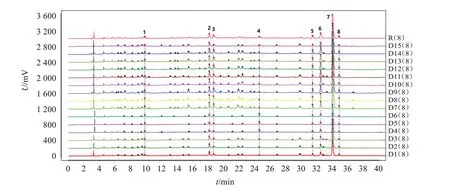
图12 15批金樱子肉配方颗粒指纹图谱Figure 12 Fingerprints of 15 batches of Rosa laevigata fructus formula granules
2.5.3 对照指纹图谱的比较 将15 批金樱子肉饮片、标准汤剂、配方颗粒指纹图谱生成的对照指纹图谱R1、R2、R3(见图13)分别导入软件“中药色谱指纹图谱相似度评价系统2012 版”,结果显示:与金樱子肉饮片比较,金樱子肉标准汤剂和配方颗粒的相似度分别为0.991 和0.992,金樱子肉标准汤剂和配方颗粒指纹图谱相似度为1.000,表明金樱子肉饮片、标准汤剂与配方颗粒成分基本一致,标准汤剂在提取、浓缩、干燥过程中,其成分种类无明显变化。
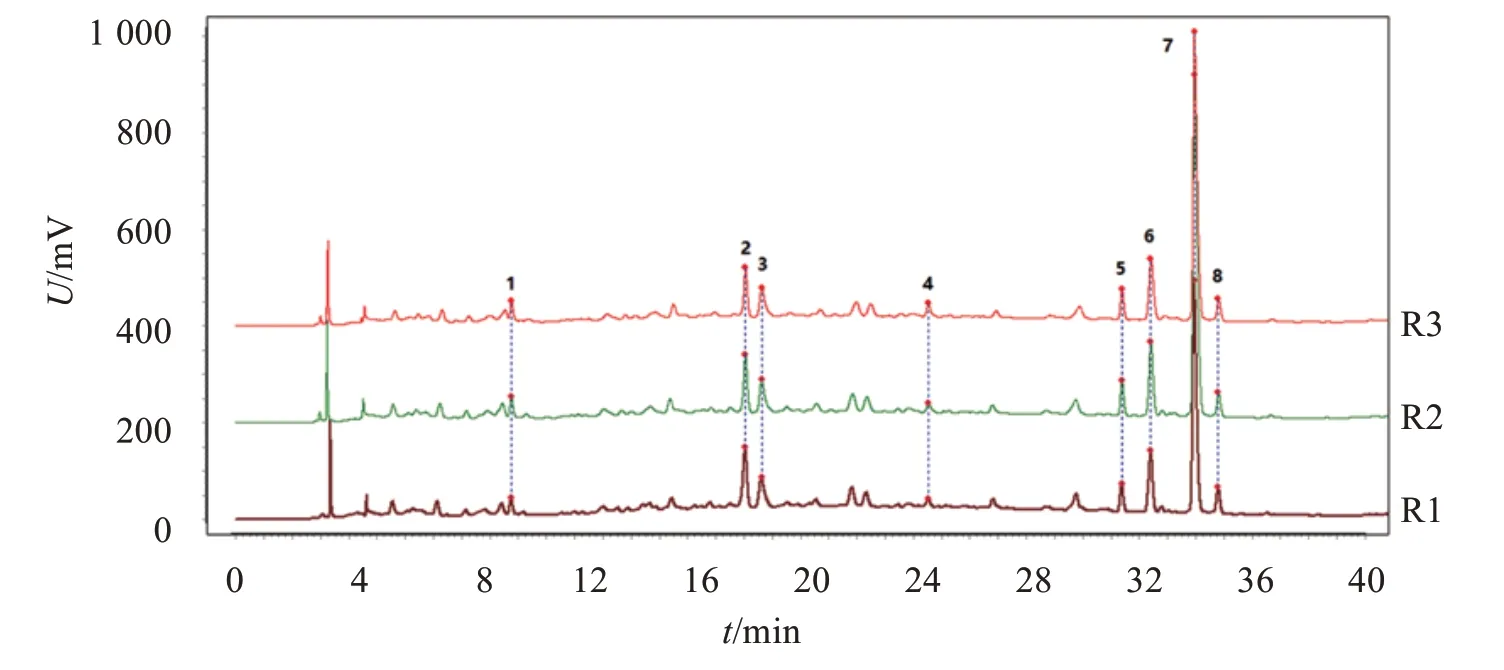
图13 金樱子肉饮片对照指纹图谱(R1)、标准汤剂对照指纹图谱(R2)和配方颗粒对照指纹图谱(R3)Figure 13 Reference fingerprints of Rosa laevigata fructus,standard decoction and formula granules by HPLC
2.6 化学模式识别研究
2.6.1 共有峰相关性分析 采用SPSS 26.0 软件,以15批金樱子肉饮片、标准汤剂和配方颗粒共45个样品各特征峰的峰面积值为变量进行皮尔逊相关性分析,结果见表2。可见,45个样品中色谱峰峰1(没食子酸)和峰5,峰2 和峰6(鞣花酸-4-O-α-L-阿拉伯糖苷)均具有显著的正相关性;峰2 和峰3、峰8(槲皮素-3-O-β-D-吡喃葡糖苷酸),峰3 和峰5、峰6(鞣花酸-4-O-α-L-阿拉伯糖苷)、峰7(鞣花酸)、峰8(槲皮素-3-O-β-D-吡喃葡糖苷酸);峰5 和峰6(鞣花酸-4-O-α-L-阿拉伯糖苷)、峰7(鞣花酸)、峰8(槲皮素-3-O-β-L-吡喃葡糖苷酸);峰6 和峰7(鞣花酸)、峰8(槲皮素-3-O-β-D-吡喃葡糖苷酸)均具有极显著的正相关性。

表2 15批金樱子肉饮片、标准汤剂、配方颗粒指纹图谱共有峰的相关性分析结果Table 2 Correlation analysis results of common peaks of Rosa laevigata fructus,standard decoction and formula granules
2.6.2 聚类分析 采用SPSS 26.0 软件,以15 批金樱子肉饮片、标准汤剂和配方颗粒共45个样品各特征峰面积为变量进行聚类分析,结果见图14。可见,当距离为10 时,45 批样品可以分为4 类,B4-B7、B14、B15、C1-C15、D1-D3、D7-D15 聚为一类,B1-B3、B8-B11 聚为一类,D4-D6 聚为一类,B12、B13聚为一类。表明饮片、标准汤剂、配方颗粒三者之间无显著性差异,且标准汤剂与配方颗粒更为接近。

图14 金樱子肉饮片、标准汤剂和配方颗粒HPLC指纹图谱聚类分析树状图Figure 14 The cluster analysis tree of Rosa laevigata fructus,standard decoction,formula granules
2.6.3 主成分分析(PCA)采用SPSS 26.0 软件,对15批金樱子肉饮片、标准汤剂和配方颗粒共45个样品各特征峰面积的标准化值(Xi)进行主成分分析,主成分结果以特征值>1 为标准提取得到2 个主成分,计算得特征值和方差贡献率见表3,主成分因子载荷矩阵见表4。由结果可知,前2个主成分累积贡献率为72.13%,表明提取的2 个主成分能反映金樱子肉指纹图谱的大部分信息。主成分1的特征值为4.176,方差贡献率为52.20%,载荷较高的峰有峰3、峰4、峰5、鞣花酸-4-O-α-L-阿拉伯糖苷、鞣花酸和槲皮素-3-O-β-D-吡喃葡糖苷酸,表明这6 个峰主要反映主成分1的信息;主成分2的特征值为1.594,方差贡献率为19.92%,载荷较高的峰有没食子酸、峰2,表明这2个峰主要反映主成分2的信息。
根据表3 和表4 的数据,由公式Fi=Wi1X1+Wi2X2+…….+WijXj(W为主成分中各个变量的权重,由成分矩阵中的第j列载荷除以对应成分特征值的算术平方根所得),计算得到主成分得分F1、F2,主成分得分图见图15。

图15 金樱子肉饮片、标准汤剂和配方颗粒HPLC指纹图谱主成分得分图Figure 15 PCA score plot of principal component analysis of Rosa laevigata fructus,standard decoction and formula granules
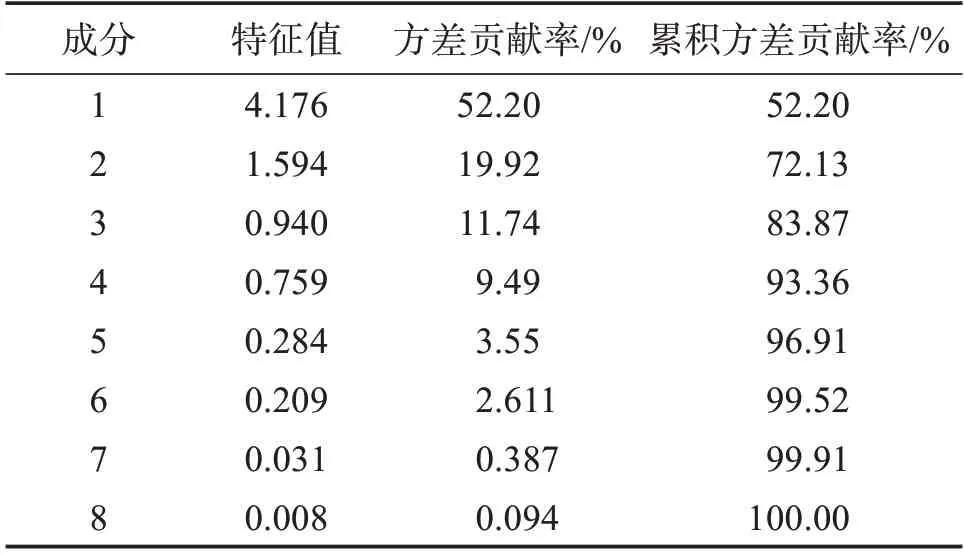
表3 金樱子肉饮片、标准汤剂和配方颗粒主成分分析特征值及方差贡献率Table 3 Characteristic values and variance contribution rates of Rosa laevigata fructus,standard decoction and formula granules
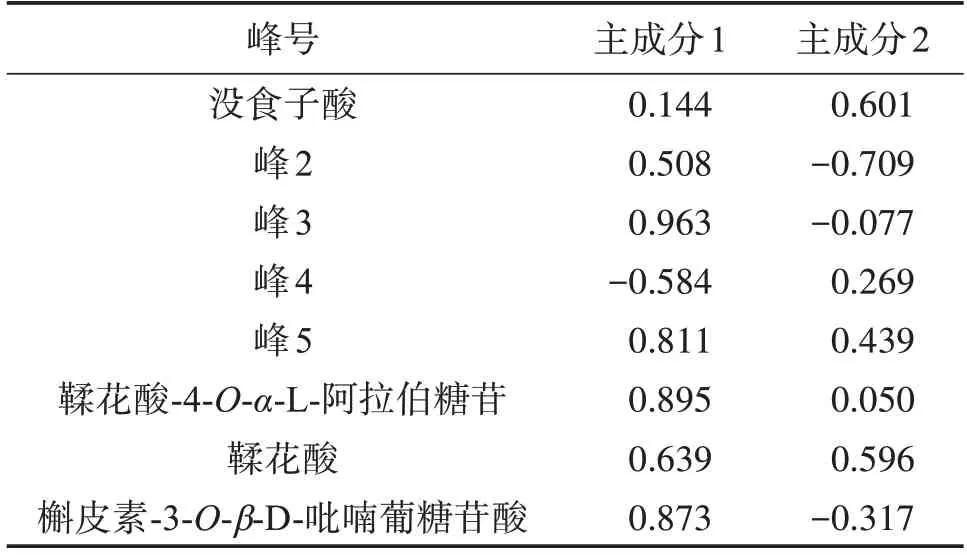
表4 金樱子肉饮片、标准汤剂和配方颗粒主成分因子载荷矩阵Table 4 Principal component factor load matrix of Rosa laevigata fructus,standard decoction and formula granules
2.6.4 正交偏最小二乘判别分析(OPLS-DA)采用SIMCA 14.1 软件,以15 批金樱子肉饮片、标准汤剂和配方颗粒共45 个样品各特征峰峰面积为变量进行OPLS-DA 分析,结果见图16-17。由模型参数可知,数据矩阵的解释率参数R2X(cum)=0.460,模型区分参数R2Y(cum)=-0.005 7,模型预测参数Q2=-0.226,均符合要求,表明该数学模型稳定可靠。45个样品可分成4类。以VIP值>1为提取标准,得到峰8(槲皮素-3-O-β-D-吡喃葡糖苷酸)、峰3、峰2、峰6(鞣花酸-4-O-α-L-阿拉伯糖苷)是影响分类的主要标志性成分。
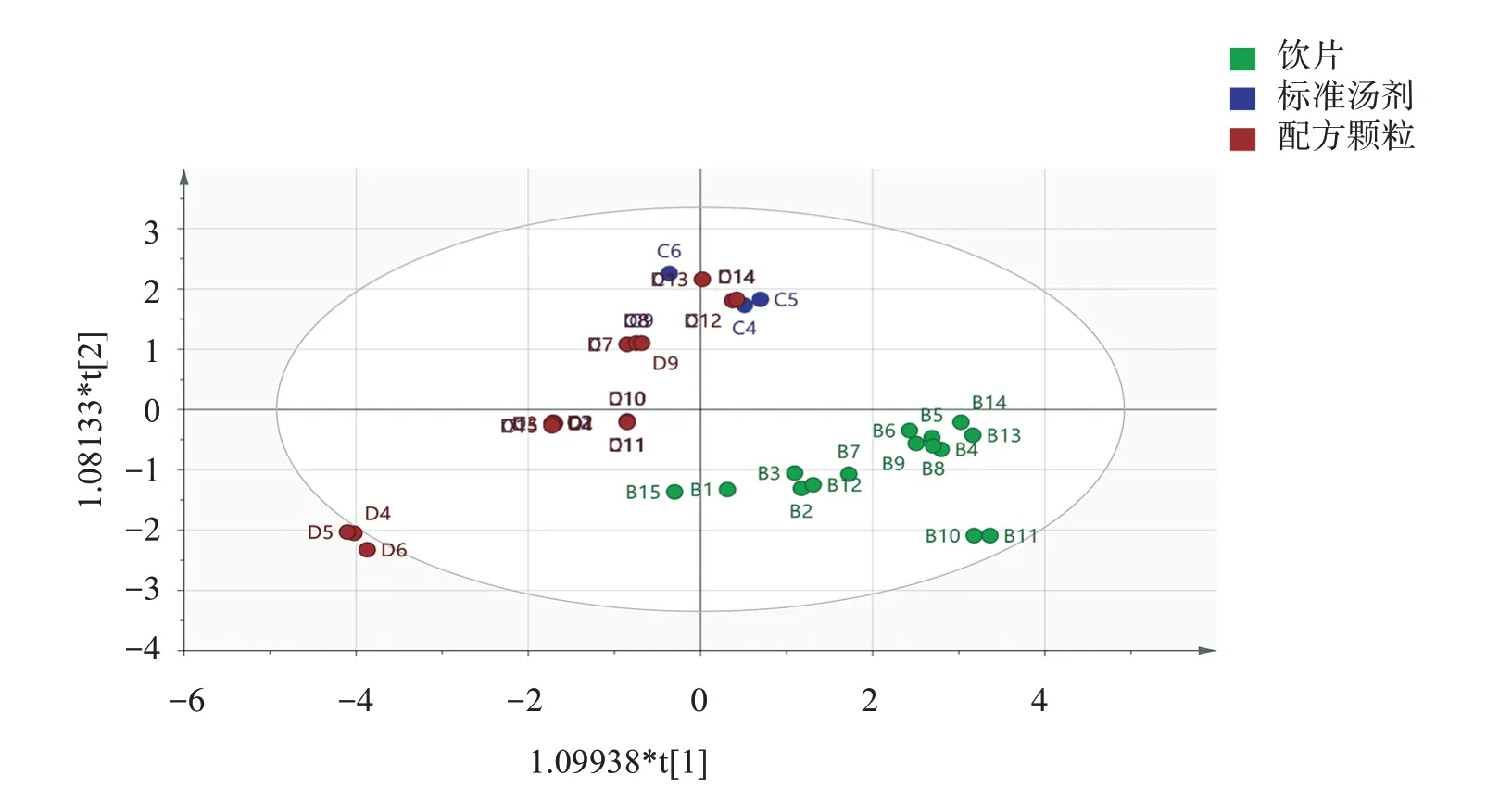
图16 金樱子肉饮片、标准汤剂和配方颗粒HPLC指纹图谱OPLS-DA得分图Figure 16 OPLS-DA score plot of Rosa laevigata fructus,standard decoction and formula granules

图17 金樱子肉饮片、标准汤剂和配方颗粒HPLC 指纹图谱VIP值Figure 17 Results of VIP values of Rosa laevigata fructus,standard decoction and formula granules
3 讨论
本研究参照《医疗机构中药煎药室管理规范》和《中药配方颗粒质量控制与标准制定技术要求》,对制备工艺关键参数进行考察研究。考察饮片吸水率和不同加水量,确定金樱子肉标准汤剂煎煮加水量为一煎加水8 倍量和二煎加水6 倍量,并通过古文中医药著作和现代临床的使用情况,确定标准汤剂的煎煮工艺为:冷浸30 min,煎煮两次,一煎加8 倍量水,煎煮30 min,二煎加6 倍量水,煎煮25 min。考察不同目数滤材,选择200 目滤布作为汤剂的过滤方式。对不同浓缩温度的影响考察,确定了减压浓缩过程中浓缩温度控制在55~65 ℃,并且确定真空度和浓浸膏相对密度等参数,并且采用冷冻干燥制备成金樱子肉标准汤剂。为了确保颗粒和标准汤剂的一致性,配方颗粒制备工艺参数与标准汤剂的制备工艺参数保持一致。
金樱子中主要含有多糖类、黄酮类、鞣质等成分,本实验以相关文献结果[4-9]为导向,针对其主要成分展开指纹图谱方法研究,通过对比不同波长的色谱图,发现当检测波长为260 nm 时,色谱图基线平稳且各特征峰响应值较高;且考察过程中发现采用乙腈∶0.1%磷酸溶液流动相洗脱、在流速1.0 mL/min和柱温30 ℃条件下,各色谱峰分离效果最好。同时,考虑到样品制备方法对指纹图谱的建立影响较大,选取了纯水、甲醇、70%甲醇、50%甲醇、30%甲醇、乙醇、70%乙醇、50%乙醇、30%乙醇作为提取溶剂,结果表明,选择70%甲醇作为提取溶剂时,指纹图谱得到的色谱峰信息量较大,峰型较好,系统适应性参数相对较优;并考察了超声提取和加热回流不同提取方式,结果显示提取方式对指纹图谱的影响较小,在此基础上,考察了提取时间30~60 min,在该范围内,各特征成分能被完全提取,综合考虑,选择45 min 为提取时间。对取样量0.4~1.0 g 进行考察,当金樱子肉标准汤剂取样量为0.8 g 时,色谱峰的响应值相对均衡,因此,取样量确定均为0.8 g。
本试验确定的金樱子肉配方颗粒8个特征共有峰在饮片、标准汤剂的色谱图中均可找到对应峰,并指认了其中的1、6、7、8号峰,分别为没食子酸、鞣花酸-4-O-α-L-阿拉伯糖苷、鞣花酸和槲皮素-3-O-β-D-吡喃葡糖苷酸;相似度评价结果显示,15 批金樱子肉饮片、标准汤剂、配方颗粒指纹图谱与相应对照指纹图谱的相似度均大于0.950,三者对照指纹图谱的相似度均大于0.990;皮尔逊相关性分析检验了共有峰两两之间的关系强度,表明大部分共有峰成显著相关关系,说明金樱子肉饮片、标准汤剂和配方颗粒在化学成分类型以及成分的含量上没有明显的差异。主成分分析(PCA)则通过少数几个主成分来解释多个共有峰间的内部结构,体现批次间的可视化,共有峰间相关程度越高,主成分分析效果越好,结果显示,两个主成分的累计方差贡献率为72.13%,金樱子肉饮片、标准汤剂和配方颗粒三者没有明显差异,且标准汤剂与配方颗粒的相似度较高。聚类分析均表明三者没有明显的差异,但标准汤剂与配方颗粒的质量更为相近,说明配方颗粒制备工艺参数的合理性和稳定性,配方颗粒生产制备过程中,各特征峰均能稳定性传递,没有发生明显的降解或者增加的情况,制得的配方颗粒的质量水平与传统标准汤剂基本一致。OPLS-DA 将45 个样品分为4 类,并筛选出4 个VIP 值大于1 的差异性成分峰8(槲皮素-3-O-β-D-吡喃葡糖苷酸)、峰3、峰2、峰6(鞣花酸-4-O-α-L-阿拉伯糖苷),目前2020 年版《中国药典》“金樱子”项下尚未有含量测定项目,而关于金樱子的含量测定的报道也比较少,因此,计划下一步从该4 个特征性成分出发,建立专属性的含量测定方法,进一步评价金樱子肉饮片、标准汤剂和配方颗粒含量的相关性。
试验中发现,金樱子对照药材指纹图谱,在特征峰的个数上与金樱子肉指纹图谱一致,说明了两者在化学成分的一致,含有毛、核等部位的金樱子对照药材图谱中,没有其他明显的特征峰的出现,说明了金樱子的有效成分主要在金樱子肉的部位,证明药典饮片炮制中“除去毛、核”等步骤的合理性,后续将结合含量测定,进一步对金樱子和金樱子肉的差异进行深入的对比研究。
本研究采用高效液相色谱法建立金樱子肉饮片、标准汤剂和配方颗粒指纹图谱,该方法专属性强,重复性好,采用多种统计方法对金樱子肉饮片、标准汤剂和配方颗粒三者的相关性进行分析,结果表明三者的相关性较好,采用该指纹图谱技术,可以用于金樱子肉配方颗粒生产制备过程中从原料到成品阶段的质量有效控制。
