基于红霉素选择性分离的分子印迹膜制备及其性能研究
2023-01-18孙冬舒周玉凤
孙冬舒,周玉凤,程 浩
(1. 吉林师范大学 工程学院,吉林 四平 136000;2. 吉林师范大学 辽源分院化学系,吉林 辽源 136200;3. 四平职业大学 学生工作处,吉林 四平 136000)
红霉素是大环内酯类抗生素,能够有效抑制微生物生长,起到抗菌的作用.但是不合理利用抗生素的现象愈演愈烈,人类和动物不能吸收的抗生素会通过排泄作用排入环境当中,对环境造成了严重的污染和负担[1-4].因此开发一种经济、环保、可实用性强的高选择性分离红霉素的方法十分必要.
分子印迹膜(Molecularly imprinted membranes, MIMs)基于膜分离技术和分子印迹技术发展而来,是一种具有选择性分离功能的膜材料.分子印迹膜使用范围较广、操作简便、可塑造性强、具有优异的特异选择性[5-8].分子印迹膜是以传统滤膜为载体基础上,结合分子印迹技术,通过在膜上留下与目标分子大小、构型相同的印迹空穴,对目标分子能够快速、高效地识别,通过共价键或非共价键结合在印迹空穴内.非目标分子则能够在同一时间顺利通过,从而达到了对目标分子选择性分离纯化的目的[9-13].目前,应用分子印迹膜定向分离抗生素的研究被广泛关注,但是对实际污水中的应用而言,自身疏水性的分子印迹膜极易被无机盐、有机污染物、微生物、蛋白质等复杂组分污染,这是分子印迹膜在污水中应用所面临的最大挑战[14].因此,提升分子印迹膜的亲水性是提高分子印迹膜综合性能、延长使用寿命的必要手段.
本文以红霉素的选择性分离为出发点,选用聚偏氟乙烯为膜基底材料,通过聚乙二醇和二氧化钛纳米颗粒对膜进行改性,使其具有更好的亲水性能以及更优异的选择性分离性能.该材料制备方法操作简单、快速,具有较高的应用价值.
1 实验部分
1.1 原料
聚偏氟乙烯(PVDF,分子量430000)粉末购自法国公司Arkema.N,N-二甲基乙酰胺(DMAc),聚乙二醇(PEG,600Da),二氧化钛(TiO2),α-甲基丙烯酸(MAA),3-(异丁烯酰氧)-丙基三甲氧基硅烷(KH-570),红霉素(Erythromycin,EM),罗红霉素(Roxithromycin,RM),二甲基丙烯酸乙二醇酯(EGDMA),偶氮二异丁腈(AIBN)购自Aladdin Reagent.实验室自制去离子水用于各种清洗工艺和水溶液.
1.2 实验步骤
1.2.1 PPT-MIMs的制备
(1) 0.1 g TiO2纳米颗粒分散到乙醇溶液中超声处理15 min.将超声完成的悬浮液倒在玻璃板上放置10~15 min后,将玻璃板上放置在真空干燥箱中在50 ℃干燥5 min,确保乙醇完全蒸发,形成TiO2薄层.
(2) 4.0 g PVDF粉末,25 mL DMAc和0.1 g PEG混合到三颈圆底烧瓶中配制成铸膜液密封,25 ℃下机械搅拌24 h,保持温度不变静置24 h,消除气泡.将得到铸膜液分别浇铸在玻璃板和含有TiO2薄层的玻璃板上,然后将玻璃板浸入到去离子水中,通过相转化过程即可制备出PVDF膜和PVDF-PEG/TiO2杂化膜.
(3) 向80 mL乙醇、20 mL去离子水加入3 mL KH570形成均匀的混合溶液,将PVDF-PEG/TiO2杂化膜浸没于上述溶液中,密封,通入氮气排出反应容器中的氧气,80 ℃恒温水浴振荡器中反应16 h,反应结束后用乙醇和去离子水进行浸泡清洗,去除掉未反应的物质,得到KH570@PVDF-PEG/TiO2.
(4) 0.1 mmol EM、0.5 mmol MAA加入到50 ml的乙腈中,密封,25 ℃恒温水浴中持续振荡12 h,获得预聚合溶液.随后将KH570@PVDF-PEG/TiO2,0.1 mol EGDMA,0.05 g AIBN依次加入到上述溶液中,密封,通入氮气,65 ℃反应24 h,分别用乙醇和水对其进行浸泡清洗;将上述膜置于200 mL体积比为9∶1的无水乙醇和冰乙酸溶液中洗脱目标分子EM,40 ℃真空烘干后得到PPT-MIMs.此外,作为对照,非印迹膜(NMIMs)的合成方法与PPT-MIMs相似,只是在印迹过程中不加入EM.
1.2.2 等温吸附实验
将一片PPT-MIMs或NMIMs分别浸入含有10 mL具有不同初始浓度的EM溶液的离心管中(10、20、30、60、80、100、120、180 mg·L-1).静置直至吸附达到平衡,然后通过UV-Vis测量溶液的浓度.整个实验过程在25 ℃下进行.实验重复三次,并计算三组平行测试的平均值.PPT-MIMs和NMIMs的平衡吸附量通过式(1)计算:
(1)
其中Qe(mg·g-1)为PPT-MIMs和NMIMs的平衡吸附量,C0(mg·L-1)和Ce(mg·L-1)为EM的初始浓度和平衡浓度.V(L)为溶液的体积,m(g)为膜的质量.
1.2.3 动力学吸附实验
将一片PPT-MIMs或NMIMs分别浸入到8个10 mL初始浓度均为100 mg·L-1的EM溶液的离心管中.在不同的时间间隔(5、10、20、30、60、90、120、180 min)将膜取出,测量剩余EM的浓度.整个实验过程在25 ℃下进行.为了得到最终数据的最精确的信息,每个实验重复三次,并计算三组平行测试的平均值.根据式(2)计算PPT-MIMs和NMIMs在不同时间的吸附量:
(2)
其中Qt(mg·g-1)为PPT-MIMs和NMIMs在不同时间的吸附量,C0(mg·L-1)和Ct(mg·L-1)分别为EM的初始浓度和t时刻的浓度.V(L)为溶液的体积,m(g)为膜的质量.
1.2.4 选择性吸附实验
将RM作为竞争因子,对所制备的PPT-MIMs和NMIMs进行选择吸附性能研究.将一片PPT-MIMs和NMIMs浸入10 mL(浓度为5、10、30、50、80、100 mg·L-1)EM和RM混合溶液中.待吸附达到平衡后,分别测定EM和RM样品的浓度.并利用式(1)计算吸附量(Qe,mg·g-1).
2 结果与讨论
2.1 SEM分析
通过SEM观察PVDF膜(图1A)、PPT-MIMs(图1B)和NMIMs(图1C)的表面形貌.如图所示,PEG作为致孔剂通过相转化过程制备而成的PVDF膜表面光滑并且具有多孔结构.与PVDF膜相比,PPT-MIMs则为更密集的多孔结构,很多纳米颗粒附着在其表面,在其表面可以清晰的看到有明显的聚合层出现,说明TiO2纳米颗粒成功接枝到PVDF膜表面,同时分子印迹聚合物成功聚合到PVDF膜表面.由于和NMIMs和PPT-MIMs合成方法相似,只是在印迹过程中不加入模板分子,因此,NMIMs呈现出与PPT-MIMs较为相似的多孔结构,以及纳米颗粒和聚合层附着在其表面.

图1 PVDF膜(A)、PPT-MIMs(B)和NMIMs(C)的SEM图
2.2 接触角分析
使用水接触角测试仪通过座滴法测量膜材料的水接触角数值,分析膜材料的亲水性,接触角的值越小说明膜的亲水性越高.PVDF膜(图2A)的水接触角值为90.1°,PPT-MIMs(图2B)的水接触角值为58.3°,NMIMs(图2C)的水接触角值为57.8°.说明相比于PVDF膜,PPT-MIMs和NMIMs的亲水性明显提高.进一步证明TiO2纳米颗粒成功接枝到PVDF膜表面,同时分子印迹聚合物成功聚合到PVDF膜表面.

图2 PVDF膜(A)、PPT-MIMs(B)和NMIMs(C)的水接触角图
2.3 等温吸附研究
为了探究PPT-MIMs的吸附能力,进行了静态吸附实验.图3为PPT-MIMs和NMIMs对EM的等温吸附曲线.如图所示,随着EM的初始浓度增加PPT-MIMs和NMIMs的平衡吸附量也随之增加.此外,PPT-MIMs对EM的吸附量要明显高于NMIMs的吸附量,是因为PPT-MIMs具有多孔的结构,内部的印迹聚合物对EM有特异性识别的能力.为了进一步研究PPT-MIMs和NMIMs与EM之间的相互作用,用Langmuir和Freundlich等温模型对等温吸附实验数据进行拟合.公式如下:
(3)
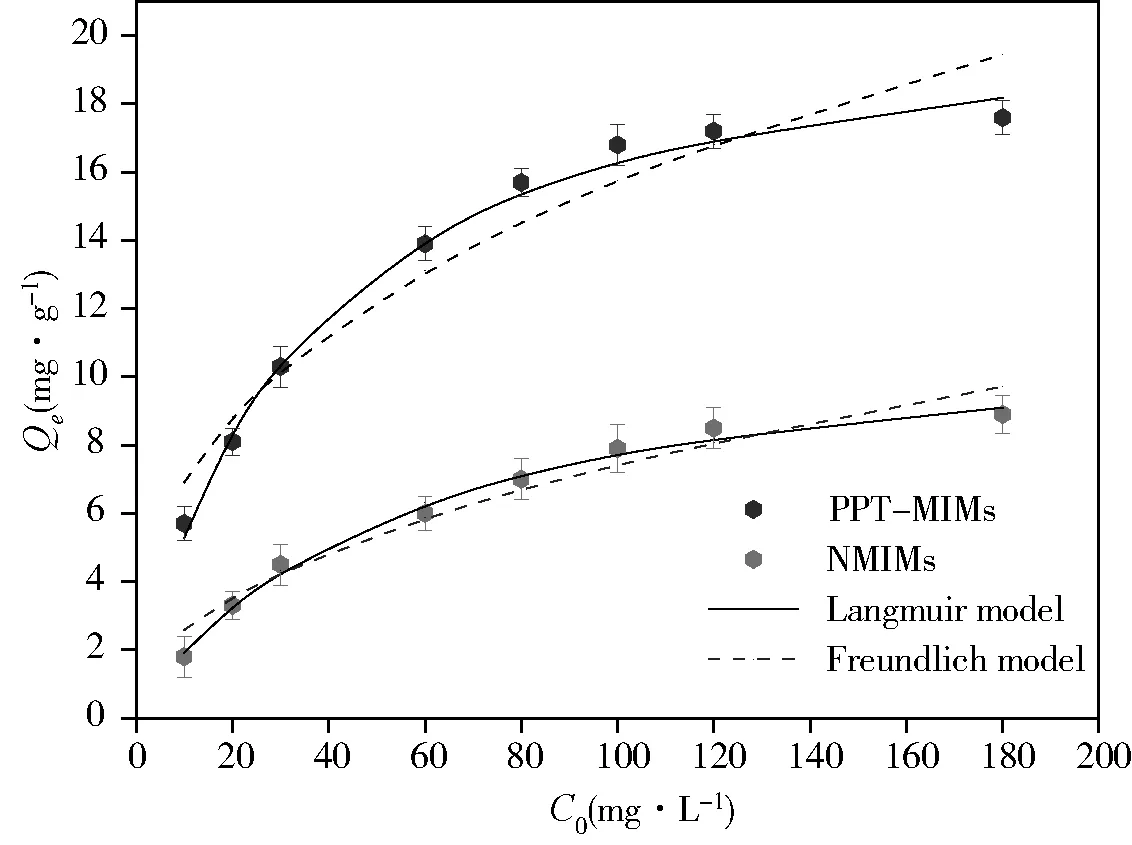
图3 PPT-MIMs和NMIMs对EM的等温吸附曲线及Langmuir和Freundlich非线性拟合曲线
(4)
式中,Qe(mg·g-1)为PPT-MIMs和NMIMs的平衡吸附量;Qm(mg·g-1)为PPT-MIMs和NMIMs饱和吸附量;C0(mg·L-1)为EM的初始溶度;KL和KF分别为Langmuir和Freundlich常数.线性回归值与Langmuir模型拟合良好(R2=0.9908)(图3),表明PPT-MIMs的吸附过程为单分子层吸附.
2.4 动力学吸附研究
动力学吸附参数能反映出膜的吸附能力,故对PPT-MIMs和NMIMs进行了动力学吸附实验.图4为PPT-MIMs和NMIMs的动力学吸附曲线.整个实验过程进行了180 min,在开始的60 min吸附反应较快,而后的过程十分缓慢.与NMIMs相比,PPT-MIMs表现出更快的动力学吸附作用,这是由于在PPT-MIMs表面存在的印迹层对EM表现出快速的吸附作用并且存在特异性识别能力的空穴.为了进一步研究PPT-MIMs和NMIMs对EM的吸附作用速度,采用拟一级动力学模型和拟二级动力学模型对PPT-MIMs和NMIMs的吸附数据进行拟合,公式如下:
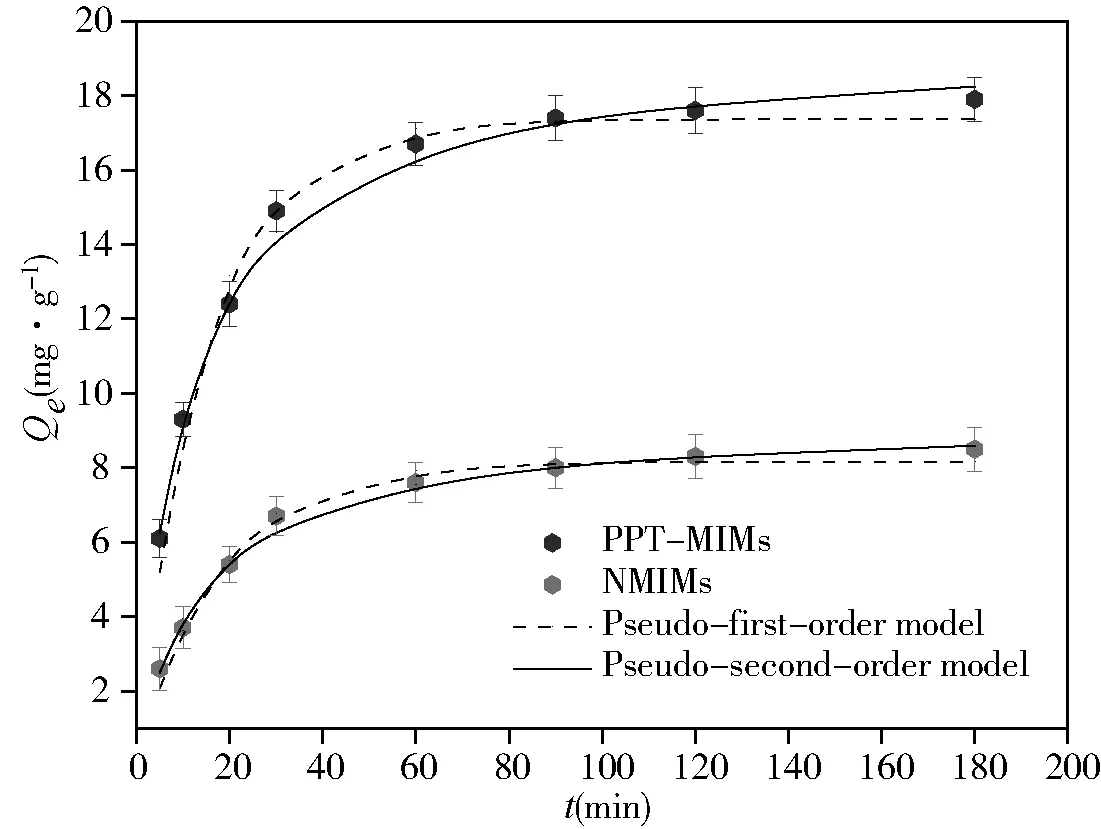
图4 PPT-MIMs和NMIMs对EM的吸附动力学曲线及动力学模型拟合曲线
Qt=Qee-k1t
(5)
(6)
Qe(mg·g-1)为PPT-MIMs和NMIMs的平衡吸附容量,Qt(mg·g-1)为不同时间的PPT-MIMs和NMIMs的吸附容量.k1(min-1)和k2(g·mg-1·min-1)分别拟一级动力学模型和拟二级动力学模型的平衡速率常数.
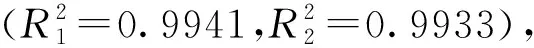
2.5 选择性吸附研究
选择性吸附性能是分子印迹膜一项重要的参数,可以体现出其在实际应用中的价值.选取与模板分子EM分子式结构类似的RM为竞争对象,以10 mL EM和RM混合溶液对PPT-MIMs进行特异性选择性能分析.如图5所示,随着混合液浓度的逐渐升高,PPT-MIMs对EM的吸附量也有明显的增高,对RM的吸附量增高的不明显.这是由于PPT-MIMs结构存在特异性识别空穴,对EM有特异的识别能力和较好的选择性吸附作用,使得PPT-MIMs和EM的相互作用更明显.
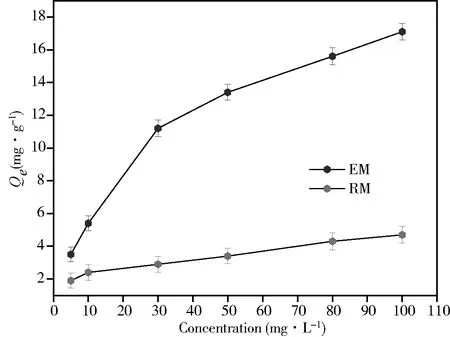
图5 PPT-MIMs对EM和RM的吸附选择性
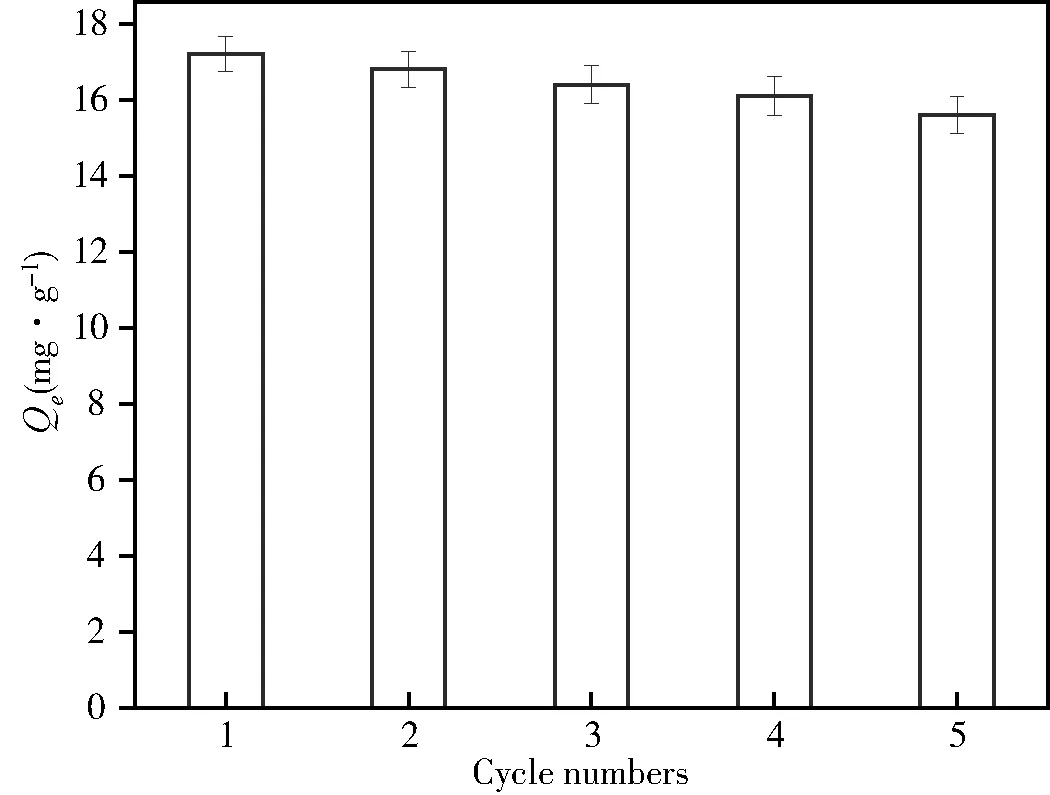
图6 PPT-MIMs的稳定性能图
2.6 稳定性研究
膜材料的稳定性是一个关键性指标,可以通过吸附/解吸附过程研究其结构稳定性.用同一片PPT-MIMs在浓度为100 mg·L-1的EM中,吸附达到平衡,测量吸附量.而后用0.5 mol·L-1的HCl溶液对其进行洗脱,使其有效识别位点重新获得.重复进行吸附/洗脱过程5次.由图可以看出,经过5次循环实验后,PPT-MIMs对EM的吸附量仍能保持为最大吸附量的90.7%,这表明PPT-MIMs具有较好的稳定性,有利于进一步实际应用.
3 结论
以聚偏氟乙烯为膜基底材料,EM为模板分子,PEG为制孔剂,利用TiO2分子对PVDF膜进行表面改性,制备出红霉素分子印迹复合膜(PPT-MIMs),并对于红霉素的吸附性能进行研究.在选择性吸附研究中发现,在与RM竞争分子共存的环境下,PPT-MIMs对EM的吸附容量远高于对RM的吸附容量.动力学吸附研究中,发现PPT-MIMs对EM的吸附过程较快,数据符合拟二级动力学模型.在5次吸附/解吸循环操作后,PPT-MIMs的吸附量容为最大吸附量的90.7%,表明PPT-MIMs具有稳定的可再生性能.本文PPT-MIMs的成功制备为构筑实用型的分子印迹膜提供了新思路和新方法.
